无阿片麻醉对腹腔镜胆囊切除术患者肠功能的影响
2021-03-27王亚丽石雯迪李汝泓王亚珍
王亚丽,石雯迪,李汝泓,王亚珍
(承德医学院附属医院麻醉科,河北 承德 067000)
0 引言
阿片类药物是目前临床缓解疼痛应用最广泛的药物。在临床上,阿片类药物引起的肠功能障碍( OIBD)是一种常见的并发症,可能会无限期持续出现并伴有不同症状,如口干、胃食管反流、呕吐、腹胀、腹部疼痛、厌食、便秘和大便不完全排空等,严重影响了患者的生活质量。快速康复外科(ERAS)指采用一系列有循证医学证据的优化的围手术期处理措施,整合麻醉、镇痛、微创手术、护理等各方面,临床多学科合作,从而降低术后并发症发生率和死亡率、缩短术后住院时间和减少住院费用。近年来,在手术快速康复理念的影响下,促进胃肠道功能恢复、预防术后肠功能障碍成为国内外许多学者的研究重点。能否在保证麻醉效果的前提下,通过最大限度的减少阿片类药物的使用从而减少OIBD,推进快速康复外科的发展,目前临床上有关此方面的研究较少。本实验观察应用阿片类药物麻醉和无阿片类药物麻醉对腹腔镜手术后肠功能的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2018 年10 月至2020 年10 月在承德医学院附属医院行腹腔镜胆囊切除术的患者60 例,采用随机数字表法分为无阿片类药物麻醉组(OFA 组)和有阿片类药物麻醉组(OA 组),每组30 例,两组患年龄、BMI、ASA 分级、手术时间及麻醉时间比较,差异无统计学意义,如表1。
1.2 纳入与排除标准
1.2.1 纳入标准
①年龄18-65 岁ASA Ⅰ~Ⅱ级择期腹腔镜下胆囊切除术患者;②体重指数BMI18.5kg/m2-28kg/m2;③既往无腹腔镜手术或腹部开腹手术史;④既往无克罗恩病、慢性溃疡性结肠炎、胃肠道肿瘤等胃肠道疾病者
1.2.2 排除标准
①长期服用阿片类药物;②长期服用非甾体类抗炎药;③腹腔镜手术过程中转开腹手术治疗者;④有精神病病史,癫痫病史,术前焦虑,抑郁,情绪管理障碍;⑤不能与研究人员合作者;⑥存在增加胃内容物反流和呼吸道误吸因素的患者;⑦咽部存在肿物、损伤、感染或其他病理改变的患者;⑧肺顺应降低的患者,尤其是预计术中气道峰压大于30cmH2O 者;⑨手术时间>1.5h 或麻醉时间>2h;⑩对试验中可能用的药过敏或有药物使用禁忌症者。
1.3 方法
患者入手术室后常规监测心电图(ECG)、动脉血氧饱和度(SpO2)、无创血压(BP)、呼气末二氧化碳分压(PETCO2)、脑电意识指数(IOC1)和伤害敏感指数(IOC2)。开放静脉通路,局部麻醉下进行桡动脉穿刺置管行有创动脉压监测。麻醉诱导和维持时,OFA 组给予酮铬酸氨丁三醇0.5mg/kg, 利多卡因1.5mg/kg、之后以2mg/(kg.h)经静持续脉泵注,丙泊酚1-2mg/kg、之后以2-4mg/(kg.h) 持续泵注,咪达唑仑 0.05mg/kg,顺式阿曲库铵0.15mg/kg,七氟烷1%-4%。OA 组给予舒芬太尼0.4ug/kg,与OFA 组利多卡因等剂量计算的生理盐水,丙泊酚1-2mg/kg、之后以2-4mg/(kg.h)持续泵注,咪达唑仑0.05mg/kg,顺式阿曲库铵0.15mg/kg,七氟烷1%-4%,术中必要时给予舒芬太尼0.1ug/kg。麻醉诱导3min 后置入喉罩,机械通气参数设定:呼吸频率12-16 次/min,潮气量6-8mL/kg,以维持呼气末二氧化碳分压35-45mmHg。术中密切关注患者生命体征,维持血流动力学稳定,维持IOC1 和IOC2值30-45。两组患者血压升高幅度超过 30%给予乌拉地尔10 mg 缓慢静注;血压降低幅度超过 30%给予麻黄碱6 mg; 心率低于 45 次/min 给予阿托品0.5 mg 以维持生命体征稳定。两组患者均于胆囊切下时停用七氟烷,手术结束前三分钟停用静脉麻醉药。关腹前0.5%盐酸罗哌卡因10mL行切口浸润麻醉。
表1 两组患者一般资料比较(±s)
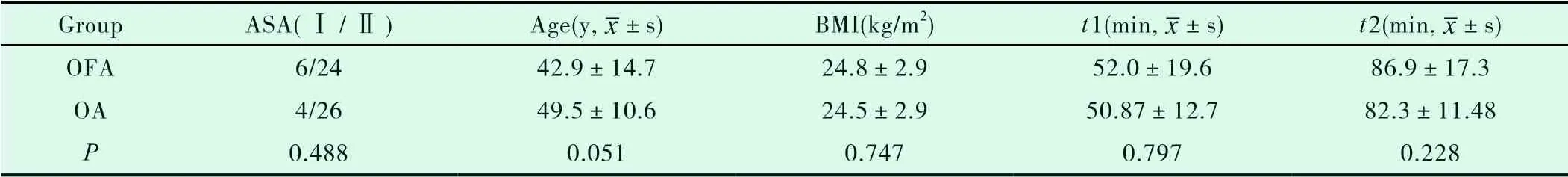
表1 两组患者一般资料比较(±s)
注:Note:t1= 手术时间;t2=麻醉时间。
Group ASA(Ⅰ/Ⅱ) Age(y,images/BZ_11_438_3177_466_3216.png±s) BMI(kg/m2) t1(min,images/BZ_11_438_3177_466_3216.png±s) t2(min,images/BZ_11_438_3177_466_3216.png±s)OFA 6/24 42.9±14.7 24.8±2.9 52.0±19.6 86.9±17.3 OA 4/26 49.5±10.6 24.5±2.9 50.87±12.7 82.3±11.48 P 0.488 0.051 0.747 0.797 0.228
表2 两组患者不同时刻MAP、HR(±s)

表2 两组患者不同时刻MAP、HR(±s)
Group T0 T1 T2 T3 T4 MAP OFA 93.7±9.9 96.4±9.1 94.2±9.2 96.5±9.8 91.2±9.2 OA 93.2±10.0 96.4±10.1 93.3±10.0 96.6±9.8 91.1±9.7 HR OFA 75.5±6.7 78.7±6.5 76.3±5.6 79.4±6.0 70.8±5.9 OA 72.4±6.1 77.9±7.1 73.7±5.3 76.8±5.4 67.8±5.7
1.4 观察指标
入室时(T0)、插管时(T1)、建立气腹时(T2)、建立气腹后1min(T3)、拔管时(T4)的平均动脉压(MAP)、心率(HR)、IOC1、IOC2;拔管时间(停药至拔除喉罩的时间);肠鸣音恢复至正常的时间,第一次排气时间,术后胃肠不适发生率(恶心、呕吐、腹胀、排尿困难等)。
1.5 统计学方法
采用 SPSS 23.0 软件进行数据处理,正态分布的计量资料以 (±s)表示,两组间比较采用t检验,组内比较采用单因素方差分析;不符合正态分布的计量资料用中位数(四分位数间距)[M(Q)]来表示,两组间比较采用Mann-Whitney U 检验。计数资料采用[n(%)]表示,比较用χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 不同时刻两组患者的MAP 和HR 比较
在IOC1 和IOC2 在30-45 范围波动且数值相近时,两组各时刻HR、MAP 相比差异无统计学意义,见表2。
2.2 两组患者拔管时间及术后VAS 评分比较
两组患者停药至拔管时间比较,OA 组较短,差异有统计学意义;术后两组患者VAS 评分比较差异无统计学意义。
2.3 两组患者胃肠功能恢复时间比较
与OA 组比较,OFA 组肠鸣音恢复时间和第一次排气时间较短,差异有统计学意义,见表3。
2.4 两组患者不良反应发生率及肠功能恢复情况比较
OA 组出现恶心/呕吐6 人、腹胀4 人、排尿困难2 人;OFA组出现腹胀3 人,恶心/呕吐2 人。OFA 组不良反应发生率低于OA 组,差异有统计学意义。
表3 两组患者肠鸣音恢复及肛门首次排气时间(±s)
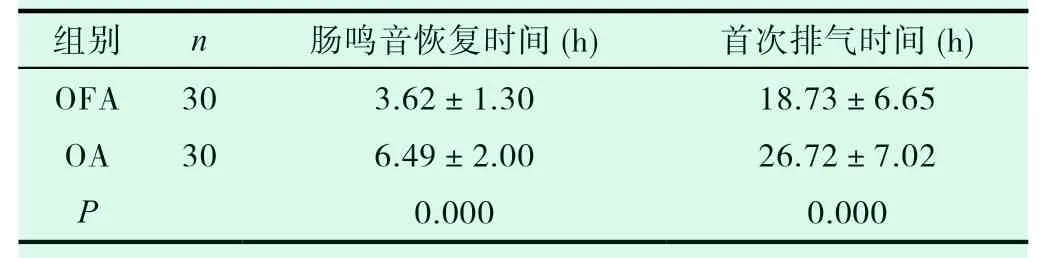
表3 两组患者肠鸣音恢复及肛门首次排气时间(±s)
组别 n 肠鸣音恢复时间(h) 首次排气时间(h)OFA 30 3.62±1.30 18.73±6.65 OA 30 6.49±2.00 26.72±7.02 P 0.000 0.000
3 讨论
术后肠功能障碍或胃肠蠕动不良在各种手术后均可出现,与以下因素有关:炎性递质释放、肠壁内炎症细胞浸润、交感神经兴奋性高、胃肠激素、麻醉药和阿片类药物。阿片类药物作用于肠神经系统,与肌间神经丛和粘膜下神经丛结合,导致肠道运动障碍,液体分泌减少和括约肌功能障碍,从而导致OIBD[1]。
ERAS 的中心原则之一是应用多模式疼痛干预以减少对阿片类药物的依赖。近年来,在多模式镇痛发展的基础上逐渐提出了无阿片类药物麻醉(OFA)和镇痛。OFA 是非阿片类药物和或技术结合的多模式麻醉,可以结合NMDA 拮抗剂(氯胺酮、硫酸镁、利多卡因)、钠通道阻滞剂(局部麻醉剂(LA))、抗炎药(NSAID、地塞米松、LA)和α-2 激动剂(右美托咪定、可乐定)等[2,3]。从而减少患者对阿片类药物的暴露,减少对阿片类药物的成瘾性和依赖性,降低术后即刻出现的镇静、呼吸抑制、肠功能障碍等不良反应。
超前镇痛是通过阻止外周损伤冲动向中枢传递及传导而建立的一种镇痛治疗方法,是防止或减轻术后疼痛而进行的术前镇痛干预,其本质是减少伤害刺激引起的中枢及外周敏化[4]。术前应用非甾体抗炎是临床上常用的超前镇痛的方式之一。酮咯酸氨丁三醇是一种异丁芬酸类非甾体抗炎药,通过抑制环氧化酶( COX) 而干扰花生四烯酸的代谢途径,从而减少前列腺素的合成,发挥镇痛、解热和抗炎作用[5]。
利多卡因是一种酰胺类局麻药,通过阻滞钠离子通道,可以抑制神经元的兴奋性和神经纤维的电活动,从而在外周和中枢发挥镇痛效果。同时利多卡因还通过阻断或抑制神经传导,降低术后疼痛的神经反应,抑制中枢和外周的疼痛敏化。此外,研究报道,利多卡因能够促进肠道功能的快速恢复[6-8]。
本试验观察发现当IOC1 和IOC2 在30-45 范围波动且同一时刻二者数值相近时,可满足术中麻醉效果。脑电意识指数(IOC1)和伤害敏感指数(IOC2)是评估全麻患者意识和伤害性刺激程度的两个参数[9,10]。IOC1 范围是0~100,0 表示无脑电活动(爆发抑制),100 表示清醒状态。IOC2 数值的量化区间也在0~100 之间的范围内,0 为机体对伤害性刺激无反应,100 为无镇痛条件下的疼痛感知。IOC1 与IOC2 联动可精确监测全麻患者的意识深度和伤害刺激敏感程度,有学者通过观察发现IOC1 位于40-60,IOC2 位于30-50 是合适的全身麻醉状态正常值[11]。
本试验中肠鸣音恢复时间及第一次排气时间均指距离麻醉结束时刻的时间。肠鸣音和肛门排气常作为临床上肠蠕动恢复的标志。肠鸣音是由于肠蠕动时肠管内气体和液体随之流动产生的断断续续的咕噜声(或气过水声),正常情况下大约每分钟4-5 次。肠鸣音听诊部位为患者左上腹、左下腹、右上腹、右下腹 及脐周5 个区,听诊时每个区域听诊2 min[12]。若听到两个及两个以上区域肠鸣音正常,则认为肠鸣音恢复正常。
本试验结果得出,两组患者血流动力学无明显差异,相关研究[13]也表明无阿片类药物麻醉能够安全有效地用于术中的麻醉与镇痛,与本结果一致。两组患者术后VAS 评分无明显差异,与Toleska M 等人研究结果不同,可能是本试验样本数量较少,术后未观察记录多个时间点的VAS 评分所造成[14]。两组患者从停药至拔出喉罩的时间(拔管时间)相比,OFA 组拔管时间较长,差异有统计学意义。与OA 组比较,OFA 组患者肠鸣音恢复时间和第一次排气时间较短,差异有统计学意义;OFA组不良反应发生率较低,差异有统计学意义。OFA 组以多模式镇痛麻醉方案代替传统有阿片类药物的麻醉方法,最大程度地减少了围术期阿片类药物使用,从而减轻了阿片类药物导致的不良反应。一项前瞻性随机对照试验观察发现妇科腹腔镜手术采用无阿片类药物全凭静脉麻醉,术后患者不良反应发生率较低,术后恢复质量显著改善[15],本实验结果与之相符。
综上所述,无阿片药物麻醉在腹腔镜胆囊切除术的应用是安全可行的,而且术中血流动力学平稳,术后肠功能恢复较快,不良反应发生率低。但是多模式镇痛中“尽量减少阿片药物的使用”并不是绝对不应用阿片类药物,最好的麻醉技术联合用法,最佳的镇痛药物复合用法及用量还需要进一步探索。
