腹腔镜尾侧入路联合中间翻页式清扫右半结肠癌根治术的临床疗效
2021-03-26何国锐张金刚朱宣进黄勇
何国锐,张金刚,朱宣进,黄勇,
(1.贵州医科大学,贵阳 550004;2.广州市红十字会医院普外科,广州 510220)
结肠癌是胃肠道常见的恶性肿瘤,近年来其发病率呈上升趋势[1]。其中,右半结肠癌是指发生于结肠右侧段的恶性肿瘤,以腹部肿块、全身症状、贫血等为主要表现,早期可无明显症状,可通过增强CT、结肠镜等检查明确诊断。在目前的临床实践中,很大一部分结肠癌患者一经确诊即为中晚期,已错过最佳治疗和手术时机,故早期诊断、早期治疗至关重要。根治性手术是治疗结肠癌的重要手段,既往常采用开腹手术,不仅创伤大,而且术后恢复慢。随着手术器械的发展以及微创理念的提出,结肠癌手术逐步进入微创时代。自Jacobs等[2]于1991年首先报道了腹腔镜右半结肠切除术以来,越来越多的报道相继证实了腹腔镜手术在右半结肠癌治疗中的显著优势[3-4]。与左半结肠相比,右半结肠解剖层次更复杂,血管变异也更大,淋巴结清扫难度大[5-6]。术中准确进入解剖平面,有效结扎根部血管以及彻底清扫淋巴结从而实现完整结肠系膜切除是手术的关键。故右半结肠癌手术对入路的选择更为慎重。目前,国内学者不断进行手术入路的改良,以探索更安全、高效的手术入路。为进一步优化入路方式,提高手术疗效,本研究主要探讨尾侧入路联合中间翻页式清扫在右半结肠癌根治术中的可行性与临床疗效,现报道如下。
1 资料与方法
1.1一般资料 收集2016年1月至2019年12月广州市红十字会医院普外科收治的120例行腹腔镜右半结肠癌根治术的病例资料进行回顾性分析。按手术入路不同分为研究组(尾侧入路联合中间翻页式清扫)和对照组(传统中间入路),各60例。纳入标准:①术前肠镜证实为单一病灶,病理活检确诊为结肠癌,肿瘤位于横结肠近肝曲、结肠肝曲、升结肠、盲肠;②美国麻醉医师协会(American Society of Anesthesiologists,ASA)术前分级为Ⅰ~Ⅲ级;③体质指数(body mass index,BMI)≤30 kg/m2;④卡氏功能状态评分≥80分。排除标准:①急诊手术(如肠梗阻、穿孔);②肿瘤最大直径>6 cm和(或)周围组织广泛浸润;③基础状况差,不能耐受腹腔镜手术;④资料不完整;⑤术前发现远处转移。本研究经广州市红十字会医院医学伦理委员会批准,患者家属均签署了手术知情同意书。
1.2手术方法 所有手术均由广州市红十字会医院同一组高年资主任医师主刀完成。两组患者均行D3根治。手术均采用气管插管全身麻醉,仰卧分腿位,观察孔位于脐下约5 cm,直径1.0 cm;术者位于患者左侧,主操作孔位于左侧锁骨中线肋缘下5 cm,直径1.2 cm;副操作孔位于左侧反麦氏点,直径0.5 cm;助手位于患者右侧,扶镜手位于两腿之间,助手操作孔位于右侧腹部,与术者操作孔位置对称,直径均为0.5 cm。建立气腹,压力维持在13~15 mmHg(1 mmHg=0.133 kPa)。从观察孔置入3D腹腔镜,常规探查腹腔,确定肿瘤部位及切除范围。
1.2.1研究组 ①尾侧入路游离层面:患者取头低脚高位,左侧倾斜15°~20°,将小肠推向左上腹。回盲部向上提起,以右侧肠系膜根部与后腹膜相融合成的“黄白交界线”(Toldt′s线)为手术切入点(图1a),切开进入右结肠后间隙(Toldt′s间隙),向内、外及头侧拓展Toldt′s间隙,右侧至右结肠旁沟腹膜反折,左侧至肠系膜上静脉左侧,上至十二指肠水平部上方[7-8]。内侧紧贴十二指肠,沿胰腺前筋膜层向头侧进入胰头及钩突前方(图1b),十二指肠外侧沿Toldt′s间隙分离至结肠肝曲,完成背侧面游离(1c),在十二指肠前方放置腔镜纱作为指引。②中间翻页式清扫:翻转右侧肠系膜,视野转至肠系膜腹侧面。在回结肠血管下方系膜自然皱褶处切开肠系膜前叶,与尾背侧游离的Toldt′s间隙贯通(1d)。沿肠系膜上静脉向上裸化游离,离断回结肠动、静脉清扫No.203淋巴结(1e);助手牵拉游离的右侧肠系膜,继续向上翻页式清扫游离,同时离断右结肠动、静脉,清扫No.213淋巴结;离断结肠中动、静脉(右支),清扫No.223淋巴结(1f)。向上裸化胃结肠静脉干(Henle干)及其分支。与后方的胰十二指肠前间隙贯通。③横结肠上区游离:沿胃网膜右血管弓外(扩大右半结肠切除时沿弓内切除)打开胃结肠韧带,分离右侧横结肠后间隙,与已游离的Toldt′s间隙贯通。离断肝结肠韧带,完成右半结肠及系膜游离。腹部切口完成肠管切除与重建。
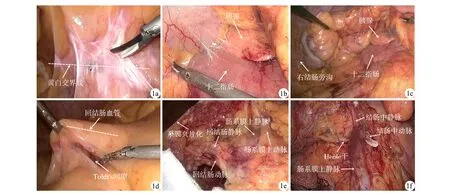
1a:尾侧入路起始标志部位;1b:游离胰、十二指肠前间隙;1c:经尾侧入路背侧面游离完成;1d:中间翻页式清扫起始标志部位;1e:离断回结肠动、静脉,清扫No.203淋巴结;1f:离断结肠中动、静脉,清扫No.223淋巴结
1.2.2对照组 在回结肠血管下方切开进入Toldt′s间隙,自回结肠动脉根部向头侧游离,同时裸化并离断右半结肠相关血管,清扫血管根部淋巴结。沿Toldt′s间隙向外侧扩展,到达外侧Toldt′s线,再向头、尾两侧扩展分别到达结肠肝曲和盲肠。沿盲肠外侧的Toldt′s线向头侧切开腹膜至肝曲,使末段回肠、盲肠和升结肠完全游离。切开大网膜和胃结肠韧带,离断肝结肠韧带。完成D3淋巴结清扫及右半结肠完全游离。肠管切除与吻合同研究组。
1.3观察指标 ①比较两组患者一般资料,包括性别、年龄、肿瘤部位、ASA分级、术前TNM分期、BMI。②比较两组患者术中情况,包括手术时间、术中出血量、血管损伤、中转开腹率。③根据患者手术标本病理报告,提取肿瘤直径、淋巴结总数、阳性淋巴结数、分化程度、病理类型等数据;手术标本质量采用West分级[9],A级(固有肌层层面):肠系膜缺损达肠壁固有肌层;B级(结肠系膜内层面):不规则切除了部分结肠系膜,但未达固有肌层;C级(结肠系膜层面):结肠系膜完整光滑切除。④记录并比较两组患者术后恢复情况(包括术后排气时间、术后住院时间)以及并发症发生率。⑤术后随访3~24个月,观察两组患者的复发和死亡情况。
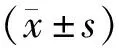
2 结 果
2.1两组患者一般资料比较 两组患者性别、年龄、肿瘤部位、ASA分级、术前TNM分期、BMI比较差异均无统计学意义(P>0.05),见表1。
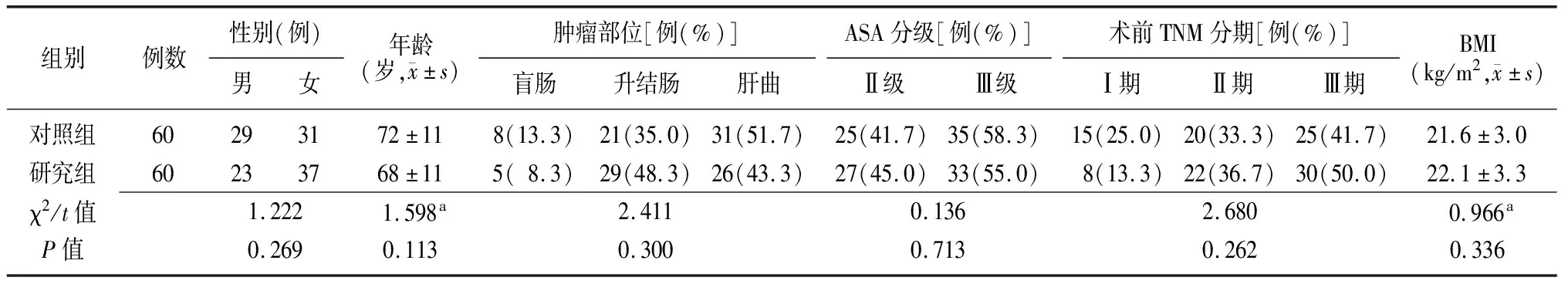
表1 两组右半结肠癌患者一般资料比较
2.2两组患者术中情况比较 研究组的手术时间、术中出血量均少于对照组(P<0.05),两组术中血管损伤及中转开腹率比较差异均无统计学意义(P>0.05),见表2。
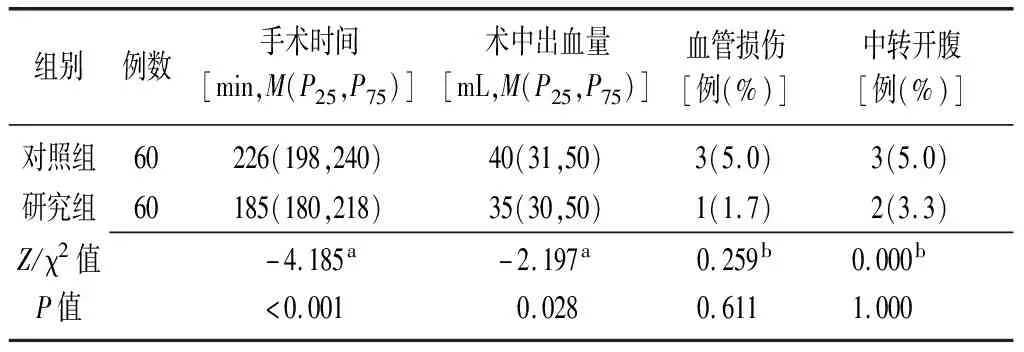
表2 两组右半结肠癌患者术中情况比较
2.3两组患者术后病理情况比较 两组患者肿瘤直径、淋巴结总数、阳性淋巴结数、肿瘤分化程度及病理类型比较差异均无统计学意义(P>0.05),见表3。研究组手术切面B级1例,C级59例;对照组B级3例、C级57例,两组不同分级比较差异无统计学意义(χ2=0.259,P=0.611)。

表3 两组右半结肠癌患者术后病理情况比较
2.4两组患者术后恢复情况及并发症发生情况比较 两组患者术后排气时间、住院时间比较差异均无统计学意义(P>0.05);研究组发生术口感染2例,肠梗阻、吻合口狭窄、吻合口瘘各1例,心血管并发症2例,对照组术口感染4例、吻合口瘘2例、肠梗阻和吻合口狭窄各1例,心血管并发症1例,肺部感染2例。两组患者总并发症发生率比较差异无统计学意义(P>0.05),见表4。所有并发症患者经保守治疗后好转出院,无30 d内死亡病例。
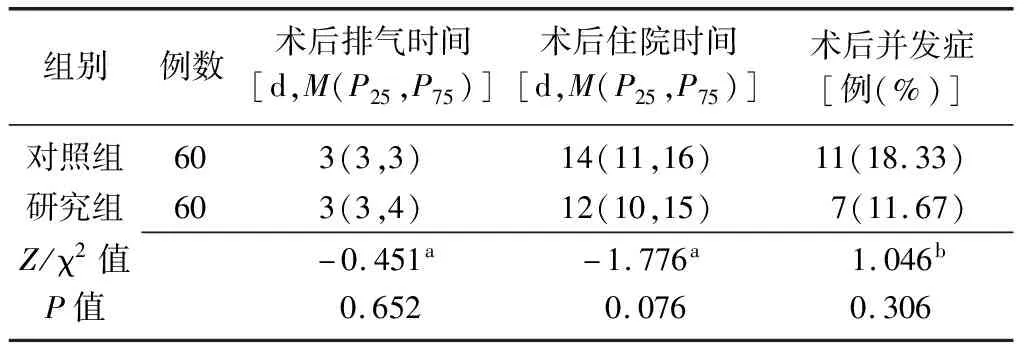
表4 两组右半结肠癌患者术后恢复情况及并发症发生情况比较
2.5随访结果 术后通过门诊、返院复查等形式随访,根据术后病理情况规范化疗。研究组60例患者随访3~24个月,中位随访15个月,失访11例,复发4例,死亡3例(2例出现肺部转移,1例肝转移,后因多器官功能衰竭死亡),肝转移1例(随访结束时仍存活);总生存率为95.00%(57/60),无瘤生存率为93.33%(56/60)。对照组随访5~24个月,中位随访18个月,失访9例,复发7例,死亡5例(3例出现肝转移,后因多器官功能衰竭死亡;2例肺部转移,后因呼吸衰竭死亡),肺转移2例(随访结束时仍存活);总生存率为91.67%(55/60),累积无瘤生存率为88.33%(53/60)。两组总生存率和无瘤生存率比较差异无统计学意义(χ2=0.068,P=0.794;χ2=0.298,P=0.585)。见图2、3。
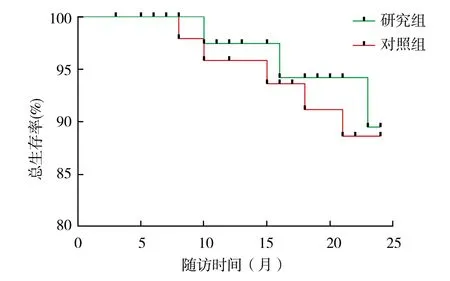
图2 两组右半结肠癌患者总生存曲线比较
3 讨 论
腹腔镜技术经过数十年的发展,已经广泛应用于结直肠癌的治疗。目前,国内外对于右半结肠癌均以腹腔镜手术治疗为主,但对于手术入路的选择仍存在争议[10-11]。在胚胎发育过程中,前肠和中肠的旋转和演变造成了右半结肠复杂的解剖层面[12]。而且右半结肠血管变异大,尤其是Henle干及其属支的解剖变异较大[13-15]。术中如何准确进入正确的解剖层面,有效处理血管是手术的难点,目前仍未形成统一、规范的入路方式。
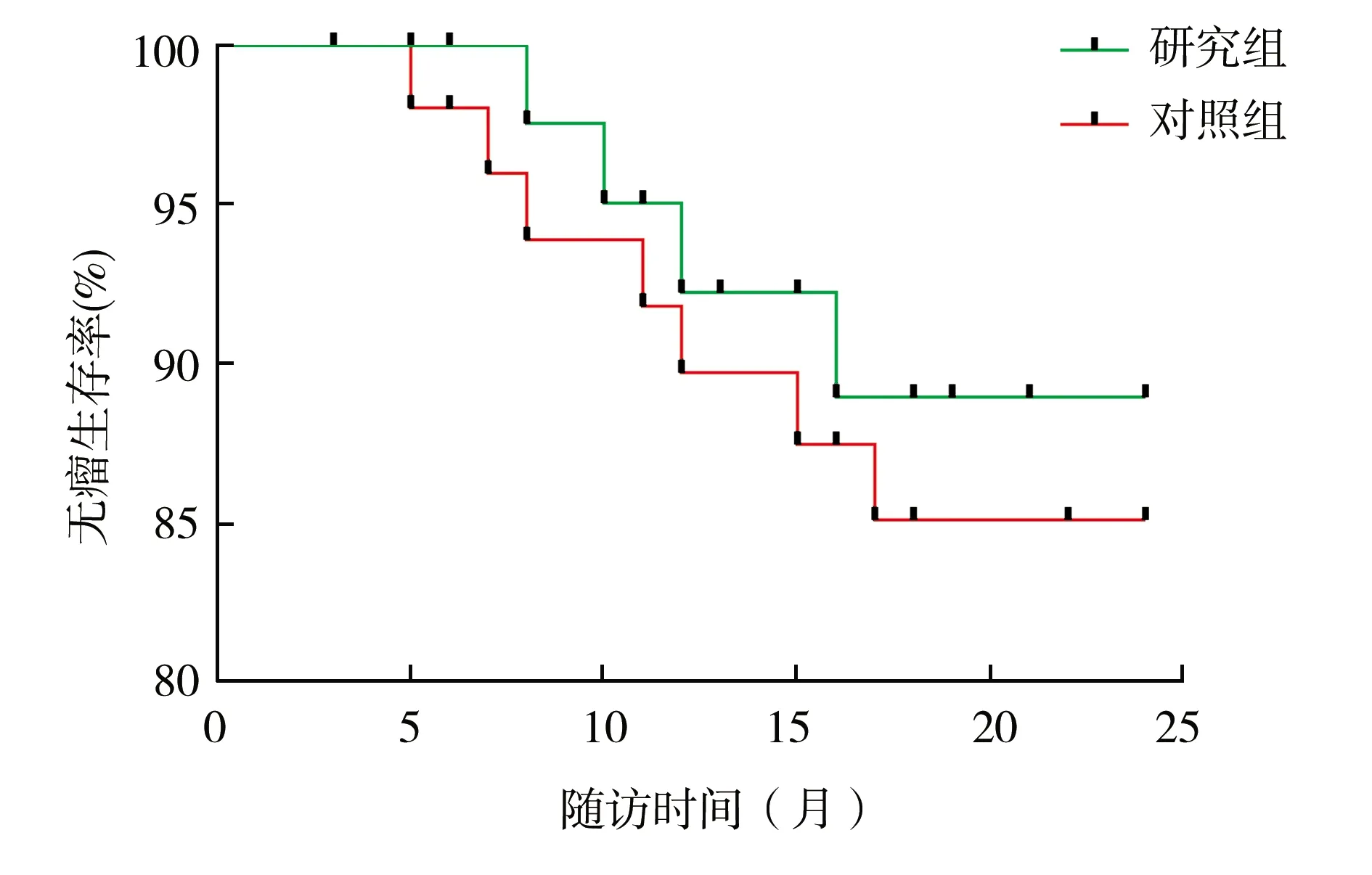
图3 两组右半结肠癌患者无瘤生存曲线比较
从手术入路分析,腹腔镜右半结肠癌手术主要有中间入路、侧方入路、尾侧入路以及各种改良入路等。合适的手术入路不仅有助于寻找正确的解剖层面,避免血管损伤,也有利于提高手术效果[16]。总之,不同入路方式具有各自的优势和不足。在腹腔镜手术开展初期,学者大多沿用开腹手术常用的侧方入路,虽然操作简单,但不符合肿瘤无接触原则,基本已被淘汰[17]。传统中间入路是目前较常用的入路方式,该入路强调优先处理血管,更符合无瘤原则。但中间入路在进入Toldt′s间隙时,往往难以把握深度,混淆层面,特别是肥胖患者,故不利于初学者掌握[18-19]。邹瞭南等[8]提出以回盲部“黄白交界线”为切入点的尾侧入路,该入路被认为在层面的寻找与维持上具有较大优势,更易于学习和掌握。本研究采用尾侧入路联合中间翻页式清扫,有效结合了尾侧入路与中间入路的优势,亦取得令人满意的效果。
本研究结果显示,研究组手术时间短于对照组(P<0.01),通过观察手术过程发现,采用尾侧入路沿解剖位置固定的“黄白交界线”切开直接进入Toldt′s间隙后可充分拓展层面,再沿中间肠系膜血管前方自尾侧向头侧翻页式清扫游离,手术操作更加流畅。首先,经尾侧入路更容易直接进入Toldt′s间隙,避免中间入路寻找Toldt′s间隙而延长手术时间。其次,先拓展Toldt′s间隙,可实现系膜的“页片化”[20],此时再以肠系膜上静脉为主线,采取中间翻页式清扫,因血管后方空虚且肠系膜松弛,从而使后续血管的裸化结扎及淋巴结清扫更快捷[21]。此外,手术过程中主刀医师不必改变站位,操作相对简单流畅[22],便于助手的辅助操作。
尾侧入路遵循“层面优先,精细解剖”的原则,强调先拓展Toldt′s间隙,提供一个天然无血管层面[23],通过助手的牵引,在清晰的视野下进行分离,后方可避免腹膜后脏器的损伤,前方显露肠系膜上动静脉及其属支的分布,尤其是Henle干的变异情况,从而避免了传统中间入路在拓展Toldt′s间隙时带来的副损伤,以及对血管变异的误判,降低出血的风险。本研究结果显示,研究组术中出血量少于对照组(P<0.05),原因可能是尾侧入路更有利于控制出血,即使出血,因血管显露彻底也可更及时准确的止血[24],在一定程度上也有助于降低并发症发生率。本研究中,两组患者中转开腹率、术后排气时间、住院时间及总并发症发生率比较差异均无统计学意义(P>0.05),提示两种入路方式对患者术后恢复的影响差异性不大,与余志清和杜江[25]的研究结果相似。说明尾侧入路手术效果同样安全可靠。
淋巴结清扫是否彻底是影响结肠癌预后的重要因素[26]。本研究手术标本的病理学结果显示,两组患者淋巴结清扫总数、阳性淋巴结数目、手术切面分级比较差异均无统计学意义(P>0.05)。说明尾侧入路联合中间翻页式清扫与传统中间入路的根治效果相当,但回顾手术录像发现,由尾侧入路先解剖右结肠后间隙及胰十二指肠前间隙,为随后的翻页式清扫识别血管做铺垫,可降低血管根部淋巴结清扫难度[27],通过“双面夹击”以及横结肠后间隙与右结肠后间隙上下贯通可有效确保完整肠系膜切除[15],避免淋巴组织残留,故淋巴结清扫更高效彻底。国外有研究认为,总生存率的多变量预测因素包括年龄、淋巴结清扫数量、分期和辅助化疗等[28]。本研究中,两组患者术后均根据病理情况按需行规范化疗,两组患者总生存率和无瘤生存率比较差异无统计学意义(P>0.05),提示两种入路方式的预后效果相当。
综上所述,尾侧入路联合中间翻页式清扫应用于腹腔镜右半结肠癌根治术可获得满意的疗效。与传统中间入路相比,尾侧入路联合中间翻页式清扫在手术时间、术中出血量上更具优势,且手术难度相对较低。因此,这种入路方式安全可行,更容易被初学者掌握。
