艾塞那肽周制剂联合二甲双胍对2型糖尿病病人血糖变异及慢性低度炎症的影响
2021-03-24韩敏敏刘子昂刘云峰
李 阳,李 静,贺 琼,韩敏敏,苏 敬,刘子昂,章 毅,刘云峰
血糖变异(glycemic variability,GV)是体内葡萄糖水平波动的不稳定状态。已有研究提出,GV与糖尿病慢性并发症,特别是心脑血管等大血管并发症密切相关[1],GV导致血糖不稳定,低血糖风险增加,而低血糖是心脑血管事件发生的独立危险因素[2],也是血糖控制达标的难点。糖尿病发病机制复杂,多项研究认为其是一种慢性低度炎症状态[3-4],炎性因子参与糖尿病进程,且与胰岛素抵抗及多种并发症密切相关。糖尿病并发症致死率、致残率高,严重影响病人生活质量,因此加强血糖控制、延缓并发症在糖尿病管理中占重要地位。艾塞那肽周制剂是一种长效的胰高血糖素样肽-1(GLP-1)受体激动剂,其独特的微球缓释技术可缓慢释放有效成分,显著降低给药频率,提高病人依从性。本研究观察艾塞那肽周制剂联合二甲双胍对2型糖尿病病人体内代谢异常、血糖变异、低血糖风险、慢性低度炎症的影响。
1 资料与方法
1.1 一般资料 选取2018年6月—2019年1月山西医科大学第一医院内分泌科门诊及住院部收治的2型糖尿病病人22例为研究对象,其中男16例,女6例;年龄(49.0±10.3)岁;病程(5.6±2.7)年。本研究已获得山西医科大学第一医院伦理委员会批准,所有病人均签署知情同意书。
1.1.1 纳入标准 诊断2型糖尿病(根据WHO 1999年2型糖尿病诊断标准)2~10年,年龄18~70岁;糖化血红蛋白(HbA1c)7.0%~11.0%;至少接受过3个月二甲双胍单药治疗(每日剂量≥1 500 mg),但血糖控制不理想;估测肾小球滤过率>60 mL/(min·1.73 m2)。
1.1.2 排除标准 根据艾塞那肽周制剂说明书有禁忌证,或对其他任何辅料有过敏史;筛选前1年内连续使用7 d以上胰岛素治疗(因急性疾病或手术除外);急性或慢性胰腺炎病史;家族性甲状腺癌病史;依从性不佳或存在精神障碍、不愿与人交流或存在语言障碍等无法配合研究的病人。
1.2 研究方法 用药前由专业医疗人员对病人进行统一的糖尿病教育和注射技术的培训,指导药品正确使用。导入期2周内保持二甲双胍剂量不变,同时佩戴快速扫描式葡萄糖监测系统(FGMS,辅理善瞬感,英国Abbott Diabetes Care Ltd公司生产,批准文号:国械注进20163212472),导入期结束后在原有二甲双胍基础上加用艾塞那肽周制剂(Bydureon,美国Amylin Ohio LLC公司生产,批准文号H20170389,规格:每支2 mg),每周于固定时间皮下注射2 mg,联合用药3个月,研究结束前两周再次佩戴FGMS。
1.3 观察指标
1.3.1 代谢指标 收集病人临床资料,分别在治疗前和治疗3个月后测量静脉血空腹血糖(FPG)、餐后2 h血糖(2 hPBG)、胰岛素抵抗指数(HOMA-IR)、血脂等代谢指标,计算用药前后HOMA-IR=FPG×空腹胰岛素(FINS)/22.5。
1.3.2 FGMS记录相关资料 导出并记录病人两次佩戴FGMS动态血糖图谱(AGP),比较平均血糖(MBG)、目标血糖范围内(3.9~8.0 mmol/L)时间(time in range,TIR)和百分比、低血糖事件发生率、低血糖持续时间等。
1.3.3 慢性低度炎症指标 治疗前后于晨起空腹状态下采集静脉血5 mL,以2 000 r/min离心20 min后取血清,保存于-40 ℃条件中,采用酶联免疫吸附法(ELISA)测量血清肿瘤坏死因子-α(TNF-α)、转化生长因子β1(TGF-β1)、鞘氨醇-1-磷酸(S1P)水平。
1.4 统计学处理 采用SPSS 21.0统计软件进行数据处理。对计量资料进行正态性及方差齐性检验,符合正态分布的计量资料以均数±标准差(x±s)表示,不符合正态分布的计量资料以中位数和四分位数表示,符合正态性及方差齐性的计量资料采用配对t检验,不符合正态性的计量资料采用秩和检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组体重、血糖、血脂代谢指标比较 用药3个月后,病人体重、HbA1c、FPG、2 hPBG、HOMA-IR、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)较治疗前降低,治疗前后比较差异有统计学意义(P<0.05或P<0.01)。详见表1。
2.2 FGMS记录相关数据比较 与首次佩戴FGMS比较,联合用药3个月后第2次佩戴FGMS期间病人MBG、高于目标血糖范围(>8.0 mmol/L)百分比下降(P<0.01),目标血糖范围内(3.9~8.0 mmol/L)百分比、TIR增高(P<0.05),血糖控制总体较用药前好转。FGMS佩戴期间低血糖事件、低血糖持续时间、低于目标血糖范围(<3.9 mmol/L)百分比未明显增加(P>0.05)。详见表2和图1。
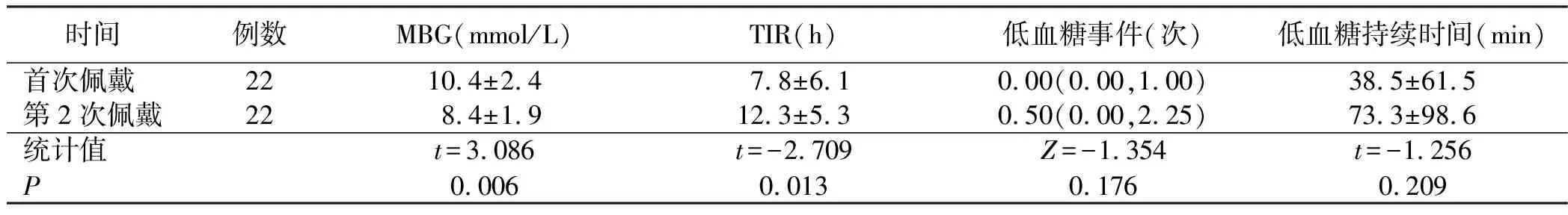
表2 两次佩戴FGMS检测结果比较
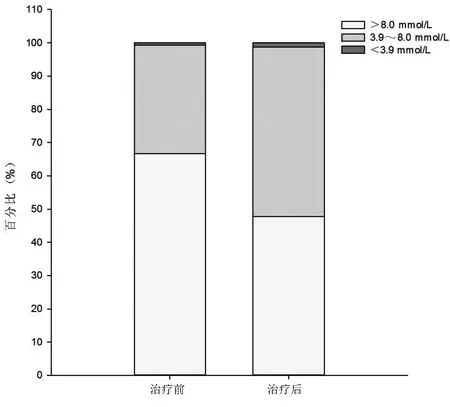
图1 治疗前后不同血糖浓度时间百分比
2.3 慢性低度炎症相关指标 与治疗前比较,病人炎性因子TNF-α及TGF-β1浓度下降,S1P浓度较治疗前升高,差异均有统计学意义(P<0.01)。详见图2。
3 讨 论
2型糖尿病是一种慢性进展性疾病,虽然近年来医疗技术飞速进步,但2型糖尿病患病率持续升高。自然病程中,除体内血糖水平进行性升高外,各类糖尿病慢性并发症的发生、进展严重危害病人生活质量和生命安全,给国家、社会、家庭带来沉重负担。因此,控制血糖、延缓并发症对糖尿病管理尤为重要。
随着胰岛素抵抗加重、胰岛β细胞分泌胰岛素能力减弱,使其对外源性血糖控制手段依赖逐渐加大。GLP-1受体激动剂因其良好的降糖、减重效果,并具有保护大血管、小血管作用备受关注,其促胰岛素分泌作用依赖体内葡萄糖浓度,并直接抑制α细胞分泌胰高血糖素,可作用于下丘脑、垂体等饱食神经元,发挥增加饱腹感、抑制食欲、延缓胃排空作用[5],帮助病人降低血糖、血脂、减轻体重。GLP-1受体激动剂的心脏获益已被学者证实[6],但具体机制尚未明确,可能通过直接抗炎、改善内皮细胞功能、减少血小板聚集或降糖、减重、调脂等间接作用保护心血管[7]。艾塞那肽周制剂是一种超长效的GLP-1受体激动剂,每周仅需皮下注射1次,可有效降低给药频率,极大提高治疗便捷性。
本研究结果显示,艾塞那肽周制剂联合二甲双胍治疗3个月后,病人HbA1c、FPG及2 hPBG、HOMA-IR均较治疗前下降,治疗前后比较差异均有统计学意义(P<0.05),表明艾塞那肽周制剂不仅可降低血糖,可能有助于胰岛β细胞修复和再生,减少外周组织对胰岛素的抵抗,与Kim等[8]和Bunck等[9]研究一致。DURATION其中一项与安慰剂研究中,使用24周艾塞那肽周制剂可降低HbA1c 0.73%,2 hPBG、体重等有不同程度减轻[10],其降糖作用除与艾塞那肽作用于体内活化的GLP-1受体外,还可能与减少注射次数、提高病人依从性有关。加用艾塞那肽周制剂治疗后,病人体重、TC、LDL-C水平降低(P<0.05),但TG、HDL-C改善不明显(P>0.05),与既往研究[11]一致。2型糖尿病病人降低体重、改善血脂作用可能通过中枢和外周通路,增加下丘脑饱食信号,抑制饥饿信号,从而抑制食欲、减少热量摄入、降低体重、间接改善血脂水平。
HbA1c是反映长期血糖平均水平的生化指标,而自我血糖监测是目前血糖监测的基本形式,但二者存在局限性,反映细微快速的血糖改变、血糖波动等方面不足。FGMS可动态监测10~14 d血糖,全面反映1 d内血糖变化情况,并可自动生成动态血糖图谱,包括MBG、目标血糖范围百分比、低血糖事件等。TIR作为直观、简单反映血糖控制的指标,受到众多学者重视。一项采用动态血糖监测技术分析TIR与糖尿病视网膜病变的相关性研究显示,糖尿病视网膜病变严重程度与TIR四分位数呈负相关,这是TIR应用于临床且与糖尿病并发症相关的证据之一[12]。临床证据显示,TIR除与糖尿病微血管并发症相关外,还与大血管疾病之间存在联系,TIR每增加10%,颈动脉内膜中层厚度(CIMT)异常风险降低6.4%[13]。本研究结果显示,目标血糖范围内(3.9~8.0 mmol/L)百分比在第2次佩戴期间升高,MBG、高于目标血糖范围(>8.0 mmol/L)百分比下降(P<0.05),且低血糖事件、低血糖持续时间未增加,表明二甲双胍联合艾塞那肽周制剂有助于较好地控制血糖,减少GV,且未增加低血糖风险。艾塞那肽周制剂降低GV,未增加低血糖风险的可能机制是其有效成分通过微球技术缓慢释放并达到稳态艾塞那肽浓度;每周注射1次,显著减少用药频率,提高病人依从性;具有葡萄糖浓度依赖性促进胰岛素分泌,单独使用未增加低血糖风险。糖尿病发病及进展过程中多种炎性因子表达增加,机体处于微炎症状态。炎性因子参与胰岛素抵抗、胰岛β细胞结构与功能障碍[14],导致机体血糖代谢紊乱,加速动脉粥样硬化、肾脏、视网膜损害等大血管及微血管并发症。因此,缓解机体炎症状态,降低炎性因子水平可能有助于延缓糖尿病进程。既往研究发现,GLP-1受体激动剂通过抑制巨噬细胞核转录因子-κB途径和炎性因子分泌,改善胰岛素抵抗[15]。
本研究同时观察加用艾塞那肽周制剂后血清TNF-α、TGF-β1和S1P变化,结果表明用药3个月后,血清TNF-α、TGF-β1表达较治疗前下降(P<0.01),S1P浓度较治疗前升高(P<0.01),说明艾塞那肽周制剂有助于改善糖尿病慢性低度炎症状态。脂肪细胞除了储存能量,同时具有内分泌功能,可分泌多种炎性因子,有研究发现,肥胖人群脂肪组织血清炎性因子较非肥胖人群高表达[16],因此推测艾塞那肽周制剂改善炎症状态可能与病人用药后体重减轻,内脏脂肪重新分布有关。TNF-α是重要的细胞炎性因子,与胰岛素抵抗和胰岛β细胞损伤关系密切[17],TNF-α导致胰岛素受体底物1(IRS-1)正常的酪氨酸磷酸化受抑制,异常的丝氨酸磷酸化导致IRS-1表达下降,阻碍IRS-1与胰岛素受体结合,引起胰岛素抵抗;TNF-α通过抑制葡萄糖转运蛋白4转录,使葡萄糖转运发生障碍,引起胰岛素抵抗发生;TNF-α诱导巨噬细胞释放白细胞介素-1(IL-1),导致一氧化氮合酶和一氧化氮增多,直接损伤胰岛β细胞。Shi等[18]研究显示,通过3个月艾塞那肽联合二甲双胍治疗,TNF-α水平表达下调。本研究结果显示,TNF-α浓度下降,HOMA-IR降低,提示艾塞那肽可能通过调节TNF-α表达改善胰岛素抵抗。TGF-β1是一种成纤维细胞因子,已发现其在糖尿病小鼠的肾小球和肾小管高表达,引起肾间质纤维化,可能作为一种关键介质参与糖尿病肾病发生[19]。加用艾塞那肽周制剂后,TGF-β1较治疗前降低,推测艾塞那肽可延缓糖尿病慢性并发症发生。S1P是一种活性脂质分子,参与免疫应答、炎症反应、肿瘤等多种生物学过程,作为一种具有保护作用的鞘脂类,促进细胞增殖和存活,保护胰岛β细胞[20],增加胰岛素敏感性。Laychock等[21]发现,S1P可抑制大鼠体内细胞因子诱导β细胞凋亡,恢复胰岛功能。本研究中S1P浓度升高提示病人用药后胰岛功能改善,艾塞那肽周制剂具有保护胰岛β细胞的作用。
综上所述,艾塞那肽周制剂联合二甲双胍能有效改善2型糖尿病病人机体代谢异常,缓解胰岛素抵抗,控制血糖平稳,有效降糖同时未增加低血糖发生,且改善机体慢性低度炎症状态,可为糖尿病综合管理、指导临床用药提供依据。
