加速溶剂萃取-气相色谱法测定土壤中11种氯苯类化合物
2021-03-24贺小敏
刘 彬,王 璠,熊 晶,吴 昊,贺小敏
(湖北省生态环境监测中心站,武汉 430072)
随着近30年来我国工业化、城市化和农业现代化的推进,土壤环境问题呈现出多样化、复杂化和区域化的发展态势[1]。企业污染物排放是土壤环境污染的重要来源,多省已发布相关土壤重点监管企业名单[2],其中化学原料和化学制品制造业比例较大。氯苯类化合物(CBs)常被作为生产原料、反应助剂、传热材料和中间体等使用,在化学原料和化学制品制造业中应用广泛[3]。CBs一般包括12种化合物,分别是氯苯(CB)、1,3-二氯苯(1,3-DCB)、1,4-二氯苯(1,4-DCB)、1,2-二氯苯(1,2-DCB)、1,3,5-三氯苯(1,3,5-TCB)、1,2,4-三氯苯(1,2,4-TCB)、1,2,3-三氯苯(1,2,3-TCB)、1,2,3,5-四氯苯(1,2,3,5-TCB)、1,2,4,5-四氯苯(1,2,4,5-TCB)、1,2,3,4-四氯苯(1,2,3,4-TCB)、五氯苯(PCB)和六氯苯(HCB)。它们是一类有刺激性气味、化学性质稳定的化合物,具有遗传致突变、致癌和致畸效应[4]。生态环境部于2018年发布GB 36600-2018《土壤环境质量建设用地土壤污染风险管控标准(试行)》,规定了部分CBs的建设用地土壤污染风险筛选值和管制值,建立相应的分析方法是落实污染物监测、管控的需要。
目前我国尚无针对土壤中CBs的分析方法标准,而涉及土壤中CBs的标准多为通用性方法,如测定挥发性有机物(国家环境保护标准HJ 605-2011《土壤和沉积物挥发性有机物的测定吹扫捕集/气相色谱-质谱法》)、半挥发性有机物(国家环境保护标准HJ 834-2017《土壤和沉积物半挥发性有机物的测定气相色谱-质谱法》)或有机氯农药(国家环境保护标准HJ 835-2017《土壤和沉积物有机氯农药的测定气相色谱-质谱法》)的相关分析方法。几个标准涉及的目标化合物种类繁多但覆盖的CBs却不多,针对性不强,无法很好满足环境管理的监测需求。
文献[5]采用吹扫捕集与色谱联用技术测定CBs,但四氯苯、五氯苯和六氯苯在捕集管、捕集阱和传输线等部件中残留严重,进样前需多次清洗、烘烤,对实际监测工作造成诸多不便。本工作采用对固体样品中污染物提取效率高且有机溶剂用量少的加速溶剂萃取法(ASE),结合具有广泛普及性且配有电子捕获检测器(ECD)的气相色谱法(GC),建立了土壤中1,3-DCB、1,4-DCB、1,2-DCB、1,3,5-TCB、1,2,4-TCB、1,2,3-TCB、1,2,3,5-TCB、1,2,4,5-TCB、1,2,3,4-TCB、PCB、HCB 等11 种CBs的测定方法。
1 试验部分
1.1 仪器与试剂
Agilent 7890A 型气相色谱仪,配自动进样器和ECD;E-916型加速溶剂萃取仪,配专用萃取池和接收瓶;FDU-2100型冷冻干燥机;Turbo VapⅡ型自动氮吹仪,配氮吹管;Visiprep TM DL 型固相萃取装置;Welchrom Florisil型硅酸镁小柱(1 000 mg/6 mL)。
11 种CBs(1,3-DCB、1,4-DCB、1,2-DCB、1,3,5-TCB、1,2,4-TCB、1,2,3-TCB、1,2,3,5-TCB、1,2,4,5-TCB、1,2,3,4-TCB、PCB、HCB)的标准储备溶液:1 000 mg·L-1,介质为正己烷。
11种CBs的标准溶液:300 mg·L-1,移取适量的1 000 mg·L-111种CBs的标准储备溶液,用正己烷稀释而成。
四氯间二甲苯(11种CBs的替代物)标准储备溶液:1 000 mg·L-1,介质为甲醇。
四氯间二甲苯(TCX)标准溶液:100 mg·L-1,移取适量的1 000 mg·L-1TCX 标准储备溶液,用正己烷与丙酮以体积比95∶5组成的混合液稀释而成。
正己烷、丙酮、二氯甲烷均为农残级;石英砂、无水硫酸钠、硅藻土均为分析纯。
1.2 仪器工作条件
1)加速溶剂萃取条件 预热5 min,静态萃取5 min;萃取压力1.03×104Pa;冲洗体积60%;溶剂冲刷1 min,气体冲刷2 min;萃取溶剂用量20 mL;萃取温度100 ℃;萃取2次。
2)色谱条件 Agilent DB-1701毛细管色谱柱(30 m×250μm,0.25μm);载气为氮气(纯度不小于99.999%),流量1.5 mL·min-1;尾吹气流量60 mL·min-1;进样口温度250 ℃,检测器温度300 ℃;不分流进样,进样量1μL。柱升温程序:初始温度50 ℃,保持0.5 min;以8 ℃·min-1速率升温至100 ℃,保持35 min;再以20 ℃·min-1速率升温至220 ℃,保持5 min。
1.3 试验方法
1.3.1 样品采集、保存与制备
在湖北省鄂州市葛店开发区某农药厂(现已停止生产)生产车间附近采集5处土壤表层样品,以未检出目标化合物的一处样品作为基体,开展了条件优化和方法精密度、准确度试验。
将采集的土壤样品放在搪瓷盘上、混匀,除去枝棒、叶片、石子等异物,于4℃以下密封保存,作为新鲜样品。
采用冷冻干燥法分析时,将上述新鲜样品放入冷冻干燥机中脱水,将干燥后的样品研磨、混匀,并密封保存于干燥器中,作为冷冻干燥样品。
1.3.2 加速溶剂萃取
称取10 g左右的新鲜样品或冷冻干燥样品与10 g左右的硅藻土掺拌均匀后加入适量11种CBs的替代物,将萃取池组装完成后,下部垫适量石英砂,将待萃取样品全部转入萃取池中,于上部铺一层石英砂并加盖滤纸片,放入加速溶剂萃取仪中,设定加速溶剂萃取条件进行萃取,收集萃取液。冷冻干燥样品的萃取溶剂为正己烷;新鲜样品的萃取溶剂为正己烷与丙酮以体积比1∶1组成的混合液。
1.3.3 萃取液的净化
分析冷冻干燥样品时,将萃取液氮吹浓缩,并用正己烷定容至1.0 mL,混匀后转移至进样小瓶中按色谱条件进行测定。
分析新鲜样品时,需先用适量无水硫酸钠对上述所得萃取液脱水,再经硅酸镁小柱净化,氮吹浓缩后按色谱条件进行测定。具体操作为:将硅酸镁小柱固定在固相萃取装置上,加入适量无水硫酸钠,用适量正己烷活化硅酸镁小柱,将约40 mL的新鲜样品萃取液氮吹浓缩至1 mL,转移至硅酸镁小柱中,用2 mL正己烷分两次洗涤氮吹管后将洗涤液全部转入硅酸镁小柱中,加入5 mL正己烷进行淋洗,收集全部淋洗液。将淋洗液氮吹浓缩,并用正己烷定容至1.0 mL,混匀后转移至进样小瓶中按色谱条件进行测定。
2 结果与讨论
2.1 色谱行为
按仪器工作条件对11种CBs的混合标准溶液(含30.0 mg·L-11,3-DCB、1,4-DCB、1,2-DCB,含3.00 mg·L-11,3,5-TCB、1,2,4-TCB、1,2,3-TCB、1,2,3,5-TCB、1,2,4,5-TCB、TCX、HCB,含1.50 mg·L-11,2,3,4-TCB、PCB)进行测定,其色谱图见图1。
2.2 11种CBs替代物的选择
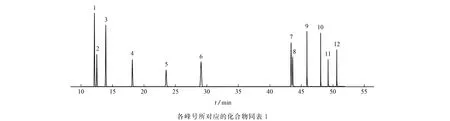
图1 11种CBs混合标准溶液的色谱图Fig.1 Chromatogram of mixed standard solution of 11 CBs
试验分别考察了12 种CBs在ECD 上的响应情况。结果表明:CB为10 000 mg·L-1(市售)时,响应值仅有10 000 Hz左右,是其他CBs响应值的千分之一以下(例如:1,2-DCB为25.0 mg·L-1时,响应值为25 000 Hz 左右,1,2,3,4-TCB 为2.50 mg·L-1时,响应值为80 000 Hz左右),不适合采用ECD 测定。同时CB 的饱和蒸气压(1 330 Pa)较大,前处理过程中其极易损失,也不适宜与其他CBs同时测定。因此,试验仅对土壤中除CB外的11 种CBs(1,3-DCB、1,4-DCB、1,2-DCB、1,3,5-TCB、1,2,4-TCB、1,2,3-TCB、1,2,3,5-TCB、1,2,4,5-TCB、1,2,3,4-TCB、PCB、HCB)进行测定。
由于土壤样品基质复杂,可以在前处理之前加入11种CBs的替代物(样品中不含有、自然环境中不存在,但物理化学性质与待测目标化合物相似的化合物),通过其回收率评价样品基体、样品处理过程对分析结果的影响。
结合11种CBs的物理化学性质,试验采用2-氟联苯和TCX 两种常见替代物进行试验,发现2-氟联苯保留时间太短、出峰易与溶剂峰重叠且响应值较低,以TCX 为替代物较为合适。试验选择11种CBs的替代物为TCX。
2.3 样品制备方法
大部分CBs属于半挥发性有机物,一般制备冷冻干燥样品或者新鲜样品进行分析。目前各级环境监测单位最普遍的选择是制备新鲜样品(一般具有较高含水率)进行分析,该法虽然操作简单,但是往往需要选择丙酮等水溶性萃取溶剂进行萃取,导致萃取液基质较复杂、干扰物较多,若不经除水和净化处理,在一定程度上会影响化合物的回收率。若将新鲜样品经过冷冻干燥成为干样,不仅省去了萃取液除水步骤、减少了化合物损失,而且萃取环节中萃取溶剂的选择增多,萃取溶剂不再局限于选择水溶性溶剂,可有效减少共萃物,缺点是冷冻干燥机有一定成本。试验对冷冻干燥样品和新鲜样品的前处理条件均进行了研究。
2.4 加速溶剂萃取条件的选择
2.4.1 萃取溶剂
各类环境样品中CBs的萃取溶剂主要有正己烷、丙酮、二氯甲烷、乙酸乙酯、石油醚、二硫化碳、乙醚、甲苯和甲醇。石油醚和正己烷极性相似;二硫化碳和甲苯毒性较强;乙醚作为麻醉剂在我国环境监测实验室使用不多;甲醇浓缩时间较长。因此,试验采用正己烷、正己烷与丙酮以体积比1∶1组成的混合液、正己烷与二氯甲烷以体积比1∶1组成的混合液、正己烷与乙酸乙酯以体积比1∶1组成的混合液等4种萃取溶剂,考察了萃取溶剂对冷冻干燥样品中CBs萃取效果的影响,结果见图2。
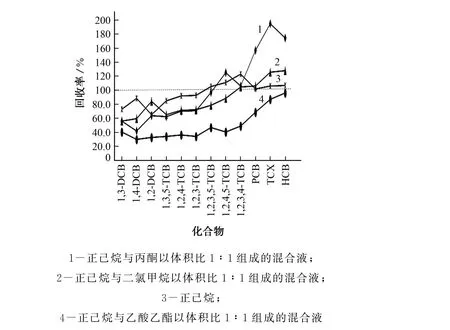
图2 萃取溶剂对冷冻干燥样品中CBs萃取效果的影响Fig.2 Effect of extraction solvent on extraction effect of CBs in the freeze-dried sample
由图2可知:萃取溶剂为正己烷与乙酸乙酯以体积比1∶1 组成的混合液时,CBs的回收率偏低(大多低于50%);萃取溶剂为正己烷、正己烷与二氯甲烷以体积比1∶1组成的混合液时,CBs的回收率相当,分别为65.3%~123%,55.9%~128%,但萃取溶剂为正己烷时,萃取液的共萃物较少;萃取溶剂为正己烷与丙酮以体积比1∶1组成的混合液时,萃取液颜色最深,色谱图中干扰峰最多,CBs的回收率为41.5%~195%。因此,当分析冷冻干燥样品时,试验选择萃取溶剂为正己烷。
新鲜样品因含水率较高,需使用水溶性萃取溶剂,最常用的萃取溶剂为正己烷与丙酮以体积比1∶1组成的混合液。因此,当分析新鲜样品时,试验选择萃取溶剂为正己烷与丙酮以体积比1∶1组成的混合液,但萃取液基质较复杂,上机测定前应净化。
2.4.2 萃取温度和萃取次数
试验以正己烷(冷冻干燥样品)和正己烷与丙酮以体积比1∶1组成的混合液(新鲜样品)为萃取溶剂,进一步考察了萃取温度和萃取次数对CBs萃取效果的影响。结果表明:固定萃取2次,萃取温度分别为90,100 ℃时,CBs的回收率相当(分析冷冻干燥样品时,CBs的回收率分别为59.8%~119%,65.3%~123%;分析新鲜样品时,CBs的回收率分别为44.9%~166%,41.5%~195%);固定萃取温度为100 ℃,分别萃取2次和3次时,CBs的回收率差别不大(分析冷冻干燥样品时,CBs的回收率分别为65.3%~123%,59.0%~125%;分析新鲜样品时,CBs的回收率分别为41.5%~195%,40.7%~188%)。为减少有机溶剂用量(每个样品每次萃取的萃取溶剂用量为20 mL),试验选择萃取温度为100 ℃,萃取2次。
2.5 萃取液净化条件的选择
2.5.1 净化方法
测定CBs时最常见的样品净化方法是浓硫酸法、硅酸镁小柱法(穿透式净化)和凝胶色谱法,其中硅酸镁小柱法操作简单、成本低廉、最易推广。试验选用硅酸镁小柱法。
2.5.2 淋洗剂
移取1 mL 新鲜样品的萃取浓缩液加标后上样,考察了正己烷、正己烷与二氯甲烷以体积比95∶5组成的混合液、正己烷与二氯甲烷以体积比9∶1组成的混合液、正己烷与二氯甲烷以体积比8∶2组成的混合液、正己烷与丙酮以体积比95∶5组成的混合液、正己烷与丙酮以体积比9∶1组成的混合液等6种淋洗剂,在用量为10 mL时的净化效果。结果表明:淋洗剂为正己烷时,净化效果最好,色素基本保留在硅酸镁小柱上,流出液较为澄清;淋洗剂为正己烷与丙酮以体积比95∶5 组成的混合液、正己烷与丙酮以体积比9∶1组成的混合液时,净化效果不佳,色素穿透现象较为明显;淋洗剂为其他3种淋洗剂时,净化效果较好。
试验进一步比较了正己烷、正己烷与二氯甲烷以体积比95∶5组成的混合液、正己烷与二氯甲烷以体积比9∶1组成的混合液、正己烷与二氯甲烷以体积比8∶2组成的混合液等4种淋洗剂对CBs回收率的影响,结果见图3。

图3 淋洗剂对CBs回收率的影响Fig.3 Effect of eluant on recovery of CBs
由图3可知:淋洗剂为正己烷时,CBs的回收率最理想(69.0%~120%);其他3种淋洗剂淋洗时,部分CBs的回收率偏高,可能与干扰物的穿透有关。试验选择淋洗剂为正己烷。
2.5.3 淋洗剂用量
移取1 mL 新鲜样品的萃取浓缩液加标后上样,以9 mL正己烷进行淋洗,淋洗液每流出1 mL收集1次,CBs的流出曲线见图4。
由图4 可知:当流出体积为8 mL 时(上样1 mL、淋洗剂用量为7 mL),所有CBs的淋洗回收率均保持稳定。试验选择淋洗剂用量为7 mL。
2.6 色谱柱的选择

图4 CBs的流出曲线Fig.4 Effluent curves of CBs
试验采用Agilent DB-5毛细管色谱柱和Agilent DB-1701毛细管色谱柱对CBs进行分离,发现大部分CBs在这两种色谱柱上的分离度差别不大,但1,2,3,5-TCB 和1,2,4,5-TCB 在Agilent DB-5毛细管色谱柱上完全无法分开。试验选用Agilent DB-1701毛细管色谱柱。
有机氯农药是采用GC-ECD测定的最常见的有机污染物。采用Agilent DB-1701毛细管色谱柱按仪器工作条件对有机氯农药进行分离。试验发现:α-六六六第一个出峰、保留时间为51.728 min,迟于CBs中最后一个出峰的HCB(保留时间为50.443 min),有机氯农药不会对CBs的测定产生干扰。
2.7 标准曲线和检出限
按仪器工作条件对11种CBs的混合标准溶液系列进行测定,以各CBs的质量浓度为横坐标,对应的峰面积为纵坐标,绘制标准曲线。11种CBs的线性范围、线性回归方程和相关系数见表1。
对空白样品进行7次平行分析,根据国家环境保护标准HJ 168-2010《环境监测分析方法标准制修订技术导则》,以测定结果的3.143倍标准偏差计算方法检出限(3.143s),结果见表1。
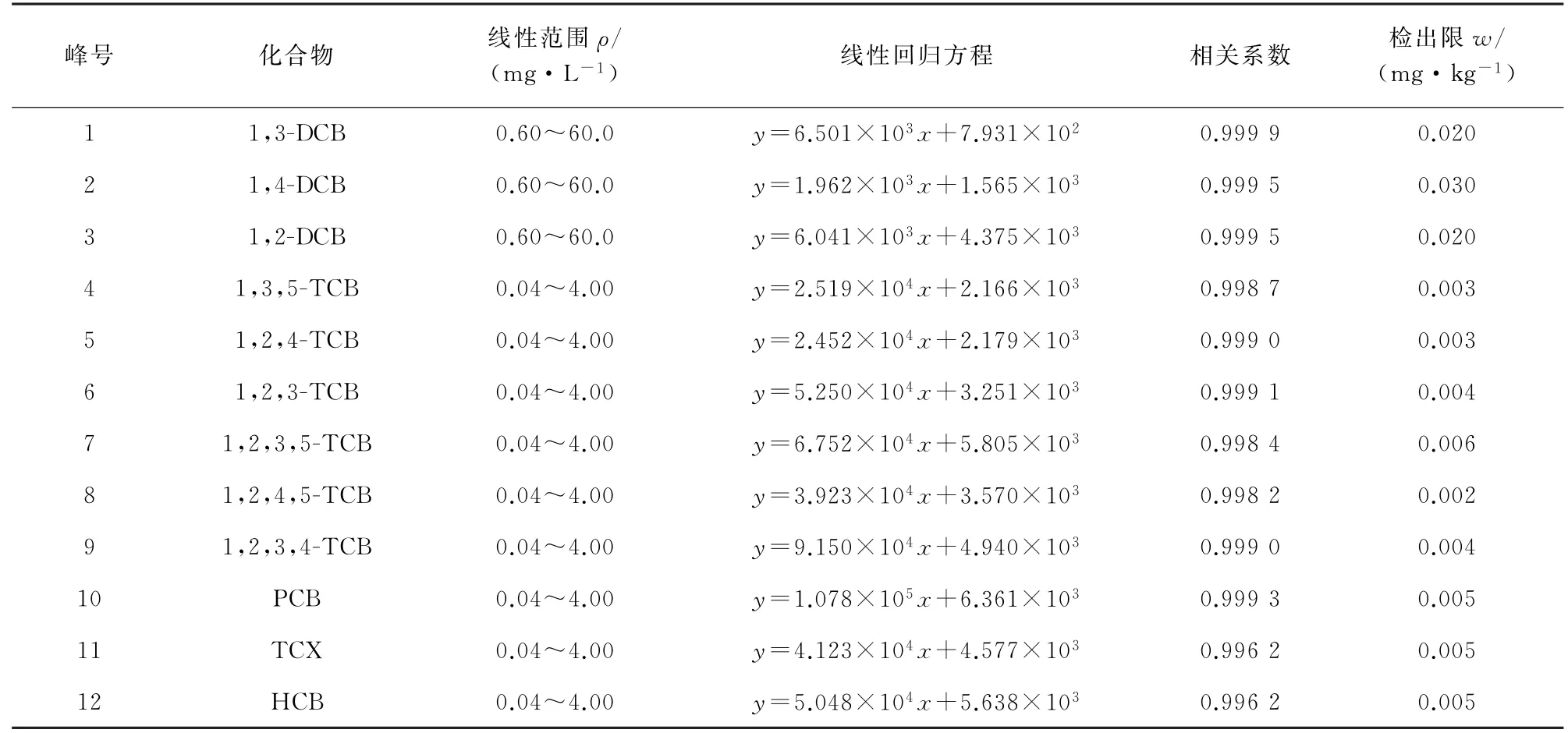
表1 线性范围、线性回归方程、相关系数和检出限Tab.1 Linearity ranges,linear regression equations,correlation coefficients and detection limits
2.8 准确度和精密度
测定CBs时,土壤样品的制备方法可以采用两种:样品经冷冻干燥后,以正己烷为萃取溶剂进行加速溶剂萃取,将萃取液浓缩后按色谱条件进行测定(简称干法);新鲜样品以正己烷与丙酮以体积比1∶1组成的混合液为萃取溶剂进行加速溶剂萃取,萃取液经脱水和硅酸镁小柱净化后收集所有淋洗液,将淋洗液浓缩后按色谱条件进行测定(简称湿法)。分别采用干法和湿法制备土壤样品,按试验方法进行分析,并进行加标回收试验,计算回收率和测定值的相对标准偏差(RSD),结果见表2。
由表2可知:回收率为45.3%~140%,RSD 为2.7%~24%。方法的准确度和精密度满足HJ 835-2017的要求。
2.9 样品分析
在湖北省鄂州市葛店开发区某农药厂(现已停止生产)生产车间附近采集5处土壤表层样品,分别为厂界西南、厂界东南、生产车间东南1#门、生产车间西南2#门和车间东面3#门。
按试验方法用干法对土壤样品进行分析。结果表明:在生产车间东南1#门、生产车间西南2#门这2处采集的土壤样品中检出HCB,测定值依次为0.018,0.024 mg·kg-1。

表2 准确度和精密度试验结果(n=6)Tab.2 Results of tests for accuracy and precision(n=6)
