美沙拉嗪联合益生菌治疗炎症性肠病的疗效及安全性评价
2021-03-23周立彬凌彩苏黄旭明
周立彬,凌彩苏,黄旭明
(深圳市宝安区石岩人民医院消化内科,广东深圳 518108)
炎症性肠病(inflammatory bowel disease,IBD)是指各类肠道炎症疾病,常会累及患者直肠、回肠以及结肠等部位,以克罗恩病、溃疡性结肠炎较为常见,其发生主要是肠道黏膜免疫系统对于肠腔内抗原物质无法正常应答造成,主要症状包括腹痛、腹泻等,情况严重者还会出现血便[1]。 目前,临床常用美沙拉嗪等氨基水杨酸类药物来治疗IBD,以减轻患者肠道炎症症状,但仍有部分患者疗效不佳[2-3]。 临床发现,肠道菌群失调在IBD 患者病情的发生发展中发挥着重要作用[4]。 因此,可以通过增加益生菌来改善IBD 患者肠道菌群失调症状,提高临床疗效。基于此,该研究选取2019 年8 月—2021 年1 月该院收治的76 例IBD患者为研究对象,分析美沙拉嗪联合益生菌治疗IBD的效果。 报道如下。
1 资料与方法
1.1 一般资料
选取该院收治的76 例IBD 患者为研究对象,随机分为对照组(n=38)与研究组(n=38)。 对照组男20例,女18 例;年龄26~58 岁,平均年龄(43.29±9.35)岁;病程10 个月~8 年,平均病程(4.83±1.20)年;疾病类型:克罗恩病9 例,溃疡性结肠炎29 例;发病情况:初发17 例,复发21 例。 研究组男21 例,女17 例;年龄25~55 岁,平均年龄(42.60±10.12)岁;病程1~7年,平均病程(4.77±1.51)年;疾病类型:克罗恩病11例,溃疡性结肠炎27 例;发病情况:初发18 例,复发20 例。 两组性别、年龄、病程、疾病类型及发病情况比较,组间差异无统计学意义(P>0.05)。 该研究经该院医学伦理委员会审批。
1.2 纳入、排除标准
纳入标准:(1) 符合炎症性肠病相关诊断标准[5],且存在不同程度的腹痛、腹泻及血便等症状;(2)所有患者均知情且自愿参与研究,并签署知情同意书。 排除标准:(1)缺血性肠炎、肠结核疾病者;(2)对该研究所用药物有过敏反应者;(3)治疗依从性不佳者。
1.3 方法
两组患者均接受常规抗炎治疗。
对照组采用美沙拉嗪治疗。美沙拉嗪肠溶片(葵花药业集团佳木斯鹿灵制药有限公司, 国药准字H199 80148,规格:0.25 g)口服,1.0 g/次,3 次/d。
研究组采用美沙拉嗪联合益生菌治疗。双歧杆菌三联活菌散(上海上药信谊药厂有限公司,国药准字S10970105,规格:1 g)口服,1.0 g/次,3 次/d;美沙拉嗪肠溶片用法用量同对照组。
两组患者均餐前服药, 用药过程中避免进食辛辣、刺激性食物以及牛奶、海鲜等可能会导致病情加剧的食物,连续治疗2 个月。
1.4 观察指标
(1)治疗效果:治疗后患者症状彻底改善,且内镜检查结果提示黏膜已恢复至正常状态为显效;治疗后患者症状有所改善,且内镜检查结果提示黏膜炎症较轻微,或出现假息肉为有效;治疗后患者症状无改善,且内镜检查结果提示黏膜炎症未见改善为无效,治疗总有效率=显效率+有效率[5]。
(2)炎症因子:分别于治疗前后采用放射免疫法测定两组的白细胞介素-6(interleukin-6,IL-6)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)水平,采用酶联免疫吸附试验法测定两组γ-干扰素(interferon-γ,IFN-γ)水平。
(3)不良反应:比较两组用药期间恶心、纳差及皮疹的发生率。
1.5 统计方法
使用SPSS 22.0 统计学软件进行数据分析,IL-6、TNF-α、IFN-γ 等计量资料均以(±s)表示,采用t 检验;治疗总有效率、不良反应总发生率等计数资料均以[n(%)]表示,采用χ2检验。P<0.05 表示差异有统计学意义。
2 结 果
2.1 治疗效果比较
研究组的治疗总有效率为94.74% ,高于对照组的76.32%,差异有统计学意义(P<0.05)。 见表1。

表1 两组治疗效果比较[n(%)]
2.2 炎症因子比较
治疗前,两组的各项炎症因子水平比较,差异无统计学意义(P>0.05);治疗后,两组的各项炎症因子水平均低于治疗前,且研究组的IL-6、TNF-α、IFN-γ水平均显著低于对照组,组间差异有统计学意义(P<0.05)。 见表2。
表2 两组治疗前后炎症因子水平比较(±s)
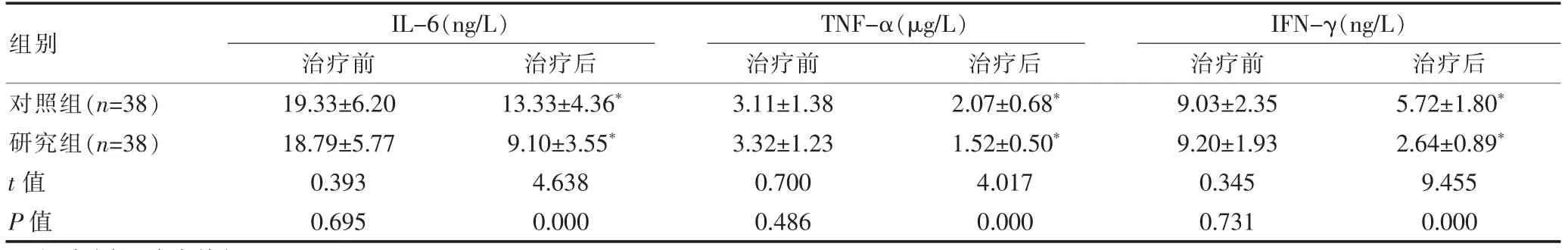
表2 两组治疗前后炎症因子水平比较(±s)
注:与同组治疗前相比,*P<0.05
组别IL-6(ng/L)治疗前 治疗后TNF-α(μg/L)治疗前 治疗后对照组(n=38)研究组(n=38)t 值P 值19.33±6.20 18.79±5.77 0.393 0.695 13.33±4.36*9.10±3.55*4.638 0.000 3.11±1.38 3.32±1.23 0.700 0.486 2.07±0.68*1.52±0.50*4.017 0.000 IFN-γ(ng/L)治疗前 治疗后9.03±2.35 9.20±1.93 0.345 0.731 5.72±1.80*2.64±0.89*9.455 0.000
2.3 不良反应比较
研究组的不良反应总发生率为2.63%,低于对照组的21.05%,差异有统计学意义(P<0.05)。 见表3。
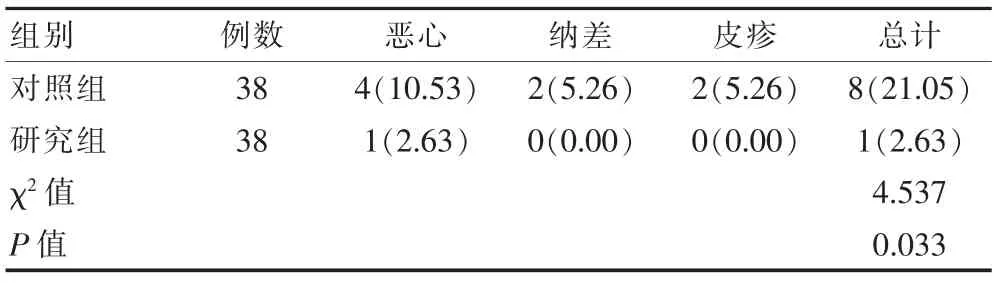
表3 两组不良反应比较[n(%)]
3 讨 论
IBD 属于一种发病率、复发率较高的慢性自身免疫性疾病,近年来发病率逐渐升高。至今为止,临床对IBD 的具体发病机制还未完全明确,只认为可能与遗传、饮食、环境及自身免疫等因素存在一定关系[6]。 近年来,临床常用美沙拉嗪治疗IBD,该药物不仅可在患者结肠、回肠尾部定向释放,有效阻滞结肠黏膜及其过氧化物酶形成的前列素E2、白三烯等,同时还可降低血小板活化因子的活性,阻滞巨噬细胞迁移至病灶,有效清除受损的氧自由基,抑制白细胞合成相关炎症递质,达到抑制机体炎症反应的目的[7]。但临床实践发现,单独用美沙拉嗪治疗,仍有部分IBD 患者症状改善不理想,且易出现恶心、纳差等不良反应,影响患者治疗依从性,形成恶性循环[8]。 因此,如何更有效地提高IBD 患者的临床疗效及安全性成为临床急需解决的问题。
临床发现,IBD 患者肠道内存在不同程度的菌群失调现象, 由此可见肠道菌群参与了IBD 患者病情的发生发展。菌群失调一方面可能与肠道免疫系统损伤有关,另一方面也可能与患者接受过大量抗生素治疗有关[9]。IBD 的发生可能是由于肠道菌群失调后,双歧杆菌、乳酸杆菌等多种有益菌减少,造成一些致病菌及其代谢产物破坏了肠道的免疫系统,导致免疫功能紊乱及上皮组织损伤,最终诱发炎症反应。 而益生菌在纠正患者肠道菌群失调、促进肠道微生物平衡方面有一定作用, 为IBD 患者的临床治疗提供了解决方案。 该研究结果显示, 研究组的治疗总有效率94.74%高于对照组的76.32%;治疗后,研究组的IL-6、TNF-α、IFN-γ 水平均低于对照组, 提示对IBD 患者采用美沙拉嗪联合益生菌治疗的效果显著,有助于减轻患者机体炎症反应。 雷伟等[10]学者指出,美沙拉嗪肠溶片联合益生菌治疗IBD 的效果显著, 可快速地减轻相关症状,促进炎症反应消失,且不会增加不良反应,与该研究结果一致。 分析原因:(1)益生菌胶囊通常为双歧杆菌、 肠球菌及嗜酸乳杆菌活菌胶囊,服用后可显著增加肠道内有益菌, 减少致病菌数量,促进肠道菌群平衡;(2)益生菌不仅可提高巨噬细胞对致病菌的吞噬能力, 还可降低巨噬细胞对TNF-α等炎症因子的释放, 发挥调节肠黏膜免疫功能的作用;(3)益生菌可于患者消化道内产生乙酸、乳酸等物质,降低消化道内pH 值,抑制致病菌的生长与繁殖,另外乳酸菌可通过分泌细菌素、生物表面活性剂等物质来抑制或消灭病原菌,提高临床疗效;(4)将美沙拉嗪与益生菌联合应用一方面可更有效地抑制IBD 患者机体炎症反应,另一方面还可通过纠正肠道菌群失调、促进肠道微生物平衡来改善患者症状,提高临床疗效。
该研究结果还显示,研究组的不良反应总发生率为2.63%,低于对照组的21.05%,提示对IBD 患者采用美沙拉嗪联合益生菌治疗的不良反应较单纯用美沙拉嗪更少。 分析原因:单独用美沙拉嗪时,仅有1 h的半衰期,与血浆蛋白的结合率仅为40%左右,而联合益生菌治疗, 药物会在机体内代谢成为乙酰化合物,半衰期长达5~10 h,且与血浆蛋白的结合率提升至80%左右, 因此美沙拉嗪联合益生菌方案的临床安全性较高。
综上所述, 采用美沙拉嗪联合益生菌治疗IBD的效果显著,可有效减轻机体炎症反应,减少不良反应的发生。
