基于ICRP 141号报告的241Am吸入后滞留份额计算及新旧模型异同
2021-03-22陈倩兰骆志平刘森林
陈倩兰,骆志平,刘森林
(中国原子能科学研究院, 北京 102413)
对于放射工作人员,最常发生的放射性内照射是吸入导致。为了计算吸入导致的剂量,辐射防护中采用核素在人体转移、吸收的生物动力学模型,最权威的内照射生物动力学模型在国际放射防护委员会(ICRP)报告中给出。ICRP生物动力学模型可分为呼吸道模型、系统模型(代表全身循环)、营养道模型(过去称胃肠道模型),随着最近几十年来各国辐射防护内照射方面的研究数据的积累,这些模型逐步修改调整,使模型预测值更接近实际内照射测量值。
为了计算吸入后的滞留份额及排泄份额,呼吸道模型(最新模型是ICRP 130、ICRP 141号报告的呼吸道模型[1-2])需结合系统模型(超铀核素最新系统模型见ICRP 141号报告[2])、营养道模型(ICRP 100号报告[3])一起计算(本文简称这3个生物动力学模型为新模型)。在新模型之前,计算吸入后的滞留和排泄是基于ICRP 66号报告中的呼吸道模型(1994年)[4]、ICRP 70号报告系列(包括ICRP 67号报告)系统模型[5]、ICRP 30号报告胃肠道模型[6]进行的(本文简称这3个生物动力学模型为旧模型)。目前很多内照射软件仍使用旧模型,旧模型是ICRP 78号报告[7]给出的内照射计算数据的依据,也是我国国标中内照射剂量转换系数和内照射监测参考数据的依据。
考虑到依据旧模型的计算结果仍在大量使用,而这些模型的最新修订会带来富集器官的滞留份额变化,这个变化会导致内照射评价结果不同,因此新旧模型的异同对于内照射评价来说很重要。
吸入内照射中,锕系核素由于半衰期长、毒性大,一旦大量进入人体需要尽快处理并长期监测,因此本文以超铀核素内照射非常关注的核素241Am为例进行计算,对新模型中影响较大的因素进行比较分析,给出新模型与旧模型的主要富集器官的滞留份额的异同,为当前超铀核素内照射直接测量给出一些参考。
1 ICRP生物动力学模型简介
1.1 ICRP呼吸道模型
由于吸入内照射的重要性和复杂性,ICRP呼吸道模型在近70年经过了多次改进。当前国标所依据的呼吸道模型来自1994年ICRP 66号报告发布的人类呼吸道模型(本文简称66号报告模型)。66号报告模型可以计算职业工作人员和公众的摄入,计算容易发生癌症的靶区域的剂量;计算气溶胶沉积,特别是对亚微米范围的沉积;可计算气载物质吸入率;假定粒子输运、吸收入血两种清除途径是竞争关系;假定每个过程清除速率随时间变化且与滞留物质的量相关;给出粒子输运过程参考值;根据人类和/或动物实验数据的一些核素数据推知核素化合物的吸收入血速率,缺乏数据时可采用依据ICRP 30号报告分类的默认值。该模型考虑了吸入核素对整个呼吸道的照射,考虑了呼吸道不同位置对辐射的敏感性;考虑了这些组织受到的剂量和剂量率可能会随着吸入物质物理性质和呼吸参数变化而有较大变化;模型可以根据生物样品数据计算剂量;可以计算摄入限值,可以计算回顾性和前瞻性剂量[4],而且还可应用于非放射性物质的沉积和廓清计算,因此它比起之前的呼吸道模型应用更为广泛。
随着近20年内照射长期测量数据的积累,实际测出的放射性核素在肺部的长期滞留份额会比呼吸道模型预测值更高,ICRP 130、141号报告对呼吸道模型做了修订,本文简称141号报告呼吸道模型。ICRP 130号报告在ICRP 66号报告呼吸道模型基础之上做的修订包括:库室的简化、粒子输运和吸收入血参数的修改、吸入粒子分类的修改[1],新模型中呼吸道模型结构及计算原理见文献[8]。2017年Puncher等人对吸入239Pu硝酸盐的狗进行的长达15年的肺部滞留研究、对美国铀和超铀注册机构(USTUR)的受照者0269(急性吸入239Pu硝酸盐)的尸体解剖和生物样品数据研究、对曾在Mayak 工厂工作的20个仅受钚硝酸盐照射工人的内照射测量数据研究,均发现呼吸道中有一个长期滞留成分存在,采用肺部束缚态库室能很好地解释这一发现,而且他的研究估算出了fb、Sb的值[2]。根据Puncher等人的3个研究确定出钚的fb=0.002、Sb=0 d-1[2],而且0269受照者的尸体解剖数据表明:束缚态库室需要用在除ET1区以外的所有呼吸道区。研究人员再次分析了70、80、90年代文献中吸入241Am的受照者、实验动物数据,证明了镅也需要束缚态库室,因此ICRP 141号报告的呼吸道模型中镅的束缚态参数直接参考钚在呼吸道模型中的束缚态参数,即fb=0.002,Sb=0 d-1。2019年底,关于超铀核素,ICRP 141号报告对ICRP 130号报告的呼吸道模型除ET1库室外的每个呼吸道库室增加了肺部的束缚态库室,让肺部的滞留保留一个较稳定的小份额,目的是增加肺部的长期滞留份额。本文计算所用的呼吸道模型见ICRP 130号报告表A.2,镅的肺部吸收参数见ICRP 141号报告表23.5。
1.2 镅的系统模型
ICRP镅的系统生物动力学模型(本文简称系统模型)及参数根据锕系元素在哺乳动物中的监测数据以及人的可控研究或长期研究成果建立,历次修改变化不大(ICRP 48、56、67、141号报告分别修订),主要是对模型结构及参数做了微调。对于镅、钚两种元素,注射量的70%~90%早期会被肝脏、骨骼富集[2],不过成年人以及大多数研究的实验动物肝脏的摄入会比骨骼更高,两种元素在人体系统行为的差异是镅初期的尿排泄速率更高,镅从肝脏的清除更快,二者在骨表面的沉积地点不同,可能这也导致两种元素从骨骼清除的净速率不同。
ICRP 141号报告给出的锕系元素的系统模型结构如图1所示[2],锕系元素在人体系统中的总体规律比镧系更为不规则,因此报告中分别给出不同锕系核素的转移速率常数,镅的转移速率常数来自ICRP 141号报告表18.9。

图1 ICRP 141号报告给出的锕系元素(Pu、U除外)的系统模型通用结构
这个通用的锕系元素系统模型将人体系统组织和体液分为五大部分[5]:血液、骨、肝、肾、其它软组织。血液被当做均匀混合库室,其它四大部分再细分为更小的库室,从而模拟锕系元素(更广泛来讲,是亲骨元素)的生物动力学数据。肝脏分为短、长期滞留库室分别为肝1、肝2库室。在肝1,放射性核素可转移回到血液、可通过胆汁分泌到达肠、可转移至肝2(从肝2中缓慢返回血液)。肾分为两个库室:肾1库室(尿通道)在几个小时或几天内将放射性核素转移到尿中;肾2库室(其它肾组织)缓慢将放射性核素转回到血液中。其它软组织库室(不包括骨髓)ST0、ST1、ST2,分别代表快速、中速、慢速与血液交换的其他软组织库室。
相对于国标依据的ICRP 67号报告(1993年)的系统模型,ICRP 141号报告在其基础上稍作修改。关于镅、锔所做的修改如下[2]:
(1)为了与锕系其他元素的系统模型一致,镅模型中的肝脏按运转速率快、慢分为两个库室:肝1(半排期30 d)、肝2(半排期1 a);
(2)性腺的半排期从10 a减到5 a,作为默认值用于锕系、镧系元素生物动力学模型的计算;
(3)内照射测量数据表明,ICRP 67号报告高估了241Am的系统排泄速率(采用骨中含量的份额计算的系统排泄速率),解决办法是将镅从皮质骨的吸收做一个局部循环,因此对骨表模型做了修改:通常模型放射性核素从骨中清除认为是转移到骨髓、再从骨髓进入血液,对于镅、锔,假设进入皮质骨骨髓的一部分(F份额)转移到皮质骨骨表(局部循环),剩余的1-F进入血液。皮质骨骨髓的半排期仍然保持默认值0.25 a。为了与文献给出的241Am在骨骼和尿中的数据保持一致(考虑文献数据的不确定性),局部循环份额F=2/3。
1.3 营养道模型
ICRP 100号报告中营养道模型的库室结构分为:口腔、食道、胃、小肠、右部结肠、左部结肠、乙状结肠直肠七个库室[3]。其中右部结肠库室是指解剖区中称为升结肠、盲肠、横结肠靠右部的那一半区域;左部结肠库室是指解剖区中称为降结肠、横结肠靠左部的那一半区域;乙状结肠直肠库室是指结肠和直肠。为了表示库室的滞留成分,又细分出其壁(口腔库室细分出口腔黏膜、牙齿)子库室。
营养道模型比起旧模型的胃肠道模型有了较大改变,考虑了消化吸收更全面的营养道解剖学区域而不仅仅关注胃肠道,不仅可以计算工作人员营养道受到的剂量,还可以计算公众和儿童营养道受到的剂量。该模型考虑了放射性核素在营养道的吸收及滞留的位置,营养道吸收核素后的排泄途径,每个区(口腔、食道、胃、小肠、结肠)各自敏感细胞受到的剂量,内腔、滞留及转移至血液的核素造成的剂量。营养道模型解决了胃肠道模型的一些问题,允许口腔、胃、结肠、小肠中发生吸收。但由于吸收位置的数据有限,因此大多数情况仍然假定吸收发生在小肠。营养道模型结构见ICRP 100号报告图5.1,计算依据的转移速率常数见ICRP 100号报告表6.6。
2 滞留、排泄份额计算程序设计
本文基于超铀核素的新模型建立人体各个库室的一阶微分方程组,肺部初始沉积量作为初值[1],求解S、M、F类241Am气溶胶吸入后在工作参考人(呼吸速率平均1.2 m3/h)体内各个库室的特定时间点的份额,采用Matlab 7.0以及其中的Simulink模块求解基于新、旧模型的一阶微分方程组,方程组求解方法为四阶五阶Runge-Kutta算法(ode45)变步长法,相对误差采用1×10-3。笔者采用ode45方法相对误差1×10-6计算对比,与相对误差1×10-3时计算值一致(均保留两位有效数字)。为了防止刚性方程问题,对于方程组求解方法笔者还采用了求解刚性微分方程的自由内插法的梯形法(ode23 t)计算对比(相对误差采用1×10-3),ode23 t方法与ode45方法计算结果一致(均保留两位有效数字)。对基于新模型的自编程序计算结果的正确性检验,对比的权威数据为ICRP 141号报告给出的OIR_Data_Viewer中的数据,验证结果一致;对基于旧模型的自编程序计算结果的正确性检验,对比的权威数据为IMBA软件(2007年版)给出的数据及ICRP 78号报告中的数据,验证结果一致。
Matlab 7.0 是MathWorks 公司的商用化专业数学软件,具有强大的计算分析能力,该软件的数值法求解一阶微分方程组方便高效。Matlab 7.0中Simulink模块能将方程求解的设计以及计算的结果可视化展示,而且相比纯编程方法更容易看到整个生物动力学方程组的结构、参数,便于修改、记录和检验,设计出的数学模型如图2、图3所示。

注:图中库室模型字母见ICRP 100号报告图5.1所指的营养道模型库室简写。
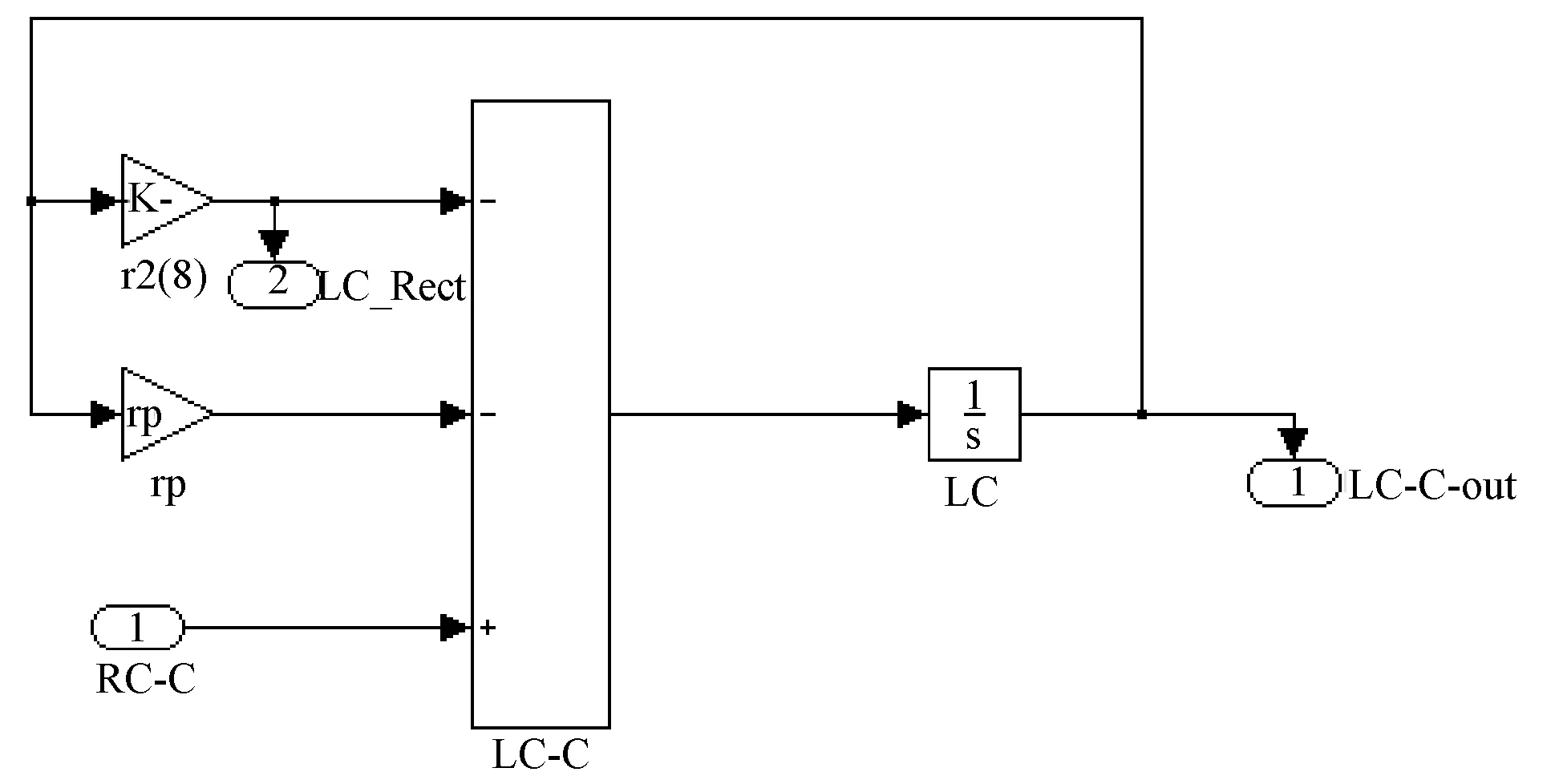
注:图中库室模型字母简写见ICRP 100号报告图5.1所指的营养道模型库简写,rp指核素的核衰变数,r2(8)指Left colon-C库室到Rectosigmoid-C库室的转移速率常数。
3 计算结果比较
验证自编计算程序正确后,基于新模型进行了不同库室、不同吸收类型、不同粒径的富集器官滞留份额分析比较;另外对新、旧模型计算结果进行了比较分析。
3.1 新模型计算结果比较
(1)不同库室份额的对比
以工作参考人(平均呼吸速率1.2 m3/h)吸入活度中值空气动力学直径(AMAD) 5 μm镅为例,采用新模型程序的计算结果,绘制出单位摄入量下各个关注库室中镅的份额随时间变化图,见图4~6。由图可见,S类镅气溶胶吸入后,1 000天以后主要滞留在肺部、骨骼;F类镅主要富集在骨骼、肝脏,因为F类核素从肺部快速吸收入血,从血液转移到富集器官;M类镅在肺部、骨骼、肝脏中均有相当的滞留份额(300天内)。因此对于不同吸收类型,内照射直接测量的重点应有所针对性。
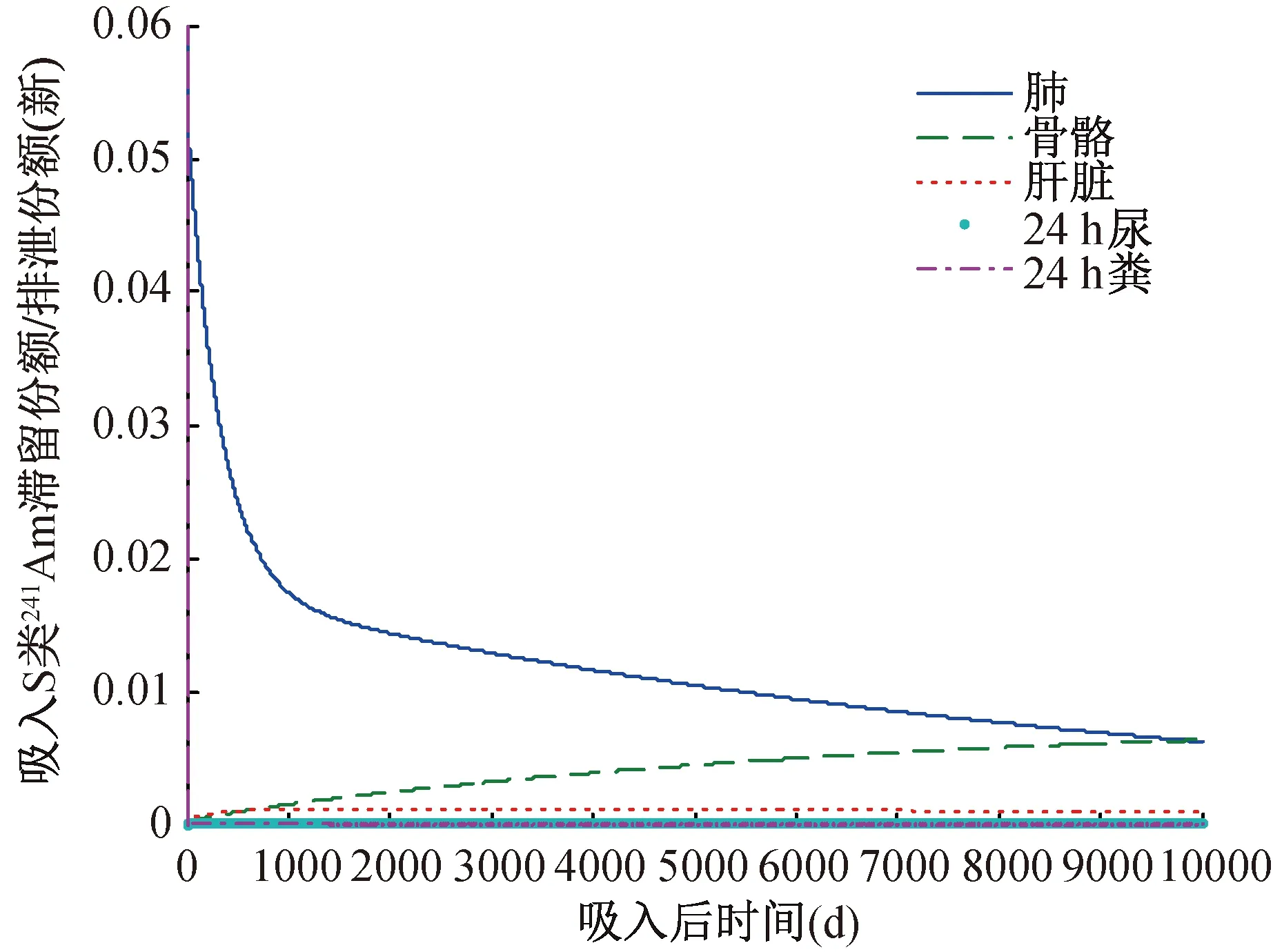
图4 吸入S类241Am气溶胶后新模型计算的库室间对比
(2)不同吸收入血类型的影响
以工作参考人(平均呼吸速率1.2 m3/h)吸入AMAD5 μm镅为例,比较了不同吸收入血类型的滞留份额随时间的变化曲线,见图7~9。对比可见S、M、F吸收入血类型在肺、骨骼、肝脏中滞留份额差异显著,因此内照射评价中,调查确定吸入核素的吸收入血类型非常重要。
(3)不同AMAD的影响
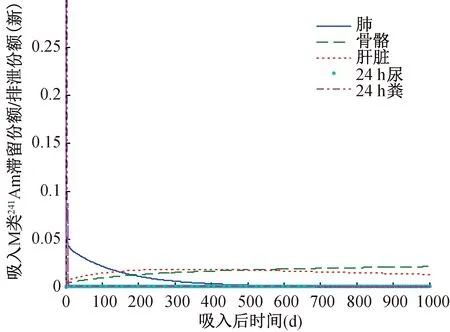
图5 吸入M类241Am气溶胶后新模型计算的库室间对比

图6 吸入F类241Am气溶胶后新模型计算的库室间对比
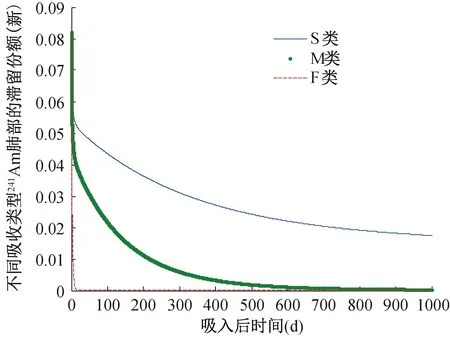
图7 吸入不同类型241Am气溶胶后肺部滞留份额对比(新模型)

图8 吸入不同类型241Am气溶胶后肝脏滞留份额对比(新模型)

图9 吸入不同类型241Am气溶胶后骨骼滞留份额对比(新模型)

图10 吸入不同AMAD粒径241Am的肺部滞留份额的差异(M类)

图11 吸入不同AMAD粒径241Am的骨骼滞留份额的差异(M类)
随着气溶胶测量技术在内照射场所的应用,现场气溶胶粒径及分布已能进行测量。为了比较气溶胶粒径对吸入后的主要富集器官滞留份额的影响,以参考工作人(呼吸速率平均1.2 m3/h)吸入241Am为例,比较AMAD粒径0.001~10 μm范围内8个不同典型粒径的滞留份额随时间的变化曲线,见图10、11和12。由图10~12可见,除了AMAD10、0.001 μm的滞留份额很小外,其他6个AMAD粒径带来差异非常显著,这是因为AMAD粒径的大小影响肺部各个库室的初始沉积,从而影响肺部的吸收入血,因此粒子吸收入血后进入富集器官的份额也受到较大影响。为了进一步定量比较粒径对滞留份额的影响,本文以工作参考人吸入M类241Am为例,将内照射场所比较关注的几种AMAD粒径(3、1、0.5、0.1 μm)的肺部、骨骼、肝脏滞留份额与AMAD5 μm的值进行对比,结果列于表1。对比发现粒径对滞留份额的影响显著,滞留份额随粒径变小而增大,同种粒径下肺部、骨骼、肝脏各个时间点的滞留份额相对值非常接近。由于所关注的AMAD粒径为0.01~5 μm范围内,粒径对吸入后的滞留份额影响显著,条件允许情况下,有必要调查受照者吸入镅气溶胶的粒径分布。
3.2 新旧模型比较
由于当前国标仍然采用旧模型的内照射数据,随着近年来ICRP对三种生物动力学模型的修改,新旧模型的异同对于当前内照射评价来说是非常重要的。因此本文以工作人员(平均呼吸速率1.2 m3/h)吸入AMAD5 μm镅气溶胶后的滞留份额为例,按照不同吸收入血类型进行新、旧模型的定量比较,比较结果列于表2~4。

表1 不同AMAD粒径相对AMAD 5 μm的滞留份额相对值(新模型, M类241Am)1)

表2 新旧模型计算的S类241Am吸入后滞留份额对比
3.2.1S类镅气溶胶吸入后新旧模型对比
由表2可见,工作参考人吸入S类AMAD5 μm的241Am气溶胶后,中长期(1 000天及以上)的肺部滞留份额,新模型计算值显著高于旧模型,一万天时高出6倍多;中长期(1 000天及以上)的骨骼、肝脏滞留份额,随着时间推移,新模型计算值比旧模型越来越高。短期(1 000天以内)的肺部、骨骼、肝脏计算值新旧模型差异不大。
3.2.2M类镅气溶胶吸入后新旧模型对比

表3 新旧模型计算的M类241Am吸入后滞留份额对比
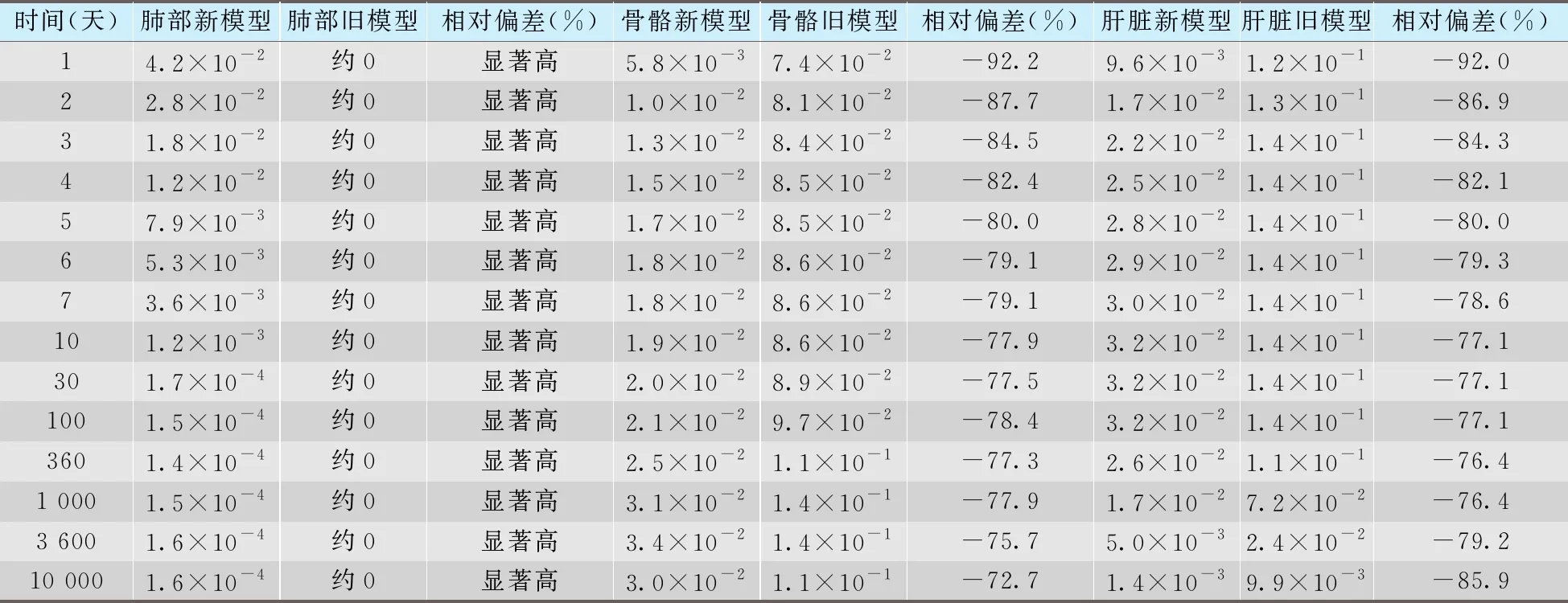
表4 新旧模型计算的F类241Am吸入后滞留份额对比

图12 吸入不同AMAD粒径241Am的肝脏滞留份额的差异(M类)
由表3可见,对于工作参考人吸入M类AMAD5 μm的241Am气溶胶后:中长期(1 000天及以上)的肺部滞留份额新模型显著高于旧模型,且差异巨大;骨骼、肝脏滞留份额新模型计算值明显低于旧模型,这是因为新模型由肺进入血液的镅更少导致。短期(1 000天以内)的肺部滞留计算值差异不大。
3.2.3F类镅气溶胶吸入后新旧模型对比
由表4可见,对于吸入F类AMAD5 μm的241Am气溶胶的工作参考人的计算,肺部滞留份额新模型比旧模型显著高,新模型肺部各个时期都保留有很小份额,这个份额从30天开始很稳定,而旧模型从第一天开始肺部镅就接近0;骨骼、肝脏滞留份额,新模型计算值比旧模型更低,这是因为新模型肺部滞留份额更多,从肺部进入血液的镅更少,导致从血液进入骨骼、肝脏的镅更少。
4 结论
与权威数据对比后,证明了基于新、旧模型的自编程序正确。以工作参考人(呼吸速率平均1.2 m3/h)吸入AMAD5 μm241Am气溶胶为例,采用新模型计算分析了所关注库室的滞留份额随时间的变化曲线,曲线对比发现:对于S类镅气溶胶吸入,1 000天以后主要滞留在肺部、骨骼;F类镅主要富集在骨骼、肝脏器官中,因为F类核素从肺部快速吸收入血,从血液转移到富集器官;M类镅在肺部、骨骼、肝脏中均有相当的滞留份额(300天内)。因此对于不同吸收类型,内照射直接测量的重点应有所针对性。另外对影响滞留份额的参数不同取值分析后发现:(1)不同吸收入血类型、不同AMAD粒径对肺、骨骼、肝脏滞留份额影响显著,内照射评价时需要对吸入粒子的吸收入血类型和AMAD粒径进行调查;(2)特定AMAD粒径的滞留份额相对AMAD5 μm的相应滞留份额的相对值比较固定。
以工作参考人吸入不同吸收类型的AMAD5 μm的241Am气溶胶为例,根据新、旧模型的自编程序计算结果对比,发现了新、旧模型计算值的异同:
(1)对于肺部滞留份额,S类、M类镅气溶胶吸入后肺部滞留在短期(1 000天以内)接近,中长期(1 000天以上)新模型显著更高(高数倍及更大),肺部长期滞留M类比S类新、旧模型差异更大;对F类镅从第一天开始新、旧模型计算的肺部滞留份额差异巨大,新模型认为F类镅在肺部一直保留较小份额而旧模型认为肺部滞留很快接近0。
(2)对于骨骼、肝脏滞留份额,S类镅气溶胶吸入后,中长期计算值新模型显著高于旧模型,短期计算值新旧模型相近。对于M、F类镅,新模型计算的骨骼、肝脏滞留份额明显低于旧模型,且F类镅新、旧模型差异比M类镅更显著。
由于相比旧模型,新模型中的呼吸道模型增大了肺部的长期滞留,吸收入血参数做了修改,新模型中的镅的系统模型的骨骼的长期沉积也做了调整,导致了上述新旧模型滞留份额预测值在一些时间段特别是中长期的差异较大。因此对基于直接测量的放射工作人员吸入镅后的内照射评价的建议是:针对新旧模型滞留份额差异较大的情况,采用新模型滞留份额预测值更符合内照射监测数据的最新研究成果。
