过渡金属氧化物催化氧化甲醛的研究进展
2021-03-15董雅鑫刘凯苏晨光卢素红郑政赵威
董雅鑫,刘凯,苏晨光,卢素红,郑政,赵威
(西安石油大学 化学化工学院,陕西 西安 710065)
甲醛(HCHO)作为典型的室内污染物之一,主要来源于装修装饰材料和家具的释放,释放周期长达3~15年。甲醛是高毒性物质,可与人体蛋白质中的氨基酸结合引起细胞死亡[1]。另外,甲醛属于挥发性有机化合物(VOCs)在大气中具有很强的光化学活性,会对环境造成一定污染[2]。因此,减弱、消除甲醛对保护空气环境和人类健康具有重大意义。
热催化氧化法利用催化剂在低温条件下将甲醛转化为CO2和H2O,操作条件易控制、效率高、无二次污染、节能,被称为最理想的方法。该方法的关键是催化剂的选择,主要包括贵金属催化剂[3-5]和过渡金属氧化物催化剂[6-9]。过渡金属氧化物催化剂因其资源丰富、成本低等优点成为学者们的研究热点。通过对过渡金属氧化物掺杂改性(如与其它金属氧化物复合、负载贵金属、添加碱金属)来提高催化剂的活性和稳定性。本文着重介绍目前较为常用的4类过渡金属氧化物催化剂,并对各类催化剂进行分析、总结,希望为开发设计催化氧化甲醛的催化剂提供参考与借鉴。
1 单一金属氧化物催化剂
1.1 锰氧化物催化剂
锰氧化物较其它过渡金属氧化物具有毒性低、活性高、稳定性强、结构和形貌多样等特点,被广泛应用于甲醛的催化降解。早在2002年,Sekine等[10]发现MnO2对甲醛的去除率高达91%且产物中不含CO等有害副产物。这一成果吸引了众多学者对锰氧化物进行大量研究,包括晶体结构、形貌、价态等。
氧化锰基于[MnO6]八面体排布出各式各样的晶型结构,如α-Mn2O3、β-MnO2、γ-MnO2、α-Mn3O4、γ-Mn2O3和Mn5O8,并形成1D隧道、2D层状和3D网状等不同维度的隧道结构,不同的结构具有不同的物理化学性质,其催化性能也存在差异。Zhang等[11]采用水热合成法制备出α-,β-,γ-和δ-等4种晶型结构的MnO2,其中,具有2D层状结构的δ-MnO2表现出最高的催化活性,在80 ℃将212.5 mg/m3的HCHO完全转化。其高活性归因于特殊的隧道结构增加了晶格氧的数量,δ-MnO2表面拥有最活跃的氧物种。锰氧化物的晶型结构受反应条件的影响,当反应温度处于120 ℃以下时,不同晶型结构的锰氧化物催化活性顺序为:隐钾锰矿MnO2>水钠锰矿MnO2>斜方锰矿Mn2O>单斜MnOOH。隐钾锰矿的有效孔径为0.26 nm与甲醛分子直径0.243 nm接近,有利于甲醛吸附至催化剂表面并进入晶格中进行氧化分解[12-13]。
不同的晶型结构呈现出粒状、棒状、管状及球状等形态迥异的MnO2,形貌的变化会影响比表面积、孔结构和活性位等因素。Yu等[13]采用不同的制备方法合成出茧状、海胆状和巢状MnO2催化剂(图1),结果发现,茧状和海胆状MnO2的比表面积(247.6 m2/g和62.3 m2/g)都大于巢状MnO2(56.9 m2/g),但催化活性顺序为巢状>海胆状>茧状。因为巢状MnO2的多孔结构有利于获得反应活性位,促进甲醛扩散和气体传输。
锰氧化物中锰元素可变的价态使锰氧化物晶体内部易存在缺陷、空位,有利于氧的移动、储存。Wang等[14]研究发现部分结晶的MnO2体系中共存Mn2+、Mn3+和Mn4+且Mn4+的含量高于Mn2+和Mn3+。该催化剂在85 ℃时可将甲醛完全转化,当RH为60%时,11 h后甲醛的消除率保持在78.6%。分析认为,高价态的Mn物种有利于催化剂表面产生更多氧空位,氧空位的增加有利于氧分子的吸附、活化和转移,形成大量表面活性氧物种,这对于甲醛氧化反应是至关重要的,因为催化性能的好坏是甲醛与表面活性氧直接反应的结果。
综上,利用氧化锰结构多变的特点设计高活性的晶相结构(水钠锰矿和隐钾锰矿)有利于甲醛吸附和氧化;特殊的形貌(如巢状、球状)有利于获得多孔结构,提高表面活性氧的迁移率;高价态的锰物种(Mn4+)有利于催化剂表面产生大量氧空位,提供更多活性位点。
1.2 钴氧化物催化剂
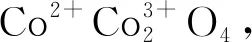
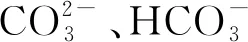
预处理对Co3O4催化剂的内在机制有着直接影响,张叶等[16]将制备的Co3O4催化剂在N2和O2气氛下于不同温度进行预处理。发现O2可修复Co3O4表面的氧空位,N2可诱导催化剂表面产生Co3+不饱和配位中心和弱配位氧负离子。在200 ℃活性氧与甲醛反应生成的双配位甲酸盐物种易转变为单配位甲酸盐物种,进而分解为CO2和H2O(转化途径见图1),因此,Co3O4-N2-200表现出最佳的催化活性、选择性和稳定性。在150 ℃甲醛的转化率为100%,100 ℃时CO2的选择性为85%,经过700 min CO2的选择性稳定在82%左右。

图1 Co3O4催化剂上甲醛反应的转化途径[16]Fig.1 Conversion pathway of formaldehyde over Co3O4 catalyst[16]

除MnOx、Co3O4外,CeO2、Fe2O3、TiO2、Cr2O3催化剂在催化氧化甲醛反应中也具有一定的活性。整体而言,MnOx和Co3O4对甲醛的催化性能高于其它过渡金属氧化物,因此研究较为普遍。然而相对于锰氧化物,钴氧化物的研究还不够透彻,有报道指出钴氧化物催化剂的形态结构对其催化性能影响较大,但迄今为止对Co3O4的形貌结构研究甚少,今后有必要对构效关系进行深入探究。另外,对其它新型过渡金属氧化物的挖掘和探索也是特别重要的。
2 复合金属氧化物催化剂
为提高单一金属氧化物的低温氧化活性和稳定性,Ce、Si、Cu、Fe等原子半径大、M—O键能弱、电负性低的金属或金属氧化物常被添加到锰和钴氧化物中制备复合金属氧化物催化剂。复合金属氧化物之间的协同作用可改善活性组分的氧化还原能力和材料的耐湿性。
2.1 锰基复合氧化物
Ce因优异的储氧性、Ce3+和Ce4+之间稳定的氧化还原循环以及与其它金属间的强相互作用,常用于催化剂的掺杂改性。Zhu等[18]研究了不同掺杂比例的Ce改性水钠锰矿MnO2催化剂,由于Ce3+的半径大,Mn4+的半径小,Ce的加入抑制了MnO2晶体生长,导致Ce-MnO2的结晶度变差,颗粒尺寸变小从而比表面积增大。CeO2与MnO2形成固溶体使得CeO2-MnO2催化剂表面活性氧数量增多,迁移率增强,Ce-MnO2(1∶10)在100 ℃将190 mg/L HCHO完全转化。
无定形SiO2较高的比表面积和高度分散活性组分的能力为催化剂提供了优良载体。朱荣辉等[19]采用自组装法合成出具有大比表面积(164.85 m2/g)和丰富活性位点(Mn3+,75.6%)的MnO2/SiO2催化剂,该催化剂在90 ℃的甲醛转化率为90%,连续反应6 h去除效率仍保持80%以上。
最早出现的铜锰复合氧化物是霍加拉特催化剂,主要用于对瓦斯气的防护,后来人们发现它对VOCs气体污染物也具有较好的催化作用。陈莹等[20]采用简单的氧化还原法制备了一系列铜锰氧化物用于降解甲醛,研究表明,Cu的掺杂缩小锰的晶格结构,增加氧空位数目,为氧物种的吸附提供更多吸附位。当n(Cu/Mn)为1/2、煅烧温度为300 ℃时,铜锰复合催化剂表现出最佳的催化性能,90 ℃将甲醛完全转化。
Fe2O3也是深度氧化VOC活性催化剂的一种。高小红等[21]通过共沉淀法合成出无定形的MnOx-Fe2O3催化剂,无定形的晶相结构有利于反应物在催化剂表面发生快速吸脱附和氧化还原反应,MnOx-Fe2O3完全转化甲醛的温度为80 ℃。500 h寿命试验发现HCHO 转化率降为95%,催化剂发生失活现象的主要原因是碳酸盐化。
由上可知,MnOx-CeO2、MnOx-SiO2、MnOx-CuO和MnOx-Fe2O3等锰基复合氧化物催化剂具有相似的甲醛催化性能,主要以固溶体形式存在,结构呈无定形态。过渡金属与Mn掺杂造成晶格畸变,增加了催化剂的比表面积和氧空位数量。但目前锰基复合氧化物催化剂在100 ℃左右能够达到理想的甲醛去除效果,其低温氧化活性还有待提高。
2.2 钴基复合氧化物
Co-Mn复合氧化物也是研究的重点,2012年,Shi等[22]首次利用Co-Mn氧化物作为氧化HCHO的催化剂,在GHSV为60 000 h-1、RH为50%的条件下,CoMn(3/1)-CP在75 ℃可将HCHO完全转化。其优异的催化性能源于Mn进入Co3O4晶格中形成MnxCo3-xO4固溶体产生大量表面活性氧基团。
与上述传统工艺制备的Co-Mn氧化物不同,Wang等[23]采用纳米铸造工艺合成的3D有序介孔Co-Mn氧化物(3D-CoMn-HT)具有独特的储存-氧化-再生循环性和耐湿性,储存容量为0.8 mmol/g,在70 ℃甲醛的转化率达100%,即使在RH=90%、空速GHSV=160 000 mL/g·h的条件下仍可保持高反应活性,主要得益于3D-CoMn-HT催化剂较大的比表面积和有序的介孔结构。
Co、Mn和Ce等过渡金属具有相近的理化性质,形成复合物后活性组分之间的协同作用可大幅度提高催化性能。Lu等[24]采用柠檬酸溶胶-凝胶法制备的Co3O4-CeO2催化剂相较与纯Co3O4和CeO2得出:CeO2加入到Co3O4后活性组分高度分散,比表面积由15.6 m2/g增加至75.6 m2/g,二者的协同作用增强了Co3O4-CeO2催化剂的氧化还原性。n(Co/Co+Ce)为0.95时Co3O4-CeO2催化剂在80 ℃可将100 mg/L HCHO完全转化。
三金属催化剂可进一步提升催化效果,成为近期研究的热点之一。Wu等[25]考察了三金属MnCo3MOx(M=Ce,La,Pr)对甲醛的去除效率,当Mn/Co/Ce的摩尔比为1/3/7时,室温下可将甲醛全部转化。分析认为,Ce进入MnCo3Ox中形成稳定的固溶体增加了MnOx-Co3O4-CeO2的比表面积,更多氧活性位点在表面暴露,有利于甲醛的氧化反应。
由此可见,钴基复合氧化物在催化氧化甲醛反应中表现出优异的催化活性,但需要指出的是,催化剂的构效关系十分复杂,目前钴基复合氧化物的反应机理尚不明确,需对此进行研究。另外,三金属催化剂为合理设计低温甚至室温下消除甲醛的催化剂提供了新选择,具有良好的应用前景。
2.3 MOFs衍生物催化剂
金属有机框架(MOFs),又称多孔配位聚合物(PCPs),是由无机金属离子或金属团簇和有机配体通过配位键连接而成的一种新型有序固体材料,具有特殊的晶体性质、超大的比表面积及可调控的结构,在各个领域应用广泛。
MOFs作为前驱体通过热分解转化的MOFs衍生物材料具有优异的催化活性。Liu等[26]通过原位热解Mn-Ce-MOFs前驱体得到一系列不同摩尔比的MnOx-CeO2,其中,MnOx-CeO2(5∶5)具有最高的低温氧化活性和稳定性,在40 ℃可完全氧化HCHO,加入5% H2O后转化率仍保持在99.0%以上。分析认为,通过煅烧Mn-Ce-MOFs前驱体增强了MnOx与CeO2之间的相互作用,使MnOx-CeO2具有较高的高比表面(560 m2/g)、良好的低温还原性和丰富的表面活性氧。Sun等[27]以MOFs为牺牲模板合成出多孔Co3O4/ZnO催化剂,焙烧温度为400 ℃时,高比表面积和多孔结构的4Co/Zn表现出优异的催化活性。
MOFs在热解过程中,金属离子直接转化为金属氧化物纳米颗粒均匀的分散在框架内;有机配体转化为多孔碳结构,避免金属氧化物纳米晶发生潜在聚集。MOFs衍生物催化剂的比表面积通常>1 000 m2/g, 高达7 000 m2/g,孔径通常为0~3 nm,高达 9.7 nm[28]。MOFs除了直接作活性组分外,还可以作为载体用于甲醛的催化氧化反应。虽然MOFs衍生物催化剂比传统金属氧化物催化剂更具优势,但MOFs材料稳定性较差以及MOFs材料的催化性能和结构关系缺乏系统研究。
3 负载贵金属的过渡金属氧化物催化剂
以过渡金属氧化物为载体负载低含量的Pt、Au、Ag等贵金属应用于甲醛催化氧化反应中可有效提高催化剂的催化性能。贵金属分解甲醛的过程基本相似(图2),甲醛首先吸附在催化剂表面形成DOM物种,然后被活性氧氧化为甲酸盐,甲酸盐直接分解为CO和H2O,最后CO与O2反应生成CO2;另一种途径是中间体DOM转化为甲酸,甲酸经氧化成为碳酸,碳酸分解为CO2和H2O。
Pt是第一个被发现在低温下对甲醛具有高催化活性的贵金属,1% Pt/TiO2在20 ℃就可将HCHO 完全转化为CO2和H2O[29-30]。Pt与载体之间相互作用产生Pt-O活性中心具有很强的活化分子氧能力,可诱导产生大量表面吸附氧,氧含量的增加可大大提高甲醛转化率。

图2 贵金属催化剂分解甲醛的反应过程Fig.2 The reaction process of HCHO decomposition on noble metal catalyst
Au常被用于打造首饰和器皿,在人们的惯有认知中是一种惰性元素,几乎不与任何物质反应,但它作为活性组分在甲醛氧化反应中却表现出良好的催化活性。Au负载在过渡金属氧化物催化剂(CeO2、α-MnO2、Co3O4-CeO2)上,带电的Au物种作为活性中心可增加活性组分表面质子数,提高催化剂的氧化还原性,Au/Co3O4-CeO2在39 ℃将HCHO完全转化[31-33]。
Ag的氧化活性略差于Pt和Au,但其价格相对低廉,因此从降低成本的角度来讲,Ag基催化剂具有广阔的发展空间。Huang等[34]制备了Ag/MnCeOx催化剂用于催化降解甲醛,表征结果显示均匀分散在载体表面的Ag纳米粒子增强了MnOx的活性,增加了表面活性氧的种类,提高了氧迁移率,削弱了表面Mn—O键,在常温下超过90%的低浓度HCHO[(1.0 ±0.5) mg/m3]在36 h内完全降解。
负载贵金属Pt、Au、Ag的过渡金属氧化物催化剂在甲醛氧化反应中表现出较高的催化效率,一方面,贵金属本身可以提供大量活性位;另一方面贵金属与载体之间形成强相互作用共同完成甲醛的氧化过程。但贵金属昂贵的价格限制了其大规模应用,相对地,Ag基催化剂价格低廉,在一定程度上可降低工艺成本。另外,对于贵金属易失活,寿命短的问题还应深入探究其原因及改进措施。
4 添加碱金属的过渡金属氧化物催化剂
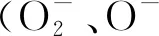
适量碱金属的引入可提升催化剂表面氧物种的活性,增加羟基含量,提高反应速率,缩短反应时间,是一种简单易行的方法。
5 结语
通过对单一金属氧化物、复合金属氧化物、负载贵金属和添加碱金属等4类过渡金属氧化物催化剂研究分析,得出以下结论:
(1)单一金属氧化物的催化性能因晶型结构、形貌、价态而异,具有高活性晶型结构、特殊形貌和高价态的金属氧化物具有较高的催化HCHO性能。相对而言,单一钴氧化物的催化性能劣于锰氧化物。
(2)复合金属氧化物催化剂主要以固溶体形式存在,结构呈无定形状。金属氧化物之间的协同效应增加催化剂的比表面积和缺陷位数目,增强氧化还原性。特别地,MOFs衍生物催化剂以其特定的结构性质最大化的发挥了催化氧化作用。
(3)负载Pt、Au、Ag等贵金属的过渡金属氧化物催化剂,一方面,贵金属的活化能力强可提供大量活性位点;另一方面,与载体形成强相互作用共同完成甲醛的氧化过程。
(4)适量碱金属添加至过渡金属氧化物中不仅能提高表面氧物种的活性,而且增加了羟基含量。
随着热催化氧化技术的不断发展,对净化甲醛催化剂的研究越来越深入。主要方向为:①每种催化剂都有各自的优缺点,在充分利用催化剂优点的同时需探寻新的方法来解决其缺点带来的不利影响,如将过渡金属氧化物负载至高度分散的载体上以避免团聚失活;②不断探索新的活性组分或具有特殊结构的材料,通过对活性组分掺杂改性或利用特殊材料固有的优势来提高催化剂的性能;③全面了解反应机理是设计开发高性能催化剂的基础,有待利用更先进的表征手段对催化剂的构效关系进行深入而具体的研究,从根本上加以认识和理解。
