双氯芬酸钠乳膏处方的优化及体外释放度考察
2021-03-15赵晓军刘影
赵晓军,刘影
(1.锦州医科大学附属第三医院;2.锦州医科大学,辽宁 锦州 121000)
双氯芬酸钠属于非甾体类抗炎药,具有解热镇痛、抗炎的作用,其镇痛活性是吲哚美辛的6倍,阿司匹林的40倍。解热作用是吲哚美辛的2倍,阿司匹林的350倍。临床上用于缓解类风湿性关节炎、骨关节炎、痛风性关节炎,是疼痛发作期的常规用药。该药口服吸收快,半衰期短,达峰时间快,临床疗效好, 但在水中溶解度较小,对胃肠道的刺激性较大,患者不易耐受,降低了双氯芬酸钠的药物疗效,限制了该药在治疗骨关节肿痛方面的广泛使用[1-2],本实验将双氯芬酸钠制成软膏剂局部外用给药。软膏剂可以避免口服药可能发生的肝首过效应及胃肠灭活,提高疗效;能够维持恒定的最佳血药浓度,减少胃肠给药的副作用;还可以延长作用时间,减少给药次数;通过改变给药面积调节给药剂量,减少个体内和个体间差异,患者可以自主用药也可以随时停药[3]。一般剂型一日多次给药后所产生的血药浓度峰谷波动性不易避免,即便是口服用的缓释剂型也排除不了胃肠道吸收部位的差异,而透皮给药制剂采用比较稳定的皮肤局部用药,在给药期间的吸收总量和速度不会出现明显的改变。
1 材 料
1.1 仪器设备
L-2000型高效液相色谱仪(日本日立分光公司);HLD型电子天平(上海力辰科技有限公司);85-2WS型磁力搅拌器(上海沪析有限公司);电热鼓风干燥箱(易诚仪器设备有限公司);BCD-235WE3CX型美菱冰箱(合肥美菱股份有限公司);SN-LSC离心机(盐城市凯特实验仪器有限公司);微孔滤膜(深圳逗点生物科技有限公司);透皮渗透吸收仪(上海玉研科学仪器有限公司)。
1.2 试剂
双氯芬酸钠原料药(批号:20180927,广州杨叶生物科技有限公司);双氯芬酸钠对照品(批号:20180723,深圳恒丰万达医药科技有限公司);吐温80(江苏省海安石油化工厂)、十八醇(江苏省海安石油化工厂)、单硬脂酸甘油酯(天山药业);羊毛脂(天山药业)、凡士林(南昌白云药业有限公司)、甘油(天津市致远化学试剂公司)、山梨酸钾(天津市致远化学试剂公司);乙腈(深圳恒丰万达医药科技有限公司)、甲醇(深圳恒丰万达医药科技有限公司)、冰醋酸(河南凯帝荣誉出品)。
1.3 动物
小鼠、家兔均由锦州医科大学动物养殖处提供。
2 实验过程
2.1 乳膏剂的制备
2.1.1 双氯芬酸钠乳膏剂的质量评估方法:(1)润滑无刺激、黏稠度适中、均匀且细腻、易于涂布;(2)耐热试验与耐寒试验:将双氯芬酸钠软膏剂放在乳膏盒中,在60 ℃的烘箱中放置6 h,-20 ℃的冰箱中放置24 h,取出乳膏待恢复到室温,观察乳膏是否出现发硬、油水分层、合并与破裂等现象;(3)离心实验:取双氯芬酸钠乳膏剂适量放在离心管中,在5000 r/min的速度下离心共25 min,观察离心试验后的乳膏剂是否会出现水油分离的现象[4-5]。
2.1.2 通过初步筛选,吐温80(A)、凡士林(B)、羊毛脂(C)、十八醇(D)是决定双氯芬酸钠乳膏剂稳定性的主要因素,将以上4个组分作为考察因素,每个因素设置3个水平[6-7],见表1。
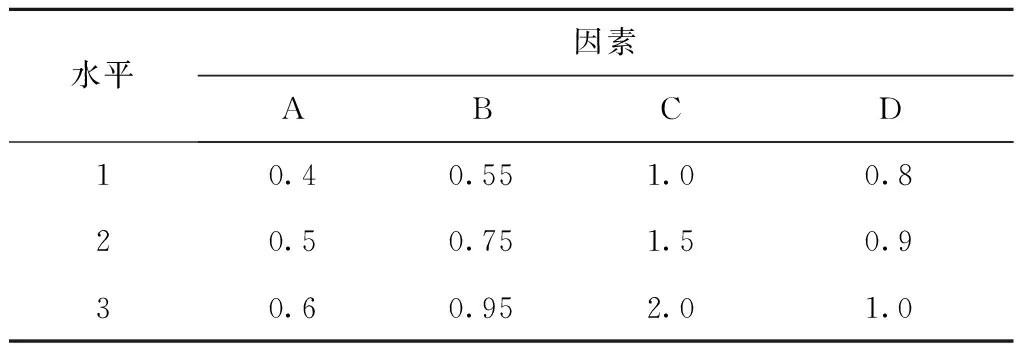
表1 正交设计因素与水平表
按照正交设计表L9(34)进行试验,共构成9组配方,每个处方总量为10 g,按照2.1.1项下双氯芬酸钠乳膏剂的质量评估方法进行评分,外观性状占10分,离心实验占10分,耐热耐寒试验占10分,正交试验设计结果见表2。
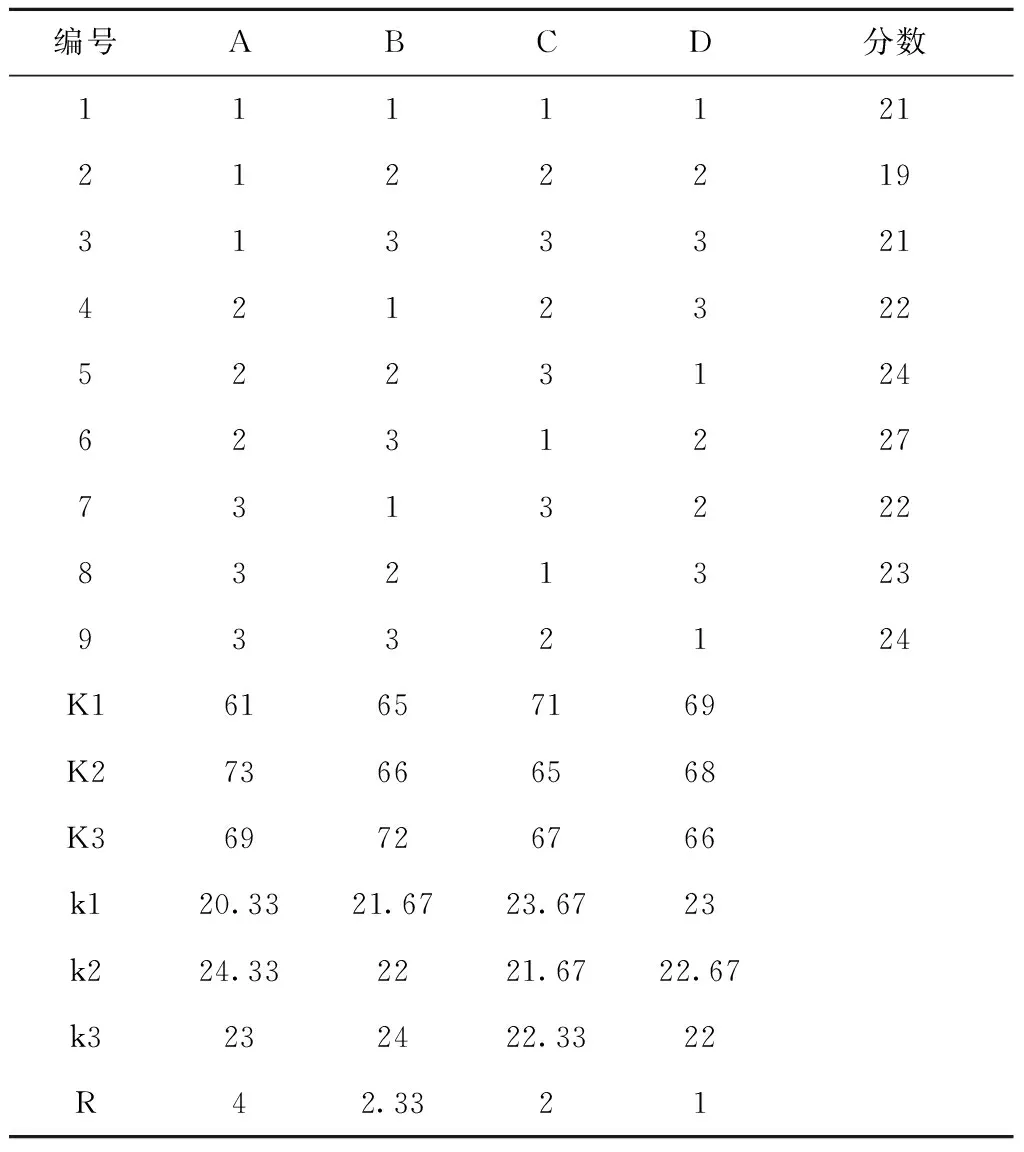
表2 双氯芬酸钠乳膏处方的正交试验设计与结果
正交设计表中R值越大对试验结果影响越大,k值最大者为最佳因素,根据表2结果,通过直观分析可以看出各因素对双氯芬酸钠乳膏剂稳定性的影响顺序为吐温80>凡士林>羊毛脂>十八醇,即A>B>C>D,乳膏剂的最佳处方为A2、B3、C1、D1。
通过方差分析得出因素A、B的P值<0.05,说明差异有统计学意义,因素C对试验结果有影响,因此A和B是主要的因素,C和D 是次要的因素,最佳处方为A2、B3、C1、D1,见表3。
2.1.3 防腐剂的选择:吐温80能与羟苯酯类、季铵盐类等络合进而抑制防腐剂的效能,使防腐剂失去活性,因此本实验选用山梨酸作为防腐剂,用量约为0.20%。
2.1.4 透皮吸收促进剂的选择:良好的透皮促进剂应该对皮肤没有任何刺激作用,没有药理作用,不致敏皮肤,物理化学性质均稳定,易溶于药物和材料,起效快,作用时间长。本实验选用月桂氮卓酮为促渗透剂,其有效浓度常在1%~6%范围内。
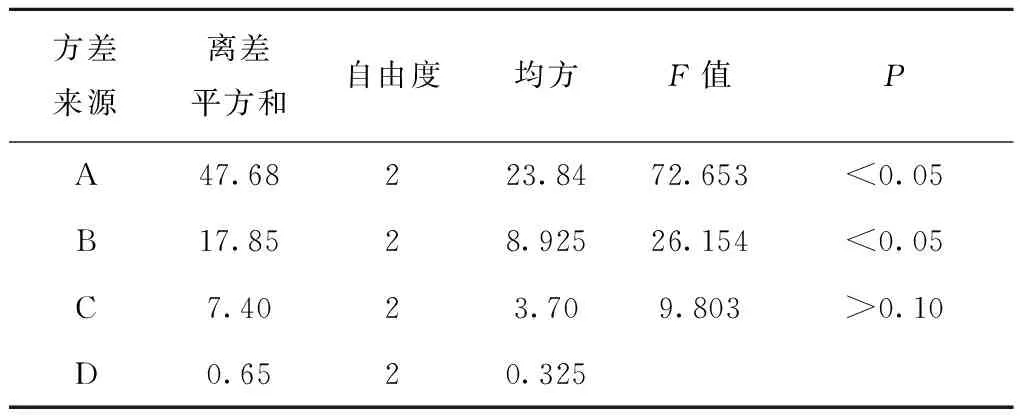
表3 双氯芬酸钠乳膏剂的方差分析结果
2.1.5 最终处方:经查阅文献[8-9]及市场上已有外用制剂双氯芬酸钠的含量为0.9%~1.3%,本处方将双氯芬酸钠含量定位1%,因此最终处方为双氯芬酸钠0.1 g,硬脂酸0.7 g,吐温80为0.5 g,十八醇 0.8 g,羊毛脂1.0 g,凡士林 0.95 g,甘油1.0 g,月桂氮卓酮0.5 g,山梨酸钾0.02 g,去离子水加至10 g。
2.1.6 软膏剂制备:按照2.1.5项下处方量将硬脂酸、十八醇、羊毛脂、凡士林、月桂氮卓酮加热到80 ℃熔化为油相,双氯芬酸钠、甘油、吐温80、山梨酸钾、去离子水加热到80 ℃溶化为水相,使油相和水相均完全溶解,然后将水相缓慢的加入到油相中,边加水相边搅拌,直到冷凝即得乳膏剂。
2.1.7 验证试验:按最优处方制备双氯芬酸钠乳膏,按照2.1.1项的方法对乳膏剂进行稳定性考察,结果显示所制得的双氯芬酸钠乳膏剂符合质量要求。
2.2 双氯芬酸钠乳膏剂的体外透皮实验
2.2.1 色谱柱:C18柱(260 mm×4.7 mm);流动相:甲醇0.005 mol/L磷酸二氢钾溶液(pH =3.8) (70∶30) ,检测波长280 nm;取对照品溶液10 μL注入液相色谱仪[10],见图1。
2.2.2 制备标准曲线:精密称取双氯芬酸钠对照品10 mg,置于50 mL量瓶中使双氯芬酸钠溶解,用甲醇稀释至刻度。然后用甲醇分别稀释成浓度为0.24、0.4、0.8、2.4、4.8、7.2 μg/mL的溶液,采用高效液相色谱法测定,双氯芬酸钠在此范围内线性方程为y=81345.1259x+21423.1893,r=0.9999。
2.2.3 仪器精密度试验:精密吸取储备液5.0 mL,配成浓度为5.0 μg/mL的双氯芬酸钠溶液,重复进样3次,双氯芬酸钠峰面积的RSD为0.87%。

图1 双氯芬酸钠对照品色谱图
2.2.4 体外透皮试验:取小鼠将其断颈处死,用剪刀将小鼠腹部体毛剃净,再用硫化钠溶液脱掉剩余鼠毛,取腹部无损伤处皮肤,用0.9%的氯化钠溶液冲洗小鼠皮肤内表面,把处理好的小鼠皮肤放在扩散池上室和下室中间,角质层应朝向上方,甲醇作为接收液,取0.5 g双氯芬酸钠乳膏均匀涂布于小鼠皮肤上,扩散池放在37 ℃水浴中搅拌,分别于2、4、6、8、10、12 h 取样,取样后同时补加同温度等体积的接受液[11-16]。样品用0.45 μm 微孔滤膜过滤,取10 μL样品注入高效液相色谱仪计算累积渗透量(Q),计算公式如下,见表4。

表4 双氯芬酸钠乳膏剂的累积渗透量(Q)

时间(h)累积渗透量(μg/cm2)123平均值(μg/cm2)225.6426.5826.8926.37434.5335.5235.8235.29645.1844.8945.7345.27857.5658.2857.7357.861071.2670.8771.5471.221283.4784.2384.3984.03
以累积渗透量Q(μg/cm2)对时间(t)制作的曲线可知双氯芬酸钠乳膏剂的渗透量随时间的延长逐渐增大,且几乎等速率增加,回归方程为Q=5.8383t+12.472,R2=0.9940,P<0.05,说明双氯芬酸钠乳膏剂具有很好的渗透性,见图2。
2.3 双氯芬酸钠乳膏剂的皮肤刺激性试验
取家兔16只,雌雄各半,给药前24 h剃净背部脊椎两侧兔毛,分为完整皮肤组和破损皮肤组。其中8只完整皮肤组随机分成两组,即空白对照组、双氯芬酸钠乳膏组,分别将1 g乳膏均匀涂抹于背部脊椎两侧,另8只家兔用注射针在完整皮肤上划出数条划痕以渗血为宜,分组及给药方法同正常皮肤组,每8 h给药1次,24 h后用生理盐水清洗掉乳膏剂。分别于给药后1、24、48、72 h时观察涂抹部位有无红斑和水肿等情况及恢复情况[17-20]。
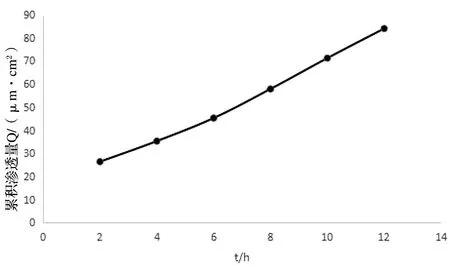
图2 双氯芬酸钠乳膏剂的释放曲线
试验结果表明完整皮肤刺激试验中涂抹双氯芬酸钠乳膏与涂抹空白乳膏的家兔皮肤均未出现红斑和水肿,表明双氯芬酸钠乳膏无刺激性。破损皮肤刺激试验中在划痕区涂抹双氯芬酸钠乳膏和空白乳膏后,均未见红斑及水肿,同样表明双氯芬酸钠乳膏无刺激性。
3 讨 论
在实际应用中发现乳膏长期贮存后有时会出现破乳、分层、絮凝等不稳定现象,本实验采用正交设计法优化双氯芬酸钠乳膏处方,结果表明本处方可以有效避免乳膏剂的不稳定问题。
吐温80为双氯芬酸钠乳膏的主乳化剂,其用量关系到乳膏制剂的稳定性和有效性;凡士林化学性质稳定,无刺激性,但仅能吸收5%的水,加入适量的羊毛脂可提高凡士林吸水性与渗透性,两者合用可以起到很好的保湿作用,十八醇既可作辅助乳化剂,又具有调节乳膏稠度的作用,提高软膏剂的稳定性能。
常用的透皮吸收促进剂有表面活性剂、二甲基亚砜及其类似物、月桂氮卓酮等,表面活性剂类促进渗透效果差,连续应用后会引起红肿、干燥或粗糙化。二甲基亚砜长时间大量应用对皮肤有刺激性和恶臭,甚至引起肝损害和神经毒性等,通过透皮渗透实验表明选用月桂氮卓酮为促渗透剂效果良好。
体外透皮渗透实验结果表明双氯芬酸钠软膏剂具有良好的渗透性能,且对完整皮肤及破损皮肤均无刺激性,进而更好的发挥临床作用。
