不同病因肝硬化失代偿患者临床特征及长期预后危险因素的前瞻性队列研究
2021-03-15杜静园颜华东
杜静园 颜华东
肝硬化是一种进行性慢性肝病[1],当病程进入失代偿阶段,反复出现并发症事件及合并器官衰竭时,患者生存质量下降,预后较差[2],近年来欧美前瞻性研究均表明器官衰竭决定了肝硬化患者的死亡率[3-4]。引起肝硬化的病因有多种,西方国家多以酒精性肝病为主[5-7],在中国乃至亚洲地区病毒性肝炎尤其是乙型病毒性肝炎则是最常见的原因[8-9]。
目前认为,肝硬化不再是不可逆转的疾病,消除病因能使得肝纤维化消退[10-11],甚至失代偿期恢复到代偿期状态,从而改善患者预后,延长中位生存时间。这一现象不仅在动物实验中得到证实,也可在不同病因的慢性肝病患者间观察到[12-16]。因此,通过病因对肝硬化失代偿患者进行临床特征及预后分析,根据不同病因制定针对性治疗方案,对控制肝硬化失代偿患者病程进展,改善其长期预后具有重要意义。本文旨在探讨病因与肝硬化失代偿患者长期预后的关系及其在DC患者长期预后预测中的作用研究。
资料与方法
一、 研究对象
收集中国科学院大学宁波华美医院肝病科2014年7月至2017年6月期间住院患者,入选患者均符合肝硬化失代偿的相关诊断标准,患者均签署知情同意书。并排除:(1)年龄<18岁或者>80岁;(2)肝脏恶性肿瘤超出米兰标准及其他晚期恶性肿瘤患者;(3)合并严重心衰、尿毒症、脑梗死、呼吸衰竭等疾病患者;(4)妊娠;(5)HIV患者。
二、 病因及基本资料
对所有纳入研究的患者均评估病因,病因分为乙型肝炎、乙型肝炎合并酒精性肝病、酒精性肝炎、其他病因和不明原因。所有入选的肝硬化失代偿患者入院时完善年龄、性别、体质指数、平均动脉压、糖尿病等基本资料,评估CTP评分、MELD评分、MELD钠评分。
三、 临床检测指标
入院后对生化、血常规、凝血酶原时间等指标进行检测,包括白细胞(WBC)、血红蛋白(HBG)、血小板(PLT)、丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、总胆红素(TBil)、白蛋白(Alb)、血清肌酐(Cr)、血钠、国际标准化比值(INR)。
四、 临床治疗及随访
所有患者入院后评估并发症,同时均接受病因治疗及利尿、护肝、止血等内科综合治疗。所有患者都接受至少2年随访,并记录随访结局。
五、 统计方法
数据均用SPSS 16.0统计软件进行统计学处理,正态分布以均数±标准差表示,2组比较采用one-way ANOVA,非正态分布以中位数(四分位数差值)表示,2组比较采用Kruskal-Wallis检验;计数资料比较采用χ2检验。对患者进行随访,以2年病死率作为患者预后的判断指标,COX单因素及多因素回归分析患者2年死亡相关的危险因素。Kaplan-Meier生存曲线分析不同病因与肝硬化失代偿患者预后的关系。P<0.05为差异有统计学意义。
结 果
一、患者基线指标水平
本研究共筛选865例患者,剔除212例,最终643例患者纳入研究,其中男性434例(67.5%),女性209例(32.5%),平均年龄(57.8±12.4)岁,体质指数为(22.8±3.4) kg/m2,MAP (88.6±13.5) mmHg,患有糖尿病116例(18.0%),既往失代偿肝硬化患者307例(47.7%)。乙型肝炎病因患者最多,共计317例,占总人数的49.3%,其次为酒精性肝炎患者,共122例,占19.0%,同时有乙型肝炎合并酒精性肝病患者共60例,占9.3%,再次为其他病因患者,共82例,占12.8%,最后为不明原因患者,共62例,占9.6%。患者入院事件中最常见的是腹水,共431例(67.0%),然后依次为上消化道出血174例(27.1%),细菌感染128例(19.9%)和肝性脑病88例(13.7%)。患者2年死亡235例,病死率36.5%(见表1)。
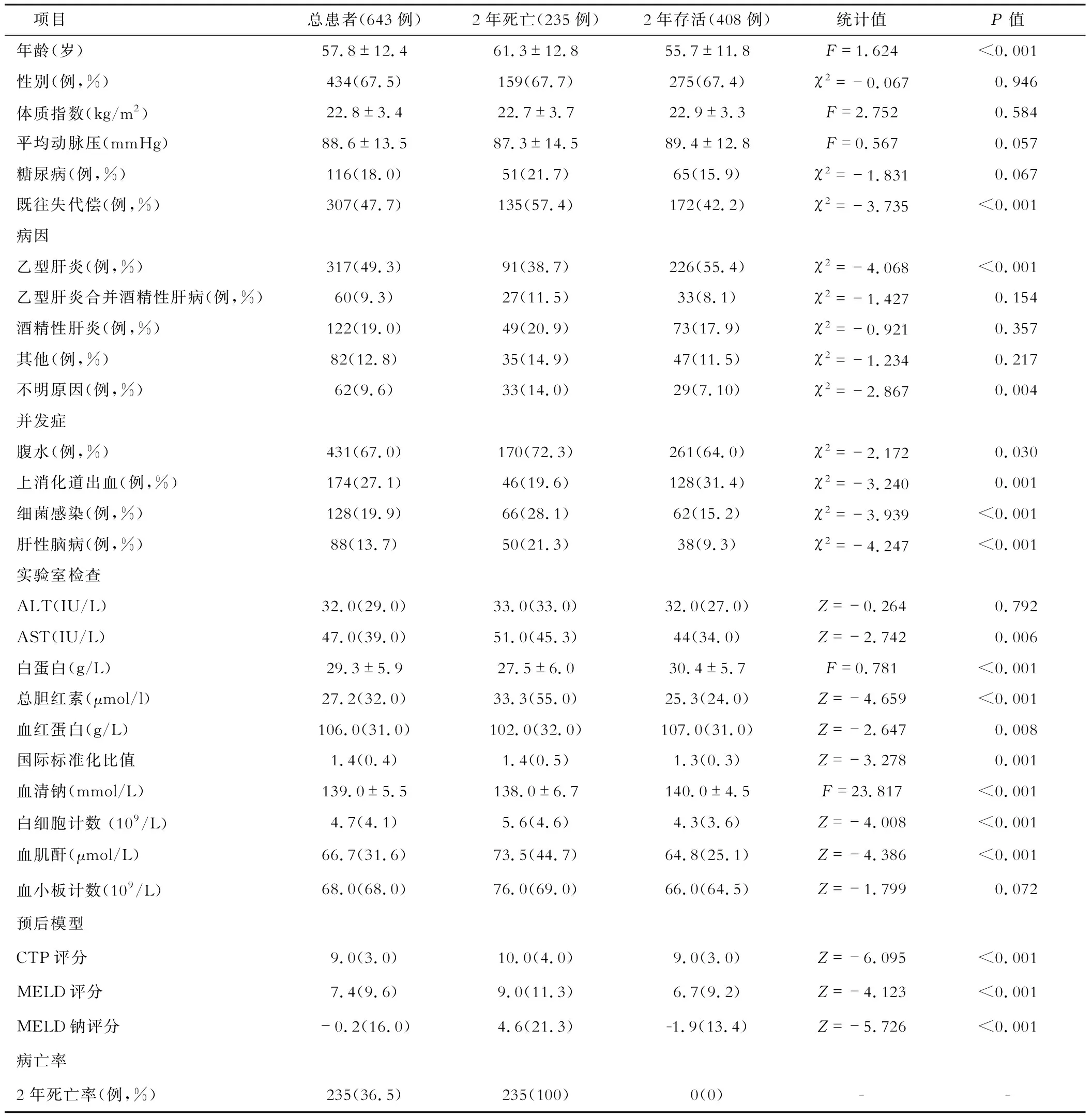
表1 肝硬化失代偿患者基线人口学及临床特征数据不同病因比较 [例,M(QR)]
二、不同病因肝硬化失代偿患者临床特征比较
对比单纯乙型肝炎病因与酒精性肝炎病因DC患者,酒精性肝硬化平均年龄大,男性占比高;酒精性肝炎患者有更高的AST、白细胞计数、血肌酐、血小板计数以及更低的血红蛋白、INR和血清钠(P值均<0.05)。乙型肝炎病因患者较酒精性肝炎患者MELD评分和MELD钠评分更高,而两者之间腹水、上消化道出血、细菌感染及肝性脑病等并发症差异无统计学意义(P值均>0.05),酒精性肝炎病因DC患者2年死亡率显著高于乙型肝炎病因患者(P值<0.05)(见表2)。
进一步分析不明原因DC和乙肝病因患者临床特征,不明原因肝硬化失代偿患者年龄显著大于乙型肝炎病因,女性占比大(P值均<0.05);并发症方面,上消化道出血的发生率更低,但细菌感染的发生率显著增加(P值均<0.05);实验室指标上有更低的ALT、AST及更高的PLT;预后方面,MELD评分、MELD 钠评分等模型得分也较低,但2年死亡率更高(P值均<0.05,见表2)。
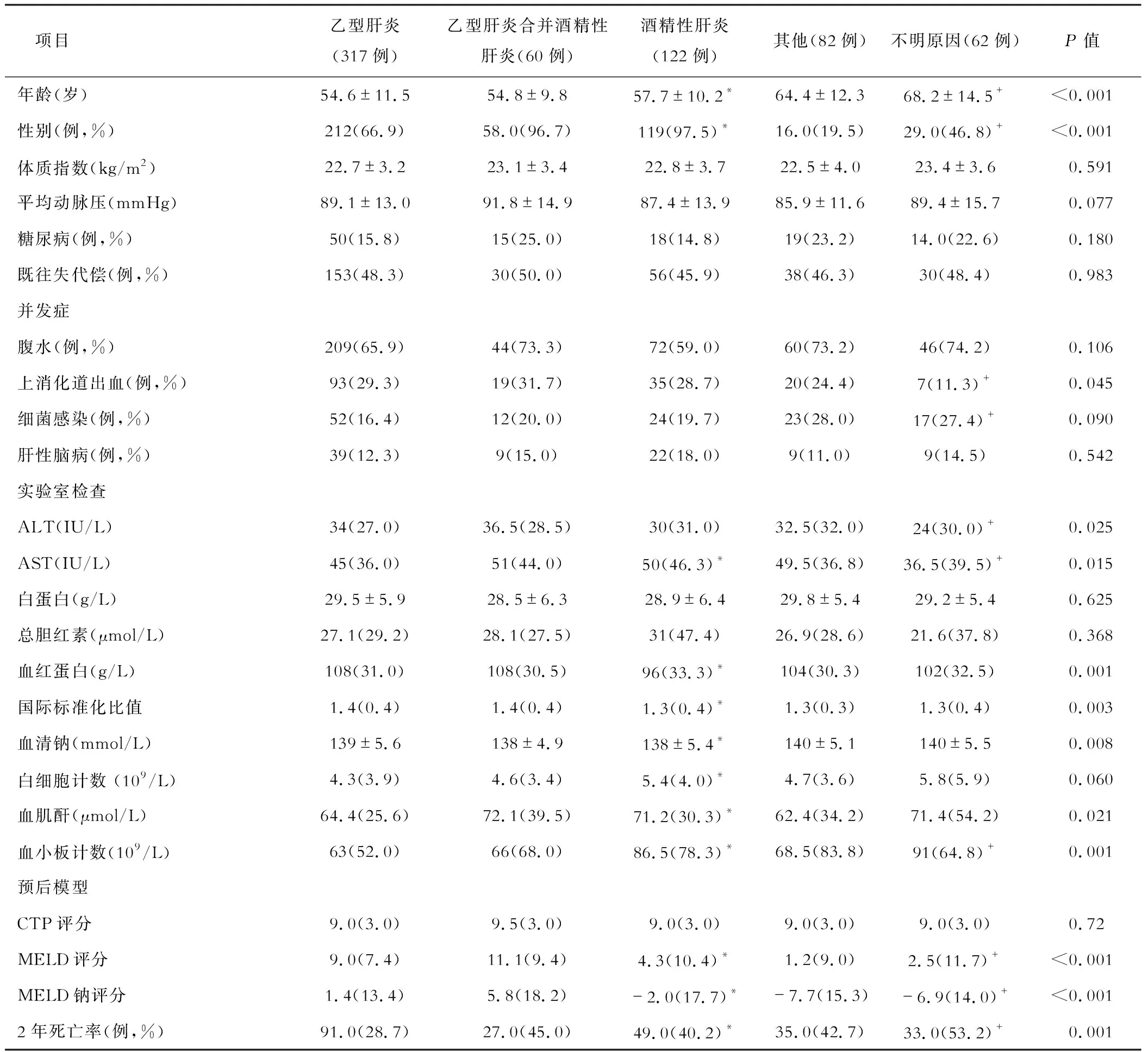
表2 肝硬化失代偿不同病因患者比较 [例,M(QR)]
三、患者2年死亡率的COX单因素与多因素回归分析结果
对随访2年存活和死亡的患者进行分组,死亡患者年龄更大,存在肝硬化既往失代偿比例更高(P值均<0.05)。在此次入院失代偿事件中,死亡组患者腹水、细菌感染及肝性脑病的发生率高于存活组,而上消化道出血的发生率低于存活组(P值均<0.05)。在实验室指标中,死亡组有更高的AST、TBil、INR、WBC、肌酐值,Alb、血红蛋白及血钠则较存活组更低(P值均<0.05)。病因上,死亡组乙肝病因患者比例明显低于存活组,且不明病因患者比例更高,其差异均有统计学意义(P值<0.05,见表1)。
COX单因素回归分析影响患者2年病死率的因素,包括年龄、MAP、糖尿病、肝硬化既往失代偿、病因、腹水、上消化道出血、细菌感染、肝性脑病、AST、Alb、TBil、INR、血钠、WBC、Cr、PLT及相关预后模型等(见表3)。对其进行COX多因素回归分析,结果显示,年龄、病因、血钠、PLT、Alb及MELD评分入选回归方程,为肝硬化失代偿患者预后的重要影响因素(见表4)。
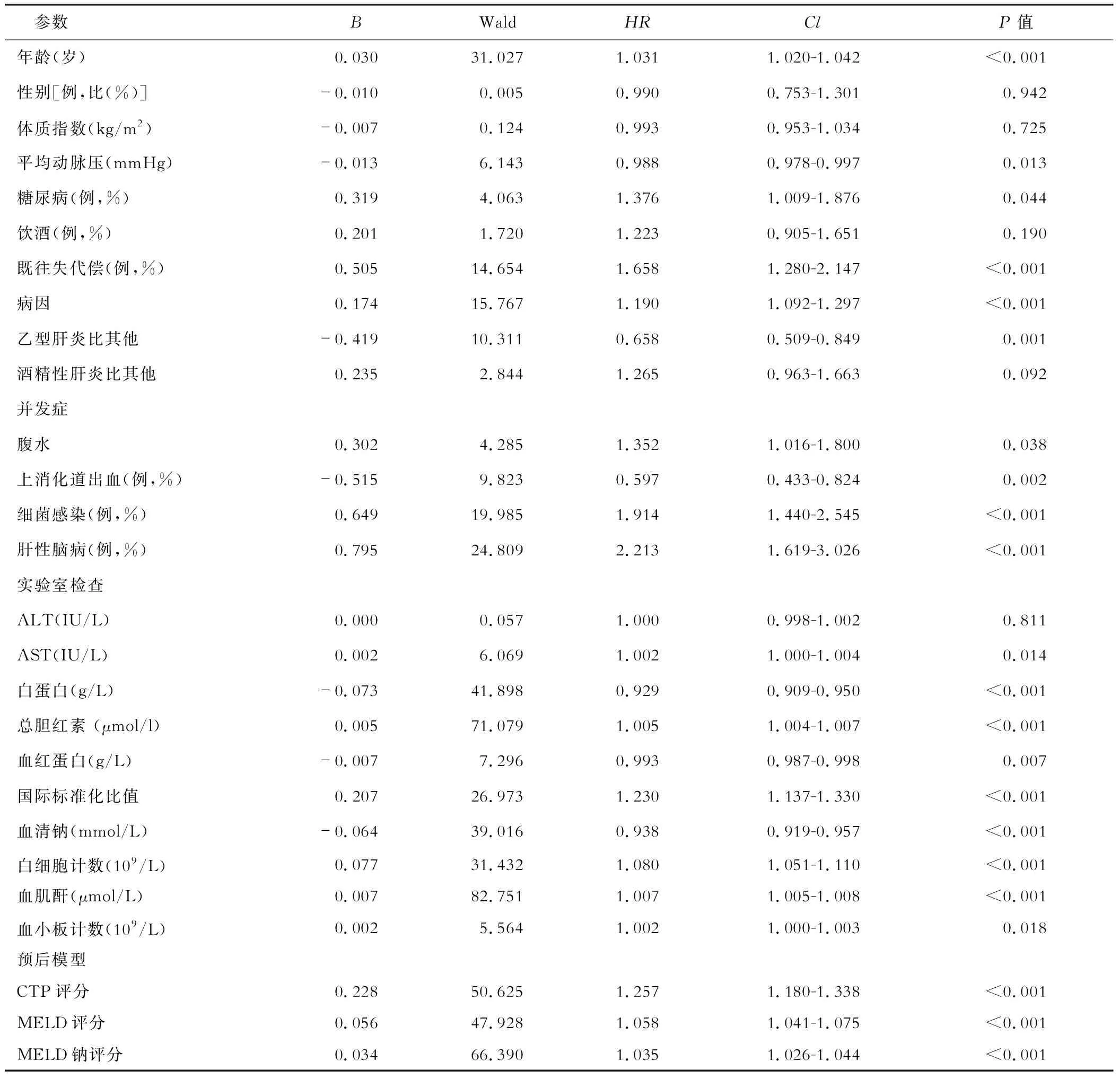
表3 影响患者2年死亡率的COX单因素与多因素回归分析结果
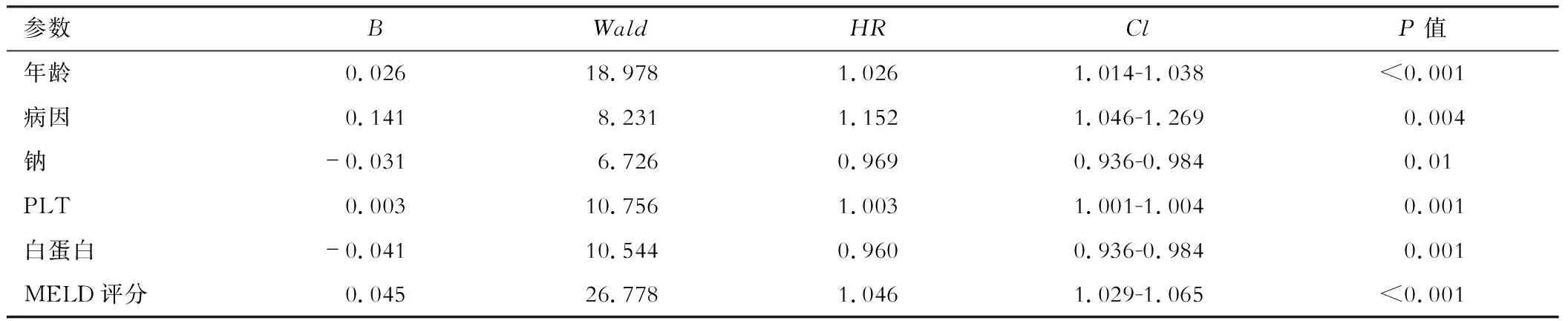
表4 影响患者2年死亡率的COX多因素回归分析结果
四、KM生存曲线
在肝硬化失代偿患者中将病因分为乙型肝炎、乙型肝炎合并酒精性肝病、酒精性肝病、其他病因和不明原因,不同病因2年和5年死亡KM曲线差异有统计学意义(P<0.05)。见图1。
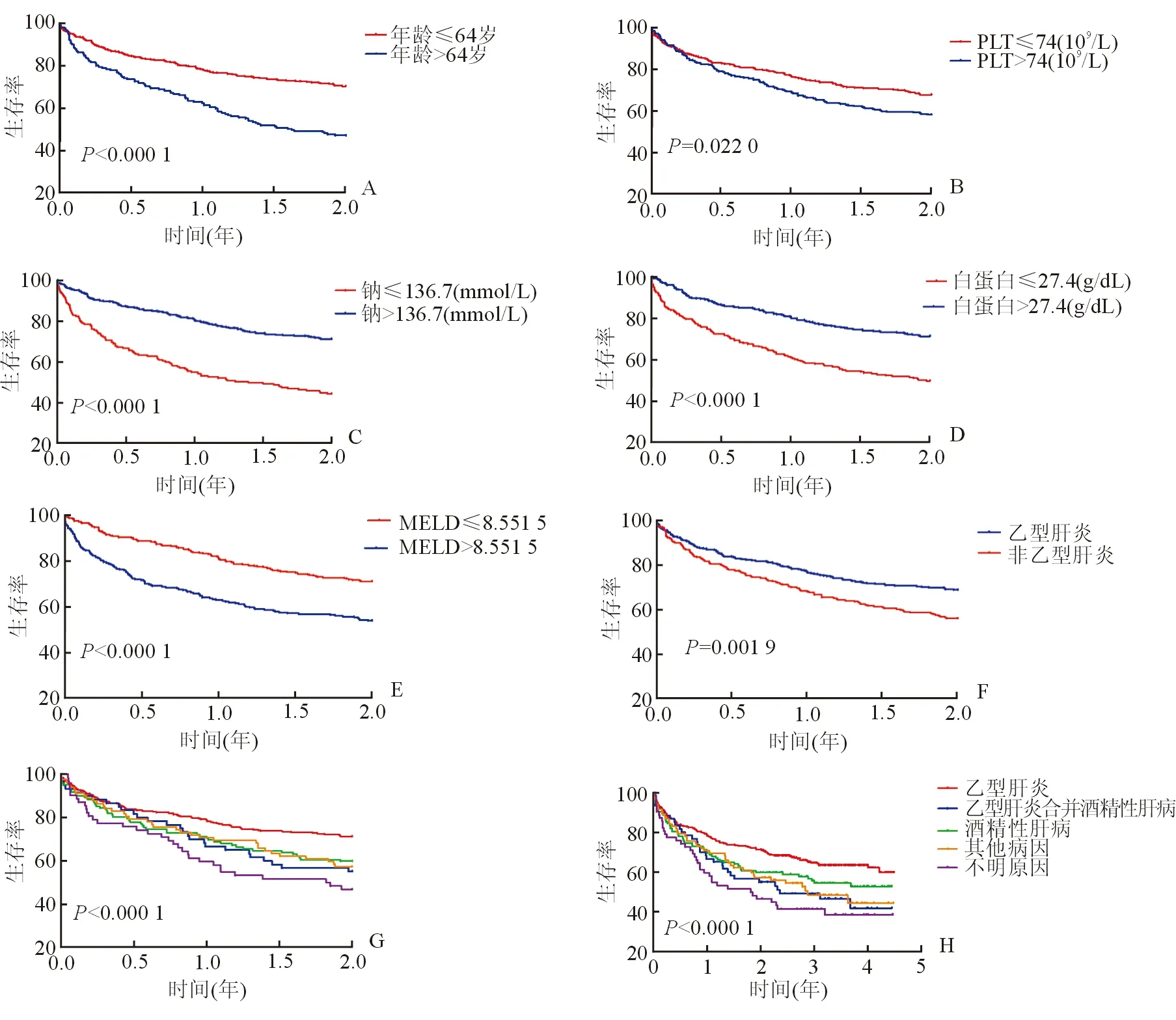
图1 肝硬化失代偿患者中长期KM生存曲线
讨 论
本研究通过前瞻性纳入643例肝硬化失代偿患者,根据病因将其分为乙型肝炎、乙型肝炎合并酒精性肝炎、酒精性肝炎、其他病因和不明原因肝病。我们发现,乙型肝炎相关性肝硬化占总研究人群的49.3%,是肝硬化失代偿患者最主要的病因,这与国内其他学者的研究结果相一致[17-18]。乙型肝炎肝硬化失代偿患者显然更年轻,具有更高的ALT和INR值,表明乙型肝炎病因的肝功能受损更严重,白细胞计数相较非乙型肝炎相关肝硬化失代偿患者更低,或许与细菌感染发生率低有关。从组间2年病亡率比较来看,乙型肝炎相关肝硬化失代偿患者长期预后最好,这可能与抗病毒手段的应用有关,干扰素的维持治疗及拉米夫定的使用能有效降低肝硬化失代偿风险并延长患者生存期[19],在已出现失代偿患者中,抗病毒治疗也能显著改善肝硬化自然史,从而提高生存率[20]。随着乙型肝炎疫苗的广泛应用,乙型肝炎相关肝病比例较既往有所下降,同时酒精性肝病比例逐渐凸显[18],本研究发现,酒精性肝病是肝硬化失代偿的第二大病因,本组患者中性别特征尤为明显,因为我国饮酒者以男性居多。目前尚无精准的酒精相关肝硬化治疗手段,唯一有效的是长期戒酒,但受患者依从性影响,效果不佳,使得酒精性肝硬化失代偿患者2年预后较乙型肝炎病因患者差。本研究发现,不明原因肝硬化失代偿患者仅占9.6%,但值得重视的是,此组患者2年预后最差,由于未找到明确病因,临床上难以制定病因治疗方案,仅靠对症处理无法延缓肝硬化自然进程。随着科技手段的发展,基因组分析或能成为临床上病因不明肝硬化的诊断工具,从组织学上提示可能的病因[21]。
本研究入组的643例本院住院患者均规范诊治管理,随访2年死亡率36.5%。对肝硬化失代偿患者2年死亡进行COX单因素及多因素分析,发现年龄(HR: 1.026;CI: 1.014~1.038)、血钠(HR: 0.969;CI: 0.936~0.984)、PLT(HR: 1.003;CI: 1.001~1.004)、病因(HR: 1.152;CI: 1.046~1.269)、白蛋白(HR: 0.960;CI: 0.936~0.984),MELD评分(HR:1.046;CI: 1.029~1.065),为死亡的独立危险因素。乙型肝炎病因肝硬化失代偿患者长期预后明显好于非乙型肝炎病因患者,将是否为乙型肝炎病因纳入长期预后评估,有利于临床医生整体了解肝硬化失代偿患者长期生存状况,更有针对性地制定治疗方案。
本研究因随访时间长,未对死亡患者进一步调查追踪死亡原因,故仍需继续完善死亡患者死因,研究不同病因患者死因的差异。
