囊内出血对儿童大囊型淋巴管畸形硬化治疗效果的影响
2021-03-13宁金波姚明木黄峥嵘陈思远
谢 民 宁金波 姚明木 陈 强 黄峥嵘 陈 斌 陈思远
近年来,因淋巴管畸形(lymphatic malformation,LM)就诊的患者人数逐渐增多,其中合并出血已成为常见多发病。淋巴管畸形以往多采用手术切除治疗,但某些特殊部位的病例切除困难,容易损伤周围神经、血管,且术后容易复发[1,2]。由于硬化治疗损伤小、不需要手术、治疗后不留瘢痕,深受病患欢迎。通过文献检索,对淋巴管畸形合并出血后进行硬化治疗的报道较少[3]。由于聚桂醇硬化治疗淋巴管畸形的疗效确切,并发症少,2016年1月至2017年12月重庆大学附属三峡医院儿外科对22例大囊型淋巴管畸形出血的患者采用聚桂醇进行硬化治疗,现报道如下:
材料与方法
一、临床资料
以重庆大学附属三峡医院儿外科收治的50例大囊型淋巴管畸形患者为研究对象,男31例、女19例,年龄1个月至13岁9个月,平均5岁2个月,均以体表包块就诊,经包块彩超和MRI确诊为大囊型淋巴管畸形。再根据包块穿刺抽出物性质将患者分为出血组(抽出物为陈旧性暗红色不凝血性液体,22例)和未出血组(抽出物为淡黄色清亮液体,28例)。其中出血组13例为突发体表包块,9例为原有包块突然增大,8例有外伤史,14例就诊原因不明;未出血组28例全部以体表包块就诊。包块位于颈部32例、腋下5例、肩背部3例、胸壁3例、腹壁2例、头顶部1例、四肢4例。两组患者的年龄及包块分布比较无显著差异。
二、方法
患者均在彩超引导下行包块穿刺,抽尽囊内液体后向囊腔内注射聚桂醇注射液,注药剂量为抽出液体量的1/8~1/4,治疗结束后局部加压包扎2~3天,对颌下包扎困难的部位可在包块上方放置2~3张与包块表面积相当的纱布块后再用下颌袋固定(图1)。15 d后随访包块大小变化,对包块未消失者采用相同方法进行第2次治疗,直至包块消失或者连续治疗3次后包块无变化为止。
三、观察指标
①通过临床观察和彩超检查测量包块大小变化判定疗效。显效:包块消失,且1年内无复发;有效:包块缩小50%以上,1年内不再增大;无效:包块缩小50%以下或治疗后1年内复发。显效率+有效率=总有效率。②用彩超测量第一次硬化治疗15 d后包块大小的变化。③治疗后包块消失或者连续治疗3次后包块无变化情况下最终包块大小。④达到显效标准所用的治疗次数。
四、统计学处理
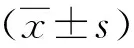
结 果
患者均成功在彩超引导下经皮穿刺抽尽囊液后向囊腔内注射聚桂醇注射液进行硬化治疗。两周后随访包块大小变化,第一次治疗后出血组显效4例,有效9例,无效9例,总有效率59.09%;未出血组显效10例,有效14例,无效4例,总有效率85.71%;两组间疗效比较差异具有统计学意义(χ2=4.539,P<0.05)。后续治疗出血组与未出血组包块的变化均不如第一次明显,但最终两组包块均完全消失(图1),有效率均为100%,其中出血组平均治疗(3.55±1.26)次;未出血组平均治疗(2.57±1.35)次,二者比较差异具有统计学意义(t=2.611,P<0.05)。治疗后4例轻微发热、11例局部肿胀伴轻微疼痛,观察2~3天后均消失,通过2个月至1年半时间随访无严重不良反应发生。
讨 论
淋巴管畸形可发生在身体的任何部位,约75%的病变发生在头颈部,其次是腋下、纵膈及四肢[4,5]。本组50例有32例位于颈部、1例位于头顶部、5例位于腋下、4例位于四肢、其余8例位于躯干,分布与报道相似。LM一般在2岁前发病,约一半的患者出生后即可被发现,表现为先天性体表包块;也有部分患者先天性体表包块不明显,往往在外伤或感染后出现包块,导致囊内出血或化脓。

图1 颈部及颌下淋巴管畸形出血的硬化治疗效果 A.治疗前颈部及颌下突发性包块; B.治疗后局部加压包扎; C.治疗4次后包块消失; D.治疗前MRI显示颈部及颌下囊性包块; E.治疗后3个月复查MRI显示包块消失
LM出血或者感染可根据囊内积血或积脓鉴别,淋巴管畸形合并出血有其特殊的临床特点,包括: ①突发性体表包块或原有包块突然增大,能准确描述的患者常伴有疼痛; ②彩超检查包块为单囊或多囊结构,其囊内液体回声有细小光点漂移; ③MRI检查包块呈多房囊状长T1、长T2信号及其线样等信号分隔影; ④包块穿刺抽出陈旧暗红色不凝血性液体。当然,LM出血后还具备其它一些特点:如包块囊壁穿刺活检可见淋巴管内皮细胞伴出血;囊腔内造影检查可显示囊腔的分布以及囊腔之间的交通情况;包块核素扫描可能会发现核素在出血的淋巴管囊腔内集聚等。但穿刺活检为有创操作,可能会加重囊内出血而带来不必要的麻烦,加之LM出血前其囊液清亮,出血以后为暗红色不凝血性液体,二者之间可以明确鉴别,因此临床上一般少用。
LM造影基本上可获得与MRI相似的影像结果,但检查比MRI复杂,需作囊腔穿刺注射造影剂,同样有加重出血的可能,临床上一般未使用。LM的出血是非活动性的,核素扫描检查价值不大。临床上遇到的特殊现象是LM出血的病例中一半以上为无先天性包块(13/22,59.1%)患者,少部分有明确外伤史(8/22,36.4%),大部分原因不明(14/22,63.6%),应当引起儿科医生的重视。
大囊型淋巴管畸形的治疗方法主要包括手术切除和硬化剂注射治疗,手术治疗与硬化治疗均可取得良好的治疗效果,对手术和硬化治疗效果不佳者也可采用西地那非口服治疗[6-9]。由于手术往往难以完整切除病灶,病灶部位特殊病例手术风险大,有损伤邻近神经、血管可能,局部遗留永久瘢痕而影响美观,甚至导致功能障碍,一些患者因此留下终身残疾,且术后复发率高[10,11]。近年来,随着硬化技术的发展,越来越多的学者主张采用硬化剂治疗大囊型淋巴管畸形[12]。硬化剂注入囊腔后通过刺激淋巴细胞产生非特异性炎症,促使局部成纤维细胞和胶原纤维增殖,抑制淋巴内皮细胞的生长,并使其膨胀和发生空泡变性,从而使淋巴管闭塞和硬化,达到缩小病变面积的目的[13]。常用的药物包括平阳霉素、博来霉素、沙培林、聚桂醇、无水乙醇等,各种硬化剂治疗大囊型淋巴管畸形的效果都比较良好,究竟使用哪一种硬化剂与淋巴管畸形类型及不同学者的经验有关[14-16]。
对于淋巴管畸形合并出血后的治疗报道较少,本组22例采用聚桂醇硬化治疗取得了比较满意的治疗效果,最终包块均完全消失。但首次治疗效果明显低于未出血组,包块完全消失治疗的次数明显增多,可能与囊腔内出血以后淋巴管内皮细胞肿胀进而影响药液吸收有关。也可能因出血时机未稳定,治疗后囊腔内继续出血,稀释硬化剂浓度影响治疗效果。还可能因囊腔内出血以后血细胞和血浆蛋白阻塞淋巴管道而影响药物在各个淋巴囊腔内的均匀分布,延迟药物作用的时机和效果。使用聚桂醇硬化治疗LM出血时的用药剂量参照未出血病例,为囊腔穿刺抽出液体量的1/8~1/4。由于使用聚桂醇泡沫与原液治疗的效果基本相当,且使用聚桂醇原液比使用泡沫更简单,还可在一定程度上避免囊腔内注入空气后导致感染,因此本组病例均采用聚桂醇注射液原液进行囊腔内注射,用药剂量为5~20 mL[3]。治疗结束后使用2~3张与包块表面积相当的纱布块局部加压包扎2~3天,对颌下等包扎困难的部位可用下颌袋固定,防止药液渗漏及囊腔内再出血稀释药液而影响治疗效果,并且有利于药液扩散进入扩张的淋巴管及囊泡内,使药液与病变部位充分接触。治疗间隔时间定为15 d是考虑到治疗后1周注入药物时间短,硬化剂尚未起到充分的作用,有部分患者治疗1周后淋巴管囊腔内囊液生成甚少,行包块穿刺和注药均困难,且这部分患者的囊腔既可能缩小,也可能增大,临床上还需继续观察,而部分患者3~4周后囊腔内囊液生成较多,造成患者家长对治疗效果满意度降低。
由于治疗时间短,病例数量有限,对大囊型淋巴管畸形并发囊内出血的病例进行硬化治疗时是否需与未出血病例区别对待、是否需选择特殊的治疗时机和药物剂量等问题需要在将来的工作中作进一步探索。
