左乳癌保乳术后瘤床同步推量断层螺旋照射与断层定角照射的放疗剂量学研究
2021-03-12袁美芳文晓博刘梦岚
袁美芳, 文晓博, 刘梦岚, 吉 维, 杨 毅, 赵 彪
(昆明医科大学第三附属医院/云南省肿瘤医院 放疗科, 云南 昆明, 650118)
研究[1-2]显示,早期乳腺癌保乳手术联合放射治疗可取得与根治术相近的治疗效果,同时很好地保留了乳房功能。乳腺癌调强放疗技术能改善乳腺受照射剂量的均匀性,同时减少周围正常组织受照射剂量,减轻正常组织放疗损伤和降低并发症的发生率[3-5]。螺旋断层放疗(TOMO)是目前较为先进的调强放疗技术之一,其主要技术特点是治疗过程中通过治疗床的移动对整个靶区进行全方位的断层旋转照射,即断层螺旋(TH)治疗模式; 同时,该技术也可以设定多个角度,对整个靶区实施定角断层照射,即断层定角(TD)治疗模式。本研究分析左乳癌保乳术后银夹标记瘤床同步推量TH和TD两种断层放疗技术的剂量学特点,现将结果报告如下。
1 资料与方法
1.1 一般资料
选取本院2018年3月—2020年5月行左乳癌保乳术后银夹标记瘤床同步推量放疗的患者20例,年龄33~67岁,中位年龄45.20岁; 肿瘤TNM分期为T1N0M07例, T1N1M07例, T2N0M06例,均为浸润性导管癌。
1.2 体膜固定和大孔径CT定位扫描
患者仰卧于体部固定板正中并双手抱住肘关节置于额头,患者体中线与固定板中线基本重合,调整患者体位至舒适状态。采用热塑体膜固定后,在大孔径CT机(Somatom Sensation Open, 24排,孔径85 cm)上进行定位扫描,扫描范围从C2椎体下缘至L3椎体上缘,层厚、层间距均为5 mm, 将医学数字图像与通讯(DICOM)数据传输至放射治疗计划系统(TPS)进行勾画和计划设计。
1.3 勾画靶区及危及器官
参考美国肿瘤放射治疗协作组织(RTOG)乳腺癌保乳术后靶区勾画标准,以银夹为中心向外扩1.5 cm, 外界为皮下0.5 cm, 内界为胸壁内缘,生成计划肿瘤靶区(PGTV)。临床靶区(CTV)的上界为锁骨头下缘,下界为乳腺皱褶下2.0 cm, 前界为皮下0.5 cm, 后界为胸壁与肺的交界处,左界为胸骨和肋骨接合处,右界为腋中线。CTV外扩0.5 cm生成计划靶区(PTV), 前界为皮下0.5 cm, 后界为胸壁与肺的交界处。危及器官包括左肺、右肺、右侧乳腺、心脏、脊髓。
1.4 治疗计划设计
采用安科锐TOMO治疗计划系统设计TH和TD计划,均给予相同处方剂量与限制条件, 6 MV的X线,处方剂量均为PGTV 5 750.0 cGy/25F, PTV 5 000.0 cGy/25F。TH计划野宽度2.5 cm, 螺距0.21, 调制因子4; TD计划以内外切线野为基础,每间隔15°添加1个照射野,一般射野角度以290、305、320、150、135、120°为基础,根据靶区形状进行微调,共6野。靶区剂量要求: ① PGTV要求98%的靶区体积受到的辐射剂量(D98)≥5 463 cGy, 50%的靶区体积受到的辐射剂量(D50)≥5 750 cGy, 2%的靶区体积受到的辐射剂量(D2)≤6 037 cGy; ② PTV要求D98≥4 750 cGy,D50≥5 000 cGy,D2≤6 037 cGy。危及器官剂量限值: 脊髓D2≤4 500 cGy, 心脏受到20 Gy辐射剂量的体积(V20)≤30%, 平均辐射剂量(Dmean)≤800 cGy; 左肺V20≤30%; 右肺受到5 Gy辐射剂量的体积(V5)≤30%,V20≤5%; 右乳Dmean≤500 cGy。
1.5 计划剂量学参数评价
靶区剂量学参数参考国际辐射单位与测量委员会(ICRU)83号报告,靶区适形指数(CI)=(Vtref/Vt)×(Vtref/Vref), 其中Vt为靶区体积,Vtref为参考处方剂量线覆盖的靶区体积,Vref为处方剂量线覆盖的体积, CI值越大提示适形度越好。均匀性指数(HI)=(D2-D98)/D50, HI值越小提示均匀性越好。危及器官评价: 左肺V5、V10、V20和Dmean, 右肺V5和Dmean, 右乳腺Dmean, 脊髓D2, 心脏Dmean。
2 结 果
2.1 两种计划的靶区剂量学参数比较
两种计划的PGTV比较, TH计划D2、D98、D50、CI高于TD计划,其中CI的差异有统计学意义(P<0.05); 两种计划的PTV比较, TH计划D98和CI高于TD计划,D50低于TD计划,但TD计划D2略优于TH, 差异均有统计学意义(P<0.05), 见表1。
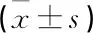
表1 两种计划的靶区剂量学参数比较
2.2 左肺、右肺、右乳腺、脊髓和心脏的剂量学参数比较
TD计划的左肺V5、V10、V20, 右肺V5、Dmean, 右乳腺Dmean, 脊髓D2以及心脏Dmean均低于TH计划,差异均有统计学意义(P<0.05), 见表2。
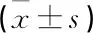
表2 左肺、右肺、右乳腺、脊髓和心脏的剂量学参数比较
3 讨 论
李益坤等[6]分析左乳癌保乳术后同步推量TH和静态调强放射治疗(IMRT)的剂量分布差异发现, TH的靶区剂量适形度和均匀性显著优于IMRT(P<0.05)。张富利等[7]比较乳腺癌保乳术后TH和IMRT的靶区剂量分布差异显示, TH适形度和均匀性显著优于IMRT(P<0.05); TH患侧肺高剂量体积V20和V30降低,低剂量体积V5和V10、对侧乳腺V3和心脏V5增大; 除患侧肺V30外,其他指标差异均有统计学意义(P<0.05), TH在延长治疗时间、改善靶区适形度和均匀性的同时也明显增加了危及器官低剂量体积,应引起高度关注。ONAL C等[8]比较30例乳腺癌保乳术后TH和容积调强弧形放射治疗(VMAT)放疗剂量差异,结果显示TH可以提供更好的靶区覆盖,在靶区适形度和剂量均匀性方面均较VMAT更好。杨波等[9]比较左乳癌保乳术后固定野调强放疗(FF-IMRT)和TH计划的差异,结果显示左乳癌TH计划靶区适形度和均匀性优于FF-IMRT计划,危及器官的保护与FF-IMRT相同甚至更优,因此TH可作为新的调强放疗技术用于乳腺癌保乳术后放疗。崔芹玲等[10]对早期乳腺癌术后TH与IMRT的Meta分析发现, TH较IMRT的PTV均匀性和适形度更好,差异有统计学意义(P<0.05), TH对危及器官高剂量区域的保护优于IMRT。
TD是基于螺旋断层放射治疗系统的一种定角断层调强放射治疗技术, TD技术较螺旋断层技术具有射线利用率高、治疗时间短、减少危及器官的低剂量范围等优势[11-13]。林金勇等[14-17]比较4野TD、6野TD和TH这3种照射方式在左乳癌保乳术后放疗计划中的差异,结果显示3种计划均能达到临床要求, TH技术的HI和CI较优,但4野TD对危及器官和正常组织,尤其是脊髓、健侧乳腺Dmax, 肺V5, 心脏Dmean的保护优于TH; 6野TD技术在保证低危及器官限量的条件下较4野TD技术提高了靶区均匀性和适形度,同时TD的机器跳数均低于TH, 有效地缩短了患者治疗时间。上述结果提示,对于左侧乳腺癌保乳术后放疗, 6野TD技术具有一定优势,与TH技术相比, 6野TD明显降低了危及器官受量; 与4野TD技术相比, 6野TD靶区均匀性和适形度较优,更适合早期乳腺癌患者。陈高翔等[18]分析了TD技术在乳腺癌保乳术后放疗的剂量学特点,结果发现, TD计划靶区适形度均显著优于IMRT和断层径照适形放射治疗(TD-CRT)(P<0.05), 而均匀性比较,差异无统计学意义(P>0.05); 患侧肺和心脏的V5、V10、V20、V30、V40和Dmean均显著低于TD-CRT和IMRT(P<0.05); 平均治疗时间方面, IMRT最长, TD次之, TD-CRT最短,差异均有统计学意义(P<0.01)。JOO C M等[19-21]比较26例早期乳腺癌保乳术后患者TD和3D-CRT计划的剂量学差异,结果显示, TD对患侧肺的保护优于3D-CRT, 差异有统计学意义(P<0.05)。
综上所述,左乳癌保乳术后瘤床同步推量放疗TH和TD均能满足临床要求, TH靶区剂量优于TD, 而TD在心肺低剂量区和对侧危及器官如右肺、右乳、脊髓的保护明显优于TH, 因此建议乳腺癌保乳术后患有心肺疾病和化疗后心脏损伤患者优先选择TD技术,以最大限度地降低放疗对心脏和肺组织的损伤,同时对右侧乳腺和右侧肺提供更好的保护,降低二次肿瘤发生的风险。
