硼铁矿绿色化高效综合利用
2021-03-12张泽熙杨艳春吕晓姝王溪尧
张泽熙,杨艳春,吕晓姝,王溪尧
(辽宁科技学院 生物医药与化学工程学院,辽宁 本溪 117004)
我国硼资源储量大,占世界硼量的18%〔1〕。其中,辽宁地区硼资源占我国总储量的56%〔2〕。辽宁硼矿有两类,即硼镁矿和硼铁矿,统称为硼镁铁矿,其中占储量20%的硼镁矿含硼品位高,经过多年的开采利用,已尽枯竭。而硼铁矿在传统工艺中磁选铁后得到硼精矿,再继续生产的目标产物。但是由于硼的含量较低,在生产中产生大量的废渣堆积,占用土地、污染环境〔3〕。
硼矿中还有大量的硅酸镁盐矿物等〔4〕,对其进行充分利用可以制备出硅、镁、铁、铝等产品,即提高了硼矿高附加值的利用,又可减少废弃物的排放,符合循环经济、清洁生产及提高矿产资源综合利用率的要求。
本文针对硼铁矿未能合理处理的现状,开展硼铁矿高附加值绿色化综合利用工艺的研究,拟采用硫酸铵法焙烧硼铁矿,矿物中的铁、镁、铝及硼与硫酸铵反应生成溶于水的物质,硼铁矿中的硅生成不溶于水的二氧化硅。焙烧熟料加水溶解,过滤。含二氧化硅为主的硅渣和滤液分离。硅渣经过氢氧化钠处理得到硅酸钙及石英产品。调控pH值,使滤液中的铁、镁、铝在不同的pH值条件下,制备出羟基氧化铁、氧化镁、氢氧化铝产品,分离。利用溶解度差异,分离硼酸铵和硫酸铵〔5-7〕。硫酸铵、氨气循环利用。该工艺过程中化工原料实现循环,无废渣、废水、废气排放,实现全流程的绿色化,符合发展循环经济,建设资源节约型和环境友好型社会的要求。
1 工艺流程设计
1.1 原料
原料为辽宁某地区的硼铁矿。其化学成分如表1。

表1 硼铁矿的化学成分(质量百分数)
硼铁矿的XRD谱如图1所示。由图1可知硼铁矿中主要矿物组成为蛇纹石(Mg3Si2O5(OH)4)、硼镁石(MgBO2(OH))、磁铁矿(Fe3O4)、镁铁矿(MgFe2O4)、利蛇纹石((Mg,Al)3〔Si,Fe〕2O5(OH)4)、硼钾镁石(KHMg2B12O16(OH)10·14H2O)。
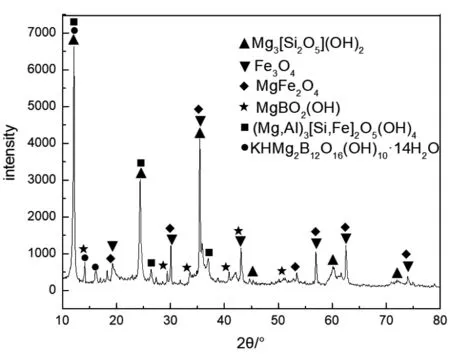
图1 硼铁矿的XRD图谱
实验所用的硫酸铵为工业级,纯度≥96%;液氨、碳酸铵、碳酸氢铵为分析级;水为去离子水。
1.2 工艺流程设计原理
根据硼铁矿的化学成分和矿相组成,设计工艺流程将硼铁矿和硫酸铵混合焙烧。硼铁矿与硫酸铵反应,其中的镁、铁、铝、硼等产物溶解于水。硅以二氧化硅的形式存在,不溶于水。将焙烧产物用水溶出、过滤。使镁、铁、铝、硼与二氧化硅分开。再利用溶液中的镁、铁、铝等生成沉淀的pH值不同。调节溶液的pH,就可以把镁、铁与铝等分离提取。此时滤液是碱性溶液,溶液中存在大量的NH4+、SO42-和B4O72-。把滤液加热蒸发结晶,使溶液逐渐变为饱和溶液,饱和溶液再逐渐变为过饱和溶液,这时溶质就开始从过饱和的溶液中析出。硫酸铵结晶出来,余下的硼酸铵浓缩液通过调节温度结晶。分离出的硫酸铵循环利用。
2 工艺简介
2.1 焙烧
把硼铁矿干燥、破碎,磨细至80 μm以下。把磨细的硼铁矿与硫酸铵按比例配料、混均。把硼铁矿中的镁、铁、铝、硼等理论上完全反应所消耗的硫酸铵的物质的量计为1∶1。硫酸铵与硼铁矿的比例为2.5∶1。温度上升到450 ℃焙烧2小时,产生的氨气和二氧化硫回收,制成液氨和硫酸铵。氨用来调节pH值分离提取镁、铁、铝,之后溶液蒸发结晶得到硫酸铵,返回配料工序。该焙烧过程发生的化学反应〔8-10〕主要有:
4Fe3O4+ O2+ 24(NH4)2SO4=12NH4Fe(SO4)2+ 18H2O↑ + 36NH3↑
Mg3〔Si2O5〕(OH)4+ 6(NH4)2SO4=3(NH4)2Mg(SO4)2+ 5H2O↑ + 2SiO2+ 6NH3↑
2MgBO2(OH) + 4(NH4)2SO4=2(NH4)2Mg(SO4)2+ B2O3+ 4NH3↑+3H2O↑
2(Mg,Al)3〔(Si,Fe)2O5〕(OH)4+ 5.5O2=6MgO+2Fe2O3+ 3Al2O3+2 SiO2+4H2O↑
Al2O3+ 4(NH4)2SO4=2NH4Al(SO4)2+ 6NH3↑ + 3H2O↑
MgO + 2(NH4)2SO4=(NH4)2Mg(SO4)2+ H2O↑ + 2NH3↑
2.2 硅渣碱浸制备硅产品
将焙烧熟料按3∶1液固比加水溶出。溶出温度60 ℃-80 ℃。边搅拌,边溶出。溶出时间1小时。熟料中的硫酸盐溶解于水,SiO2不溶解。滤渣(硅渣)主要成分为二氧化硅,三次洗涤后即为硅产品,也可以深加工成硅灰石或白炭黑。
滤液为含硫酸镁、硫酸铁和硫酸铝的溶液。
将硅渣与碱液按液固比3∶1混合。控制碱浸温度130 ℃,碱浸时间1小时。过滤得到滤液为硅酸钠溶液,滤渣为石英粉,过滤去除残渣。
2.2.1 制备硅酸钙
向滤液(硅酸钠溶液)中加入石灰乳,在90 ℃以上反应2小时,得到硅酸钙沉淀。过滤洗涤,烘干得到硅酸钙产品,NaOH溶液蒸发浓缩后返回碱浸溶出硅渣,循环利用。
2.2.2 制备白炭黑
向滤液(硅酸钠溶液)中通入CO2,发生如下化学反应。
Na2SiO3+ CO2+ H2O=H2SiO3↓+ Na2CO3
过滤、洗涤,得到偏硅酸,加热分解得到白炭黑。
H2SiO3=SiO2+ H2O↑
向滤液中加入Ca(OH)2,化学反应为:
Na2CO3+ Ca(OH)2=2NaOH + CaCO3↓
过滤,洗涤,得到轻质CaCO3产品,NaOH 溶液返回溶出工序。
2.3 分离提取铁
保持除硅液温度在40 ℃以下,向溶液中加入双氧水,使溶液中的Fe2+氧化成Fe3+。然后提高溶液温度在40 ℃以上,通NH3气,控制pH值为3。或者加入(NH4)2CO3或NH4HCO3,搅拌,溶液中的铁生成羟基氧化铁(FeOOH)。反应结束后过滤,滤渣为羟基氧化铁,洗涤干燥后作为炼铁原料。实验得到优化的工艺条件为pH值为3,温度60 ℃、反应时间2小时。
也可以在焙烧工序加一段过烧。将温度升到750 ℃以上,硫酸铁铵分解。发生的化学反应为:
NH4Fe(SO4)2=Fe2O3+2NH3↑+4SO3↑+H2O↑
生成的NH3、SO3、H2O进入烟气,分尘吸收,得到(NH4)2SO4。
Fe2O3经溶出过滤后,与SiO2一起成为滤渣。可以采用选矿的方法将其与SiO2分开。或碱溶、过滤,Fe2O3成为滤渣与SiO2分开。
2.4 精制氢氧化铝
向沉铁后的溶液中通入氨气(或(NH4)2CO3或NH4HCO3),调节溶液pH值至5,溶液中的铝生成氢氧化铝沉淀,发生的主要化学反应为:
NH4Al(SO4)2+ 3NH3+3H2O=Al(OH)3↓ + 2(NH4)2SO4
实验得到沉铝的优化工艺条件为温度30 ℃,pH为5,把沉铝后的溶液过滤,过滤得到铝渣。铝渣用于制备氧化铝。滤液为精制硫酸镁溶液。
把铝渣加入NaOH溶液中,发生如下化学反应:
Al(OH)3+ NaOH=NaAlO2+2H2O
过滤去除残渣。向溶液中加入Al(OH)3晶种,析出Al(OH)3晶体,过滤得到Al(OH)3产品。滤液返回溶出工序,循环利用。
2.5 分离提取镁
除硅、铁、铝精制硫酸镁溶液中加氨,调节溶液pH值至11,温度保持在40 ℃~60 ℃,反应生成氢氧化镁沉淀,过滤洗涤得到氢氧化镁产品及滤液。实验得到沉镁的优化工艺条件为:温度30 ℃,反应时间2小时,pH值为11,搅拌强度为400 r·min-1。
2.6 蒸发结晶硫酸铵和硼酸铵
把沉镁后的滤液加热,蒸发结晶得到硫酸铵产品,返回配料,循环利用,蒸馏水回收。
硫酸铵晶体结晶的同时,滤液中硼酸铵浓缩。控制滤液中的硼酸铵达到最大溶解度。就不再蒸发结晶。浓缩液通过控制温度利用硼酸铵和硫酸铵溶解度随温度变化的差异,浓缩后,通过控制温度,结晶得到硼酸铵,余下的硫酸铵溶液返回混料工序,循环使用。
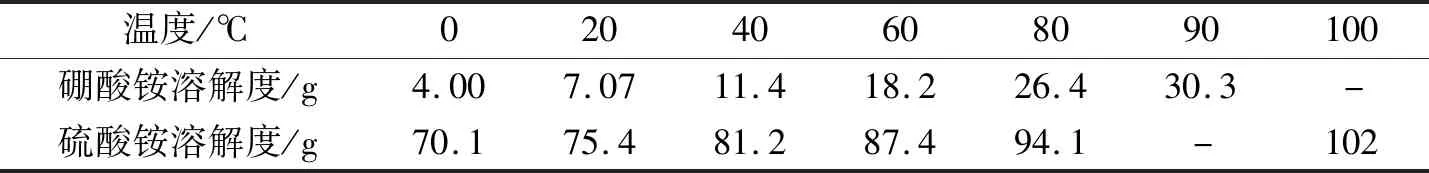
表2 不同温度下硼酸铵和硫酸铵的溶解度
2.7 煅烧
将硫酸铵和硼酸铵的混合物在500 ℃煅烧,硫酸铵分解成NH3、SO3和H2O,硼酸铵分解成四硼酸和NH3。烟气降温冷却,得到硫酸铵,返回混料,循环利用。过量NH3回收用于沉镁。硼酸加热分解得到三氧化二硼。
3 结论
(1) 采用硫酸铵焙烧硼铁矿,可以把硼铁矿中的镁、铁、铝、硼等转化为可溶解于水的产物。硅转化为不溶于水的二氧化硅,溶出,过滤,把二氧化硅分离出来,深加工成硅灰石或白炭黑。
(2) 采用添加NH3气(或(NH4)2CO3或NH4HCO3),调节pH的方法,使溶于水的镁、铁、铝生成沉淀,过滤,分离,进一步制成产品。
(3) 采用蒸发结晶的方法,把硫酸铵结晶出来,循环使用。
(4) 该工艺可以把硼铁矿中有价组元都分离提取,化工原料循环利用,不造成环境污染,是绿色化、高附加值的工艺流程。
