基于人工智能识别心电图的一种低钾血症快速辅助诊断模型
2021-03-10朱彩华张伊楚王晨曦葛尚华娄伟明邓立彬陈琦
朱彩华 张伊楚 王晨曦 葛尚华 娄伟明 邓立彬, 陈琦
低钾血症是临床上最常见的电解质紊乱之一,是指血清钾浓度低于3.5 mmol/L[1]。低钾血症可致心肌细胞的兴奋性和自律性增高,传导性减慢,从而导致心律失常,严重者可出现室性心动过速、心室颤动及心源性猝死等恶性心律失常[2-5]。目前诊断低钾血症最准确的方法是静脉血清钾测定,但临床上急查血钾通常需要等待1~2 h,采血不仅有创,且随着采血次数的增多,患者依从性也会下降。这些因素在一定程度上限制了低钾血症快速诊断的效率,从而可能增加低血钾所致的相关并发症风险。
当钾水平<2.7 mmol/L时,心电图(ECG)可发生T 波低平或倒置、ST 段压低、Q-T 间期延长和U波的改变等一系列变化[6-11]。说明ECG 有助于快速识别低钾血症,然而,大多数低钾血症患者临床症状及人工ECG 识别缺乏特异性,Wrenn等[12]研究结果表明人工分析ECG 识别低钾血症的敏感性及准确率非常低。
人工智能(artificial intelligence,AI)泛指模拟人类智慧的方法、技术及应用的一门技术学科,其应用目前已逐渐地从传统领域渗透到医学等专业领域。Galloway等[13]研究发现AI可通过ECG 筛选高钾血症。迄今为止,没有应用AI识别ECG 筛选低钾血症的相关研究报道。因此,笔者试图创建AI识别ECG 的模型,从而实现快速无创筛选低钾血症。
1 资料与方法
1.1 研究人群
选取2017年9月至2019年5月在南昌大学第二附属医院所有的就诊患者共474 633 名,其中标准12 导ECG 277 000 份,血清钾378 680份。同时,收集患者住院号、采集与ECG 相对应时间的前后3 h(ECG±3 h)血清钾的标本、血清肌酐、N 末端脑钠肽氨基酸前体(pr o-BNP)、血清钙、血清镁、血清钠、急诊肌钙蛋白I(超敏肌钙蛋白)、游离甲状腺激素(FT4、FT3)等。该研究经南昌大学第二附属医院伦理委员会审批同意,其研究流程见图1。
1.2 纳入及排除标准
纳入标准:选取2017年9月至2019年5月在南昌大学第二附属医院所有的就诊患者的ECG。排除标准:①死亡ECG(各导联未见顺序发生的PQRS-T 波群的ECG);②采集ECG 与血清钾标本期间给予了补钾或利尿治疗的血液标本。
1.3 混杂因素
混杂因素ECG 的定义:指诊断为心房颤动(AF)、完全性左束支传导阻滞(CLBBB)、完全性右束支传导阻滞(CRBBB)及起搏的ECG(包括心房起搏和心室起搏)。

图1 研究方法流程图
1.4 数据与深度学习
1.4.1 数据匹配 根据患者住院号及采集ECG 与血清钾标本的时间差为±3 h(如ECG 对应的血清钾值>1,则取时间相隔最近者)的原则进行匹配,获得有效的ECG-血钾对数据集。
1.4.2 深度学习模型(DL M) 本研究的DL M 是在anaconda平台上用Python语言和tensorflow 神经网络框架构建的。该框架具有11层的卷积神经网络(CNN),前10层是卷积层和全连接层,最后1层是完全连接soft max层。神经网络能从同时采集的任意数量的ECG 导联中接收5 s时长的ECG 信号,并生成一个参数,输出0或1(如图2,3)。并计算出敏感性、特异性及接受者操作特性(ROC)曲线下的面积(AUC)值等统计学指标。
1.5 人工识图诊断低钾血症
将验证集中的排除混杂因素ECG(n=1 748)进行诊断归类,记录并统计人工诊断低钾血症或提示低钾血症的数量,并将其与相对应的生化检测血钾水平进行对照,以计算其人工分析ECG 识别低钾的敏感性、特异性及准确率。
1.6 统计分析
应用3.4.2版本的R 软件及卡方检验分析。除AUC以外,均取可信区间(CI)为95%来评估诊断性能。AUC的可信区间是通过应用R(R Foundation)中 的p ROC 软 件 包 对Del ong 方 法 做Sun 和Su优化来确定的[16]。双侧P<0.05表示有统计学意义。

图2 神经网络心电图分类的原理图
2 结果
2.1 数据筛选流程
排除混杂因素ECG 后,获得9 161 对份数据集,80%(n=7 413)作为训练数据集,20%(n=1 748)作为验证数据集;交叉验证后,评估模型通过识别ECG 筛选低钾血症的性能。
2.2 数据的基线特征
排除混杂因素12导联模型如表1,2所示,训练集共7 413份ECG,验证集有1 748份ECG,研究中笔者发现,N 末端pr o-BNP>300 pg/ml或血清镁<0.75 mmol/L的患者可能更易患低钾血症。血清钾值>1所对应的ECG 更有可能是低钾ECG。
笔者针对排除混杂因素12 导ECG 建造了模型,其验证集中筛选低钾血症的AUC 值为0.796(95%CI,0.766~0.815),取临界值为0.536时,敏感为71.4%,特异性为77.1%,阴性预测值为75.1%,阳性预测值为73.5%。

图3 模型在其验证集中识别低钾血症ROC曲线及混淆矩阵
2.3 模型的ROC曲线和混淆矩阵
为了更客观得评价模型的效能,笔者做了排除混杂因素12导模型的ROC曲线及混淆矩阵图,如图3所示,低钾模型的AUC值为0.796,准确性为74.4%。
2.4 DL M 在混杂因素ECG 中识别低钾血症
为进一步验证DL M 在混杂因素ECG 中识别低钾血症的性能,笔者应用未被混杂因素ECG 训练过的排除混杂因素ECG 12导联模型从混杂因素心电图中筛选低钾血症。随机抽取混杂因素AF心电图111份、CRBBB 心 电 图56 份、CLBBB 心 电 图6份及起搏ECG 3份作为验证数据集。验证结果如表3显示,该模型在AF 心电图中识别低钾血症的敏感性和特异性分别为74.2%和72.0%,准确率为72.7%;在CRBBB心电图中的敏感性和特异性分别为55.0%和56.0%,准确率为55.3%;在CLBBB心电图中的敏感性和特异性分别为0和25.0%,准确率为16.7%;在起搏ECG 中的敏感性和特异性分别为100%和100%,准确率为100%。
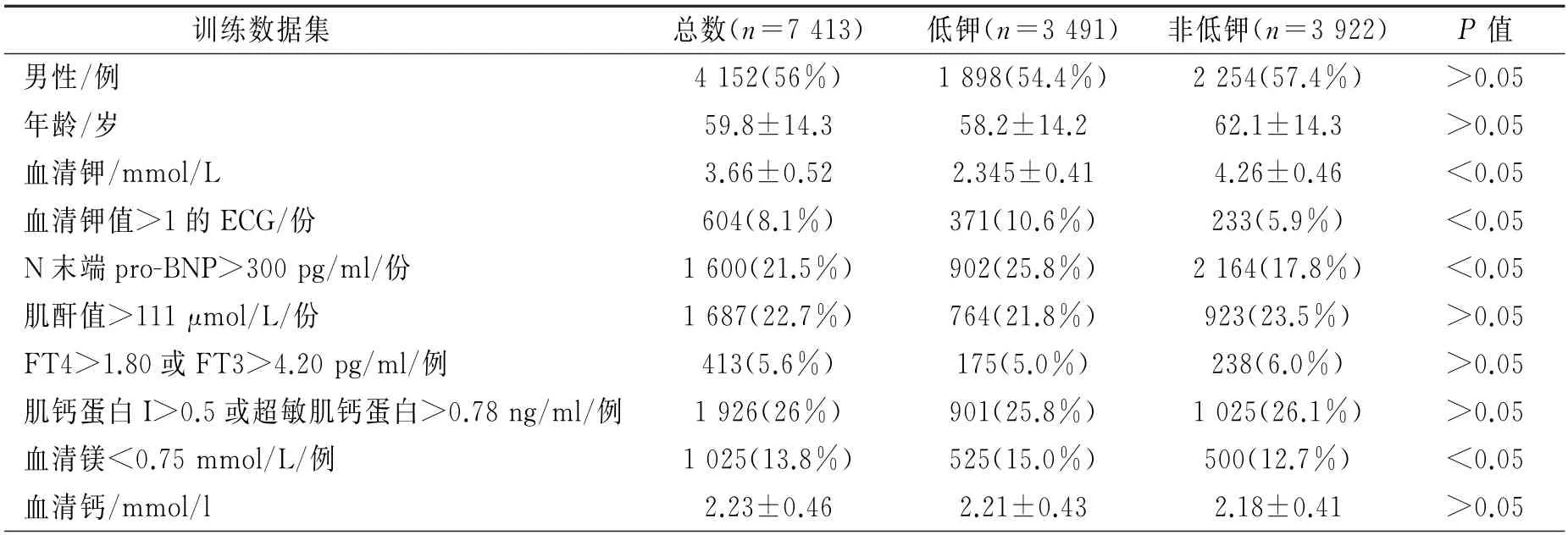
表1 排除混杂因素ECG 12导联模型的训练数据集的基线特征

表2 排除混杂因素ECG 12导联模型的验证数据集的基线特征
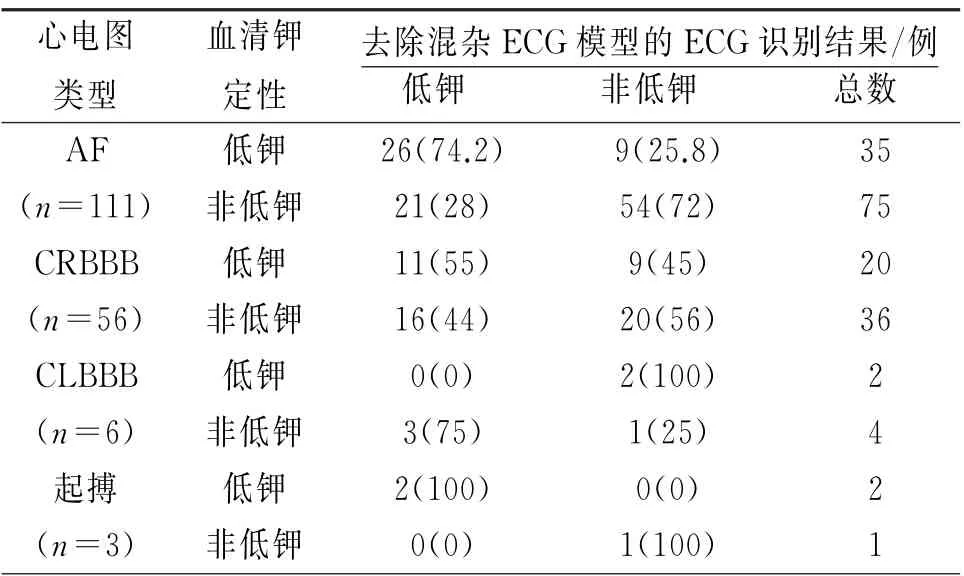
表3 DL M 在混杂因素ECG 中识别低钾血症的结果
2.5 AI比人工识别低钾ECG 的准确性更高
笔者应用验证集中1 748 份排除混杂因素的ECG,根据ECG 的诊断,结果如图4表明:人工仅识别出180张低钾ECG、116张非低钾ECG,准确度为16.9%、敏感性为21.9%,阳性预测值为60.8%。而在排除混杂因素ECG 模型中,识别低钾血症的AUC为0.796,准确率、敏感性、特异性、阴性预测值、阳性预测值分别74.4%、71.4%、77.1%、75.1%及73.5%。
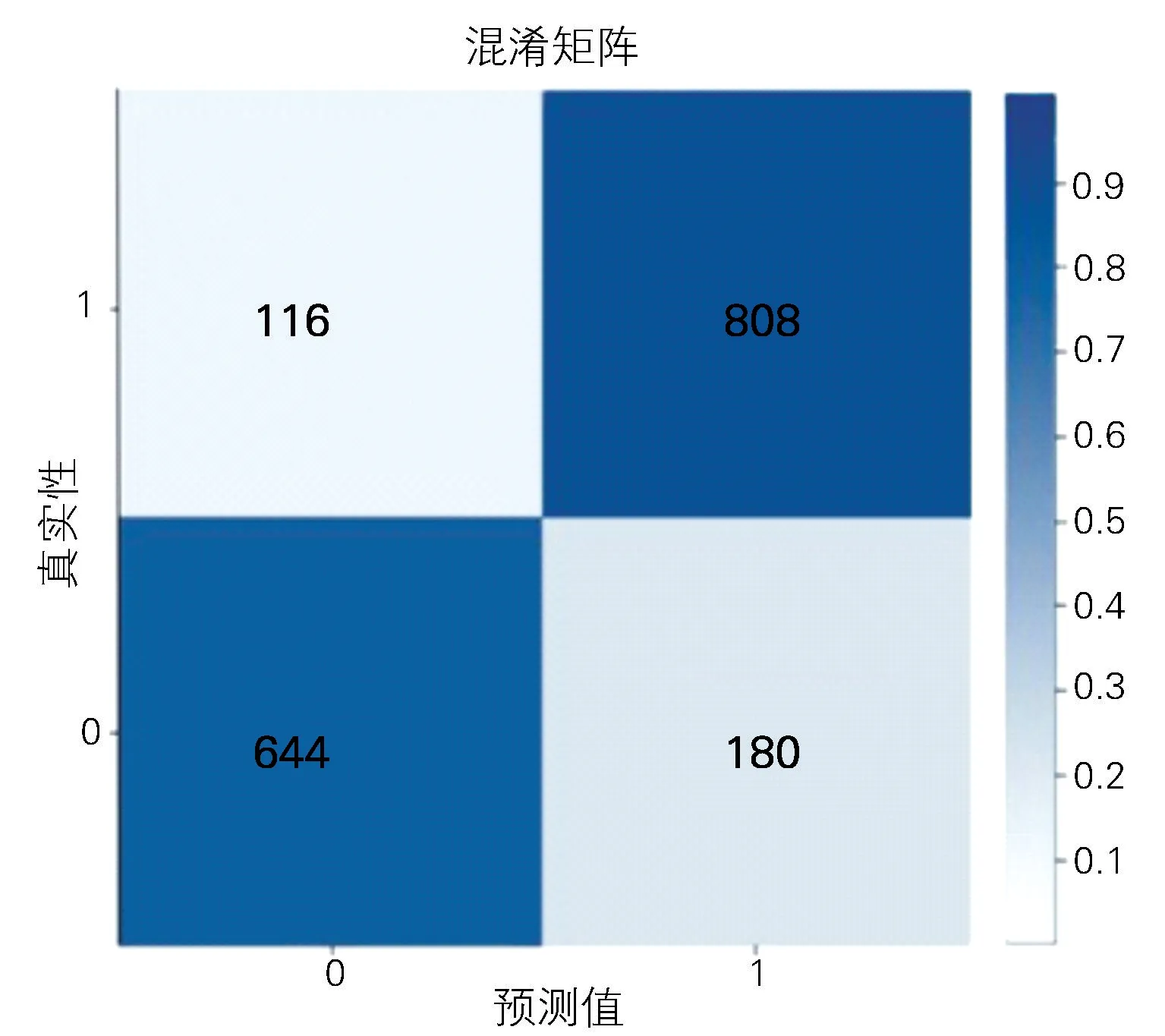
图4 人工判读低钾血症的混淆矩阵
3 讨论
随着AI在医学领域取得突破性进展,诊疗智能化已成为重要发展趋势,在过去10年,深度学习(DL)应用于心血管领域的研究越来越多,并在心脏收缩功能障碍、高钾判读等方面取得良好的效果[14]。DL可模仿人脑的工作模式,使用多层神经网络对数据集进行训练并形成自动预测,与传统的统计学方法相比,DL M 具有更好的自我驱动性和更高的准确度,在分析图像等复杂数据时表现良好,主要用于图像识别。但是DL M 不提供算法透明性:我们无法精确地理解算法的启发式算法如何到达其最终目的地[15]。
在这项研究中,笔者发现利用ECG 训练11层CNN,提取图像特征,建立预测低钾血症的DL M 模型,具有令人满意的筛选能力,12导ECG 的低钾模型中准确度明显高于ECG 专家。此外,笔者还发现,N 末端pro-BNP>300 pg/ml或血清镁<0.75 mmol/L的患者可能更易患低钾血症,心力衰竭患者和低镁血症患者是否比非心力衰竭和非低镁的患者更易发生低钾,有待进一步研究分析。需要注意的是,血清中钙、镁、肌钙蛋白、肌酐以及游离甲状腺素等指标的浓度变化,均可导致ECG 发生改变,而这些改变可能会影响或掩盖低钾ECG 特征。
尽管在医院通过静脉血测定获得血清钾浓度已经比较快捷,但在院外(比如社区诊所),因低钾血症患者通常没有特征性的症状,低钾血症的诊断仍面临很大的困难。使用ECG 无创筛查患者低钾血症的实现,将为早发现这种危及患者生命的疾病提供强有力的帮助。当然,AI作为低钾血症的初步筛选工具,不管其评估结果是否为真阳性,均是一个定性的预警性诊断方法,生化检测仍是低钾血症明确诊断的金标准。在DL M 中效果最佳的排除混杂因素ECG12导联模型,其假阳性率也高达22.9%,而特异性仅有77.1%,但通过ECG 测试得出的钾水平可能比血液化验更能反应出患者心律失常的风险。因ECG 取决于心脏组织对血钾水平的反应,所以基于ECG 的测试比基于化学的血液测试更具生理性[16],此外,基于ECG 的测试不易受到温度、污染或与加工血液相关的其他潜在干扰因素的影响。一项研究发现,有30.2%的正常血钾血症患者有假性高钾血症血液检查结果[17]。或许通过对同一患者的多个血钾-ECG 对进行学习训练,建立个体化DL M,可提其高特异性。
