津力达颗粒对高脂饮食诱导的肥胖小鼠代谢紊乱及FGF21/AMPK信号通路的影响
2021-03-09李翠茹常丽萍高怀林
刘 妍,李翠茹,常丽萍,,高怀林
1.河北中医学院,河北 石家庄 050091
2.石家庄以岭药业股份有限公司,络病研究与创新中药国家重点实验室,河北 石家庄 050035
3.河北以岭医药研究院,国家中医药管理局重点研究室(心脑血管络病),河北省络病重点实验室,河北 石家庄 050035
4.河北以岭医院,国家中医药管理局中医络病学重点学科,河北 石家庄 050091
2005年国际糖尿病联盟公布的数据显示,我国代谢综合征患病率为14%~16%,且80%糖尿病患者、50%糖尿病前期患者均患有代谢综合征[1-2]。腹型肥胖是代谢综合征最重要的特征,目前临床上对肥胖所致的代谢综合征尚无有效的治疗方法。成纤维细胞生长因子21(fibroblast growth factor 21,FGF21)是FGF 家族中的一员,可作用于肝脏、脂肪等组织,增强肝脏脂肪的氧化,促进白色脂肪组织脂质分解并增强其胰岛素敏感性[3]。刺激FGF21表达可抑制高脂饮食诱导的体质量增加,增加胰岛素敏感性,改善胰岛素抵抗,改善糖、脂代谢,从而治疗肥胖[4]。FGF21 可通过激活成纤维生长因子受体1(fibroblast growth factor receptors 1,FGFR1)/β-Klotho 蛋白的受体复合物发挥生物性能[5]。磷酸腺苷活化蛋白激酶(AMP-dependent/activated protein kinase,AMPK)是一种能量代谢传感器,在调节脂质代谢和葡萄糖稳态中起重要作用,当机体缺氧、缺血、葡萄糖消耗过多时,磷酸化的(p-AMPK)被激活[6-7]。内分泌FGF21 信号可通过FGFR1/β-Klotho 通路直接激活AMPK 途径,也可通过刺激脂联素和皮质类固醇分泌间接激活AMPK 信号,调控代谢紊乱[8]。沉默信息调节因子1(silent information regulator 1,SIRT1)是FGF21介导的AMPK 信号通路的下游靶点,与FGF21 具有双向激活作用,均在调节糖脂代谢过程中发挥重要调控作用。
津力达颗粒由人参、黄精、苍术、苦参、麦冬、地黄等中药组成,具有保护胰岛β 细胞结构与功能、增加胰岛素分泌、减轻体质量、改善糖脂代谢水平、增强胰岛素敏感性等作用[9-13]。但其改善胰岛素抵抗及代谢综合征的具体作用机制尚不明确,因此,本研究探讨了津力达颗粒对高脂饮食诱导的肥胖小鼠相关代谢综合征的作用及与FGF21/AMPK 信号通路的相关性,为津力达颗粒的临床应用提供参考依据。
1 材料
1.1 动物
SPF 级雄性C57BL/6J 小鼠,5~6 周龄,体质量18~22 g,购自北京维通利华实验动物技术有限公司,许可证号SYXK(冀)2015-0064。动物饲养于河北省中西医结合医药研究院以岭药业新药安全评价研究中心,温度20~25 ℃,相对湿度50%~70%,12 h 昼夜光照交替,5 只/笼,自由进食饮水,适应性饲养1 周。动物实验经河北以岭中医研究所动物伦理委员会批准,批准号SYXK(冀)2020-003。
1.2 药品与试剂
津力达颗粒(9 g/袋,批号S-130901)购自石家庄以岭药业股份有限公司;总胆固醇(total cholesterol,TC)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)、三酰甘油(triglycerides,TG)试剂盒(批号分别为19-0115、19-0514、19-0418、19-0605)购自北京九强生物技术有限公司;血糖试纸购自美国强生公司;葡萄糖购自美国Sigma 公司;Eastep®Super 总RNA 提取试剂盒(批号0000343931)购自上海普洛麦格公司;反转录试剂盒、荧光定量PCR 试剂盒购自日本Takara 公司;引物购自上海生工生物科技有限公司;FGF21 抗体、甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)抗体、SIRT1 抗体、羊抗兔二抗(批号分别为UD275587、GR3298310-2、GR3250046-11、GR309266-5)购自美国Abcam 公司;FGFR1 抗体、β-Klotho 抗体(批号分别为10002055、00060022)购自美国Proteintech 公司;AMPK 抗体、p-AMPK抗体购自美国CST 公司;蛋白上样缓冲液、RIPA裂解液购自北京索莱宝科技有限公司;BCA 蛋白定量试剂盒、蛋白酶、磷酸酶抑制剂、蛋白Marker染液购自美国Thermo Fisher Scientific 公司。
1.3 仪器
Tek TEC 5 组织包埋机(樱花医疗科技有限公司);Leica SM2010R 平推式切片机(德国Leica 公司);KA-1000A 离心机(中国飞鸽公司);PrimoVert倒置显微镜(德国Zeiss 公司);5417R 高速冷冻离心机(美国Eppendorf 公司);XW-80A 漩涡混合仪、TS-8 转移脱色摇床(海门其林贝尔仪器制造有限公司);ABT220-5DM 万分电子天平(德国Kern 公司);7300 Real-Time PCR System(美国ABI 公司);稳豪血糖仪(美国强生公司);7080 全自动生化分析仪(日本日立公司);HZ-2011K-C 恒温摇床(太仓华利达实验设备有限公司);ACCUBLOCK 数显干式加热器(美国Labnet 公司);221BR 半干转膜仪(日本Bio-Rad 公司);ERS301 电泳仪(美国CE 公司);MDF-U73V 超低温冰箱(日本Sanyo 公司);Milli-Q Integral 3 纯水机(美国Millipore 公司)。
2 方法
2.1 分组与给药
根据文献方法[14],将小鼠随机分为对照组、模型组、津力达颗粒(3.8 g/kg)组,每组15 只。对照组小鼠喂食标准饲料,其余各组小鼠喂食高脂饲料;津力达颗粒于研钵中研碎,溶于0.5%羧甲基纤维素钠溶液,配制成质量浓度为0.19 g/mL 的混悬液,给药组ig 混悬液(20 μL/g),对照组和模型组ig 等体积0.5%羧甲基纤维素钠溶液,1 次/d,连续13 周。每日观察小鼠毛色、活动、食欲、死亡及精神状态状态等情况;每周称定小鼠体质量并记录小鼠日摄食、饮水量。
2.2 小鼠腹腔内葡萄糖耐量实验
根据文献方法[15],末次给药后,各组小鼠ipD-葡萄糖(1.5 g/kg),分别在0、15、30、60、90、120 min 用血糖仪测定各组小鼠血糖水平。将各时间点的血糖值绘制成糖耐量曲线并计算血糖曲线下面积(GTT-AUC)。
2.3 津力达颗粒对小鼠血清中TC、TG、LDL-C和HDL-C 水平的影响
末次给药后,各组小鼠禁食不禁水16 h 后,ip 10%水合氯醛(10 μL/g)麻醉,摘眼球取血,4 ℃、4000 r/min 离心15 min,吸取上清,按照试剂盒说明书检测各组小鼠血清中TC、TG、LDL-C、HDL-C水平。
2.4 津力达颗粒对小鼠肝脏和脂肪组织病理变化的影响
小鼠脱颈椎处死,置于冰上,剪开背部皮肤,迅速分离两侧肩胛部棕色脂肪组织、附睾白色脂肪组织和肝脏组织,分别称定质量,固定于4%多聚甲醛溶液中,脱水、切片、脱蜡、水化、染色、封片后进行常规HE 染色,于显微镜下观察各组小鼠肝脏、脂肪组织病理变化。
2.5 津力达颗粒对小鼠肝脏和脂肪组织中FGF21/AMPK 通路相关基因表达的影响
按照试剂盒说明书提取脂肪和肝脏组织的总RNA 并合成cDNA,进行qRT-PCR 分析。引物序列:FGF21 上游引物为5’-TGGAATGGATGAGATCTAGAGTTGG-3’、下游引物为5’-GAGCTCCAGGAGACTTTCTGGA-3’;FGFR1 上游引物为5’-TACAAGGTTCGCTATGCCAC-3’、下游引物为5’-TGCGGAGATCGTTCCACGAC-3’;GAPDH 上游引物为5’-CCTGGAGAAACCTGCCAAGTATG-3’、下游引物为5’-GAGTGGGAGTTGCTGTTGAAGTC-3’。
2.6 津力达颗粒对小鼠肝脏和脂肪组织中FGF21/AMPK 通路相关蛋白表达的影响
分别称取肝脏、脂肪组织,研磨后加入50 μL含蛋白酶抑制剂的RIPA 蛋白裂解液,于冰上裂解30 min,使用超声波细胞破碎仪破碎细胞,4 ℃、12 000 r/min 离心20 min,吸取上清液,按照BCA试剂盒说明书测定蛋白质量浓度,加入蛋白上样缓冲液,95 ℃加热10 min,使蛋白变性。蛋白样品经12%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳,转至PVDF 膜,封闭2 h 后,分别加入FGF21、FGDR1、Klotho、AMPK、p-AMPK、SIRT1、GADPH 抗体,4 ℃孵育过夜;加入二抗,孵育1 h。采用Odyssey成像系统扫描并通过图像分析软件进行分析。
2.7 统计学分析
实验数据采用SPSS 19.0 软件进行统计分析,数据结果以±s表示,多组间比较采用单因素方差分析。
3 结果
3.1 津力达颗粒对肥胖小鼠体质量和脂质累积的影响
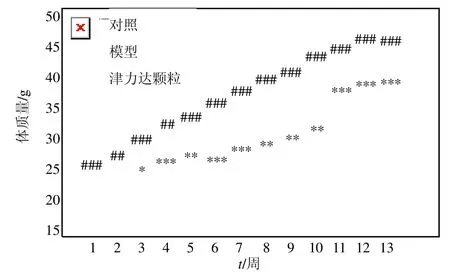
图1 津力达颗粒对肥胖小鼠体质量的影响 (±s,n=15)Fig.1 Effect of Jinlida Granules on body weight of obese mice (±s,n=15)

图2 津力达颗粒对肥胖小鼠棕色脂肪质量 (A)、白色脂肪质量 (B)、肝脏质量 (C)、食物摄入量 (D) 和饮水量 (E) 的影响 (±s,n=15)Fig.2 Effect of Jinlida Granules on brown fat weight (A),white fat weight (B),liver weight (C),food intake (D),and water intake (E) of obese mice (±s,n=15)
如图1所示,与对照组比较,自第1 周起,模型组小鼠体质量显著升高(P<0.05、0.01、0.001);与模型组比较,自第3 周起,津力达颗粒组小鼠体质量显著降低(P<0.01、0.001)。如图2所示,与对照组比较,模型组小鼠棕色脂肪质量、白色脂肪质量、肝脏质量明显升高(P<0.05、0.001),食物摄入量和饮水量显著降低(P<0.001);与模型组比较,津力达颗粒组小鼠棕色脂肪质量、白色脂肪质量、肝脏质量显著降低(P<0.05、0.001),食物摄入量和饮水量无明显变化。
如图3所示,与对照组比较,模型组小鼠脂肪细胞体积增大,肝脏脂肪性空泡增多;与模型组比较,津力达颗粒组棕色脂肪组织和白色脂肪组织细胞体积变小,肝脏脂肪变性程度减轻。表明津力达颗粒可有效预防高脂饮食诱导的肥胖小鼠棕色脂肪组织、白色脂肪组织、肝脏脂质积累。
3.2 津力达颗粒对肥胖小鼠糖脂代谢紊乱的影响
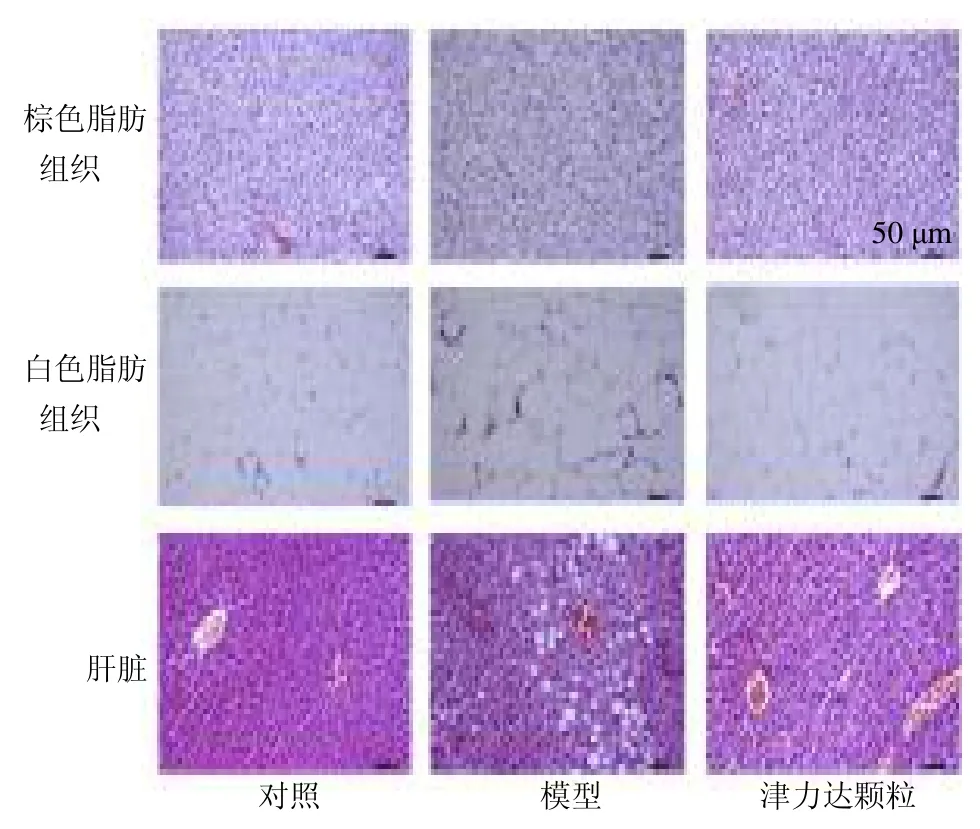
图3 津力达颗粒对肥胖小鼠棕色脂肪组织、白色脂肪组织和肝脏组织病理变化的影响 (HE,×200)Fig.3 Effect of Jinlida Granules on pathological changes of brown adipose tissue,white adipose tissue,and liver tissue in obese mice (HE,× 200)
糖脂代谢紊乱是高脂饮食诱导的肥胖小鼠的显著特征。如图4所示,与对照组比较,模型组小鼠血清TC、TG、LDL-C、HDL-C 水平明显升高(P<0.001);与模型组比较,津力达颗粒组小鼠血清TG、LDL-C 水平显著降低(P<0.01、0.001),HDL-C 水平显著升高(P<0.001)。如图5所示,与对照组比较,模型组不同时间点血糖水平及GTT-AUC 均明显升高(P<0.001),葡萄糖耐量受损明显;与模型组比较,津力达颗粒可显著改善葡萄糖注射后的血糖水平(P<0.01、0.001)及GTT-AUC(P<0.001)。表明津力达颗粒可有效改善高脂饮食诱导的肥胖小鼠糖脂代谢紊乱。
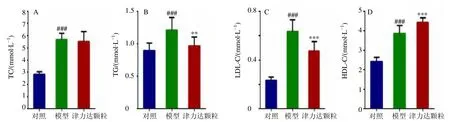
图4 津力达颗粒对肥胖小鼠血清TC (A)、TG (B)、LDL-C (C) 和HDL-C (D) 水平的影响 (±s,n=15)Fig.4 Effect of Jinlida Granules on levels of TC (A),TG (B),LDL-C (C),and HDL-C (D) in serum of obese mice(±s,n=15)
3.3 津力达颗粒对肥胖小鼠肝脏FGF21/AMPK 通路相关基因和蛋白表达的影响
如图6-A、B 所示,与对照组比较,模型组小鼠肝脏FGF21 mRNA 水平升高,FGFR1 mRNA 水平降低;与模型组比较,津力达颗粒组小鼠肝脏FGF21、FGFR1 mRNA 水平均显著升高(P<0.05、0.01)。如图6-C、D 所示,与对照组比较,模型组小鼠肝脏FGFR1、p-AMPK/AMPK 蛋白表达水平明显降低(P<0.05),Klotho、AMPK、p-AMPK 蛋白表达水平明显升高(P<0.05、0.01、0.001);与模型组比较,津力达颗粒组小鼠肝脏FGF21、p-AMPK、p-AMPK/AMPK 蛋白表达水平明显升高(P<0.05、0.001),Klotho、AMPK、SIRT1 蛋白表达水平明显降低(P<0.05)。表明津力达颗粒可有效激活FGF21/AMPK 信号通路,从而改善肝脏脂质代谢紊乱。
3.4 津力达颗粒对肥胖小鼠脂肪组织 FGF21/AMPK 通路相关基因和蛋白表达的影响
如图7-A 所示,与对照组比较,模型组小鼠脂肪组织FGF21 mRNA 水平降低;与模型组比较,津力达颗粒组小鼠脂肪组织FGF21 mRNA 水平显著升高(P<0.01)。如图7-B、C 所示,与对照组比较,模型组小鼠脂肪组织FGFR1 蛋白表达水平明显降低(P<0.01),Klotho、p-AMPK、SIRT1 蛋白表达水平均明显升高(P<0.05、0.01、0.001);与模型组比较,津力达颗粒组小鼠脂肪组织FGF21、AMPK、p-AMPK 蛋白表达水平明显升高(P<0.05、0.001)。表明津力达颗粒可有效激活FGF21/AMPK信号通路,从而改善脂肪组织脂质代谢紊乱。
4 讨论
研究表明,FGF21 可促进能量消耗、脂肪利用和脂质排泄,FGF21 已成为治疗肥胖、血脂异常、2 型糖尿病、脂肪肝疾病、代谢综合征的新型靶点[16-17]。在肥胖小鼠中,FGF21 的激活可减少脂质积累、改善葡萄糖耐量,进而增强胰岛素敏感性[18-20];此外,FGF21 可有效增加棕榈酸酯诱导的分化型人骨骼肌成肌细胞HSMMs 对葡萄糖的摄取,可有效改善相关胰岛素信号转导通路[21]。然而,肥胖小鼠和2 型糖尿病患者中FGF21 表达升高,但其胰岛素敏感性降低、下游信号调节受损,推测可能与机体在肥胖状态下,产生FGF21 抵抗,FGF21代偿性增高密切相关[22-23]。此外,相关研究表明,艾蒿[24]、新橙皮苷[25]、艾塞那肽[26]、n-3 长链多不饱和脂肪酸[27]等中药及小分子化合物可激活FGF21,改善肝脏、脂肪组织脂质积累。
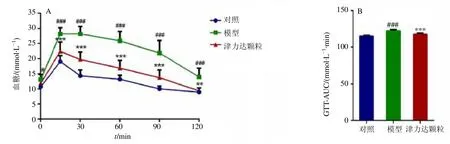
图5 津力达颗粒对肥胖小鼠不同时间点血糖水平 (A) 和GTT-AUC (B) 的影响 (±s,n=15)Fig.5 Effect of Jinlida Granules on blood glucose level at different time points (A) and GTT-AUC (B) in obese mice(±s,n=15)
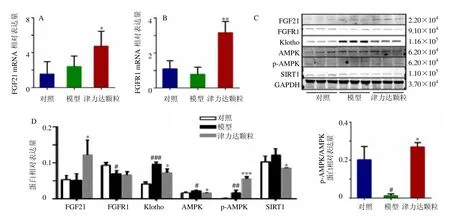
图6 津力达颗粒对肥胖小鼠肝脏FGF21/AMPK 通路相关基因和蛋白表达的影响 (±s)Fig.6 Effect of Jinlida Granules on expression of FGF21/AMPK pathway related genes and proteins in liver of obese mice(±s)
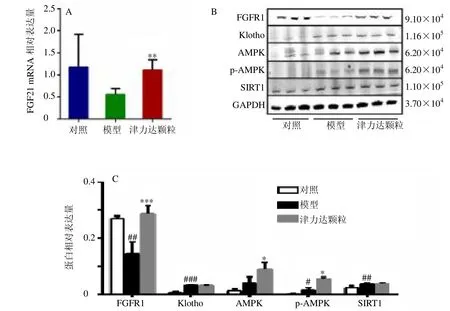
图7 津力达颗粒对肥胖小鼠脂肪组织FGF21/AMPK 通路相关基因和蛋白表达的影响 (±s)Fig.7 Effect of Jinlida Granules on expression of FGF21/AMPK pathway related genes and proteins in adipose tissue of obese mice (±s)
中成药津力达颗粒由人参、黄精、苍术、苦参、麦冬、生地黄、制何首乌、山茱萸、茯苓、佩兰、黄连、知母、淫羊藿、丹参、葛根、荔枝核、地骨皮17 味中药组成。人参为君药,补益脾之络气,使脾气旺而津液自生。黄精滋养脾阴,辅助人参,使脾阴足,运化自健;苍术燥湿解郁运脾,苦参清热燥湿,使热清湿化,气化自畅,3 药共为臣药,养脾阴、化脾湿、泻脾热、运脾气,并行不悖,相得益彰。佐药麦门冬生津止渴,生地黄壮水滋阴,何首乌善补益肝肾;山茱萸补肾涩精,诸药共佐黄精,不仅脾阴得滋,肝肾之阴亦得以滋填。佐药茯苓,淡渗利湿,助脾健运,佩兰芳香悦脾,以除陈气,用佐苍术,奏效尤速。黄连清热燥湿、泻火解毒用之佐苦参效力倍增,又佐以知母,滋阴降火、清热止渴。地骨皮去骨热消渴,佐苦参,泻肝肾虚火而不伤阴。淫羊藿扶肾阳而温脾土,丹参祛瘀生新、调经顺脉亦为佐药。葛根、荔枝核共为使药,葛根“气味皆薄,最能升发脾胃清阳之气”,荔枝核“行散滞气”使得气机畅达,津液自易输布;二药共用,调畅气机,使益气滋阴之药直达病所。全方诸药合用,补益脾之络气、滋养脾之阴津,配以清脾热、化脾湿、温脾阳、活血、行气诸药,治脾诸法并行不悖、相得益彰,使脾气旺而运化健,脾阴足而津自生,消渴病诸症悉除。津力达颗粒中的活性成分达森海因钠、葛根素、丹酚酸B、淫羊藿苷B、淫羊藿苷C、淫羊藿苷、人参皂苷Rb1、人参皂苷Rc 和人参皂苷Rb2具有抗脂质过氧化、清除氧自由基、抑制炎症反应等多种药理活性[28-29]。
长期的高脂饮食饲养可导致小鼠能量失衡、代谢紊乱。本研究发现,与对照组比较,高脂饮食诱导的肥胖小鼠脂肪和肝脏组织中产生了脂质蓄积和胰岛素抵抗;津力达颗粒显著抑制高脂饮食诱导的肥胖小鼠体质量、脂肪组织和肝脏组织质量,显著降低血清TG、LDL-C 水平,升高血清HDL-C 水平,并有效改善葡萄糖耐量。表明津力达颗粒可有效改善脂质代谢紊乱及葡萄糖稳态,可显著降低高脂饮食诱导的肥胖小鼠发生高脂血症和胰岛素抵抗的风险。
为了考察津力达颗粒调节糖脂代谢作用与FGF21 的相关性,本研究检测了肝脏、脂肪组织FGF21 及其相关受体基因及蛋白表达情况,结果显示,津力达颗粒组小鼠肝脏FGF21 mRNA 和蛋白表达均显著上调,表明津力达颗粒可激活FGF21,从而改善肝脏脂质积累。FGF21 能否发挥生物活性与其受体FGFR1、共受体β-Klotho 密切相关[30]。结果显示,津力达颗粒组小鼠肝脏FGFR1 mRNA水平升高,表明FGF21 敏感性增加,但FGFR1 蛋白表达水平未见明显差异,可能与其磷酸化水平相关。津力达颗粒组共受体β-Klotho 蛋白水平较模型组降低,但显著高于对照组,此结果与在高热量喂养条件下,Klotho-/-小鼠能量升高、β-Klotho 效能降低,产生抵抗,进而代偿性分泌增多一致[31];津力达颗粒组小鼠脂肪组织FGF21 mRNA 表达显著上调,表明津力达颗粒可激活FGF21、改善脂肪蓄积;津力达颗粒组FGFR1 蛋白表达升高,表明FGF21 敏感性增加,β-Klotho 未出现显著差异。综上,津力达可通过激活FGFR1/β-Klotho 受体复合物,进一步增强FGF21 在调节葡萄糖、脂质代谢、保存能量稳态方面的积极作用。
FGF21 可能通过激活AMPK 调节脂肪细胞的能量稳态,从而增强线粒体的氧化功能[32]。AMPK作为细胞能量传感器,AMPK 的激活可调节细胞和体内的能量代谢,改善胰岛素敏感性[33]。然而,当暴露于持续的代谢负担时,如代谢综合征或2 型糖尿病中,AMPK 活性失调[34]。本研究进一步考察肝脏、脂肪组织AMPK 信号通路中相关基因及蛋白的表达,结果显示,津力达颗粒组小鼠肝脏、脂肪组织中p-AMPK、p-AMPK/AMPK 蛋白表达水平明显升高,表明AMPK 途径在津力达颗粒激活FGF21、改善糖脂代谢中发挥重要作用。此外,SIRT1 作为AMPK 的下游分子,可调控能量代谢相关基因表达[35]。津力达颗粒可有效降低小鼠肝脏中SIRT1 蛋白表达水平,可能与其中枢抑制效应增强有关,而脂肪组织中其蛋白表达水平无明显变化。
综上所述,津力达颗粒可有效改善高脂饮食诱导的代谢紊乱,如肥胖、血脂异常、葡萄糖耐受异常、肝脏脂肪变性、白色脂肪过度蓄积等。津力达颗粒对肝脏、白色脂肪组织形态和分子生物学有显著影响。此外,津力达颗粒可通过激活FGF21/AMPK 信号通路,改善肝脏、脂肪组织脂质代谢紊乱。
利益冲突所有作者均声明不存在利益冲突
