LAA%预测肺癌合并慢性阻塞性肺疾病患者肺叶切除术后心肺并发症的价值
2021-03-04李晓冬王钺许晶晶
李晓冬,王钺,许晶晶
(沧州市人民医院医专院区 影像科,河北 沧州061000)
在肺癌切除术中,慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)是术后心肺并发症的危险因素[1]。根据全球慢性阻塞性肺疾病倡议(GOLD),第一秒用力呼气容积(FEV1)占用力肺活量(FVC)的比值(FEV1/FVC)与COPD 严重程度有关。手术后FEV1/FVC 与术后心肺并发症也存在关联[2]。然而,很少有研究评估影像学肺气肿改变与术后心肺并发症的关系。因此,本研究回顾性分析肺癌合并COPD 患者肺叶切除术前CT 图像中肺气肿区域比例与术后心肺并发症的关系。
1 资料与方法
1.1 一般资料
收集2013年3月—2018年6月在沧州市人民医院医专院区治疗的80 例行肺叶切除术的肺癌合并COPD 患者。纳入标准:①年龄≥18 岁;②行肺叶切除术。排除标准:①术前CT 图像显示间质和其他弥散变化;②支气管哮喘史;③术前感染引起并发症,如肺炎或脓肿形成;④肺癌肺叶切除术史。本研究经医院医学伦理委员会批准,患者及其家属签署知情同意书。
1.2 方法
1.2.1 一般资料收集记录所有患者的基线资料和临床特征,包括年龄、性别、吸烟史、体重指数、动脉氧分压、动脉二氧化碳分压、肺活量、FEV1/FVC,以及肺叶切除、淋巴结分离、手术时间及失血量等。
1.2.2 胸部CT采用64 排螺旋CT 扫描仪(荷兰飞利浦医疗有限公司)对所有患者行吸气末全肺平扫。CT 检查时患者取仰卧位,双臂上举抱头,从头到脚方向扫描,在患者吸气末屏气状态下自肺尖至肺底进行全肺扫描。CT 扫描前叮嘱患者练习吸气末屏气动作。胸部CT 扫描参数,管电压:120 kV,自动电流,扫描准直:128.000×0.625,旋转时间:0.5 s,螺距:0.915,床速:146.4 mm/s。CT 检测完成后将数据传输至后处理工作站,测量低衰减区占肺野面积百分比(percentage of the low attenuation area, LAA%),即吸气末HU 值低于阈值(-950 HU)占全肺体素总数的百分比。典型CT 扫描图像见图1、2。
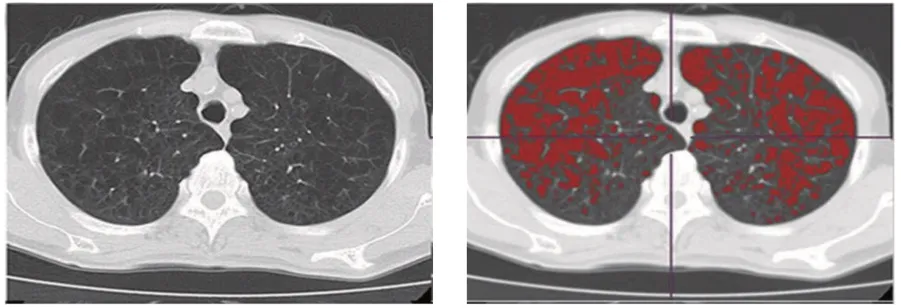
图1 患者LAA%为28.9%的CT图像

图2 患者LAA%为0.5%的CT图像
1.3 心肺并发症
观察患者手术后6 个月的心肺并发症,包括脓胸、支气管胸膜瘘、肺炎(体温>38℃、持续48 h,产生化脓性痰,X 射线检查显示胸部浸润)、肺不张、急性肺损伤、长期漏气(>7 d)、氧气供应时间长(>7 d)及心律失常等。
1.4 统计学方法
数据分析采用SPSS 19.0 统计软件。计量资料以均数±标准差(±s)表示,比较用t检验;计数资料以率(%)表示,比较用χ2检验;绘制ROC 曲线,影响因素的分析用多因素Logistic 回归模型,P<0.05 为差异有统计学意义。
2 结果
2.1 两组病例资料比较
共30 例(37.5%)患者出现术后心肺并发症,包括脓胸1 例、支气管胸膜瘘1 例、肺炎和肺不张5 例、急性呼吸窘迫综合征1 例、持续漏气>7 d 8 例、氧气供应持续时间>7 d 18 例及心律失常8 例,部分患者出现多种并发症。本研究中,围手术期无死亡患者。并发症患者中,从前吸烟者18 例,目前吸烟者12 例。单因素分析显示,年龄、失血量、FEV1/FVC、LAA%与术后心肺并发症有关(P<0.05)。见表1。
2.2 LAA%预测心肺并发症的ROC曲线
经ROC曲线分析,1%作为LAA%最佳截点值预测心肺并发症,其敏感性为75.7%(95%CI:1.78,8.94),特异性为62.5%(95%CI:1.07,6.43)。见图3。

表1 肺癌合并COPD患者有并发症组与无并发症组病例资料比较

图3 LAA%预测心肺并发症的ROC曲线
2.3 心肺并发症影响因素的多因素Logistic 回归分析
将有无心肺并发症作为因变量(有心肺并发症=1,无心肺并发症=0),以单因素分析中有统计学意义并可能促进心肺并发症发生的因素,包括年龄、FEV1/FVC、GOLD 分类、动脉氧分压、LAA%及失血量作为自变量,进行逐步Logistic 回归分析,α入=0.05,α出=0.10。结果显示,年龄、LAA%是患者术后发生心肺并发症的独立预测因子(P<0.05)。见表2。

表2 心肺并发症影响因素的多因素Logistic回归分析相关参数
3 讨论
目前,LAA%被认为是肺气肿指数最准确的定量指标[3]。其可由放射科医生在几分钟内测量出,具有良好的客观性和可重复性。在低衰减阈值下,可以很容易地计算肺气肿面积比值。此外,与肺功能检查相比,LAA%能更有效地评估早期肺气肿的变化[4]。GOLD 分类法已广泛用于胸部CT 来评估COPD。然而,这是一种主观评价方法,不同观察者会存在评分差异。以往研究指出,LAA%与COPD 患者肺功能和运动能力相关,同时也是肺癌危险因素[5]。目前定量CT 在临床肺容积减少手术中的临床应用已有报道[6],但报告根据CT 图像定量肺气肿相关参数来预测术后心肺并发症的研究少有。在以往的研究中,LAA%未被证实是心肺并发症相关指数[7]。而动脉血氧饱和度和术后FEV1/FVC 被证明是术后心肺并发症重要的预测因子[8]。上述研究提示,采用LAA%结合肺活量测定法可能有助于预测术后心肺并发症。
本研究的Logistic 回归分析结果表明,LAA%是心肺并发症的独立预测因子。一项研究报告指出,肺活量检测基线气道无阻塞患者随访期肺气肿变化高于未发生阻塞患者[9]。这表明除非肺气肿严重程度超过特定阈值,一般情况下气流不受限制,LAA%可用于评估亚临床可能导致气道阻塞的COPD。此外另有研究报道,10.4%肺气肿和COPD患者显示肺活量测定结果正常[10]。通过以上研究笔者可得出结论,与肺活量检测相比,LAA%能更灵敏地检测与吸烟相关的肺泡疾病。本研究中,53例患者属于GOLD 1 级,表明气道轻度阻塞。LAA%可能是肺癌合并COPD 患者肺叶切除术后发生心肺并发症的客观预测指标。
本研究中,从前吸烟者心肺并发症发生率与目前吸烟者无差异。这表明吸烟对肺泡结构破坏和肺血管床减少不可逆转,戒烟不能减少心肺并发症。此外,采用LAA%作为心肺并发症预测因子仍存在一些限制,例如不能用LAA%来评价肺间质性病变;另外,采用LAA%不能评估以小气道阻塞为主的COPD 患者术后心肺并发症。因为COPD 最重要气流阻塞点是直径≤2 mm 的气道,在呼气CT扫描中,空气潴留被认为是小气道功能障碍的间接表现。最近,呼气CT 中肺体素百分比<−856HU被提议用于COPD 患者空气潴留的检测[11]。
总之,LAA%可用于预测行肺叶切除术的肺癌合并COPD 患者术后心肺并发症。对年龄≥70 岁且LAA%≥1.0%的患者,必须谨慎地进行术中和术后处理。
