基于隧道实验机动车苯并噻唑及其衍生物排放特征研究*
2021-03-04常俊雨门正宇孙露娜金嘉欣毛洪钧
常俊雨 门正宇 孙露娜 魏 宁 金嘉欣 吴 琳 王 婷 毛洪钧
(南开大学环境科学与工程学院,城市交通污染防治研究中心,天津 300071)
苯并噻唑及其衍生物(BTs)是一组由1,3-噻唑环与苯环熔合而成的杂环芳香族化合物,常在橡胶产品生产过程中被用做硫化促进剂[1]11580,还可用做金属表面的缓蚀剂和汽车用油的防冻剂[2]。常见的BTs有苯并噻唑(BT)、2-氨基苯并噻唑(2-NH2-BT)、2-羟基苯并噻唑(2-OH-BT)、2-巯基苯并噻唑(MBT)、2-甲硫基苯并噻唑(MTBT)和N-环己基-2-苯并噻唑次磺酰胺(CBS)等。
BT常应用于制备偶氮染料光敏剂[3]、农药[4]、杀菌剂[5-6]、除草剂[7]的化学中间体和紫外线稳定剂[8],BT还被斯洛伐克共和国(欧盟2013)定为重点研究物质之一[9]。MBT经常作为轮胎主要硫化促进剂,与贵金属及Zn、A1、Cu、Hg等形成稳定的配合物,广泛作为贵金属的沉淀剂及萃取剂[10-11]。BTs因具有应用广泛、持久难降解、生物毒性等特征而引起了广泛关注[12-15]。AVAGYAN等[1]11582研究表明,沥青样品中MBT浓度低于检出限,BT的质量分数低于空气颗粒物样品,轮胎磨损可能是城市环境中MBT和BT的主要来源。2-NH2-BT常用作抗氧化物和热固性塑料的黏合剂。CBS主要用于制造轮胎、电缆等各种橡胶制品。由于BTs具有较强的环境迁移潜力,人体不可避免地通过皮肤、口腔或吸入等途径与BTs接触[16]。BTs已被证明是皮肤致敏剂[17],也与微生物的致突变性和人类的致癌性有关[18]。流行病学研究表明,橡胶厂工人特别是那些暴露于MBT的工人患膀胱癌、肺癌和白血病癌症的风险更高[19]。
WAN等[20]40在车库样品中测得BTs,均值为14.2 ng/m3。ASHEIM等[21]在道路尘中测得6种BTs,质量浓度为93.4~1 903 ng/L。MACEIRA等[22]在康斯坦蒂港和塔拉戈纳港采集到10个气态颗粒物样本,测得其中的BTs分别为0.17~8.9、0.009~3.3 ng/m3。ZHANG等[23]在17个不同轮胎品牌的轮胎磨损颗粒物样品中均检测到BT和2-OH-BT,且为主要化合物,占总化合物质量的56%~89%。
轮胎磨损是城市环境中气态BTs的主要来源之一,由于隧道环境相对密闭,污染物主要来自机动车排放,容易获取车队整体排放水平与变化趋势,因此隧道实验成为国内外研究机动车排放的重要手段之一[24-27]。本研究通过测定青岛嵩山隧道内PM2.5和PM10中6种BTs的分布特征并计算其排放因子,研究机动车源BTs的排放特征;通过计算人体对BTs的呼吸日暴露量,明确机动车对BTs的贡献及环境危害。
1 实验部分
1.1 主要试剂及材料
BT(97%,CAS号:95-16-9)、2-NH2-BT(98%,CAS号:136-95-8)、2-OH-BT(98%,CAS号:934-34-9)、MBT(97%,CAS号:149-30-4)采购于德国Alfa Aesar公司;MTBT(>98%,CAS号:615-22-5)、CBS(95%,CAS号:615-22-5)采购于日本Tokyo Kasei Kogyo公司;D4-BT内标(CAS号:164423-51-3)采购于加拿大Toronto Research Chemicals公司;甲醇(色谱纯);Poly-Sery HLB固相萃取小柱;固相萃取小柱连接管;色谱柱(ACQUITY UPLC BEH SHIELD RP 18 column,100.0 mm×3.0 mm×1.7 μm)和保护柱(BEH C18,5.0 mm×2.1 mm×1.7 μm)均为美国Waters公司生产。
1.2 样品采集与分析
1.2.1 采样地点与方法
嵩山隧道位于青岛经济技术开发区以东、丁家河以西的烟固墩山,隧道为双洞四车道,左线隧道总长550.00 m、暗洞全长453.00 m,右线隧道总长550.00 m、暗洞全长458.00 m。隧道设计净高7.00 m、净宽10.97 m。本次隧道观测选取右线隧道,在暗洞左侧平台入口和出口布置HY-100WS型采样器和MTC-10型交通调查仪(见图1),采集时段为2018年6月16日(周六)至22日(周五),共28个有效样品,期间包含端午节假期(6月16-18日)。
以100 L/min的速率使用中流量采样器和PM2.5、PM10切割头采集23.5 h,采样前石英纤维滤膜(Φ90 mm)先在马弗炉内600 ℃烘焙2 h,随后置于恒温(20 ℃)、恒湿(50%)天平室中平衡48 h以上,用1/100 000天平称重3次取均值,误差为-0.000 05~0.000 05。采样后石英纤维滤膜使用采样前的处理步骤,并保存于冰箱(约4 ℃)。
使用交通调查仪采集各车道所有过往车型和车流量数据。
1.2.2 样品分析
每张滤膜样品取1/2张置于15 mL的带盖玻璃离心管中,每隔10个样品加入1个空白对照样品。先在每个离心管中添加10 ng D4-BT内标,室内平衡至内标溶剂挥发。再添加8 mL提取剂(即5 mL甲醇+3 mL超纯水),密封后置于超声波水浴槽中超声60 min,4 000 r/min离心10 min,使用0.45 μm孔径的尼龙有机相滤头和一次性注射器提取上清液至40 mL棕色样品瓶中,离心管加入相同的8 mL提取剂重复上述过程一次,每个样品得到约16 mL的溶剂。然后样品瓶中添加甲醇水溶液(甲醇和超纯水体积比为1∶3),最后用固相萃取小柱净化样品。

图1 嵩山隧道采样点位示意图Fig.1 Sampling site in the Songshan tunnel

表1 BTs的检出限、定量限和加标回收率
先用5 mL甲醇和5 mL超纯水对固相萃取小柱进行活化和平衡;再使用真空泵抽取,样品以4 mL/min上样;然后用10 mL甲醇水溶液(甲醇和超纯水体积比为1∶5)进行洗杂,真空泵抽真空干燥固相萃取小柱;最后用5 mL甲醇洗脱目标物,取1.5 mL于2 mL 9 mm棕色螺纹口自动进样瓶进样。
使用美国Waters公司生产的超高液相色谱仪(Waters ACQUITY UPLC)串联三重四极杆质谱仪(Xevo TQ-S)对标准溶液和样品进行分离测试。
1.2.3 质量控制
为检验前处理和检测方法的可靠性,通过向空白滤膜样品中添加20、50 μg/L的标准溶液(即处理1、2)和10 ng D4-BT内标,每个样品做3个平行样,并完整进行提取—纯化—浓缩定容等过程,经D4-BT内标校正后的6种物质的回收率具体见表1。除2-NH2-BT外,其他5种物质的加标回收率均在92.00%~125.77%,各物质标准曲线的R2均大于0.99。通过添加空白样品来评估实验室耗材和试剂的背景影响,每隔10个样品加一个空白样品,结果表明,空白样品中BTs浓度均低于样品中浓度多个数量级。
1.3 隧道BTs的排放因子计算
将隧道看作一个理想的圆柱状活塞,一定时间内机动车污染物排放总量等于隧道进出口污染物浓度差与通风量的乘积。基于此原理,利用式(1)计算隧道内机动车排放因子(EFs,ng/(km·辆))。
(1)
式中:Cout、Cin分别为隧道出、入口BTs质量浓度,ng/m3;A为隧道横截面积,m2;v为隧道内空气流速,m/s;t为采样时间,s;N为采样时间内的车流量,辆;L为隧道入口与出口的距离,km。
1.4 人体对隧道BTs呼吸暴露计算
机动车排放位于人体呼吸带高度,吸附在PM10或PM2.5表面的潜在致癌物质主要通过呼吸的方式进入人体,因此通过计算人体对BTs的呼吸日暴露量,研究隧道环境对人体健康的潜在风险。人体对空气颗粒物中BTs的呼吸日暴露量(DIinh-air,ng/(kg·d))计算见式(2)[28]。
(2)
式中:Cair为空气颗粒物中BTs质量浓度,ng/m3;LnhR为呼吸速率,m3/d,成人取16.7 m3/d;EF为暴露频率,d/a,取180 d/a;ET为平均日暴露时长,d/d,取0.08 d/d;ED为暴露年限,a,成人取30 a;BW为平均体重,kg,成人取58.55 kg;AT为平均作用时间,d,取365ED[29]。
2 结果分析
2.1 车流量分析
青岛没有限号政策,嵩山隧道日车流量为1.5万~1.9万辆,其中节假日(6月16-18日)的车流量低于非节假日(6月19-22日),6月18日达到最低(15 454辆)。交通调查仪将车辆分为9类车型(摩托车、微型客车、小型客车、中型客车、大型客车、微型货车、轻型货车、中型货车和重型货车),由于部分车型数量较少,故本研究分为3类(其他车型、小型客车和微型货车)。由图2可见,居主导地位的是小型客车((12 190±647)辆),其次是微型货车((3 968±457)辆),两者之和约占总日车流量的93.8%以上。

图2 隧道中不同车型的日车流量Fig.2 Daily traffic flow of different types of vehicles in the tunnel
2.2 隧道BTs分析
隧道中BTs质量浓度分布见表2,其中CBS均低于检出限,其他5种BTs检出率均为100%。AVAGYAN等[1]11583也得到相似结果,在PM10和总悬浮微粒(TSP)样品中检测不到CBS。这是因为在轮胎硫化过程中,CBS硫化促进剂发生了化学反应。WAGNER等[30]研究表明,只有不到1%(质量分数)的CBS能在橡胶硫化过程中保存下来。
隧道PM10和PM2.5中BTs的浓度分布较相似,且浓度顺序为2-OH-BT>BT>MTBT>MBT>2-NH2-BT>CBS,其中2-OH-BT和BT质量浓度总和占BTs的70%以上。2-OH-BT浓度高于BT,其原因可能是在轮胎磨损过程中,一部分BT发生氧化产生2-OH-BT。WANG等[31]实验发现,轮胎碎屑在高温中会引发BT向2-OH-BT的转化。WAN等[20]40在检测7种环境的空气样本中发现,汽车环境样品中MTBT检出质量浓度为0.23~3.77 ng/m3,与本实验数值类似。
隧道中BTs的排放源主要是机动车,PM10中2-OH-BT浓度与车流量密切相关。使用JMP软件分析PM10中2-OH-BT和3类车型的相关性,结果见表3。PM10中2-OH-BT与3类车型都有很好的显著相关性,表明2-OH-BT可作为机动车排放的标识物。隧道出口PM10中2-OH-BT与3类车型的相关度总体高于隧道入口,这是受到隧道活塞效应影响,机动车排放的2-OH-BT在隧道中得到累积。
2.3 隧道BTs的排放因子
PM2.5、PM10和BTs的排放因子见表4。PM2.5、PM10排放因子分别为(18.58±8.10)、(52.21±30.10) mg/(km·辆),PM2.5、PM10中BTs排放因子分别为(733.14±54.00)、(1 281.94±92.05) ng/(km·辆)。截至目前,隧道中机动车排放因子计算以颗粒物居多,这是首次计算隧道中机动车BTs的排放因子。在相同的60 km/h限速条件下,深圳隧道中PM2.5的排放因子((64.00±13.50) mg/(km·辆))[32]约为本研究结果的3.4倍,这可能与重型车占比不同有关,本研究中重型车客货车数量只占到2.4%,而深圳隧道中重型车高达33.8%。
2.4 人体对隧道BTs的呼吸暴露

表2 隧道中BTs质量浓度分布
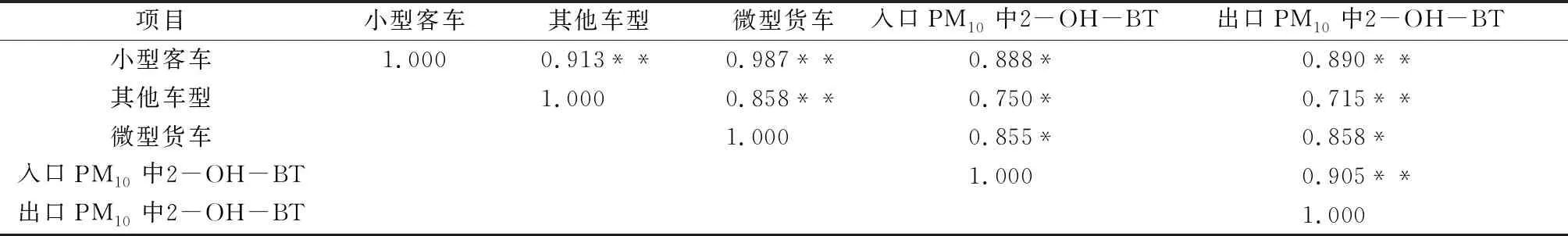
表3 PM10中2-OH-BT和3类车型的相关性分析1)

表4 PM2.5、PM10和BTs的排放因子1)

表5 人体对隧道PM2.5和PM10中BTs的呼吸日暴露量
人体对隧道PM2.5和PM10中BTs的呼吸日暴露量分别为(11.45±1.72)、(29.60±3.05) ng/(kg·d)(见表5),机动车排放BTs对路边环境人群具有较大健康风险。WAN等[20]41计算了在汽车环境中,一个成年人的日暴露量为83.50 ng/(kg·d),约是本研究隧道PM10中BTs的呼吸日暴露量的2.82倍。根据式(2),本研究核算的综合暴露因子((EF×ET×ED)/AT)为0.98,反而高于WAN等[20]41选用的综合暴露因子(0.80),造成这样差异主要是因为WAN等[20]40检测的BTs浓度高于本研究。
3 结 论
(1) 青岛嵩山隧道日车流量为1.5万~1.9万辆,其中主要以小型客车和微型货车为主,两种车型之和占到总日车流量的93.8%以上,节假日车流量低于非节假日。
(2) 隧道入口PM2.5、PM10中BTs分别为(1.85±0.33)、(5.49±0.38) ng/m3;隧道出口PM2.5、PM10中BTs分别为(2.66±0.44)、(6.48±1.01) ng/m3;2-OH-BT和BT为主要成分,两者质量浓度总和占BTs的70%以上。
(3) 2-OH-BT可作为机动车排放的标识物。
(4) PM2.5、PM10中BTs排放因子分别为(733.14±54.00)、(1 281.94±92.05) ng/(km·辆)。
(5) 人体对隧道PM2.5和PM10中BTs的呼吸日暴露量分别为(11.45±1.72)、(29.60±3.05) ng/(kg·d),机动车排放BTs对路边环境人群具有较大健康风险。
