HPLC-HG-AFS联用测定茶叶中四种砷的形态化合物
2021-03-04黄田富张著森丘则海
黄田富,张著森,丘则海
HPLC-HG-AFS联用测定茶叶中四种砷的形态化合物
黄田富,*张著森,丘则海
(龙岩学院化学与材料学院,福建,龙岩 364000)
建立了茶叶中砷形态的高效液相色谱-氢化物发生-原子荧光光谱(HPLC--HG-AFS)分析方法。该方法以5.0%作为盐酸载液的浓度,2%作为还原剂硼氢化钾的浓度,选择Na2HPO4和KH2PO4混合液作为流动相,pH值为5.92。在7min之内,砷形态:亚砷酸根As(Ⅲ)、二甲基砷酸( DMA)、一甲基砷酸(MMA)、砷酸根As(Ⅴ)依次出现峰,实现了完全分离。在0~100ng/mL的线性范围内,砷的4种形态标准曲线线性良好,线性相关系数分别为0.9995、0.9991、0.9993、0.9993,检出限分别为0.064、0.127、0.089、0.095 ng/mL,精密度分别为2.26%、1.84%、2.05%、1.59%,加标回收率为94%~105.15%。测试结果表明,该方法能够准确、快速和灵敏检测茶叶中砷的4种形态化合物。
高效液相色谱-氢化物发生-原子荧光光谱;茶叶;砷形态
砷是一种有毒的非金属元素,长期接触砷会对人体多种组织、器官造成危害,甚至致癌和致畸等[1-2]。而在生物体内和环境中存在的砷的形态化合物高达30多种[3]。元素的毒性与元素的存在形态密切相关。毒理学研究表明,亚砷酸盐As(Ⅲ)>砷酸盐As(Ⅴ)>一甲基砷酸MMA>二甲基砷酸DMA>砷胆碱AsC>砷甜菜碱AsB,无机砷的毒性较大,有机砷的毒性较小,AsC和AsB常被认为是无毒的[4-6]。因此,传统分析检测方法只对测定样品中砷的总量进行测定,不能够充分满足食品药品监测与毒理学评价的要求,因此对砷形态进行分离分析检测具有重要意义[7-8]。
茶叶因富含茶多酚、氨基酸、维生素、生物碱及多种微量元素等,被世界公认为天然绿色饮料,作为不含酒精的世界三大饮料之一,广受全球人民的推崇[9-10]。但是,随着全球工业化的快速发展,工业“三废”的排放、含砷化肥、农药使用,导致砷污染已成为非常严重的环境问题之一。而茶叶在此环境中种植,比较容易吸收富集砷,导致砷是茶叶中6大有害元素之一[11-13]。随着茶叶生长,砷发生氧化还原、甲基化等生物化学反应过程,其化学存在形态发生了一系列变化。因此,对茶叶中砷形态进行分析和测定,科学、客观地对茶叶中砷的安全作出评价,进行风险评估,为更科学地评价茶叶中砷对人体健康造成的危害提供理论依据。
目前砷形态的检测主要有HGLC-ICP-MS[4]、LC-HG-AAS[1]、LC-ICP-AES[1]、LC-HG-AFS[14]等,其中电感耦合等离子质谱(ICPMS)操作复杂,成本昂贵,原子吸收光谱(AAS)不能连续进样等问题。本研究采用高效液相色谱、在线消解、氢化物发生原子荧光在线联用系统,测定4种As形态As(Ⅲ)、As(Ⅴ)、一甲基砷酸MMA、二甲基砷酸DMA,建立了一种新的茶叶中砷形态检测方法,该法操作简单、成本低、灵敏度高、结果准确可靠。
1 实验部分
1.1 主要仪器和试剂
AFS-9800全自动四灯位原子荧光光度计:北京海光仪器有限公司;砷高强空心阴极灯:北京有色金属研究总院;台式离心机:长沙英泰仪器有限公司;阴离子色谱交换柱:Hamilton PRPX-100 (250 mm×4.1 mm,10 μm),瑞士Hamilton公司;在线消解仪:FUV-300,北京海光仪器公司,0.22 μm滤膜,上海市新亚净化器件厂。
硼氢化钾、磷酸氢二钠、磷酸二氢钾、磷酸二氢铵、磷酸二氢钠、氢氧化钠:分析纯,国药集团化学试剂有限公司;盐酸、硝酸:优级纯;砷形态标准溶液:As(Ⅲ)亚砷酸根溶液标准物质(GBW08666),As(Ⅴ)砷酸根溶液标准物质(GBW08667),一甲基砷酸MMA溶液标准物质(GBW08668),二甲基砷酸DMA溶液标准物质(GBW08669),规格2 mL,网购于国家标准物质中心;实验用水为超纯水(达到GB6682-92规定一级水要求)。所用器具均在10%硝酸中浸泡24 h后用超纯水洗净。
1.2 实验方法
1.2.1 液相色谱条件及原子荧光条件
液相色谱条件:阴离子色谱交换柱:Hamilton PRPX-100(250 mm×4.1 mm,10 μm);流动相流量:1.00 mL/min;进样体积:100 μL。
原子荧光条件:原子化器高度:8.0 mm,原子化方式:火焰原子化,光电倍增管负高压:300 V,砷空心阴极灯电流:主电流60 mA,辅助电流30 mA,氩气流量:载气400 mL/min,屏蔽气900 mL/min。还原剂:硼氢化钾2%和氢氧化钠0.5%混合溶液,备用。载液:5%HCl溶液,流速为4 mL/min。测量方式:标准曲线法;读数方式:峰面积。
1.2.2 标准储备液的配置
用移液枪分别精密吸取As(Ⅲ)亚砷酸根溶液标准物质、As(Ⅴ)砷酸根溶液标准物质、一甲基砷酸MMA溶液标准物质、二甲基砷酸DMA溶液标准物质适量,放入100 mL容量瓶,加入超纯水定容,摇匀得到浓度均为1000 ng/mL的单标储备液,备用。再分别精密吸取上述4种单标储备液0、0.25、0.50、1.00、2.00、3.00、4.00、5.00 mL置于50 mL容量瓶中,加入超纯水定容,得到浓度为0、5.0、10.0、20.0、40.0、60.0、80.0、100.0 ng/mL的系列砷混合标准溶液,现配现用。
1.2.3 样品中砷形态提取
样品为市售茶叶,产地为龙岩市,用超纯水洗净,切成薄片,放入80 ℃烘箱,烘12 h,转移真空干燥箱,继续80 ℃烘6 h,取出研磨,过80目筛,备用。样品中砷形态提取参照文献[15]方法提取。准确称取样品0.5 g(精确到0.0001 g),置于10 mL比色管中,加入4 mL10% HCl,在70 ℃水浴振荡器中以100 r/min震摇1 h,然后再加入4 mL水并继续震摇1 h,然后用0.22 μm滤膜过滤,得到溶液用于上机测定。
1.2.4 实验过程
先将系列砷混合标准溶液放入仪器进样口,经高效液相色谱分离,FUV-300在线消解处理,氢化物发生原子荧光在线联用测试系统,进行分离产物荧光强度的测定。采用标准曲线法得到荧光强度与浓度关系的直线方程。最后将1.2.3得到的待测液放入进样口,用同样的测试方法测定待测物的荧光强度,代入直线方程,得到待测物的浓度。
2 结果与讨论
2.1 盐酸浓度对荧光强度的影响

图1 不同盐酸浓度对荧光强度的影响
载液盐酸浓度对砷荧光强度有重要的影响。取40.0 ng/mLAs(Ⅴ)砷酸根标准溶液、2%的硼氢化钾溶液,考察9种盐酸浓度(1.0%、2.0%、3.0%、4.0%、5.0%、6.0%、7.0%、8.0%、9.0%)对产生荧光强度的影响,结果如图1所示。由图1可知,荧光的强度先递增后递减,浓度为5.0%时,荧光强度值最大。因此,选择5.0%作为盐酸载液的浓度。
2.2 还原剂硼氢化钾浓度对荧光强度的影响

图2 不同硼氢化钾浓度对荧光强度的影响
配置8种不同质量浓度的硼氢化钾溶液(0.5%、1.0%、1.5%、2.0%、2.5%、3.0%、3.5%、4.0%),取40.0 ng/mLAs(Ⅴ)砷酸根标准溶液、5%的盐酸载液,荧光强度测试结果如图2所示。由图2可知,当硼氢化钾浓度小于2%时,随着硼氢化钾浓度的增加,荧光强度值递增;当质量分数达到2%时,荧光强度值达最大,随后荧光强度逐渐递减。产生这种现象的原因是,当硼氢化钾浓度低时,反应不完全而产生的气态砷化氢少,因此,荧光强度低;当硼氢化钾浓度过量时,反应虽完全,但产生的过量氢气会对砷化氢产生稀释作用,导致荧光强度降低。因此,选择2%作为还原剂硼氢化钾的浓度。
2.3 流动相的选择
分别对NH4H2PO4溶液、NaH2PO4溶液、Na2HPO4和KH2PO4混合液作为流动相进行选择。以12 mmol/L NH4H2PO4溶液为流动相,进行分离测定时,砷的四种形态出峰时间长,二甲基砷酸DMA和As(Ⅲ)亚砷酸根信号强度低,分离效果差。以15 mmol/L NaH2PO4溶液为流动相,pH值为9.0 进行分离时,As(Ⅲ)亚砷酸根、二甲基砷酸DMA和一甲基砷酸MMA信号强度较低,出峰的位置比较接近,分离效果较差。以Na2HPO4和KH2PO4混合液为流动相,pH值为5.92,超声脱气后,进行分离时,As(Ⅲ)亚砷酸根、二甲基砷酸DMA、一甲基砷酸MMA和As(Ⅴ)砷酸根在7 min内完全分离,依次出现,峰尖锐,且信号强度高,因此选择Na2HPO4和KH2PO4混合液作为流动相,pH值为5.92。这与相关文献[3]结论一致。
2.4 色谱图分析

图3 砷混合标准溶液的色谱图
在1.2.1液相色谱条件及原子荧光条件下,5.0%盐酸载液,2%还原剂硼氢化钾,对浓度为60.0 ng/mL的砷混合标准溶液进行测试,色谱图见图3。从图3可知,在7 min之内,砷形态:亚砷酸根As(Ⅲ)、二甲基砷酸( DMA)、一甲基砷酸(MMA)、砷酸根As(Ⅴ) 依次出现峰,实现了完全分离,其保留时间分别为2.21、2.76、3.50、5.52 min。
2.5 砷形态分析的标准曲线、检出限与精密度。
表1 标准曲线方程、线性范围、精密度值及检出限
Table 1 Standard curve equation, linear range, precision value and detection limit
砷元素形态线性方程相关系数线性范围(ng/mL)精密度值(%)检出限(ng/mL) As(Ⅲ)y=8.925x+17.7260.99950~1002.260.064 DMAy=6.8348x-16.3590.99910~1001.840.127 MMAy=6.382x+10.1250.99930~1002.050.089 As(Ⅴ)y=3.566x+36.0210.99930~1001.590.095
在1.2.1液相色谱条件及原子荧光条件下,5.0%盐酸载液,2%还原剂硼氢化钾,对浓度为0、5.0、10.0、20.0、40.0、60.0、80.0、100.0 ng/mL的系列砷混合标准溶液进行测定。以荧光强度为纵坐标(),以砷形态的质量浓度为横坐标()进行线性回归,分别得到4种砷形态的线性方程,并计算出相关系数(R)。对标准空白溶液连续11次测定荧光强度,根据下列公式求得:


上式中:为检出限;为相对标准偏差;为标准偏差,即连续11次测量空白溶液的荧光强度的标准偏差;为单次标准溶液的测量值;为工作曲线的斜率。
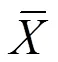
2.6 市售茶叶中砷形态分析测定
表2 茶叶中4种砷形态的测定结果
Table 2 Determination results of four arsenic forms in tea
次数As(Ⅲ)(μg/kg)DMA(μg/kg)MMA(μg/kg)As(Ⅴ)(μg/kg)四种砷形态之和(μg/kg) 15.260.841.2523.8231.17 25.340.791.2323.7531.11 35.210.821.2722.9830.28 45.330.861.2924.1231.60 55.270.851.2623.6731.05 平均值5.2820.8321.2623.66831.042
通过所建立的方法检测了市售茶叶中的4种砷形态,测定的结果表2所示。由表2可知,平行测定5次求平均值,确定茶叶中亚砷酸根As(Ⅲ)含量5.282 μg/kg,二甲基砷酸(DMA)含量0.832 μg/kg,一甲基砷酸(MMA)含量1.26 μg/kg,砷酸根As(Ⅴ)含量23.668 μg/kg,四种砷形态之和为31.042 μg/kg。茶叶中砷酸盐As(Ⅴ)含量最多,亚砷酸盐As(Ⅲ)含量其次,一甲基砷酸(MMA)含量第三,二甲基砷酸(DMA)最少。
2.7 加标回收率
表3 各形态As的加标回收率
Table 3 Recovery rates of different forms of arsenic
形态测定值(μg/kg)加入量(μg/kg)加标后测定值(μg/kg)回收率(%) As(Ⅲ)5.29510.1697.4 DMA0.8811.93105 MMA1.2712.2194 As(Ⅴ)23.592044.62105.15
在1.2.1液相色谱条件及原子荧光条件下,5.0%盐酸载液,2%还原剂硼氢化钾,对茶叶各形态As的测定作加标回收试验,结果见表3。从表3可知,各形态As的回收率在94%~105.15%之间,说明HPLC-UV-HG-AFS联用测定茶叶中四种砷的形态化合物是可靠的。
3 小结
(1)5.0%作为盐酸载液的浓度,2%作为还原剂硼氢化钾的浓度,原子荧光光度计产生的荧光信号最强。
(2)选择Na2HPO4和KH2PO4混合液作为流动相,pH值为5.92。在7 min之内,砷形态:亚砷酸根As(Ⅲ)、二甲基砷酸( DMA)、一甲基砷酸(MMA)、砷酸根As(Ⅴ) 依次出现峰,实现了完全分离,其保留时间分别为2.21、2.76、3.50、5.52 min。
(3)在0~100 ng/mL的线性范围内,砷的4种形态标准曲线线性良好,相关系数(R)在0.9991~0.9995范围内。HPLC- HG-AFS方法检出限低,精密度高。
(4)HPLC-HG-AFS联用测定茶叶中四种砷的形态,该方法快速简便、准确和灵敏度高、重复性好,加标回收率为94%~105.15%。
[1] 苑春刚,X.Chris Le.砷形态分析[J],化学进展,2009, 21(2):467-473.
[2] 刘香丽,汪倩,宋超,等. 不同砷形态在水产品中的毒理及转化研究进展[J].农学学报,2019,9(12):33-38.
[3] 曹晓钢,王君,李建民,等. HPLC-HG-AFS法分析西藏冬虫夏草中的砷形态化合物[J].中成药,2015,37(9): 1985-1989.
[4] 陈绍占,刘丽萍,杜振霞,等. 高效液相色谱-电感耦合等离子体质谱联用技术测定畜禽肉制品中八种砷形态化合物[J].质谱学报,2015,36(1):33-39.
[5] 李凤标,郑巨瑞,周柳金,等. 高效液相色谱-电感耦合等离子体质谱法测定婴幼儿谷类辅助食品中无机砷及其他砷形态[J].食品安全质量检测学报,2019, 20(10): 7001-7005.
[6] 孟珊,邵阳,胡伟杰,等. 高效液相色谱-电感耦合等离子体质谱法测定植物源保健食品中6种砷形态化合物[J].分析化学,2019,47(07):1121-1123.
[7] 严国,梅光明,常家琪,等. 电感耦合等离子体质谱法分析海蟹中的砷元素分布特征[J].食品科学,2019,40(12):3 32-339.
[8] 胥佳佳,冯鑫,汤静,等. 超声辅助提取-高相液相色谱-电感耦合等离子体质谱法测定香菇中6种形态砷化合物[J].食品科学,2016, 37(24):216-221.
[9] 颜明娟,吴一群,张辉,等. 福建茶园土壤及茶叶重金属监测及污染评价[J].茶叶学报,2016,57(2):71-75.
[10] 李杨,何勇,刘淑燕. 福建省4类茶叶中重金属含量规律的研究[J].安徽农学通报,2018,24(8):46-51.
[11] 缪德仁,李晓,杨婉秋. 云南凤庆茶叶中铜、铅、锌、镉、铬和砷的健康风险评估[J]. 昆明学院学报,2019,41(03): 56-60.
[12] 柯华南,刘志鹏,郭剑雄,等. ICP-AES法测定茶叶中As、Cd、Ni、Pb等元素的含量[J].广东微量元素科学, 2013,20(2):40-43.
[13] 张俊,罗梦,沈露,等. 工业型城市不同道路两侧土壤重金属污染状况对比分析[J].井冈山大学学报:自然科学版,2017, 38(4):38-44.
[14] 夏拥军.高效液相色谱-原子荧光光谱法测定水产品中4种砷形态[J].化学分析计量,2017,26(5):46-58.
[15] 刘守廷,蒋天成,李健梅,等.HPLC–AFS联用测定海产品中砷的形态[J].化学分析计量,2013, 22(1):11-14.
DETERMINATION OF FOUR ARSENIC SPECIATION COMPOUNDS IN TEA BY HPLC-HG-AFS
HUANG Tian-fu,*ZHANG zhu-sen, QIU ze-hai
(College of Chemistry and Material Science, Longyan University, Longyan, Fujian 364000, China)
An analysis method has been established for the determination of Arsenic speciation compounds in tea by High Performance Liquid Chromatography-Hydride Generation-Atomic Fluorescence Spectrometry (HPLC-HG-AFS). In this method, the concentration of the hydrochloric acid carrier and the reductant Potassium Borohydride were 5.0% and 2%, respectively, the mixture of Na2HPO4and KH2PO4was used as mobile phase, and the pH value was 5.92. The peaks of As(Ⅲ), DMA, MMA and As(Ⅴ) of the arsenic speciation appeared in turn, and achieved to separate completely in seven minutes. The standard curves of four forms of arsenic showed good linearity within the linear range of 0~100 ng/mL, the linear correlation coefficients were 0.9995, 0.9991, 0.9993 and 0.9993, respectively, the detection limits were 0.064, 0.127, 0.089 and 0.095 ng/mL, respectively, and the precisions were 2.26%, 1.84%, 2.05% and 1.59%, respectively, the recovery rate was 94%~105.15%. The test results indicated that the method could detect four speciation compounds of arsenic in tea accurately, quickly and sensitively.
HPLC-HG-AFS; tea; arsenic speciation
O653/659
A
10.3969/j.issn.1674-8085.2021.01.006
1674-8085(2021)01-0030-05
2020-09-08;
2020-11-27
福建省教育厅科研项目(JAT170566);龙岩市科技计划项目(2018LYF5001)
黄田富(1978-),男,福建龙岩人,副教授,硕士,主要从事分析检测研究工作(E-mail:36977764@qq.com);
*张著森(1970-),男,福建龙岩人,高级实验师,硕士,主要从事分析工作(E-mail:50073658@qq.com);
丘则海(1970-),男,福建龙岩人,副教授,硕士,主要从事分析检测研究工作(E-mail:122070741@qq.com).
