径向超声支气管镜下应用引导鞘对肺外周结节的诊断价值
2021-02-25林辛锋方凌翔史洪辉胡颖张秀霞林芳吴翔
林辛锋,方凌翔,史洪辉,胡颖,张秀霞,林芳,吴翔
目前肺外周结节的病理诊断通常是经皮肺穿刺活检、手术切除或支气管镜检查获得,但是,使用常规支气管镜进行肺活检的诊断率低[1]。技术的进步使得外周超声支气管镜检查技术成为一种有效且创伤较小的支气管镜技术[2]。根据之前的研究结果,用于肺外周结节的径向超声支气管镜(EBUS)下应用引导鞘(GS)检查方法被认为是相对安全的、患者可耐受的手段[3]。由于其广泛使用,可能会出现相关的并发症,根据先前的荟萃分析,总体并发症发生率为0~7.4%,但病死率为0[4]。在最近一项965例的大规模研究中源性气胸的发生率为0.8%,需要胸腔闭式引流的发生率为0.3%,肺部感染的发生率为0.5%,均明显低于经皮肺穿刺活检[5]。为了了解EBUS-GS检查对肺外周结节的诊断价值,故收集医院气管镜室进行EBUS-GS操作的肺外周结节患者80例资料进行分析,现报道如下。
1 资料与方法
1.1 一般资料 收集2019年1月-2020年6月福州市第一医院呼吸内科住院治疗的肺外周结节患者80例均接受EBUS-GS检查,操作者都有10年以上的常规气管镜操作经验和2年以上的EBUS-GS手术经验。本项目经福州市第一医院医院伦理委员会批准,经所有患者及家属知情同意并签署知情同意书。对于所有肺外周结节的胸部计算机断层扫描(CT)扫描均在EBUS-GS之前2周内进行。CT扫描的厚度为0.625 mm,间隔为0.625 mm。测量每个肺外周结节的大小是根据CT肺窗图像上的平均直径。当肺部病变位置在段支气管以下部位时定义为肺外周结节病灶。根据CT影像的特点把肺外周结节病变分为纯磨玻璃结节、部分实性结节和实性结节[6]。患者基线特征见表1。
1.2 方法 EBUS-GS操作过程 所有行EBUS-GS手术患者均要求住院。每位患者均置入20 MHz径向探头EBUS(UM-S20-17S,奥林巴斯)及GS套件(K-201,奥林巴斯)。每位患者常规给予利多卡因雾化吸入加气道表面喷洒麻醉,使用奥林巴斯BF-P260F支气管镜检查,检查大气道及外周气道。根据CT图像将支气管镜推进到目标支气管,GS包裹的径向EBUS探针向前伸出直到遇到阻力为止,然后EBUS探针稍微向后退并进行超声扫描。当EBUS识别好目标病变,GS保持原位并固定好,抽出超声探头,依次由GS孔道送入细胞刷刷检和活检钳活检。根据超声下目标病灶与GS的位置关系,将肺部病变分为三类:病灶内部、毗邻病灶和病灶外(表1)[7]。通过GS进行支气管镜下活检、刷检采样。如果病变位于EBUS探及的范围外,由操作者决定下列采样方法,如刷检、活检或支气管肺泡灌洗等。为了确定是否发生医源性气胸,在手术后4 h进行初次X线胸片检查,并在24 h后进行胸片随访。严重的肺部出血被定义为需要输血、气管插管或经支气管动脉介入治疗的气道内出血。同时也记录需要气管插管的呼吸衰竭、肺部感染、空气栓塞或因其他意外并发症而提前终止手术的病例。术后仔细检查EBUS及GS是否损坏。
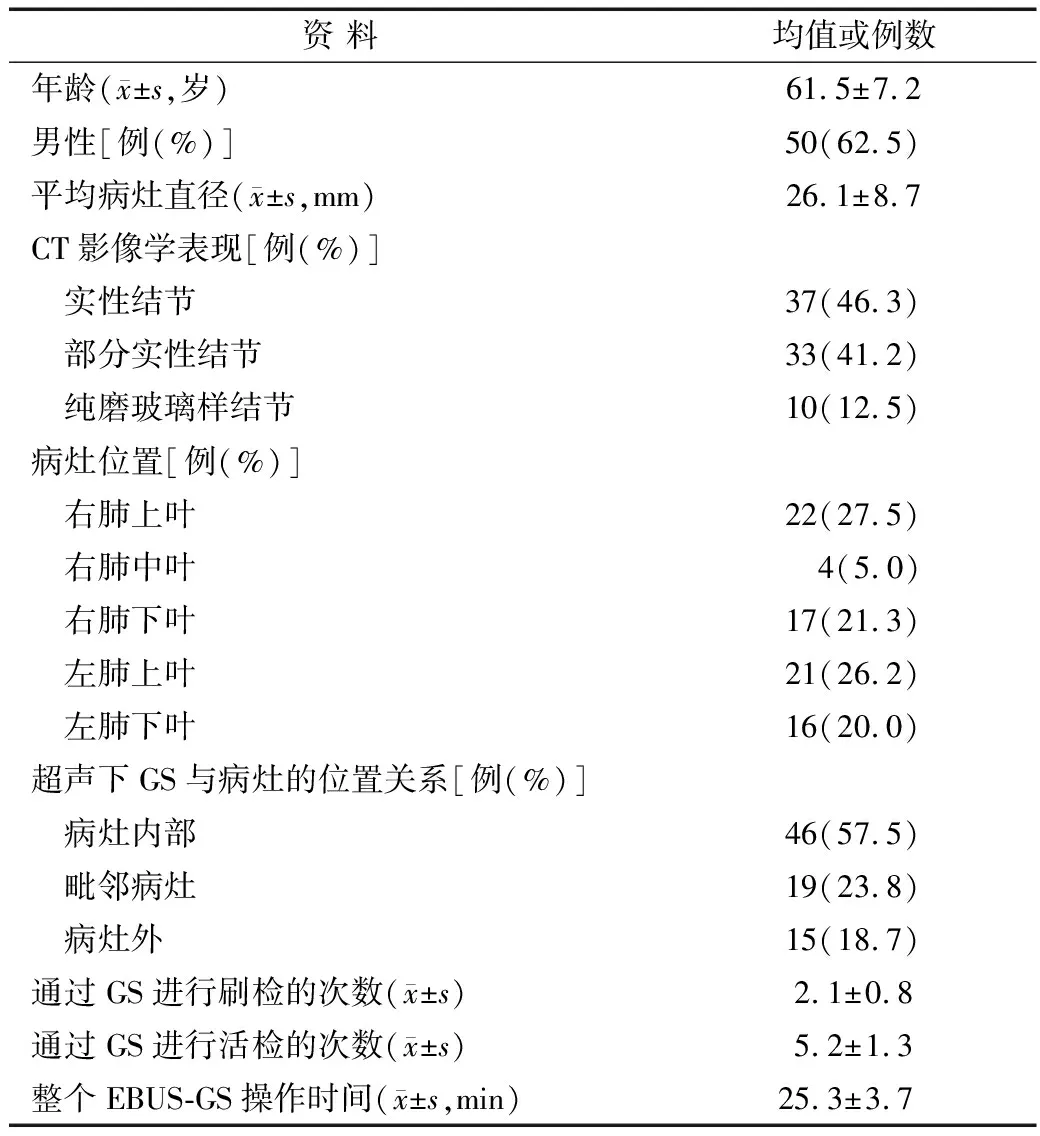
表1 80例肺外周结节患者的基线特征
2 结 果
2.1 诊断结果 80例患者诊断结果为EBUS-GS的总诊断率为75.0%。病灶直径不同的患者之间诊断率存在显著差异。实性病变和部分实性病变的诊断率差异无统计学意义(86.5% vs. 75.8%,P>0.05),显著高于纯磨玻璃样结节的诊断率(30.0%)。EBUS-GS对于超声定位位于病灶内部的诊断率,明显高于毗邻病灶和病灶外的病例(分别为95.7%、73.7%和13.3%,P<0.05)。见表2、表3。

表2 80例行EBUS-GS患者的临床诊断结果

表3 根据病灶大小的EBUS-GS诊断率
2.2 相关并发症 观察到2例患者(2.5%)出现相关并发症:包括1例 (1.3%)出现气胸,自行吸收而不需要放置胸管引流;1例(1.3%)出现术后肺部感染。在所有参与研究的患者中,未出现严重出血、空气栓塞或呼吸衰竭,手术中未出现过早终止的情况,也无患者因手术而死亡。1个径向探针EBUS发生了断裂。
3 讨 论
本研究中EBUS-GS的总并发症发生率为2.5%,与之前一项涉及965个肺外周结节的研究中记录的2.3%的并发症率无明显差异[7]。在无任何导航辅助的情况下,EBUS-GS的诊断率先前报道为69.2%~77.3%[8]。本研究中,80例患者EBUS-GS的总体诊断率为75.0%。对于直径<20 mm的肺外周结节病变,EBUS-GS也是有一定的诊断价值(诊断率56.7%)。根据该研究结果,对于肺外周结节病灶EBUS-GS的诊断率通常与肺病变的大小密切相关[9]。
先前对EBUS-GS的荟萃分析报道,任何气胸或需要肋间导管引流的气胸的合并率分别为1%和0.4%[2]。与经皮肺穿刺活检术后气胸相对较高的发病率相比,这种低气胸发病率是EBUS-GS的重要优势[1]。本研究中,气胸的发生率为1.3%,并无患者需要放置胸腔闭式引流管来处理气胸。EBUS-GS术后肺部感染是一种罕见的并发症,据研究其风险为0.5%[7]。在本研究中,这个比率是相同的。到目前为止,还未有关于针对EBUS-GS患者使用预防性抗生素的临床指南或共识。在另一项荟萃分析中,EBUS-GS患者术后呼吸衰竭发生率<1‰[6]。此外,所有研究均未报道严重出血或手术相关死亡的病例[10]。同样,本项研究中,也未包括呼吸衰竭等致命的并发症。
EBUS径向探针的脆弱性是众所周知的,每把探针应用于50~100次后可出现损坏[10]。此研究中,1个径向探针EBUS发生了断裂。在单例气管镜断裂病例中,气管镜与GS的2个长轴不一致,在垂直于气管镜长轴的压力作用下,GS发生弯曲受损。这种情况的发生多是由于支气管镜未足够地靠近靶病灶所致。
最近的研究表明,由导航系统和径向探头EBUS组成的组合模态比单独使用每一模态提供更高的诊断率[11],然而导航系统是一种昂贵的医疗资源。基于上述的研究结论表明,EBUS-GS是一种安全、稳定和实用的诊断肺外周结节的方法。
