超声在非复杂动静脉内瘘穿刺定位管理中的作用
2021-02-25张丽红王玉柱詹申张闻娣肖光辉
张丽红 王玉柱 詹申 张闻娣 肖光辉
动静脉内瘘是维持性血液透析(maintance hemodialysis,MHD)患者的“生命线”,是确保患者透析顺利进行的基本保障。MHD患者每年至少需要穿刺312针(6×52),因此,内瘘安全穿刺已成为血液透析护理领域关注的焦点[1]。安全穿刺包括顺利进针,针尖处于理想位置,拔针后顺利止血,无穿刺相关急性并发症。对于复杂内瘘,各国指南及专家共识均推荐超声实时引导穿刺,可以显著提高穿刺安全性[2-4]。但对于非复杂内瘘,并未进行相关推荐,大多中心采用盲法穿刺,进针顺利,能提供透析处方流量即认为安全穿刺,该状态下针尖位置及穿刺相关并发症的研究较少。理想的穿刺针尖位置应位于血管中央,不仅能将维持体外循环的穿刺针所致局部湍流对于血管的损伤减至最小,还可以为透析全程提供稳定血流量[5]。针尖位置不当则可引起多种并发症,包括血肿、假性动脉瘤、穿刺相关增生狭窄、血栓等,进而对血管通路的使用寿命造成影响。本研究拟通过前瞻性研究,了解非复杂内瘘盲法穿刺顺利且满足透析处方血流量患者针尖位置及穿刺相关并发症情况,以明确超声在非复杂内瘘穿刺定位管理中的作用。
1 资料与方法
1.1 一般资料 选择自2020年1~3月于我院透析室以自体动静脉内瘘(arteriovenous fistula,AVF)为通路进行规律血液透析患者127例,复杂内瘘定义为初期AVF(新建立6个月以内的AVF)、使用超过6个月但穿刺困难(包括穿刺距离短、血管周围支撑组织过少、血管距皮距离>6 mm等)的内瘘[6]。
1.2 纳入与排除标准
1.2.1 纳入标准:①年龄18~80岁;②规律血液透析治疗≥3个月,3次/周,4 h/次;③以上肢AVF为透析通路,且经我院内瘘监测小组结合物理检查及彩色多普勒超声测量数据评估内瘘不存在异常问题如狭窄、血栓等。
1.2.2 排除标准:①复杂内瘘;②预期存活时间≤3个月;③拒绝超声检查;④存在精神性疾病或其他情况无法配合治疗。
1.3 研究方法 所有符合标准患者依次纳入研究,收集患者基本资料:性别,年龄,原发病,透析龄;通路信息:透析龄,通路类型,位置;由专家级护士对AVF进行物理评估后盲法穿刺(穿刺针型号16-G钢针(JMS,中国),有落空感后,用10 ml注射器和0.9%氯化钠溶液手动测试穿刺针是否在管腔内,如果抽吸或推注0.9%氯化钠溶液均无阻力,则用胶带固定针头,并连接体外循环开始透析。透析30 min时超声(索诺星Uprobe)评估穿刺针针尖在管腔内的位置,由接受过超声培训的本科室血管通路专家级护士[3]进行AVF的纵向和横向扫描,测量并记录穿刺点血管内径、距皮距离,针尖在血管内的位置(前壁,中间,后壁)。是否存在急性并发症如(血肿,渗漏,假性动脉瘤等),发现问题者超声引导下调整针尖位置或重新穿刺,该部分患者不纳入管腔内针尖位置分析。分析针尖位置与AVF深度及内径的关系。
1.4 相关定义 (1)盲穿穿刺成功定义:在没有超声辅助时盲法穿刺顺利,且能满足处方血流量,且没有因为透析机动脉压力、静脉压力监测异常而中断透析。(2)针尖位置:可将血管分为前、中、后三区域,当针尖位于血管中心或血管直径的中间1/3时,则认为针处于正确的位置;处于其他位置时认为位置不当。
2 结果
2.1 入组基线资料 127例中,男84例,女43例;原发病:糖尿病肾病36.22%(46/127),慢性肾炎23.62%(30/127),高血压22.05%(28/127),其他18.11%(23/127);内瘘位置:左上肢77.95%(99/127),右上肢22.04%(28/127),前臂82.68%(105/127),上臂17.32%(22/127)。其中9例患者穿刺失败,给予超声引导穿刺,2例患者穿刺后流量不足,超声提示针尖贴壁,给予超声引导调整针尖位置后流量正常;4例患者发现血肿,3例患者出现渗漏,并发症发生率14.17%(18/127),最终纳入针尖位置分析患者119例(238针)。见图1。

图1 盲法穿刺穿刺针刺破血管后壁导致渗漏,图示后壁血管壁不完整,血液自血管破口溢出,渗漏导致周围组织水肿
2.2 针尖位置分布 穿刺238针中,位于血管中间、前壁1/3、后壁1/3分别为69针(28.99%)、142针(59.66%)、27针(11.34%);其中动脉针中,位于血管中间、前壁1/3、后壁1/3分别为28.57%(34/119)、60.50%(72/119)、10.08%(12/119);静脉针中位于血管中间、前壁1/3、后壁1/3分布为29.41%(35/119)、57.98%(69/119)、12.61%(15/119)。见表1,图2。

盲法穿刺后针尖位于血管中间 盲法穿刺后针尖位于血管前壁1/3 盲法穿刺后针尖位于血管后壁1/3(红色箭头为血管前壁,黄色箭头为血管后壁,绿色箭头针尖

表1 盲法穿刺顺利患者超声评估针尖位于血管中位置分布表 例(%)
2.3 针尖位置与内瘘深度关系 内瘘深度与针尖位置具有相关性(χ2=110.26,P=0.00),当距皮距离>0.3 cm时,针尖位置更多位于血管前壁。见图3,表2。

表2 穿刺点血管深度与针尖位置分布表 例(%)
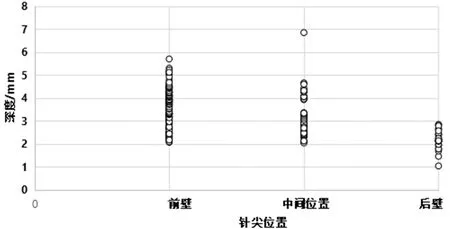
图3 针尖位置与内瘘深度关系图
2.4 针尖位置内瘘直径关系 内瘘直径与针尖位置
内瘘深度与针尖位置具有相关性(χ2=116.64,P=0.00),当内瘘直径<0.5 cm时,针尖位置更多位于血管后壁。见图4,表3。

图4 针尖位置与内瘘直径关系图

表3 穿刺点血管直径与针尖位置分布表 例(%)
3 讨论
目前对于非复杂内瘘缺乏相关推荐,大多数中心并不借助超声辅助,而是运用物理检查(即视诊,听诊和触诊)进行动静脉内瘘穿刺前的评估,然后凭手感盲法穿刺,有突破感后,如果在抽吸及推注0.9%氯化钠溶液均无阻力,则用胶带固定针头,并开始透析。如果机器没有警报,则认为针尖在血管腔内处于最佳位置;当机器触发报警时,血泵停止并且透析被中断,在确认没有渗透之后,将针进行“重新定位”通过改变穿刺方向和角度或旋转斜面来调整直到可以恢复透析[7,8]
但盲法穿刺成功透析过程顺利,并不意味着针尖位于血管腔的最佳位置。本研究对于盲法穿刺成功且透析顺利的患者针尖进行超声定位发现仅有28.99%处于理想的血管中央,与既往研究[9,10]类似。当针尖靠近血管壁时一方面导致对血管壁的直接机械损伤风险增加[11];另一方面,在血液透析体外循环过程中穿刺针引血或回血会导致血管壁的剪应力大大增加,进而增加由湍流引起的内皮损伤[12,13]。剪切应力的增加可导致内皮激活,最终增加血管通路狭窄的风险。对针尖具体定位分析发现,11.34%的患者针尖处于后壁位置,该位置与更高的穿刺渗漏及血管损伤风险相关,较严重的穿刺损伤往往需要超过一周的内瘘休整期,更重者甚至要输血或紧急干预[14],并且与随后的血栓形成、导管的延长使用等有关,增加患者的医疗成本。
在本研究中,盲法穿刺有14.17%穿刺相关并发症,均在超声实时引导下予以调试或重新穿刺成功[15],恢复正常透析。其中有1例患者发现后壁血管损伤,由于抗凝剂应用,导致较严重渗漏及假性动脉瘤,超声很快定位血管损伤部位,有的放矢,即刻给予精准按压止血,避免了动静脉内瘘由于按压力度过小导致无法达到止血效果或按压力度过大而导致的内瘘失功,同时也避免了更严重渗漏及相关并发症。
对于触诊不满意的内瘘,最好穿刺前利用超声评估其深度、内径,确定穿刺角度来优化穿刺参数,减少穿刺相关并发症。
目前缺乏与内瘘穿刺过程相关的功能异常或并发症的敏感监测指标,无法确保盲穿针头处于理想位置并降低潜在的血管损伤风险[16],研究认为,由接受过超声培训的操作人员选择性应用超声确定穿刺针尖位于正确位置,可以预防穿刺并发症[2]。本研究进一步验证了超声定位评估在内瘘尤其是非复杂内瘘安全穿刺管理中的应用价值。
目前缺乏与穿刺过程异常相关敏感监测指标,对于非复杂内瘘超声定位评估可优化穿刺并确保理想的针头位置,最大程度减少与穿刺相关的并发症,延长动静脉内瘘的使用寿命,值得临床推广。
