混合二元酸分离提纯丁二酸
2021-02-12王志彦
彭 胜,王志彦
(1.华北理工大学,河北 唐山 063210;2.唐山开滦化工科技有限公司,河北 唐山 063020;3.唐山市煤化工副产品精深加工与资源综合利用重点实验室,河北 唐山 063020)
0 引言
丁二酸(Succinic acid,C4H6O4,118.09,简称SA)又名琥珀酸,因1550 年首次从琥珀中蒸馏获得而得名,广泛存在于微生物中和动植物体内,是三羧酸循环的重要中间产物。作为重要“C4 平台化合物”被美国能源部确定为未来最具发展前景的12 种大宗生物炼制产物之一,是可持续生物基化学品之一。丁二酸广泛用于医药、食品、香料、农药、染料及塑料等工业,传统丁二酸的工业生产工艺主要有石蜡氧化法、催化加氢法、电化学法以及生物法,其中石蜡氧化法由于产物复杂分离困难以及环境污染问题逐渐淘汰。
丁二酸在中国的生产始于20 世纪60 年代末期,起步较晚,但是生产发展较快,到2013 年丁二酸的产量占世界总产量的40%。基于新型生物可降解塑料的产业化,丁二酸的生产和发展得到新机遇,预计2020 年国内可降解生物塑料市场需求量为300 万t,未来国内丁二酸的年需求量将达到180 万t 左右,加上下游市场的不断开发,需求量也将保持10%以上的年增长率,市场缺口巨大。
随着尼龙66 产品的需求日益增大,作为原料的己二酸产能也不断增大。而在己二酸生产工艺中,每生产1 t 己二酸产品一般要产生50~60 kg混合二元酸(DBA)副产物。混合二元酸中戊二酸约占60%,丁二酸约占28%,己二酸约占12%。目前,国内己二酸的产能为170~200 万t,因此我国每年DBA 产量将达近10 万t。将其中的丁二酸分离出来,既提高产品的附加值,又降低环境污染。但传统工业分离丁二酸多采用硝酸进行分离,存在腐蚀严重、硝酸回收能耗大等问题。以混合二元酸和混合二元酸分离戊二酸后残渣(也属于混合二元酸,后简称戊二酸残渣)为原料,使用有机溶剂分离提纯丁二酸,系统考察了二元酸溶解度及其相互影响,研究了液固比和原料配比对产品丁二酸纯度的影响,从而通过简单操作获得了较高纯度丁二酸产品,具有较好应用前景。
1 实验部分
1.1 试剂
丁二酸(SA)、戊二酸(GA)、己二酸(AA),阿拉丁,分析纯;丙酮、正丙醇、正丁醇、卤代烃,国药,分析纯;混合二元酸(即DBA,丁二酸19.3%,戊二酸64.7%,己二酸14.3%),唐山中浩化工有限公司提供;戊二酸残渣(丁二酸55.2%,戊二酸22.8%,己二酸19.3%),实验室分离副产物。
1.2 溶解度测定
采用动态法测定丁二酸、戊二酸和己二酸在溶剂中的溶解度。其测定装置主要由激光光源和全功率计组成,具体操作方法是:在一个通有恒温循环水的玻璃溶解釜中加入一定量的溶质和溶剂,不断搅拌。将激光发射器和激光接受器分别放在溶解釜的两端。缓慢升高水浴温度,直至激光接收器的示数达到最大值,此时溶质刚好在溶剂中溶解完全,即达到固-液平衡。记下此时的温度和溶剂、溶质的量,从而可以得到该温度下的溶解度。
1.3 检测分析方法
采用安捷伦GC-7980 气相色谱进行定量分析,中等极性毛细管柱,氢火焰离子化检测器(FID),产物中3 种二元酸的含量均采用面积归一法进行定量分析。由于丁二酸、戊二酸和己二酸的沸点都比较高,因此在分析前,先用重氮甲烷将样品酯化变成相应的二元酸甲酯,使其沸点降低。使用重氮甲烷酯化二元酸,误差小,反应快。
2 结果与讨论
2.1 不同溶剂中二元酸的溶解度
丁二酸的分离本质是利用3 种酸在溶剂中的不同溶解度进行分离,同时溶剂在满足分离需要外还应该常见易得、价格便宜;毒性低、安全环保;沸点适宜,既利于回收,又能降低挥发损失。因此,初步选取了正丙醇、丙酮、正丁醇和卤代烃等四种溶剂,分别测定了丁二酸、戊二酸和己二酸在其中的溶解度如图1 所示,其中丁二酸在卤代烃中的溶解度很低未能测出。


图1 丁二酸、戊二酸和己二酸在不同溶剂中的溶解度Fig.1 Solubility of succinic acid,glutaric acid and adipic acid in different solvents
由图1 可见,所有溶剂中,都是戊二酸溶解度大于丁二酸和己二酸,这是由于在亚甲基个数相近时,偶数碳二元羧酸的2 个羧酸处于对角线位置,相互距离较远斥力小,保证亚甲基都处于完全交叉式构象,有利于晶体层与层之间更好的堆积,晶格能较大。而奇数碳二元羧酸的羧酸处于同一侧,相互排斥导致亚甲基链的扭转,使得其层与层之间排列不紧密,晶格能小。因此,戊二酸溶解度大于丁二酸和己二酸,而4 种溶剂极性相对较小,而丁二酸由于极性基团占比较己二酸大,因此极性也略大,根据相似相溶原理,己二酸溶解度略高于丁二酸。由于丁二酸溶解度小,可以采用溶剂将原料中的戊二酸和己二酸溶解脱除的原理获得丁二酸产品。
同时,丁二酸和己二酸在正丙醇和丙酮中的溶解度差别不明显,正丁醇在溶解度上基本能满足条件,但由于正丁醇粘度较大,不能从最终产物中脱除干净。因此最终选定卤代烃作为丁二酸分离提纯的最佳溶剂。
2.2 溶剂中戊二酸对己二酸溶解度的影响
实验利用卤代烃来溶解戊二酸残渣,结果发现与所测得的单一酸在溶剂中的溶解度差别较大,这可能是由于戊二酸残渣中同时含有3 种二元酸,它们的溶解相互影响。
由于戊二酸溶解度最大,实验考察了戊二酸的存在对己二酸的溶解度的影响,实验中,当溶剂中存在一定量戊二酸时,可以明显增大己二酸的溶解度,而且丁二酸的溶解度随溶剂中戊二酸的含量越大而增大。这是由于在该溶剂中戊二酸远没有达到其饱和条件下,戊二酸的溶解形成类似相溶作用,一定程度上促进己二酸的溶解。
己二酸在卤代烃(1-w)+戊二酸(w)中的溶解度如图2 所示。
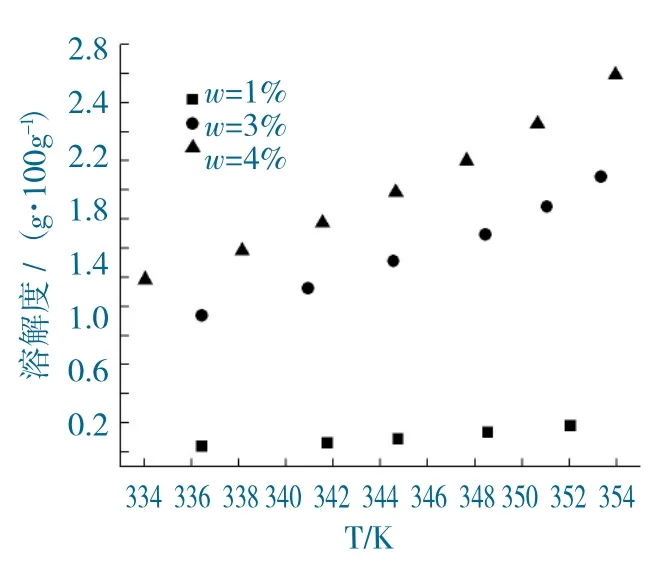
图2 己二酸在卤代烃(1-w)+戊二酸(w)中的溶解度Fig.2 Solubility of adipic acid in halohydrocarbon(1-w)+glutaric acid(w)
2.3 液固比对产品纯度的影响
考虑己二酸溶解度低的原因,实验在80 ℃水浴条件下,为考察液固比对产品纯度的影响,将100 g 原料和若干溶剂依次加入1 L 烧瓶中,搅拌溶解1.5 h 后趁热过滤,滤渣经过干燥后取样进行色谱分析。
液固比对丁二酸产品纯度的影响如图3 所示。

图3 液固比对丁二酸产品纯度的影响Fig.3 Effect of liquid-solid ratio on the purity of succinic acid
由图3 可见,随着液固比的升高,产品中丁二酸的纯度先上升,在液固比为11 时达到最高,约为92.2%,然后降低。这是由于在溶质质量一定时,溶剂量(溶解度)和溶剂中戊二酸浓度对产品中丁二酸的纯度都有影响,在液固比<11 时,溶剂量起主导作用,溶剂量增加,戊二酸和己二酸的溶解增加,但液固比>11 时,戊二酸的浓度起主导作用,溶剂量的继续增加,戊二酸浓度降低,导致戊二酸和己二酸溶解量降低。
2.4 原料配比对产品纯度的影响
尤其对于卤代烃溶剂,丁二酸在该溶剂中的溶解度几乎为0,但是当溶剂中含有戊二酸时,己二酸的溶解度明显升高(见图2),这显然对丁二酸的分离是有利,因此提出戊二酸残渣同DBA 互配方案。在溶剂温度为80 ℃,液固比为11,溶解时间1.5 h 条件下,对原料中添加DBA 进行了研究,原料配比对丁二酸纯度的影响见表1。
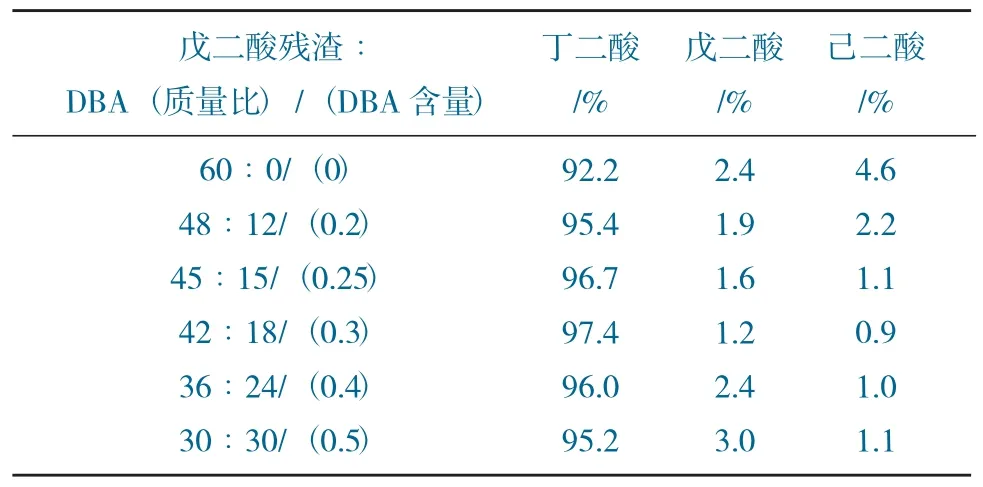
表1 原料配比对丁二酸纯度的影响Table 1 Effect of raw material ratio on the purity of succinic acid
由表1 可见,当适量添加DBA 后,虽然原料中丁二酸含量降低,戊二酸含量升高,但由于溶剂中二元酸之间的相互作用,丁二酸纯度有较大提升。但同理论计算结果仍有一定差距,分析原因是由于实际溶解过程并不是理想过程,溶质颗粒是存在颗粒大小的,丁二酸的难溶解使得其包裹的戊二酸和己二酸与溶剂接触困难,一定程度上阻碍了溶解过程。同时从结果中可以看出DBA 含量的增加,己二酸的溶解度逐渐升高,产品中的己二酸含量降低,丁二酸纯度提高。DBA 含量为0.3 时,丁二酸纯度可达97.4%。当DBA 含量>0.3 时,虽然己二酸的溶解度增加,但由于颗粒尺寸和丁二酸溶解度低的原因,产品中的己二酸含量基本保持不变,而增加的戊二酸导致丁二酸纯度降低。由于进一步减小原料颗粒尺寸综合效率较低,因此确定原料中DBA 添加量为0.3。由于丁二酸的溶解度很低,该条件下丁二酸的回收率超过98%。
3 结语
通过动态溶解度测定,获得4 种溶剂中丁二酸、戊二酸和己二酸的溶解度,选取卤代烃作为溶剂。借助于丁二酸溶解度小和二元酸之间溶解相互促进,通过将原料中的戊二酸和己二酸溶解脱除回收丁二酸。在溶解温度为80 ℃、液固比11 为、DBA 含量为0.3、溶解时间为1.5 h 条件下,一次溶解过程即可获得纯度达到97.4%的丁二酸产品,丁二酸回收率>98%。相比于传统先用水作为溶剂对混合二元酸进行粗提得到纯度为80%左右的丁二酸,该工艺流程简单,操作简便,产物纯度高,回收率高,为进一步获取更高纯度丁二酸提供了方向和基础,且提高混合二元酸附加值,具有较好的工业化前景。
