结核分枝杆菌实验室检测产品和技术应用进展
2021-02-05王玉峰高兴辉汤一苇
逄 宇,王玉峰,高兴辉,汤一苇
结核病是全球面临的重大公共卫生问题。据世界卫生组织估计,2019年全球新发结核病患者1 000万例,死亡141万例[1]。结核病患者的早期快速检测对提高患者的疗效,并有效阻断结核人际传播至关重要,但目前病例发现率和报告率仍然较低,特别是在结核病高负担国家,估算超过1/3的病例并未被登记报告[1,2]。结核病诊断能力不足是导致这一现象的根本原因,尤其在患者面对交通、经济负担等一系列问题时,进一步加剧患者的漏诊[3]。此外,当患者感染利福平耐药或耐多药(同时对利福平和异烟肼耐药)的结核分枝杆菌时,患者的临床管理将更为复杂,但是全球仅有33%的新发菌阳结核患者开展了抗结核药物敏感性检测,提高对结核病和耐药结核病的快速诊断迫在眉睫[1,4]。然而传统的病原学检测方法已无法满足临床的实际需求,亟待在结核病高负担国家使用和推广新型诊断技术。近年来随着分子生物学及免疫学的发展,涌现出一批结核病快速检测产品和技术(见表1)[5~7],本文就这些产品的主要研究应用进展进行系统回顾。

表1 结核病诊断路径(翻译和修改于参考文献[6]的图1)

续表1
1 传统病原学实验室检测
直接观察到结核分枝杆菌或者分离到结核分枝杆菌是结核诊断的重要方法,特别是痰涂片和痰培养在结核病防治历程中发挥了重要的作用,然而受限于痰涂片的灵敏度以及痰培养时效性,限制了其在结核诊断中的应用,如何充分发挥其优势服务临床检测是传统病原学诊断的基础。近年来结核特有的抗原也可作为结核诊断的重要标志物之一,其在特殊人群的应用得到世界卫生组织的认可和推荐,下面主要对四类技术进行系统介绍。
1.1痰涂片镜检 痰涂片镜检作为结核病诊断的主要手段,应用时间已经超过120年[8]。它操作相对简单且对实验室的要求较低,目前仍是许多结核病高负担国家的主要诊断技术。大多数实验室采用直接涂片联合萋尼氏染色的方法。通过收集晨痰、夜痰和即时痰等方式提高患者发现率,但是由于需要多次往返医疗机构,世界卫生组织建议在医院采集两份质量良好的痰标本也可满足检测要求。多种对涂片和染色方法的改进,包括离心集菌、荧光染色、添加漂白剂等,可以提高痰涂片的检测灵敏度[9]。但是痰涂片检测阳性的标本需要痰中菌的浓度达到10 000个结核杆菌/ml,对于含菌量较少的患者,如儿童结核、HIV/TB双感、肺外结核患者,痰涂片诊断能力较差[10]。来自不同研究结果表明,痰涂片镜检在培养阳性的肺结核患者中的阳性率为20%~70%[11],提示不同实验室人员能力对于痰涂片镜检产生明显的影响。痰涂片显微镜还有多项其他缺点,包括不能区分菌体的死活,不能区分结核和非结核分枝杆菌,无法开展后续的药物敏感性试验(以下简称药敏试验)等。因此,世界卫生组织推荐采用快速的分子生物学方法作为痰涂片的替代方法用于结核病及耐药结核病的患者筛查[12~14]。
1.2分枝杆菌培养 结核分枝杆菌最快分裂增殖速度为18 h一代,培养时长一般为2~6周,因此结核分枝杆菌的分离培养时间相比普通微生物耗时更长。此外,由于生物安全原因,分枝杆菌的培养需在生物安全Ⅱ级及以上级别实验室才可以开展。在中低收入国家,一般在结核病参比实验室开展培养,主要包括固体培养法和液体培养法(MGIT)两种,从采集样本至报告阳性培养结果,固体培养法一般需4~6周,而MGIT由于培养基营养丰富,可能提前到1~2周上报阳性结果[15]。我国大多数结核病实验室使用罗氏固体培养基培养分枝杆菌,在结核病可疑症状者中阳性率为28%~34%,其所需时间较长,不利于早期发现肺结核病患者和早期诊断耐药肺结核病患者[16]。Brum等[17]评估了MGIT320诊断结核病的价值,在涂片阳性的患者中,固体培养和MGIT的报阳时间分别为17.3 d和8.8 d,在涂片阴性的患者中分别为24.1 d和13.2 d。可见MGIT诊断结核病阳性率更高,用时更短,在结核病早期诊断非常有效。
1.3药敏试验 表型药敏试验(phenotypic drug sensitivity test,PDST)是在含一定药物浓度的固体培养基上接种一定数量的分枝杆菌,当分枝杆菌能在该培养基上生长时被界定为耐药菌株,反之则定为敏感菌株。目前结核分枝杆菌PDST方法有绝对浓度法、固体比例法、液体药敏法以及7H10或7H11琼脂法。固体法药敏试验根据操作方法不同分为绝对浓度法和比例法,丁北川等[18]按照世界卫生组织规定的绝对浓度法进行药敏试验,结果与比例法差异无统计学意义。刘宇红等[19]研究表明比例法和国内绝对浓度法结果存在明显差异的药物是异烟肼、乙胺丁醇,而浓度界限接近的利福平则差异不明显,有差异的菌株最低抑菌浓度(minimal inhibitory concentration,MIC)均在比例法和绝对浓度法浓度界限之间。说明两种检测方法之间主要差异是耐药界限。液体药敏试验作为比例法药敏试验的一种,因培养和药敏检测到出报告的时间大大缩短,而被越来越多的实验室采用。但液体药敏试验需专用设备和专用试剂,成本较高,因此,限制了液体药敏方法的广泛推广,尤其是在中低收入国家或地区[7]。目前,世界卫生组织推荐用于结核分枝杆菌药敏检测的方法中,可进行MGIT液体法药敏的检测药物为11种,多于其他LJ固体法和7H10/7H11法。目前基于MGIT的液体药敏是诊断二线抗结核药物,特别是贝达喹啉、利奈唑胺等药物耐药性的核心方法。
1.4结核抗原检测 脂阿拉伯糖(lipoarabinomannan,LAM)是分枝杆菌细胞壁脂多糖的组成成分,其核心骨架为甘露聚糖,侧链为甘露糖、阿拉伯糖单位,分子以磷脂酰肌醇锚定在胞质膜上,具有高免疫原性。具有免疫缺陷症状的HIV-TB共感染患者的尿液中可检测到LAM抗原,使用酶联免疫吸附测定(enzyme-linked immunosorbent assay,ELISA)方法或者TB-LAM检测试纸条,这种检测试纸条造价便宜且在30 min内可以获得结果[20,21]。在HIV-TB共感染、免疫缺陷(CD4<200个/μl)人群,其诊断结核病灵敏度超过70%[7]。Broger等[22]研究了检测感染HIV患者使用便携式的商业化LAM检测试剂盒进行尿检,发现改进后的SILVAMP-LAM在检测CD4细胞数量≤100个/μl时灵敏度为87.1%(95%CI:79.3%~93.6%),高于未改进的LF-LAM检测方法,同时比较了感染HIV患者CD4细胞数量分布为≤100个/μl,101~200个/μl和>200个/μl时SILVAMP-LAM检测灵敏度,发现在CD4≤100个/μl时灵敏度最高。世界卫生组织推荐其用于HIV阳性住院患者有结核病症状,伴CD4≤100个/μl或者重症HIV阳性患者[23]。
2 免疫学检测
传统病原学检测方法效果有限,无法真正满足临床需求,基于宿主和病原相互作用的免疫学检测技术在结核病辅助诊断中可能具有重要作用,传统的检测方法包括结核抗体、结核菌素皮肤试验(TST)、γ干扰素释放试验(interferon-γ release assay,IGRA)等,其中后两种方法对于区分潜伏感染和健康人群具有重要价值,近年来基于转化医学的新型宿主诊断标志物的筛选和应用为结核病免疫学诊断提供了新的思路,下面主要对此类技术进行介绍。
2.1结核抗体检测 基于血液标本的活动结核诊断产品已应用多年,特别是在结核病高负担国家。世界卫生组织于2008年对不同国家报送的19种结核病血清学快速诊断产品进行系统评估,结果表明,与痰培养相比,这些试剂盒在涂阳患者中检测的灵敏度在1%~60%之间,特异度在53%~99%之间[24]。在涂阴患者和HIV阳性患者的灵敏度和特异度比涂阳患者平均低22%左右。后续的对抗体检测方法的荟萃分析也表明这类检测方法准确性偏低,因此,世界卫生组织不建议将抗体检测方法用于活动性结核的诊断[25]。尽管有学者认为这种灵敏度的差别是由于结核感染的不同阶段分泌不同的蛋白从而产生不同抗体,并建议使用多种抗体的组合以提升试剂盒检测的灵敏度,但是这种改良方法在提高灵敏度的同时,导致检测特异度的显著下降,因此,对基于抗体的免疫学诊断方法需要不断的改进和优化。
2.2TST 在IGRA出现前,TST一直是诊断潜伏感染及辅助诊断活动性结核病的金标准[26]。借助皮下注射结核分枝杆菌复合群菌株蛋白衍生物,观察人体对其免疫应答,从而判断患者是否被结核分枝杆菌复合群感染。早期使用的TST是牛型分枝杆菌的蛋白衍生物,因此无法有效区分卡介苗(BCG)接种与结核分枝杆菌感染造成的阳性结果。近来,出现了以人型结核分枝杆菌制备的蛋白衍生物,可以有效排除BCG接种造成的假阳性结果。但是TST对于部分特殊人群,包括营养不良和HIV感染引起的免疫抑制人群,容易由于免疫应答不足造成假阴性的情况[27,28]。此外,注射方式及判读结果等都可能影响最终的检测结果,48~72 h后的判读方式可能会影响TST在人群中的使用范围。
2.3IGRA IGRA是近10余年新型的一种潜伏感染人群的免疫诊断方法。通过检测受试者外周血中是否存在结核抗原特异性的记忆淋巴细胞,此方法能够精准鉴定其结核感染状态[29]。相比于TST,IGRA具有更高的特异性,可能区别结核自然感染和BCG疫苗诱发的细胞免疫反应。然而其在临床中使用的主要问题在于无法区分潜伏感染和活动性结核,因此,IGRA阳性结果不能作为活动性结核的确诊标准[30]。尽管有研究表明结核抗原特异性的γ干扰素释放水平随着治疗过程明显下降,但是世界卫生组织在相关指南中不建议在结核病高负担国家诊断活动性结核,同时反对用于预测结核病患者的治疗转归或者疫苗接种后的保护效力评价[31]。然而,IGRA对于部分菌阴结核、儿童结核等缺乏病原学依据的活动结核病患者的临床诊断存在一定的价值。
2.4结核宿主反应 结核感染人体后,宿主的免疫系统启动一系列应答反应应对结核分枝杆菌的入侵,寻找基于宿主特异性的诊断标志物成为解决菌阴结核诊断难题的突破口。多项研究利用转录组学的方法探究活动性结核患者全血细胞转录组图谱,鉴定出干扰素诱导的多个基因标志物可用于诊断活动性结核,这些标志物仅在活动性结核患者中高表达,可有效排除健康人群及潜伏感染者[32]。一项小范围的病例对照研究显示,FCGR1B基因仅在活动性结核患者外周血中高表达,且与CD64、LTF、GBP5和GZMA四个基因联合应用时,对于活动性结核和潜伏感染者的鉴别诊断灵敏度和特异度分别达到94%和97%,具有良好的应用前景[33]。此外,Kaforou和其合作者研究了活动性结核、潜伏感染和其他疾病的外周血转录组后,筛选获得44个基因组成的标志物组合,在病原学阳性的结核病患者和其他患者的鉴别诊断中,其灵敏度为100%,特异度为96%[34]。上述结果均表明,基于宿主的免疫学诊断标志物将成为结核病诊断的重要组成部分[35]。结核-宿主免疫互作机制的深度挖掘和大队列的临床验证将帮助我们建立诊断活动性结核的新方法。英国Berry等[36]学者应用转录芯片技术对众多结核患者血中393种转录因子水平进行系统分析。结果发现有86种转录因子水平在活动性结核与其他炎症或感染性患者之间有明显区别。美国斯坦福大学Sweeney团队分析筛选了来自11个国家的14个独立队列的2 572例结核患者全血中结核感染相关的转录因子的表达水平,结果发现3个基因表达水平在活动性结核与其他患者之间有显著不同。其中GBP5和DUSP3两个因子在活动性结核患者中表达上调,而另一个KLF3表达则下调[37]。Warsinske等[38]进一步将这3个转录因子的表达因子相加减创建了一个3-基因结核分数(3-gene TB score),可以在临床上用于隐匿性结核感染和活动性结核的鉴别诊断以及治疗效果的快速准确监测。赛沛Xpert MTB HR产品将这一技术移植到GeneXpert系统中,该试剂盒采用0.1 ml末梢或采集静脉血,随到随测,可以在30 min完成检测。结果直接应用3个因子的CT值加减获得,期望在结核病的快速筛查、鉴别诊断以及治疗监测上起到一定作用[39]。
3 基因检测与分子耐药检测产品
随着分子生物学技术的不断发展,使结核分枝杆菌的检测、鉴定和药敏试验技术取得了很大的进展。分子生物学技术可特异性扩增结核分枝杆菌的目标基因,直接检测痰液、支气管肺泡灌洗液等样本,快速得到检测结果,极大缩短了结核病诊断时间,提高了结核病诊断的准确性和效率。目前应用在结核分枝杆菌基因检测与分子耐药检测方面的产品主要有实时PCR产品、等温扩增产品和基因测序产品等(见表2)[40]。

表2 世界卫生组织支持肺结核检测和药物敏感性检测的分子检测产品(翻译和修改于参考文献[40]的表1)
3.1实时定量PCR产品 实时定量PCR技术是通过荧光基团标记的特异性探针或分子信标对基因扩增产物进行标记跟踪,实时在线监控反应过程,结合相应软件对产物进行分析。与传统的细菌学检查相比,实时定量PCR技术具有灵敏度高、检测快、特异性强、可重复性好、可自动化且通量高等优点。目前实时定量PCR主要用于临床标本是否存在结核分枝杆菌复合群及其对药物的耐药性,主要有赛沛的Xpert MTB/RIF、Xpert MTB/RIF Ultra、Xpert MTB/XDR产品,罗氏的Cobas TaqMan MTB产品,雅培的RealTime MTB和MTB RIF/INF产品,Hain公司的Genotype MTBDRplus、Genotype MTBDRsl、FluoroType MTBDR产品,BD公司的MAX-MDR-TB产品,厦门致善公司的MeltPro-TB产品等。
3.1.1 赛沛Xpert MTB/RIF产品 这是一种基于巢式实时荧光定量PCR方法,能自动进行核酸提取扩增检测,可直接从痰液标本中检测结核分枝杆菌及其对利福平的耐药性,整个过程在密闭环境中进行,手动操作时间不超过1 min,对操作者和周围环境安全,全程约110 min即获得结果。在结核分枝杆菌检测方面,Xpert MTB/RIF的灵敏度约为88%,特异度约为99%[40];对涂片阳性、培养阳性患者有较高的敏感性(灵敏度为98.2%),显著高于涂片阴性、培养阳性患者(灵敏度为72.5%)[41];在HIV阴性患者中灵敏度约为88%,HIV阳性患者中灵敏度约为81%,特异度在两种人群中约为98%[42]。在57项利福平耐药检测研究中,其灵敏度约为96%,特异度约为98%[42]。在15项儿童肺结核研究中,与培养相比,其在咳痰或诱导痰样本中检测结核分枝杆菌的合并灵敏度和特异度分别为62%和98%;在胃液中合并灵敏度和特异度分别为66%和98%。相比涂片镜检,其检测结核分枝杆菌的灵敏度提高了36%~44%。其在检测利福平耐药方面合并灵敏度和特异度分别为86%和98%[43,44]。Xpert MTB/RIF不仅在肺结核得到广泛应用,而且也可用于肺外结核病及非痰标本的结核分枝杆菌检测和耐药检测。但其研究结果尚不一致,部分灵敏度欠佳,但其特异度较高,总体上显示上较好的诊断效能[40,43,45]。
3.1.2 赛沛Xpert MTB/RIF Ultra产品 通过改进试剂盒设计、PCR和突变检测,提高对低细菌负荷肺疾病和肺外疾病的结核患者检出率和改善利福平耐药检测,同时检测时间缩短为80 min。在结核分枝杆菌检测方面,Ultra比MTB/RIF更灵敏(88% vs 83%),但特异度略差(98% vs 96%);在利福平耐药方面,两者的灵敏度和特异度是相似的,分别为95%和98%。在痰标本中,Ultra的灵敏度为87.5%,而MTB/RIF为81%;在痰涂片阴性Ultra灵敏度为78.9%,MTB/RIF为66.1%,两者的特异度均为98.7%,且两者在利福平耐药性检测结果一致[42,46]。世界卫生组织在全球结核病报告中强烈推荐了Xpert MTB/RIF和Ultra技术的临床应用。Xpert MTB/RIF和Ultra被强烈推荐作为有肺结核症状和体征的成人及儿童的初始检测;在有肺结核体征和症状或胸片存在肺部异常或两者兼有的普通成人中被推荐作为肺结核初始检测;被推荐作为有肺结核症状和体征的成人和儿童的重复检测;被推荐作为成年人和儿童怀疑MDR-TB感染或并发HIV感染的首选检测方法,从而替代传统的涂片镜检、培养和药物试验方法;被推荐对疑似肺外结核患者的肺外标本如脑脊液、淋巴结和其他组织进行检测;还被推荐用于痰标本镜检的后续检测,特别是对于痰涂片检测阴性的患者[1,47]。
3.1.3 赛沛Xpert MTB/XDR产品 它可检测对异烟肼(靶基因:inhA启动子、katG、fabG1、aphC-oxyR基因间区)、乙氧酰胺(inhA启动子)、氟喹诺酮类(gyrA和gyrB)以及二线注射药阿米卡星、卡那霉素、卷曲霉素(rrs和eis启动子)的耐药性,并被定位为MTB/RIF或Ultra检测到利福平耐药患者的附加检测。在结核分枝杆菌阳性痰标本与临床分离株中,以PDST为参考标准,异烟肼检测耐药性的灵敏度和特异度分别为98.3%和95%;氟喹诺酮类耐药性的灵敏度和特异度分别为91.4%和98.5%;阿米卡星耐药性的灵敏度和特异度分别为91%和99%;卡那霉素耐药性的灵敏度和特异度分别为98.1%和97%;卷曲霉素耐药性的灵敏度和特异度分别为70%和99.7%;乙氧酰胺耐药性的灵敏度和特异度分别为65.4%和97.3%。当以测序结果为参考标准时,其灵敏度为:异烟肼99.7%,氟喹诺酮类97.5%,阿米卡星100%,卡那霉素96.5%,卷曲霉素94.1%,乙氧酰胺88.5%;除了乙氧酰胺特异度为97.3%,其他药物的特异度均为100%[48,49]。Xpert MTB/XDR旨在作为结核分枝杆菌阳性标本的反射试验,并作为诊断结核分枝杆菌/广泛耐药结核中存在的主要耐药类型的辅助诊断。为应对全球耐多药结核病危机和加快诊断,世界卫生组织确定扩大快速检测和检测耐药结核病是当务之急。获得快速、敏感和安全的基因型检测方法,如Xpert MTB/RIF、Ultra和Xpert MTB/XDR,这些方法通过识别已知的突变来检测大多数临床菌株对一线和二线药物的抗药性,将最大限度地减少生物危害,并将样品制备减少到几个手动步骤,更便于在护理点使用。当与Xpert MTB/RIF或Ultra联合使用时,Xpert MTB/XDR可将结核病检测和耐药性检测扩展到医疗服务不足的人群[50]。
3.1.4 罗氏Cobas TaqMan MTB产品 这是一种基于实时定量PCR技术、针对16S RNA基因的高通量检测试剂盒。由于标本需要用NALC-NaOH进行液化、去污和浓缩,容易出现假阴性的结果。与培养方法相比,该产品在呼吸道标本中的灵敏度为88.4%,特异度为98.8%;非呼吸性标本中灵敏度为63.6%,特异度为94.6%[51,52]。
3.1.5 雅培RealTime MTB和MTB RIF/INF产品
RealTime MTB也是一种基于实时定量PCR的检测方法,可与全自动DNA提取平台接口,可以从痰或支气管肺泡灌洗液中检测结核分枝杆菌。9项研究发现其在检测结核分枝杆菌的合并灵敏度为96%,特异度为97%。4项研究表明雅培MTB RIF/INF产品对利福平和异烟肼的合并灵敏度为88%,合并特异度为99%,同时未发现偏倚[53]。
3.1.6 Hain公司Genotype MTBDRplus、Genotype MTBDRsl、FluoroType MTBDR产品 Hain公司的Genotype MTBDRplus产品是基于PCR-线性探针杂交技术,检测结核分枝杆菌及其异烟肼和利福平耐药性的分子诊断试剂盒。多个研究表明其对利福平与异烟肼的灵敏度分别为83.4%、94.6%,特异度分别为99.6%、98.2%,而Xpert MTB/RIF对利福平的灵敏度和特异度更高,分别为96.8%和98.4%[54]。Genotype MTBDRsl产品是一种用于检测结核分枝杆菌复合体中与氟喹诺酮类和二线注射药物耐药相关的特异突变检测试剂盒。多项研究发现其在氟喹诺酮耐药性方面性能:直接检测,其灵敏度和特异度分别为97%和98%;涂阳标本:80%和100%。二线注射药物方面:直接检测,其灵敏度和特异度分别为89%和90%;涂片阳性标本:80%和100%。广泛耐药结核病:直接检测,其灵敏度和特异度分别为79%和97%;涂片阳性标本:50%和100%[55]。FluoroType MTBDR产品在涂片阳性和涂片阴性标本中检测结核分枝杆菌复合物的灵敏度分别为98%和92%。涂片阴性标本对利福平耐药的灵敏度和特异度分别为100%和97%;异烟肼耐药性的灵敏度和特异度分别为100%和98%;耐多药结核病的灵敏度和特异度分别为100%和100%。同时能鉴定rpoB、katG和inhA启动子突变的灵敏度分别为98%、97%和97%。该产品可用于利福平和异烟肼的快速药敏试验,此外能同时识别rpoB、katG和inhA启动子中几乎所有突变的能力,可能对个体化治疗有用[56]。
3.1.7 BD公司MAX-MDR-TB产品 这是一款检测临床标本中结核分枝杆菌复合物并同时检测异烟肼和利福平耐药性的分子平台。与培养相比,该产品的总体灵敏度和特异度分别为86.6%和100.0%;涂片阳性和涂片阴性标本的灵敏度分别为100%和64.5%。与PDST相比,异烟肼和利福平耐药的灵敏度和特异度分别为58.3%、99.3%和100%、98.2%;与Genotype MTBDRplus相比,异烟肼和利福平耐药的灵敏度和特异度分别为100%、99.4%和100%、99.4%[57,58]。
3.1.8 厦门致善公司MeltPro-TB产品 这是一种基于熔融曲线分析的实时PCR检测方法,有结核分枝杆菌检测和利福平、异烟肼、链霉素和氟喹诺酮等耐药突变检测等多种产品。耐药检测产品可检测痰标本的耐多药和广泛耐药,以PDST为参考标准,该产品检测利福平耐药的灵敏度为94.2%,异烟肼耐药的灵敏度为84.9%;二线药物耐药氧氟沙星灵敏度为83.3%,阿米卡星耐药的灵敏度为75.0%,卡那霉素耐药灵敏度为63.5%。总体而言,MeltPro-TB法检测耐多药结核分枝杆菌和广泛耐药结核分枝杆菌具有良好的性能,其灵敏度分别为86.7%和71.4%[59]。链霉素耐药突变检测产品在临床菌株种的检测灵敏度和特异度分别为88.8%和95.8%[60]。在疑似脊柱结核的患者中,MeltPro-TB检测结核分枝杆菌的灵敏度为57.68%,高于培养法(51.72%)和涂片法(24.45%),但显著低于Xpert MTB/RIF(85.27%)[61]。MeltPro-TB法业已作为我国检测耐多药和广泛耐药结核病例的可选择方法。
3.2等温扩增产品 等温扩增技术基于其独特的扩增原理,其灵敏度高但特异度相对较低,对防污染措施要求严格,其自动化程度越高,检测结果可信度越高。常见的等温扩增技术有环介导核酸等温扩增技术(loop-mediated isothermal amplification,LAMP)、交叉引物扩增技术(cross primer amplification,CPA)等。LAMP的特点是针对靶基因的6个区域设计4种特异引物,利用一种链置换DNA聚合酶在等温条件下保温30~60 min,即可完成核酸扩增反应。CPA可在恒定的温度条件下,通过特殊设计的引物和探针,高效扩增指定的目标核酸。与常规PCR相比,恒温扩增技术不需要模板的热变性、温度循环、电泳及紫外观察等过程。LAMP和CPA是全新的核酸扩增方法,具有简单、快速、特异性强的优点,主要用于检测临床标本中是否存在结核分枝杆菌复合群。
3.2.1 TB-LAMP产品 日本荣研株式会社TB-LAMP产品是利用环介导等温扩增技术,快速、高效、特异性检测结核分枝杆菌复合群新型分子诊断产品。在375例结核培养阳性痰标本中,TB-LAMP检出率为75.6%,其中涂阳肺结核样本检出率为97.9%,痰涂片阴性结核样本检出率为46.6%。477例未接受结核病治疗的培养阴性受试者特异度为98.7%[62]。另一项研究发现以培养作为参考标准时,TB-LAMP的总体灵敏度为99%,特异度为94%,而Xpert MTB/RIF灵敏度和特异度更高,分别为99.1%和96%,说明TB-LMAP有较高的灵敏度和特异度[63]。世界卫生组织推荐TB-LAMP或许可替代显微镜检查(有条件推荐),以帮助诊断有结核病症状和体征的成人肺结核。对于有肺结核症状和体征的成人,特别是痰涂片阴性标本需要进一步检测时,或许也可考虑作为显微镜检查的后续检查[13]。但TB-LAMP不能代替快速分子试验来检测TB和利福平耐药,尤其是MDR-TB高危人群[13]。
3.2.2 DeFast.TB产品 广州迪澳公司的DeFast.TB结核分枝杆菌复合群核酸检测试剂采用恒温扩增法。在初诊肺结核患者中其检出率为48.4%,高于涂片法;对涂阳患者的总检出率为90.2%,对涂阴患者的检出率为15.4%[64]。
3.2.3 EasyNAT TB-CPA产品 优思达的EasyNAT TB-CPA产品是基于交叉引物恒温扩增技术,检测结核分枝杆菌DNA试剂盒,用于结核分枝杆菌感染的辅助诊断。研究发现与培养法相比,该产品的灵敏度为66.7%,对涂片阴性和培养阳性患者的灵敏度仅为10%,对培养阳性患者的特异度为100%[65]。在结核性淋巴结炎儿童中,以培养和(或)细胞学综合参考标准,Xpert-MTB/RIF和EasyNAT的灵敏度和特异度分别为58%和93%、19%和100%[66]。
3.3基因测序分析 基因测序是通过对结合分枝杆菌的靶标基因中基因序列的测定,并与国际核酸数据库中的标准序列进行比对,实验对结合分枝杆菌及其耐药性的精准检测,目前主要用于分枝杆菌病原菌的耐药检测和菌种鉴定。应用于结核检测方面的测序分析主要有Sanger测序、焦磷酸测序、二代测序(next-generation sequencing,NGS)等。
3.3.1 Sanger测序 这是根据核苷酸在某一固定的点开始,随机在某一个特定的碱基处终止,并且在每个碱基后面进行荧光标记,产生以A、T、C、G结束的四组不同长度的一系列核苷酸,然后在尿素变性的聚丙烯酰胺凝胶上电泳进行检测,从而获得可见DNA碱基序列的一种方法。Sanger测序是最为经典的一代测序技术,目前仍是获取核酸序列最为常用的方法。与DST方法相比,Sanger测序在耐多药和广泛耐药结核中检出率分别为84.31%和83.33%,其中利福平、异烟肼和氟喹诺酮耐药性的灵敏度和特异度分别为96.92%和98.35%、86.89%和99.20%、77.5%和97.26%[67]。同时Sanger测序法也用于结核耐药表型结果和基因结果不一致时确认[68]。
3.3.2 焦磷酸测序 这是利用引物链延伸时所释放的焦磷酸基团激发荧光,通过峰值高低判断与其相匹配的碱基数量。由于使用了实时荧光监测的概念,焦磷酸测序实现了对特定位点碱基负荷比例的定量,因此在SNP位点检测、等位基因(突变)频率测定、细菌和病毒分型检测方面应用广泛。通过16S rRNA焦磷酸测序检测肺结核患者痰液标本,发现其中的微生物群比健康人多,且发现许多外来细菌,如狭养单胞菌、铜绿假单胞菌、嗜热菌、鞘氨醇单胞菌、甲基杆菌、发汗杆菌、单胞菌和运动菌等,这些细菌都是肺结核患者特有的[69]。用16S rRNA焦磷酸测序法检测了结核病感染患者的痰菌群发现硬壁菌、蛋白细菌、拟杆菌、放线杆菌和梭杆菌是五大细菌门,它们共同构成了98%以上的微生物群落。结核标本中蛋白质细菌和类杆菌较多,对照组中硬壁菌更为突出。在所有结核病标本中均发现放线菌、梭杆菌、瘦肉杆菌、普雷沃特菌、链球菌和维管束菌,可能代表了结核痰菌群的核心属。用高通量焦磷酸化测序技术分析了结核病患者痰中微生物群的组成和多样性。它为研究不同微生物群在结核病发病和发展中的潜在作用奠定了框架,并最终促进了结核病治疗的进展[70]。
3.3.3 NGS 其最大特征是通量高,可测定几百万甚至上亿条DNA或者RNA序列,大大加快了宏基因组测序的速度,从而可以极大地降低单个碱基测序的成本。NGS还提供了更大的检测能力,通过深度测序发现新的或罕见的变体。NGS诊断传染病的灵敏度和特异度分别为50.7%和85.7%,优于培养法,尤其对结核分枝杆菌诊断优势比达到4,但也存在假阳性结果,可能是定植、潜在感染等原因导致[71]。同时NGS更多应用于结核分枝杆菌耐药性测定,为指导耐药结核病合理治疗提供准确的依据。通过NGS获得的数据使得检测结核分枝杆菌遗传变异的能力无与伦比,通过对数据的分析有助于重建结核分枝杆菌的系统发育,这有助于我们更好地了解结核分枝杆菌的全球分布[72]。NGS已被用来解答有关结核病传播的问题,并将在不久的将来成为结核分枝杆菌分型的常规方法,因为它比传统的分型方法具有更高的分辨率。NGS的高分辨率能够区分结核的复发和再感染[73]。这对于准确评估治疗和预防方案至关重要。NGS已被用于了解结核高负荷环境下的传播动力学,证明了这种方法在确定高负荷环境下结核分枝杆菌传播动力学方面确实具有最大的影响[74,75]。NGS分析得出一线和二线药物的易感结果,这些数据也可能是了解各国结核病流行病学的宝贵资源。NGS已成功地用于乌干达的一项耐药性调查,该调查使用NGS分析了一小部分对异烟肼和利福平具有表型抗性的菌株,以尝试了解耐药性的程度。随着技术的迅速发展,NGS的成本继续下降。然而,这项技术仍然昂贵,而且对于高负担、低收入的环境来说是不可能的。预计在不久的将来,结核分枝杆菌NGS将适用于低收入、高负担的环境中,用于定期进行耐药性监测,以了解耐药机制,并为设计更廉价的分子诊断提供依据[76,77]。
4 总结与展望
结核分枝杆菌培养及其耐药性检查等表型方法技术仍然是结核病诊断中的金标准。但由于其操作复杂、周转时间冗长、生物安全要求比较高等难以在结核病诊疗中发挥主导作用。分子生物学技术以及宿主反应检测具有快速敏感的特点,但特异性有待提高(见表3)[6]。在研发中的一系列结核病的新技术方法中,以定性或定量检测感染后的结核病原体以及宿主反应的代谢产物的代谢质谱技术值得关注[78]。2014年Choi等[79]教授应用Gas Isotope Ratio质谱技术建立呼吸实验快速测定异烟肼药物的敏感性。来自南非的Mahapatra等[80]利用液相质谱方法检测患者尿液中特异代谢产物去早期判断治疗效果。来自巴西的学者[81]采用基于质谱的代谢组学技术检测并鉴别敏感、多重和广泛耐药结核菌落。这一系列结果提示组学技术检测结核菌感染后代谢产物可能成为结核感染诊断以及治疗效果监测的新兴重要技术。
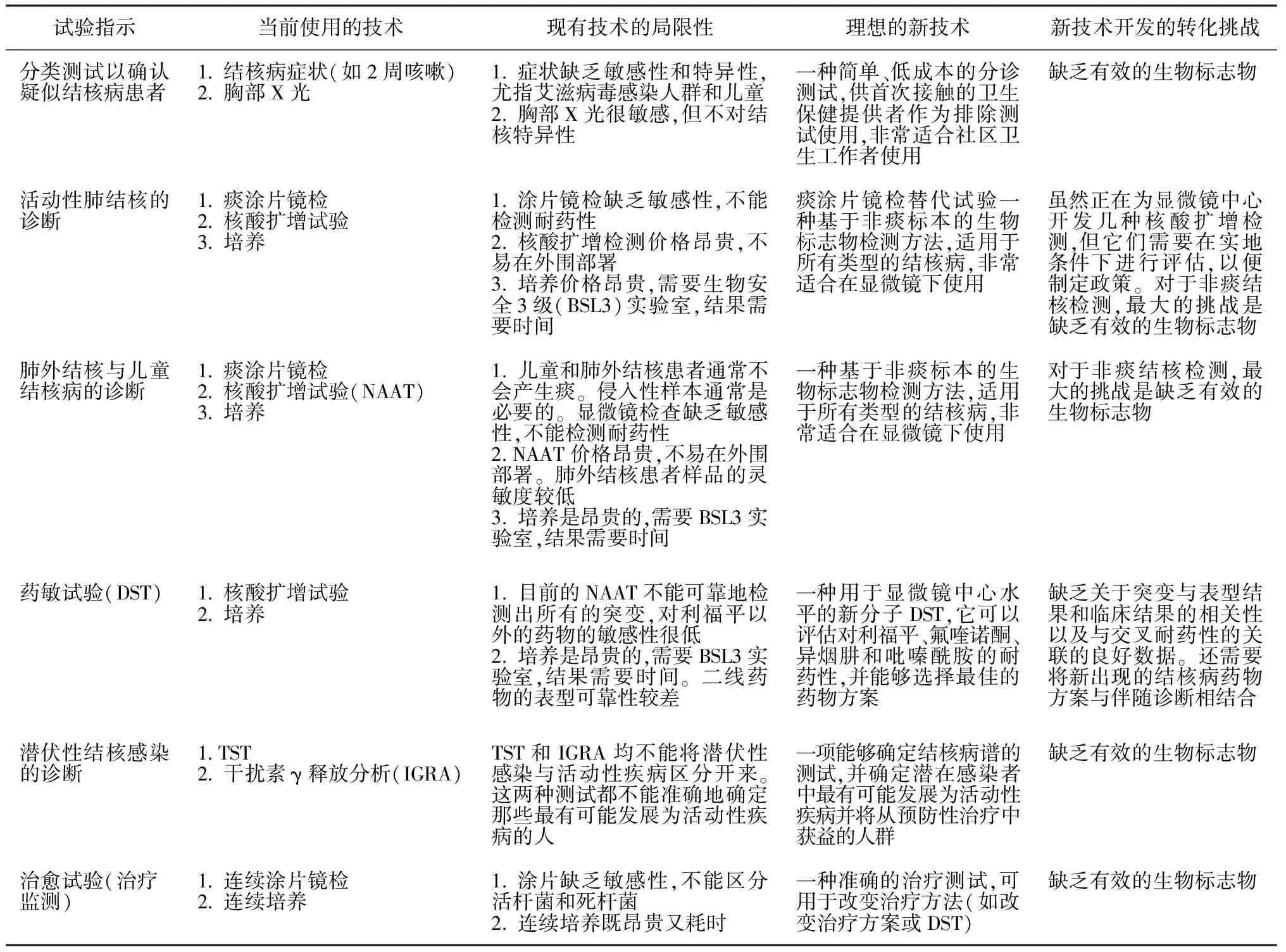
表3 开发能够满足需求的创新结核病技术的转化挑战(翻译和修改于参考文献[6]的表3)
