炎症相关因子对血管性痴呆患者继发癫痫的影响及预测价值分析
2021-02-05许超王鹏陈育松李冬辉周颖任倜
许超 王鹏 陈育松 李冬辉 周颖 任倜
血管性痴呆(vascular dementia,VaD)是由脑梗死、脑出血等脑区低灌注疾病所致的严重认知功能障碍综合征。随着国内老龄化不断增加,脑血管意外事件发生率逐年增加,VaD 患者数量也逐年增加,且部分患者出现继发癫痫[1-2]。继发癫痫是一种特殊的癫痫类型,抗癫痫药物对其治疗效果欠佳,积极去除原发疾病是根治疾病的最佳方法[3]。VaD 患者癫痫症状可反复发作,若不能有效控制可使VaD患者痴呆症状加重,明确继发癫痫出现的危险因素并积极寻找早期预测因子,对疾病的早期干预、预后改善等具有重要意义。不少研究证实炎症参与了VaD 的发生、发展过程[4],但其在VaD 继发癫痫中的作用研究少有报道。本研究分析VaD 继发癫痫患者血清肿瘤坏死因子(tumor necrosis factor alpha,TNF-α)、白介素1β(interleukin-1β,IL-1β)水平对血管性痴呆患者继发癫痫的影响及预测价值,现将结果报道如下。
1 对象和方法
1.1 对象 选取2016 年9 月至2018 年9 月长兴县人民医院收治的VaD 患者120 例,VaD 诊断标准参照中国医师协会神经内科分会认知障碍专业委员会制定的《2019 年中国血管性认知障碍诊治指南》[5]。患者出院后进行随访,随访时间截至2019 年9 月1日。根据随访结束时是否继发癫痫,将患者分为单纯VaD 组98 例、继发癫痫组22 例。纳入标准:(1)符合继发癫痫诊断标准:属于癫痫局限性发作,脑电图出现弥漫性节律性慢活动为主的改变,存在痫样放电,且既往无癫痫病史及家族史;(2)心肝肾功能基本正常;(3)临床资料完整。排除标准:(1)合并颅内感染、脱髓鞘疾病等非血管因素所致认知功能损伤;(2)合并其他严重疾病导致无法配合相关检查完成;(3)合并甲状腺功能减退症、严重自身免疫性疾病、结缔组织病等可能导致检查结果出现异常改变的情况;(4)酗酒、药物成瘾史。所有患者或家属签署知情同意书。
1.2 方法
1.2.1 一般资料收集 收集并比较两组患者的临床资料,包括性别、年龄、文化程度、合并症(高血压、糖尿病、冠心病)、生活习惯(吸烟、饮酒)、病灶位置、病灶面积、美国国立卫生研究院卒中量表(National institute of health stroke scale,NIHSS)评分。
1.2.2 血清TNF-α、IL-1β 水平测定 所有患者采集清晨空腹外周静脉血5 mL,采用美国BD 公司BD FACSCanto Ⅱ流式细胞分析仪检测,分离血清后测定TNF-α、IL-1β 水平。
1.3 统计学处理 采用SPSS19.0 统计软件,计量资料以表示,比较采用t 检验;计数资料以百分率表示,比较采用χ2检验。影响因素分析采用单因素、多因素logistic 回归。采用ROC 曲线分析炎症因子对继发性癫痫的预测价值。P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者一般资料比较 见表1。
由表1 可见,两组患者病灶位置、病灶面积、NIHSS 评分比较差异均有统计学意义(均P<0.05)。与单纯VaD 组比较,继发癫痫组出现在皮质的病灶较少,病灶面积也较小(P<0.05)。两组性别、年龄、文化程度、合并症、生活习惯的分布差异均无统计学意义(均P>0.05)。
2.2 两组患者血清TNF-α、IL-1β 水平比较 见表2。
由表2 可见,继发癫痫组患者血清TNF-α、IL-1β 的水平高于单纯VaD 组,差异均有统计学意义(均P<0.01)。
2.3 影响VaD 患者继发癫痫的多因素分析 见表3。
由表3 可见,将表1、表2 中差异有统计学意义的因素赋值作为自变量进行logistic 回归分析,病灶位于皮质下、病灶面积较大、NIHSS 评分较高、血清TNF-α 及IL-1β 水平较高是VaD 患者继发癫痫的独立危险因素(均P<0.05)。
2.4 血清TNF-α、IL-1β 水平对VaD 患者继发癫痫的预测价值 见图1。
由图1 可见,血清TNF-α、IL-1β 预测VaD 患者继发癫痫的截断值分别为9.32 pg/mL、7.495 pg/mL,相应的AUC 分别为0.812(95%CI:0.719~0.905)、0.820(95%CI:0.703~0.899),对应的灵敏度、特异度分别为77.27%、73.47%,72.73%、83.67%。
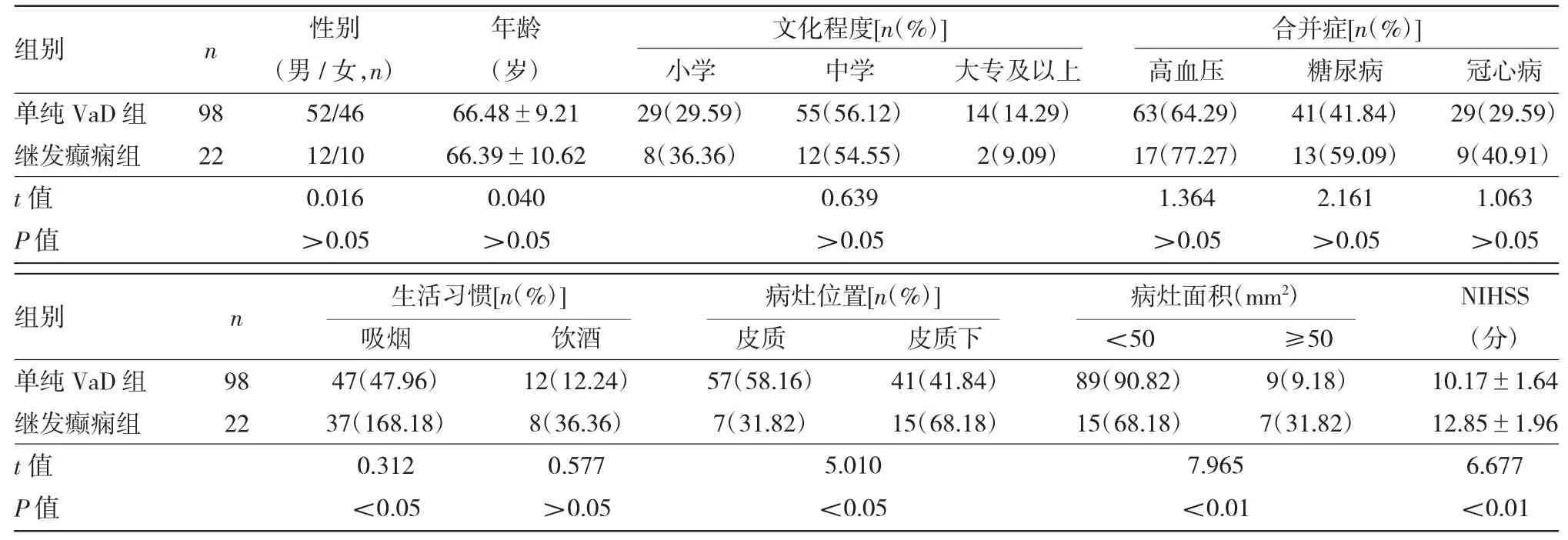
表1 两组患者一般资料比较
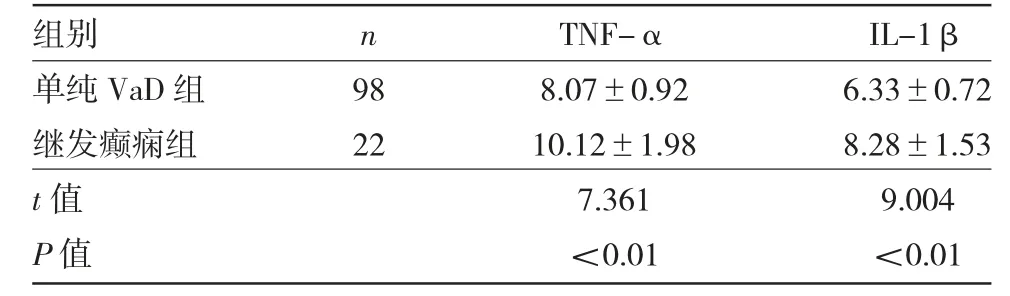
表2 两组血清TNF-α、IL-1β 水平比较(pg/mL)
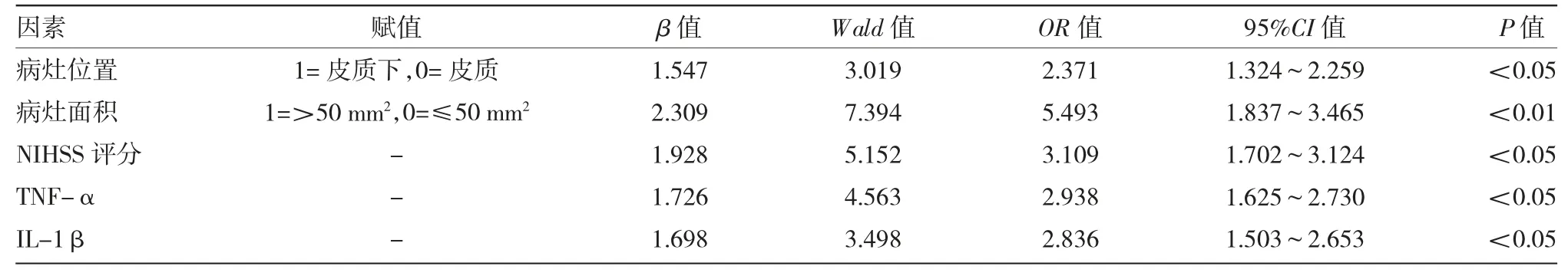
表3 影响VaD 患者继发癫痫的多因素分析
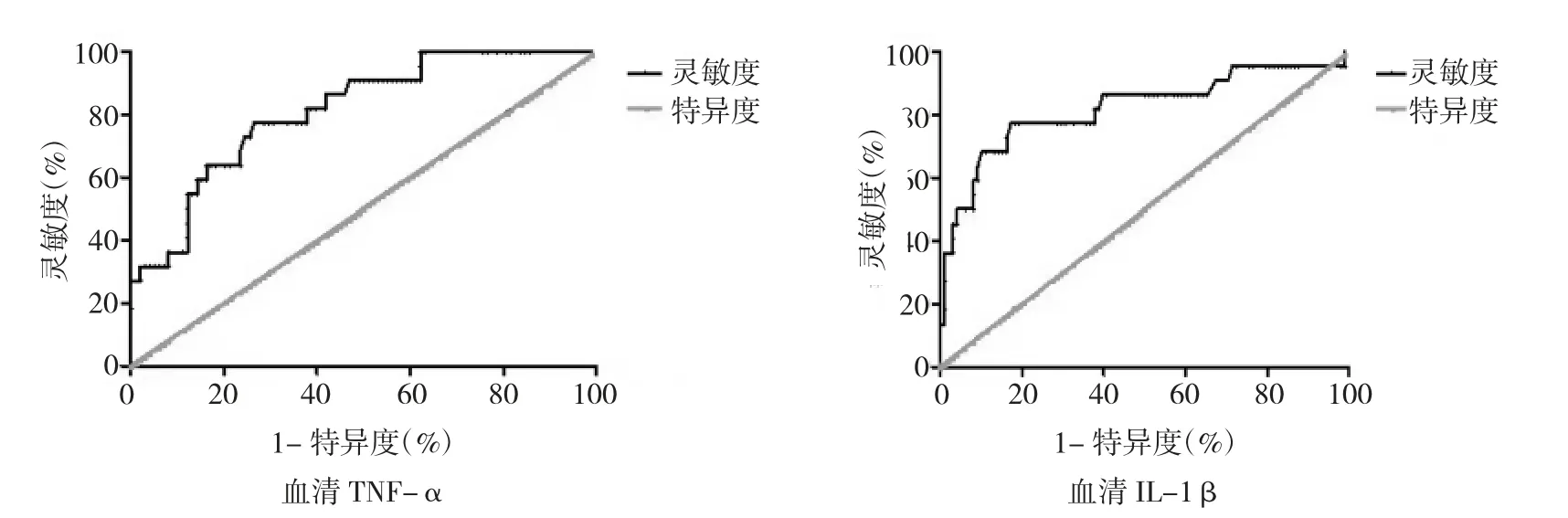
图1 血清TNF-α、IL-1β 水平预测VaD 患者继发癫痫的ROC 曲线(TNF-α 为肿瘤坏死因子-α,IL-1β 为白介素-1β)
3 讨论
继发癫痫是VaD 患者病情严重、预后不佳的重要原因之一,Imfeld 等[6]研究显示癫痫发作或癫痫在VaD 患者中较无痴呆患者更常见,而目前国内对VaD 继发癫痫的研究尚不多。Du 等[7]研究指出,针刺可抑制txnip 相关的氧化应激和炎症从而减轻VaD大鼠的认知障碍;陈粤瑛等[8]研究显示炎症因子可能通过诱导神经细胞损伤、凋亡,诱发脑白质病变等促进VaD 发生、发展。以上研究结果均提示炎症在VaD 发病中扮演重要角色,推测其在VaD 激发癫痫中可能也发挥一定作用,本文以此为切入点展开研究。
有研究指出高血压、糖尿病等心脑血管疾病危险因素使机体长期处于微炎症状态,是诱发脑卒中等发生的独立危险因素之一,也最终增加VaD 风险[9-11]。TNF-α、IL-1β 均是最具代表性的炎症因子,Liu 等[12]研究指出VaD 患者存在Th1/Th2 失衡及TNF-α 表达增加;Guo 等[13]研究证实IL-1β 可促进海马细胞凋亡并影响VaD 大鼠的学习能力。本研究中继发癫痫组患者血清TNF-α、IL-1β 的水平较单纯VaD 患者有明显提升,初步说明VaD 继发癫痫患者存在一定全身炎症状态。单因素分析发现,继发癫痫患者的病灶位置、病灶面积、NIHSS 评分与单纯VaD 患者存在明显差异,其中继发癫痫患者病灶位于皮质下、病灶面积>50 mm2的比例及NIHSS评分较高。logistic 回归分析最终证实病灶位于皮质下、病灶面积较大、NIHSS 评分较高、血清TNF-α及IL-1β 水平较高是VaD 患者继发癫痫的独立危险因素。脑卒中皮质下病灶一般经检查可发现皮质区域也存在缺血现象,可能是癫痫发生率较高的原因;病灶面积扩大患者神经功能损伤程度加重,可降低神经元胞膜稳定性并导致过度去极化、促使癫痫发作;NIHSS 评分值与神经损伤程度密切相关,而神经损伤较重者发生癫痫概率增加[14-15]。TNF-α、IL-1β 可活化小胶质细胞并损伤神经元,同时可能参与细胞程序性坏死途径启动,导致海马区神经细胞死亡及认知功能障碍[16-17],TNF-α、IL-1β 对神经损害的加重作用可能间接促使癫痫发生,但关于其具体机制尚无定论,有待后续更多基础研究明确。
VaD 患者癫痫一旦发作,其认知功能可能出现进行性下降,故在寻找癫痫发生危险因素之外,筛查易感人群并进行早期干预是从根源上减少继发癫痫病例的方法。ROC 曲线显示,TNF-α、IL-1β 水平预测继发癫痫的截断值分别为9.32 pg/mL、7.495 pg/mL,相应的AUC 分别为0.812(95%CI:0.719~0.905)、0.820(95%CI:0.703~0.899),对应的灵敏度、特异度分别为77.27%、73.47%,72.73%、83.67%,上述结果提示早期检测TNF-α、IL-1β 水平对VaD 继发癫痫具有早期预测价值,可能在未来该病早期筛查中发挥重要作用。
综上所述,炎症因子TNF-α、IL-1β 水平增加是VaD 继发癫痫的独立危险因素,且在疾病的早期预测方面具有肯定作用,可能在未来VaD 患者继发癫痫风险评估及早期干预中发挥重要作用。需要说明的是病灶面积大小区间尚无统一标准,相关文献较少,笔者依据临床观察选中(≤50 mm2,>50 mm2)区间,将在后续研究中进一步予以合理划分。本研究纳入比例数有限,可能使数据产生一定偏倚,有待后续大样本研究的进一步开展。