纳米级四氧化三铁回收水中铅离子实验
2021-02-04许端平陈丽媛孔岳
许端平,陈丽媛,孔岳
(辽宁工程技术大学 环境科学与工程学院,辽宁 阜新 123000)
吸附法是简单、经济且能有效去除废水中重金属离子的方法之一[1-8]。传统的吸附剂有粘土、氧化铁、沸石、活性炭以及生物吸附剂等,但使用的化学试剂易对环境造成污染[9]。四氧化三铁具有较大的比表面积并具有磁性,可通过磁场分离的方法进行回收利用且不会产生二次污染,因此在处理重金属污水方面已引起相当关注[10-16]。
1 实验部分
1.1 试剂与仪器
三氯化铁、氯化亚铁、氨水、无水乙醇、硝酸、硝酸铅标准溶液等均为分析纯。
新芝SB25-12DTD超声波清洗机;富华600型数显恒温水箱;JJ-4六联数显电动搅拌器;精宏DZF-6050真空干燥箱;JA2003电子天平;PHS-3C pH计;TAS-990原子吸收分光光度计;BS-S空气浴恒温振荡器;湘仪L550离心机。
1.2 吸附剂的制备
称取6.95 g三氯化铁、3.83 g氯化亚铁于烧杯中,加入适量纯水后超声振荡10 min,同时用玻璃棒搅拌,待其溶解后定容至50 mL。加入50 mL氨水,在50 ℃下置于搅拌器中搅拌2 h,搅拌结束后,在搅拌器中恒温放置1 h。用外置磁铁将沉淀物从水中分离,用去离子水和无水乙醇洗涤3次,至中性,置于70 ℃干燥箱内干燥24 h。在研钵中研磨后装入塑封袋中备用。
1.3 吸附实验
称取0.05 g四氧化三铁于50 mL离心管中,加入200 mg/L的硝酸铅溶液25 mL,将离心管放入振荡机,振荡24 h,反应温度为25 ℃。放入离心机中,转速3 800 r/min离心8 min。取上清液,用孔径0.45 μm滤膜过滤、稀释。用原子吸收分光光度计测铅的浓度。
2 结果与讨论
2.1 材料的表征
由图1可知,制备的Fe3O4粒子呈球形或近球形分布,粒径均在100 mn以内,为纳米级粒子。

图1 纳米级四氧化三铁粒子的SEM表征Fig.1 SEM characterization of nano-Fe3O4 particles
由图2中581 cm-1处峰值可知,其符合纳米级四氧化三铁的红外吸收峰值,制备出的材料为纳米级四氧化三铁。

图2 优化工艺后制备的磁性纳米Fe3O4粒子红外图谱Fig.2 Infrared spectra of magnetic nano-Fe3O4 particlesprepared by optimized process
2.2 吸附动力学[17]
由图3可知,四氧化三铁对铅的吸附量随着时间的增加而迅速升高,达到一定值后,增加趋势趋于平缓稳定。0~4 h四氧化三铁对铅的吸附量快速升高,因为起始阶段吸附剂表面的吸附位点较多,且重金属浓度较高,易发生反应,属于快速吸附阶段。4~24 h,四氧化三铁对铅吸附速度变慢,吸附量随时间变化不大,因为这个阶段的吸附剂点位逐渐饱和,且重金属浓度相对较低,因此吸附速率减慢,属于慢速吸附阶段。24~48 h,四氧化三铁对铅的吸附量基本没有变化,属于平衡阶段。平衡时最大吸附量为33.93 mg/g。

图3 吸附时间对纳米级四氧化三铁吸附铅离子的影响Fig.3 Effect of adsorption time of nano-Fe3O4 on lead
采用准一级动力学模型和准二级动力学模型拟合实验数据,结果见表1。

表1 纳米级四氧化三铁对铅的吸附动力学拟合参数Table 1 Kinetic parameters of leadadsorption by nano-Fe3O4
由表1可知,四氧化三铁对铅的吸附更符合准二级动力学方程,四氧化三铁对铅的吸附过程属于化学吸附[18]。
2.3 pH对四氧化三铁吸附铅的影响
pH是影响吸附剂吸附铅离子的重要因素之一,pH不仅会影响铅离子在水中的存在形式,而且会影响纳米级四氧化三铁吸附剂的表面电荷[19-20]。图4为不同初始pH下纳米级四氧化三铁对铅离子的吸附容量曲线。

图4 pH对纳米级四氧化三铁吸附铅的影响Fig.4 Effect of initial pH on lead adsorption by nano Fe3O4
由图4可知,四氧化三铁吸附性能随着pH的增大而增大,pH=5时,四氧化三铁吸附性能最好。这可能是因为pH为5时,较多含量的氢离子占据了吸附重金属阳离子的点位;pH>5时,四氧化三铁的吸附性能随着pH的增大而减小,这可能是因为pH在接近中性时,重金属阳离子与溶液中的氢氧根生成了氢氧化物微沉淀,使能够吸附在四氧化三铁上的重金属阳离子减少[21-22]。
2.4 温度对四氧化三铁吸附铅的影响[23]
由图5可知,四氧化三铁的吸附量随原始浓度的增加而增大,浓度超过200 mg/L时,四氧化三铁吸附量趋近于饱和,随温度的升高,四氧化三铁的吸附量逐渐下降,在25 ℃,四氧化三铁的吸附性能最好,吸附量为88.15 mg/g。
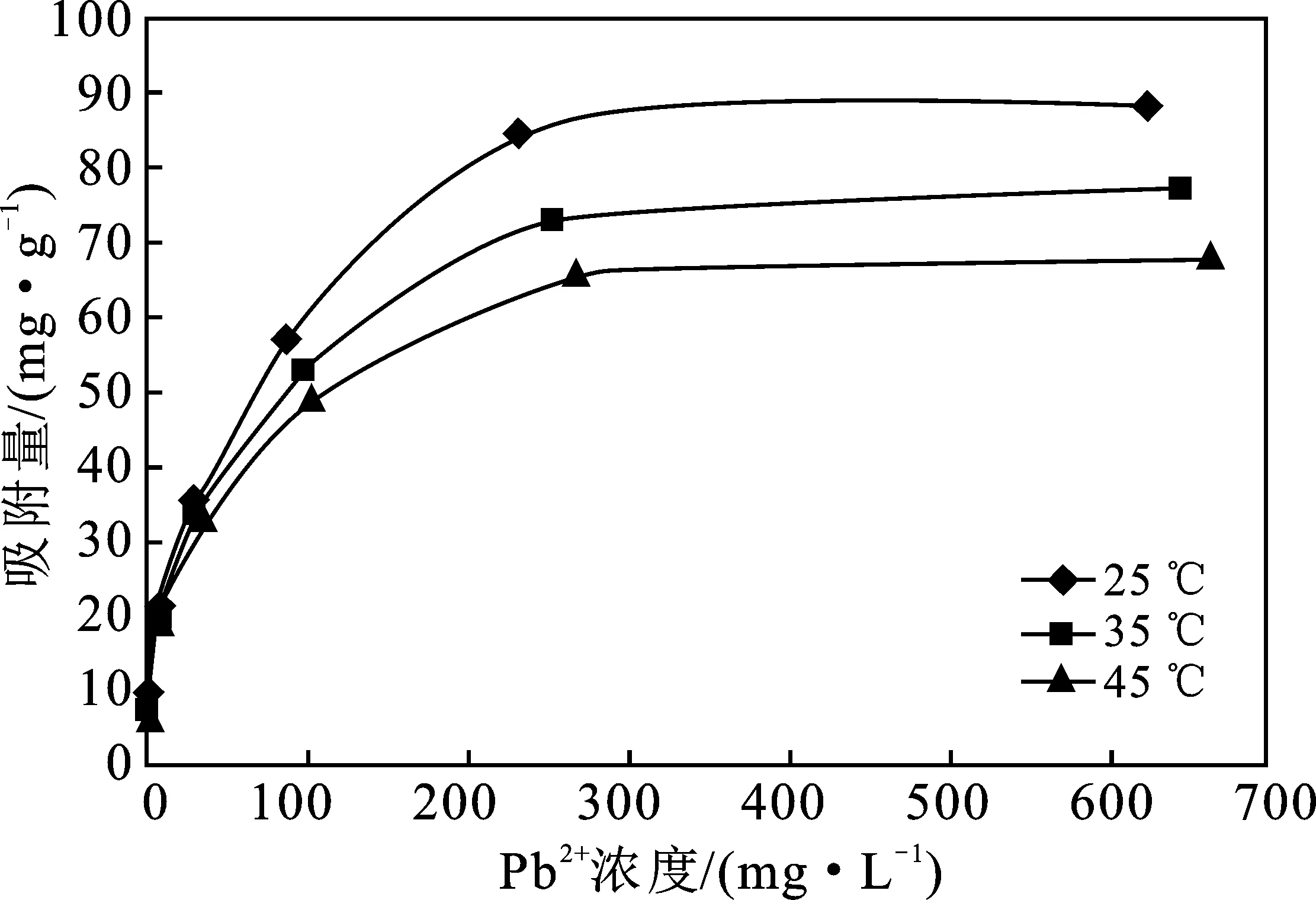
图5 纳米级四氧化三铁对铅的吸附等温线Fig.5 Adsorption isotherms of nano-Fe3O4on lead at three temperatures
分别用Langmuir和Freundlich等温吸附方程拟合不同温度下四氧化三铁对铅的吸附数据,结果见表2。

表2 不同温度下纳米级四氧化三铁吸附铅的拟合参数Table 2 Fitting parameters for adsorption of lead bynano-Fe3O4 at different temperatures
由表2可知,不同温度下四氧化三铁对铅的吸附等温数据更符合Langmuir方程,是化学吸附。另外,随温度升高,Langmuir方程中的系数(KL)降低,吸附剂的吸附性能越低。由此可知,温度升高不利于四氧化三铁对铅离子的吸附。
2.5 吸附热力学
自由能变是吸附优惠性和吸附驱动力的表现[24]。化学吸附的自由能变化范围在-400~-80 kJ/mol,物理吸附则在-20~0 kJ/mol范围内变化[25]。自由能变的计算结果见表3。

表3 纳米四氧化三铁吸附铅的热力学参数Table 3 Free energy variation parameterof nano-Fe3O4 on lead
由表3可知,吸附自由能变ΔG=-103.57~-97.97 kJ/mol,表明纳米级四氧化三铁对铅的吸附为化学吸附。ΔG<0,表示纳米级四氧化三铁对铅的吸附反应随着温度的升高,自发进行反应的趋势变弱。ΔH0<0,反应为放热反应,且ΔS0>0,四氧化三铁吸附铅的反应可以自发进行。
3 结论
(1)纳米四氧化三铁在24 h,pH=5,温度为 25 ℃ 时对铅的吸附效果最好,最大吸附量为 88.15 mg/g。
(2)纳米四氧化三铁对铅的吸附符合Langmuir等温吸附模型,其吸附过程遵循准二级动力学方程,R2均大于0.99,以化学吸附过程为主,反应为放热反应,且可以自发进行。
