基于GC-MS技术及网络药理学探讨醒脑静注射液入脑成分抗脑缺血损伤的作用机制
2021-02-03吴京霓刘瑞敏许丹妮李玥璇常中满郝佳雪郑晓晖
吴京霓,刘瑞敏,许丹妮,李玥璇,常中满,郝佳雪,贾 璞,廖 莎,郑晓晖
西北大学生命科学学院,陕西 西安 710069
脑卒中是一种急性脑血管疾病,是我国成年人群致死、致残的首位病因,具有发病率高、致残率高、死亡率高和复发率高的特点[1]。脑卒中可分为缺血性和出血性卒中,其中缺血性脑卒中占比85%以上[2]。众所周知,脑缺血损伤机制是一个复杂的过程,包括兴奋毒性、自由基损伤、炎症反应、细胞凋亡等[3]。化学药主要通过神经保护、抗炎、清除自由基等途径来治疗脑缺血,但结果不尽人意。中药具有多成分、多靶点、多效应的特点,在治疗复杂的脑缺血疾病中具有优势;临床用药大多数为中药制剂,如补阳还五汤、四君子汤、醒脑静注射液等[4]。
醒脑静注射液(简称醒脑静)是经典凉开方剂安宫牛黄丸的减方,是由麝香Moschus、冰片Borneolum Syntheticum、栀子Gardeniae Fructus、郁金Curcumae Radix4 味药材经过2 次水蒸气蒸馏法制得[5-6]。临床上其常用于气血逆乱、脑脉瘀阻所致的中风昏迷、偏瘫口喎等的治疗。研究表明,醒脑静能减轻意识障碍严重程度、改善神经功能缺损症状,并能加强日常生活活动[7-8];还可降低脑缺血再灌注损伤大鼠血脑屏障通透性[9],缓解再灌注损伤引起的各种炎症反应[10],调节细胞凋亡及自噬[11-12]。但其药效物质基础仍然不明,质量不可控,严重限制其临床应用[13]。
网络药理学融合多个学科,结合多种高新技术平台、软件,将数据进行可视化,从而直观阐述中药复方与复杂疾病之间的关联,也能充分体现中药及其复方多成分、多靶点、多途径的优势[14]。血脑屏障(blood brain barrier)为正常的神经元功能和突触传递维持安全稳定的环境,相反,血脑屏障也是药物进入中枢神经系统的主要障碍[15]。因而本研究拟采用气相色谱-质谱联用技术( gas chromatography-mass spectrometry,GC-MS)识别醒脑静入脑成分,同时运用网络药理学及分子对接技术,构建“药物-成分-靶点-通路”网络,探索醒脑静治疗脑缺血药效物质基础及潜在分子机制,为其临床使用提供一定的理论依据。
1 材料
1.1 仪器及试剂
醒脑静注射液(批号1909032),大理药业有限公司;GCMS-TQ8040 气相色谱质谱联用仪、SH-Rxi-5Sil 弱极性色谱柱(日本岛津公司);正己烷(色谱级)。
1.2 实验动物
SPF 级雄性8 周龄左右SD 大鼠,动物合格证号SCXK(陕)2018-001,体质量(240±20)g,由西安交通大学医学院动物研究中心提供。购回后适应性喂养1 周,实验间饲养环境的温度为(25±1)℃,湿度(55±5)%。所有实验动物方案都通过了西北大学动物伦理委员会,所有程序均符合相关道德规范,动物实验伦理证明决议编号:NWU-AWC-20190102M。
1.3 网络药理学数据库及软件
中药系统药理学数据库与分析平台(traditional Chinese medicine systems pharmacology database and analysis platform,TCMSP,http://tcmspw.com/tcmsp.php);Swiss Target Prediction 数据库(http://www.swisstargetprediction.ch/);CTD 数据库(http://ctdbase.org/);PubChem 数据库(https://pubchem.ncbi.nlm.nih.gov/);Drugbank 数据库(https://www.drugbank.ca/);STRING 数据库(https://string-db.org/);OMIM 数据库(https://omim.org/);GeneCards数据库(https://www.genecards.org/);DisGeNET 数据库(https://www.disgenet.org/)。R 语言R-3.6.3 软件、Cytoscape3.7.2 软件、MOE Dock 软件、Venny 2.1软件;Uniprot(https://www.uniprot.org/);OmicShare(https://www.omicshare.com/)。
2 方法
2.1 动物分组、给药及样品处理
SD 雄性大鼠20 只,自由饮水和进食,适应性喂养1 周后开始实验。实验设置对照组(2 只)和给药组(8 只),对照组尾iv 生理盐水0.5 mL/100 g、给药组尾iv 醒脑静1.5 mL/100 g,给药后于枕骨大孔处抽取脑脊液。
将空白脑脊液、给药后脑脊液12 000 r/min、4℃离心10 min,取上清;然后分别用与上清等倍量正己烷溶剂萃取醒脑静、空白脑脊液、给药后脑脊液。涡旋2 min 后,12 000 r/min、4 ℃离心10 min,取上清氮气吹干,-20 ℃保存。将上述得到样品用150 μL 正己烷溶液复溶,0.22 μm 微孔滤膜滤过,用于GC-MS 分析。
2.2 分析条件
2.2.1 色谱条件 采用岛津SH-Rxi-5Sil 毛细管色谱柱(30 m×0.32 mm,0.32 μm),进样量为2 μL,分流比6∶1,体积流量1.6 mL/min,进样口温度250℃,FID 检测器温度280 ℃,载气为高纯He、H2(99.999%)。升温程序:初始温度70 ℃,以2 ℃/min升温至110 ℃;以5 ℃/min 升温至150 ℃;以1℃/min 升温至180 ℃。
2.2.2 质谱条件 四级杆温度250 ℃、溶剂延迟时间2 min,质量扫描模式全扫描,扫描范围:m/z50~500。比较质谱碎片图谱与NIST14 质谱库,鉴别醒脑静成分及其入脑成分。
2.3 醒脑静入脑成分及靶点预测
调研文献获取醒脑静入脑成分,并通过GC-MS分析对其进行补充[16-17]。运用PubChem 数据库获取成分的3D 结构,将其导入TCMSP[18]和Swiss Target Prediction[19]数据库进行靶点预测,合并2 个数据库的靶点信息。最后采用Uniprot 平台将靶点转化成“Gene Symbol”[20]。
2.4 疾病靶点的查询
通过CTD、OMIM、GeneCards、DisGeNET、DrugBank 数据库分别搜索“cerebral ischemia”,合并各数据库疾病靶点,去重后得到脑缺血疾病靶点。
2.5 药物与疾病共有靶点
将上述得到的药物靶点和疾病靶点上传至Venny 2.1 软件构建韦恩图。将得到的药物与疾病共有靶点传至STRING[21]平台,选择蛋白种属“Homo sapiens”,构建药物与疾病共有靶点间蛋白互作(protein-protein interaction,PPI)网络。并采用R-3.6.3 软件对其核心靶点进行可视化。
2.6 基因本体(gene ontology,GO)、京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)富集可视化
将药物与疾病共有靶点通过Uniprot 转化成“ensembl”格式,上传至OmicShare 云平台进行GO、KEGG 富集及可视化[22]。
2.7 网络构建
将上述得到的醒脑静入脑成分、治疗脑缺血靶点、涉及通路上传至Cytoscape 3.7.2 软件构建网络图。
2.8 分子对接验证
从PDB(Protein Data Bank)数据库下载靶点的晶体结构,随后采用MOE Dock 软件将靶点与其对应的入脑成分进行分子对接验证[23]。
3 结果
3.1 醒脑静入脑成分汇总及靶点预测
为了得到更全面的醒脑静入脑成分,在调研文献的基础上,基于上述分析条件对醒脑静及其入脑成分进行定性分析,共得到13 种入脑成分。其中栀子苷、栀子苷酸、京尼平龙胆双糖苷3 种成分均由文献查询获得[16]。GC-MS 得到龙脑、麝香酮、莪术二酮等10 种原注射液入脑成分,总离子流图见图1,结果见表1,各成分质谱图见图2,13 种入脑成分归属见表2。运用TCMSP、Swiss Target Prediction 数据库对13 种入脑成分进行靶点预测,共得到基于入脑成分的237 个潜在作用靶点,提示醒脑静入脑成分分布于4 味药材,且均作用于多个靶点。
3.2 药物与疾病相关靶点及PPI 网络构建
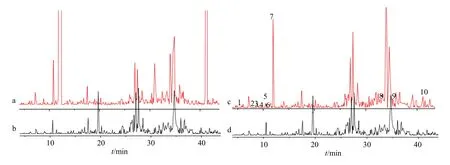
图1 醒脑静成分、入脑成分GC-MS 总离子流图Fig.1 GC-MS total ion current diagram of Xingnaojing Injection components and brain absorption components
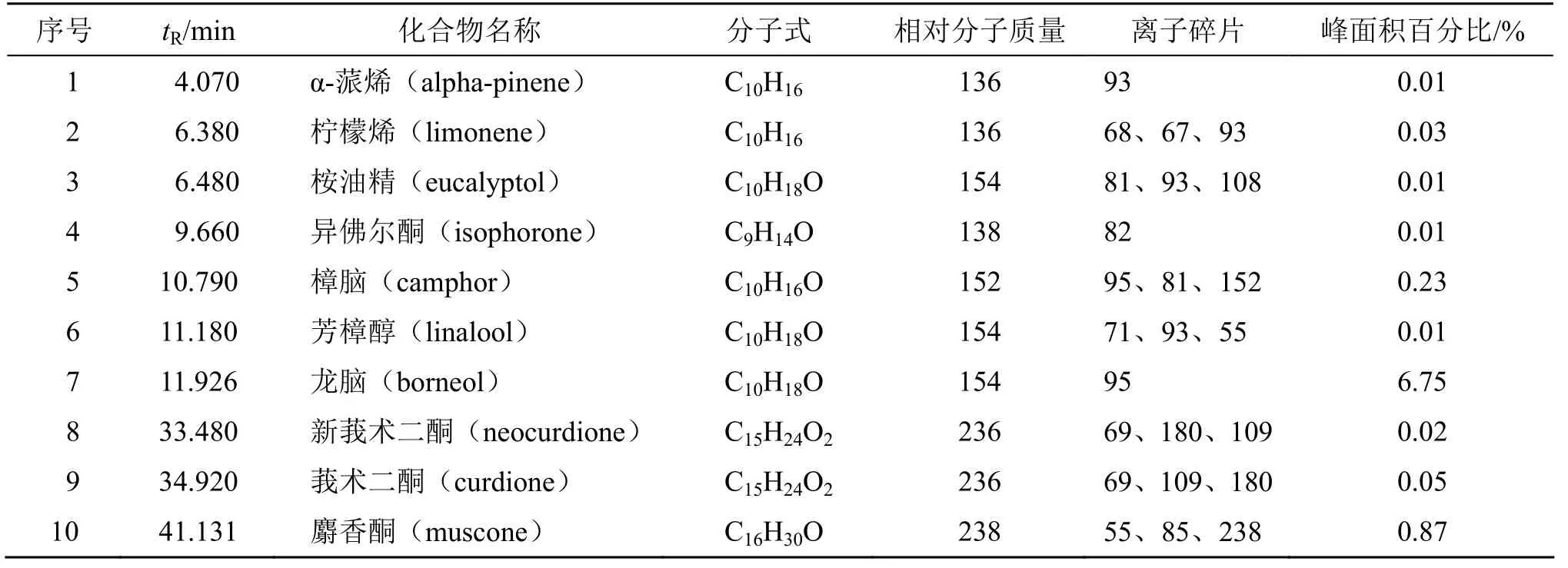
表1 GC-MS 测得醒脑静入脑成分Table 1 Summary of brain absorption components of Xingnaojing Injection measured by GC-MS
为了更好地阐明药物与疾病的关系及靶点间相互作用。通过CTD、OMIM、GeneCards 等数据库得到1720 个脑缺血靶点,将上述得到的药物靶点和脑缺血靶点取交集,得到93 个醒脑静入脑成分治疗脑缺血损伤的靶点,如图3-A 所示。将药物与脑缺血相关靶点上传至STRING 平台得到PPI 互作图,如图3-B 所示;并采用R 软件对其进行可视化处理,结果如图3-C 所示;其中度(degree)值排名前30 靶点信息见表3,涉及靶点蛋白激B(protein activated B,AKT)、丝裂原活化蛋白激酶3(mitogen activated protein kinase 3,MAPK3)、丝裂原活化蛋白激酶8(mitogen activated protein kinase 8,MAPK8)、前列腺素G/H 合酶2(prostaglandin G/H synthase 2,PTGS2)、内型皮一氧化氮合酶(endothelial nitric oxide synthase,eNOS)等。提示醒脑静入脑成分可能有93个直接作用于脑缺血损伤的靶点,度值越高的靶点可能在治疗脑缺血损伤中越关键。
3.3 GO、KEGG 通路富集
为了更好地研究候选靶点涉及的机制,对其参与的基因功能和信号通路进行富集分析。将93 个药物与疾病共有靶点上传至OmicShare 云平台进行GO、KEGG 富集及可视化,保留前25 条P值≤0.01 的KEGG 通路(pathway)进行可视化分析,见图4-A,排名较前的信号通路有神经营养蛋白信号通路、鞘脂信号通路、环磷酸腺苷(cyclic adenosine monophosphate,cAMP)信号通路、血管内皮生长因子(vascular endothelial growth factor,VEGF)信号通路及白细胞介素-17(interleukin-17,IL-17)信号通路等,见表4。由此可见,富集的信号通路主要涉及神经、血管、炎症等方面,这与醒脑静注射液功能主治开窍醒脑相吻合,提示本研究的合理性。
GO 富集结果见图4-B~D,分别从生物过程(biological process)、细胞组成(cellular component)、分子功能(molecular function)进行注释。其中生物过程主要涉及含氧化合物反应、含氮化合物反应、血液循环等,同时这些靶点与细胞组成中的神经元、突触膜、突触前膜等密切相关;也涉及神经递质受体活性、核受体活性等分子功能。

图2 醒脑静入脑成分GC-MS 质谱图Fig.2 Mass spectrum of brain absorption components of Xingnaojing Injection measured by GC-MS
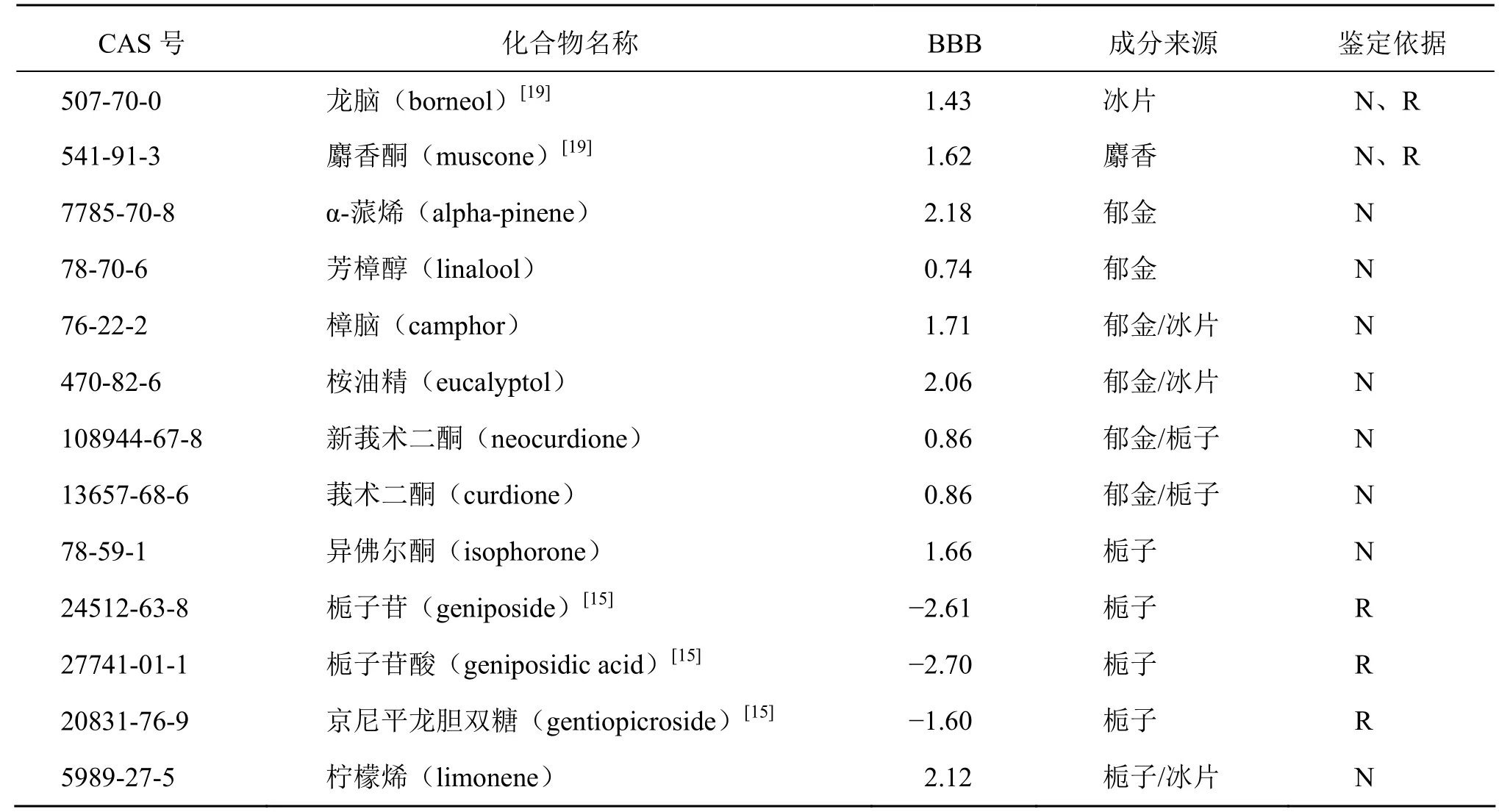
表2 醒脑静入脑成分归属Table 2 Summary of brain absorption components of Xingnaojing Injection

图3 药物与疾病共有靶点Venn 图 (A)、PPI 图 (B) 和可视化结果 (C)Fig.3 Venn diagram (A),PPI diagram (B) and visualization results (C) of common targets for drugs and diseases
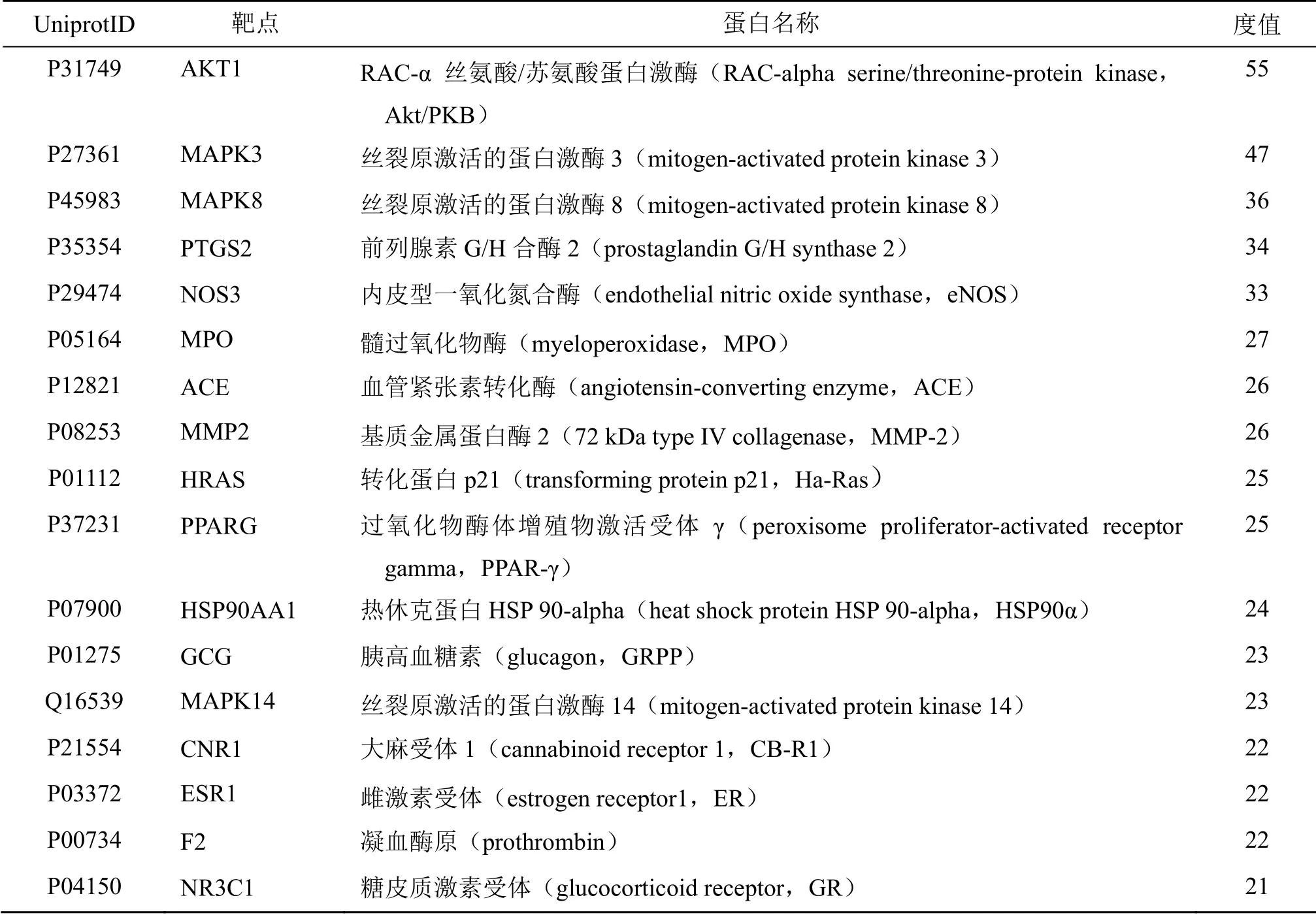
表3 药物与疾病共有靶点信息汇总 (前30)Table 3 Summary of common targets for drugs and diseases (Top 30)

续表3
3.4 网络构建
通过构建醒脑静入脑成分与其治疗脑缺血靶点及KEGG 通路网络图,可进一步揭示入脑成分靶点的协同治疗作用及治疗脑缺血机制。如图5 所示,13 种入脑成分靶点频次较高的为莪术二酮(35)、新莪术二酮(31)、芳樟醇(27)、栀子苷(23)、麝香酮(19)等。入脑成分涉及脑缺血靶点93 个,其中4味药材共有靶点有3个,环氧合酶类(COX-2、COX-1)及重组人碳酸酐酶-2(carbonic anhydrase 2,CA-2);3 味药材共有靶点有15 个,过氧化物酶体增殖物激活受体α(peroxisome proliferator-activated receptor alpha,PPARA)、eNOS、γ-氨基丁酸受体类(GABRA1、GABRB2)、单胺氧化酶类(MAO-B)、雌激素受体(estrogen receptor,ESR1)、过氧化物酶体增殖物激活受体γ(peroxisome proliferatoractivated receptor gamma,PPARG)、P2X 嘌呤受体7(P2X purinoceptor 7,P2X7)、聚[ADP-核糖]聚合酶1(poly [ADP-ribose] polymerase 1,PARP-1)等;2 味药材共有靶点有27 个;栀子特有靶点25 个,郁金特有靶点13 个,麝香特有靶点6 个。在25 条通路中,4 味药材入脑成分共同参与的有16 条,包括cAMP 信号通路、VEGF 信号通路、IL-17 信号通路等;其余9 条为郁金、栀子、麝香共同参与的通路,神经营养蛋白信号通路、叉头盒O(FoxO)信号通路等。成分-靶点-通路网络揭示了入脑成分靶点协同治疗作用及靶点与通路间相互作用,从而体现中药复方的整体性的特点。
3.5 整合醒脑静治疗脑缺血通路
为了更好地理解醒脑静注射液入脑成分治疗脑缺血的整体调控,根据上述结果建立了一条整合的醒脑静治疗脑缺血通路,如图6 所示。22 个靶点分别分布在整合通路的上下游,可被醒脑静入脑成分直接靶向,表明醒脑静可直接作用于这些靶点发挥治疗作用。醒脑静的入脑成分通过调控鞘脂信号通路、cAMP 信号通路、VEGF 信号通路、IL-17 信号通路、PI3K(磷脂酰肌醇3 激酶)/蛋白激酶B(AKT)信号通路、松弛素信号通路中部分靶点,主要集中在细胞增殖、细胞凋亡、炎症、神经保护、血管生成及花生四烯酸代谢方面发挥治疗脑缺血损伤作用。
3.6 分子对接验证
分子对接技术可研究活性成分与关键靶点的结合能力,有利于验证网络中的关键成分和靶点。将PPI 网络中前30 个靶点与其对应成分进行分子对接,结合能≤-5.0 kJ/mol,表明其结合性好[24]。分子对接结果显示栀子苷、莪术二酮、新莪术二酮可能为醒脑静治疗脑缺血的关键活性成分,分别选取4 组亲和力较强的靶点构建分子对接的3D 及2D 模式图(图7)。分子对接结果(表5)表明,多数醒脑静入脑成分与关键靶点具有较好的结合力。
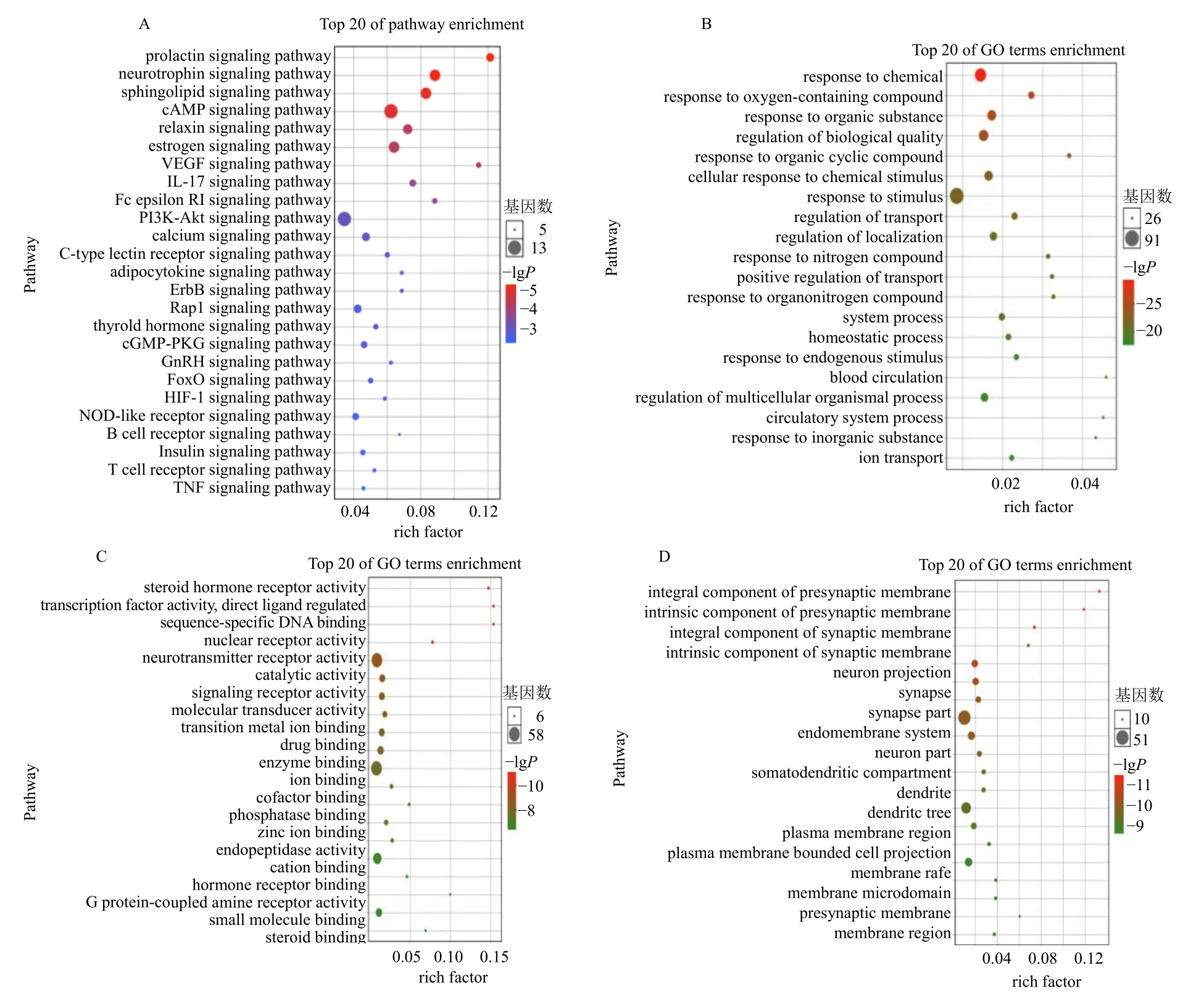
图4 KEGG、GO 富集可视化结果Fig.4 KEGG and GO enrichment visualization results
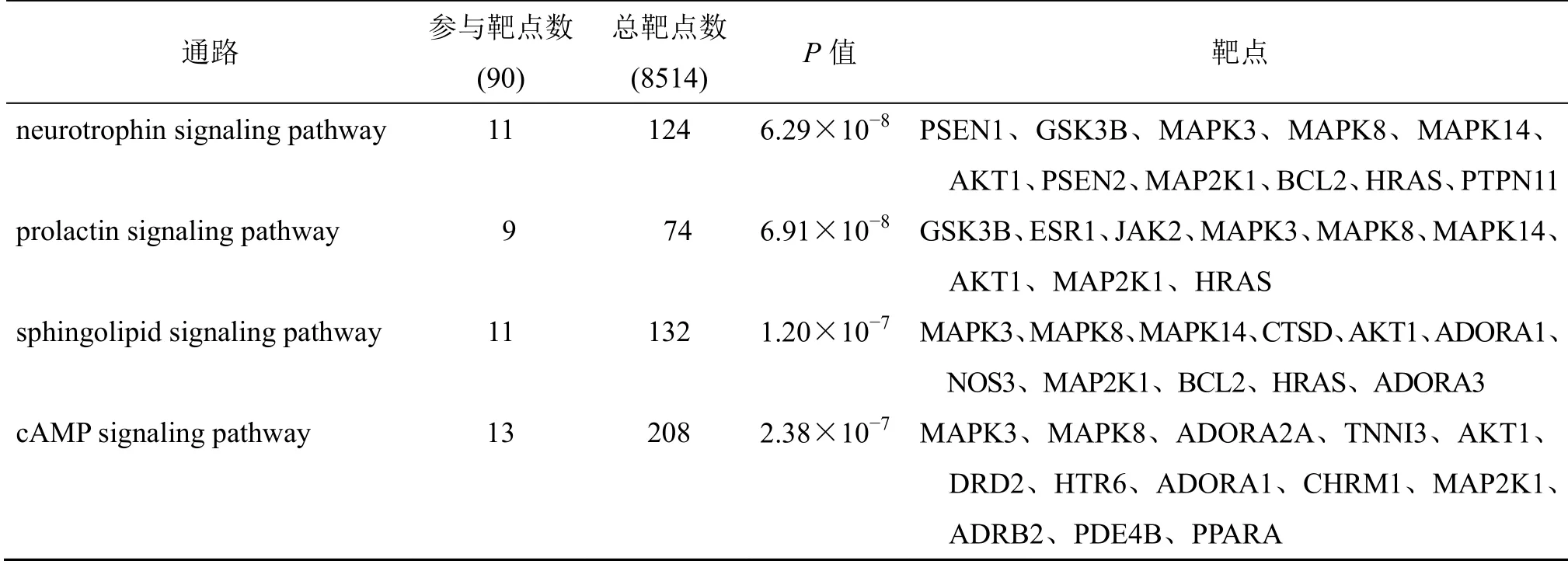
表4 KEGG 富集后的主要通路 (前10)Table 4 Main pathways after KEGG enrichment (Top 10)
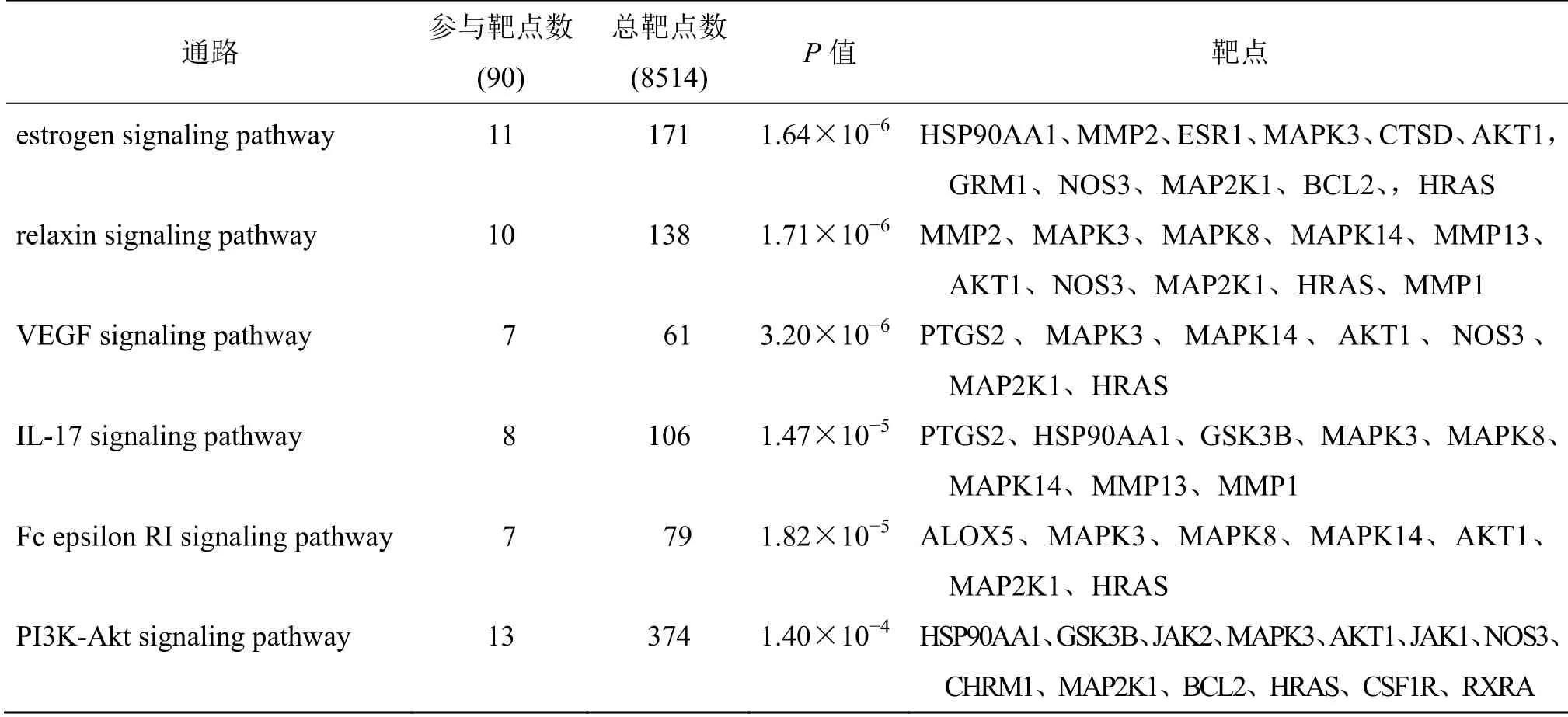
续表4

图5 醒脑静入脑成分-脑缺血靶点-KEGG 通路网络图Fig.5 Brain absorption components of Xingnaojing Injection-cerebral ischemic target-KEGG pathway network diagram
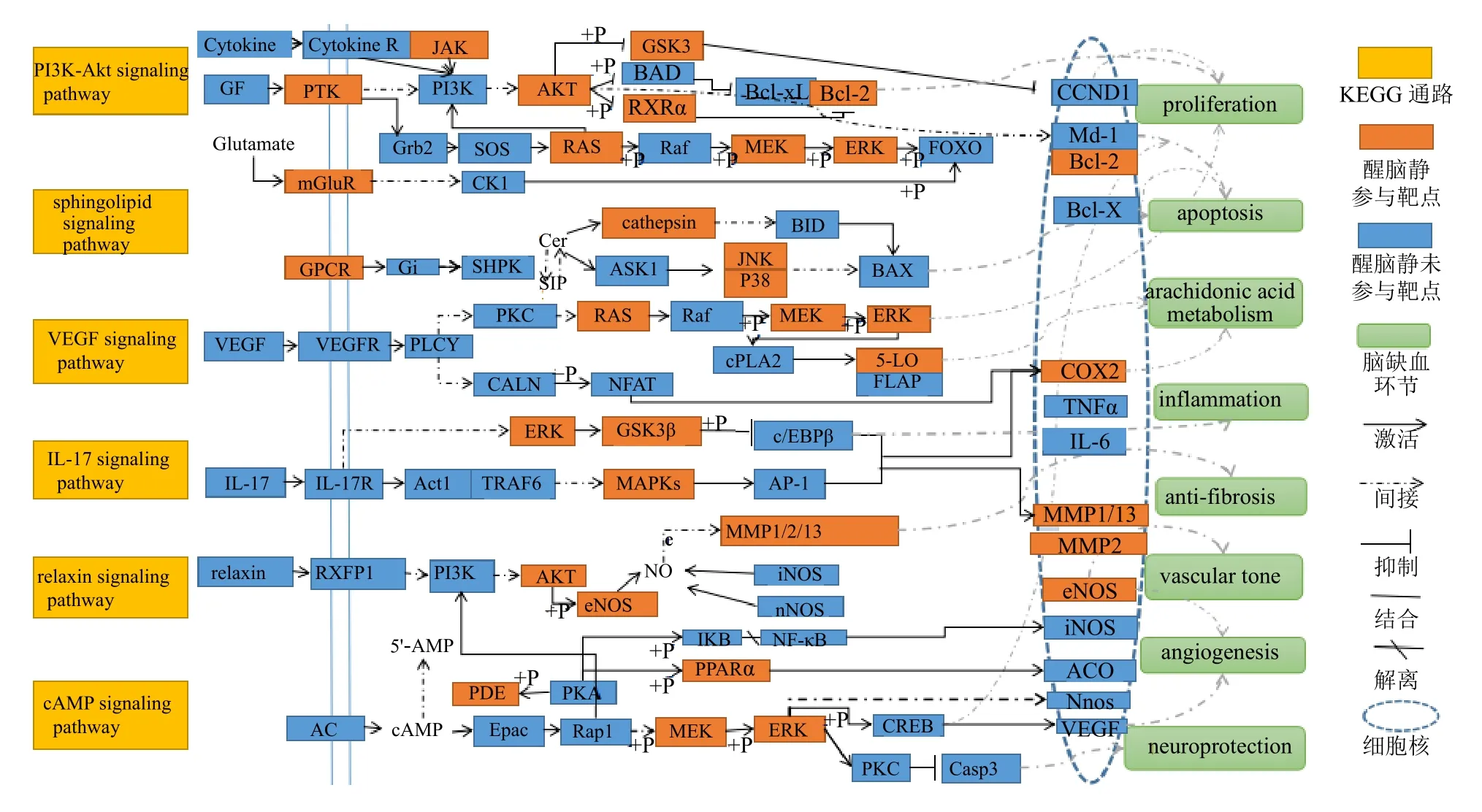
图6 醒脑静注射液治疗脑缺血主要通路图Fig.6 Mian pathway diagram of Xingnaojing Injection for treatment of cerebral ischemia
4 讨论

图7 部分分子对接结果Fig.7 Part of molecular docking results
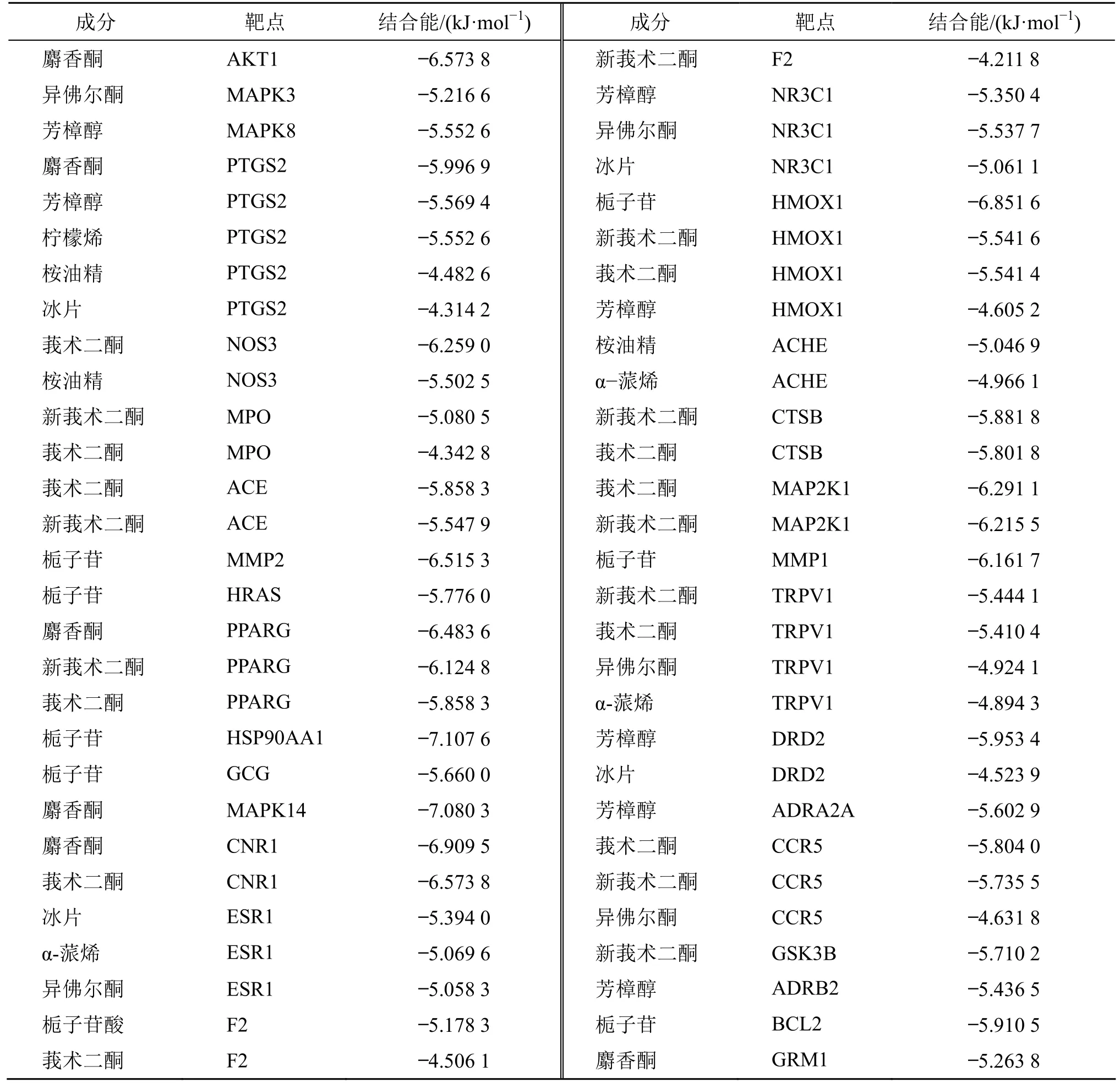
表5 分子对接结果Table 5 Molecular docking results
本研究通过TCMSP 查询醒脑静成分,得知除了栀子中的环烯醚萜类成分外,其余成分TCMSP 预测得到的BBB≥0.56。对于脑部疾病的治疗,血脑屏障是其一大障碍,良好的BBB 值为其治疗脑部疾病提供了可能[25]。通过文献调研及GC-MS 鉴定得到13 种醒脑静注射液入脑成分,郁金涉及成分6 种(特有4 种,共有2 种);栀子涉及成分7 种(特有4 种,共有3 种);冰片涉及成分3 种,均为共有成分;麝香涉及1 种特有成分。其中莪术二酮、新莪术二酮、麝香酮、栀子苷靶点频次较高,据报道栀子苷可以下调基质金属蛋白酶( matrix metalloprotein,MMP)、星形胶质细胞水通道蛋白4(aquaporin 4,AQP4)表达从而保护脑缺血再灌注大鼠模型血脑屏障[26];麝香酮可以抑制神经细胞凋亡从而具有神经保护的特性[27]。
本研究关于入脑成分龙脑、麝香酮、莪术二酮、栀子苷、桉油精、芳樟醇、柠檬烯、α-蒎烯、栀子苷、栀子苷酸、京尼平龙胆双糖苷的靶点预测结果与其他文献报道高度一致。文献中预测龙脑的靶点有雌激素受体1(estrogen receptor 1,ESR1)、前列腺素G/H 合酶1(prostaglandin G/H synthase 1,PTGS1)、前列腺素G/H 合酶2(prostaglandin G/H synthase 2,PTGS2)、内皮型一氧化氮合酶 3(endothelial nitric oxide synthase 3,eNOS3)、羟甲基戊二酸单酰辅酶A 还原酶(HMG-CoA reductase inhibitors,HMGCR)、过氧化物酶体增殖物激活受体γ ( peroxisome proliferator-activated receptor gamma,PPARG)、基质金属蛋白酶3(stromelysin-1,MMP3)等,研究中预测到的靶点有ESR1、PTGS1、PTGS2、NOS3、MAOB、GABRA1、DRD2 等,龙脑靶点参与多条抗炎通路,其中以花生四烯酸(arachidonic acid,AA)代谢通路为主[28-29]。
文献中预测到麝香酮的靶点有 AKT1、MAPK14、ADRB1、PTGS2、转化生长因子-β(transforming growth factor-β,TGF-β)、白细胞介素-6(interleukin-6,IL-6)等[20],研究中预测到的靶点有AKT1、MAPK14、ADRB1、PTGS2、ALOX5、NOS2 等;文献中预测到莪术二酮的靶点有NOS3、PTGS2、PDE4B、ADRB1 等[30],本研究预测到的靶点有 NOS3、PTGS2、PDE4B、HMOX1 等;文献中预测到栀子中环烯迷萜类成分(栀子苷、栀子苷酸、京尼平龙胆双糖苷)涉及靶点有BCL2、MMP12、HSP90AA1、NOS3、ALOX5等[31-32],本研究预测到的靶点为BCL2、MMP12、HSP90AA1、HMOX1、F2 等。在本研究预测的入脑成分靶点中,龙脑、麝香酮、莪术二酮、桉油精均涉及靶点PTGS2,龙脑、莪术二酮、桉油精均涉及靶点NOS3,龙脑、芳樟醇、柠檬烯、蒎烯涉及靶点GABRA1 等,说明这些入脑成分在治疗脑缺血疾病时可能存在协同作用。本研究预测的是与脑缺血相关的靶点,其他文献为不同疾病的靶点,如冠心病、哮喘等,因而存在差异。
醒脑静注射液可能作用于93 个脑缺血靶点,这些靶点有潜在的协同治疗作用,如COX-2、MAO等可介导脑缺血损伤的炎症反应,COX-2 作为花生四烯酸代谢产生前列腺素的主要限速酶,被称为“炎症反应基团”,参与合成前列腺素,调控有丝分裂、细胞生长[33];说明醒脑静可能通过降低COX-2活性减轻脑缺血损伤炎症反应从而改善脑缺血造成的脑组织损伤[34]。有研究表明单胺氧化酶可参与调控神经方面的疾病[30]。AKT1、Bcl-2、eNOS 等调节细胞凋亡,AKT1 又称蛋白激酶B,对脑缺血神经细胞凋亡起重要的调控作用[33]。磷酸化的eNOS 可抑制细胞凋亡,改善脑缺血损伤[10]。
丝裂原活化蛋白激酶家族(JNK、P38)在氧化应激、DNA 损伤等条件下可被激活。说明醒脑静主要调节COX-2、MAO、AKT1、Bcl-2、eNOS、MAPKs等靶点参与炎症、凋亡、血管、神经等脑缺血相关环节。
根据预测结果醒脑静主要参与神经营养蛋白信号通路、VEGF 信号通路、IL-17 信号通路、PI3K-Akt 信号通路、松弛素信号通路等,神经营养蛋白信号通路主要调节脑源性神经营养因子和神经生长因子发挥神经保护作用[35];VEGF 能够增加血管通透性,醒脑静可能通过调节花生四烯酸通路及VEGF通路,抑制炎症因子造成的脑缺血损伤[10];IL-17 参与了血管生成、免疫调节等环节,拮抗IL-17可有效抑制ERK 通路的活化[36];PI3K-Akt 信号通路是一条重要的抗细胞凋亡、促细胞增殖信号通路,多种神经营养因子可激活该通路发挥脑保护作用[37];松弛素可舒张血管、促进血管再生等来改善脑卒中患者的血管状态[38]。综上所述,醒脑静可能通过调节VEGF 信号通路、PI3K-Akt 信号通路、神经营养蛋白信号通路、IL-17 信号通路参与炎症、血管、凋亡、神经因子等的调节来达到治疗脑缺血目的,充分体现中药复方“多成分、多靶点、多途径”的特性。本研究仅对醒脑静治疗脑缺血的物质基础进行了初步预测,后期还需要通过细胞和动物实验对其入脑成分治疗脑缺血机制进行深入验证。
利益冲突所有作者均声明不存在利益冲突
