糖皮质激素和环磷酰胺及奥曲肽治疗Graves眼病的临床疗效
2021-02-01宋娅琴马晓梅
杨 露,宋娅琴,马晓梅
0引言
Graves眼病(Graves’ ophthalmopathy,GO)系Graves病特殊表现之一,属成人发病率较高的眼眶疾病,发病机制尚未完全明确,治疗相对棘手[1]。目前多认为GO发病与机体免疫系统在甲状腺球蛋白、促甲状腺素受体等自身抗原长期刺激后产生大量甲状腺刺激性抗体引起眼眶及其他组织广泛性损害有关,导致眼球突出、眼睑挛缩、眼球活动受限、结膜充血,造成视神经功能障碍及复视等一系列问题[2]。根据以上病因对GO多主张采用免疫抑制剂治疗,常用药物以糖皮质激素、环磷酰胺等为主,前者可快速缓解GO充血、水肿、疼痛等症状,改善突眼、眼肌麻痹,但不良反应居多[3]。后者可调节机体体液、细胞免疫,改善畏光、充血等眼部刺激征,适宜于糖皮质激素疗效欠佳患者,被证实可减轻GO眼部症状[4]。奥曲肽则为人工合成生长抑素类药物,早期多用于内分泌肿瘤及消化系统疾病治疗中[5],近年来发现其可通过抑制T淋巴细胞活性,调节机体免疫,抑制葡糖胺聚糖生成,改善GO球后组织浸润[6]。但对以上三种药物用于GO中的疗效对比鲜少见报道。本研究现对糖皮质激素、环磷酰胺及奥曲肽治疗GO的疗效及安全性进行比较,旨在确立GO治疗综合价值最优药物选择,以期为指导GO临床治疗提供新依据。
1对象和方法
1.1对象回顾性选取2018-06/2019-10我院收治的GO患者102例152眼。纳入标准:(1)符合GO诊断及分级标准[7];(2)有甲状腺功能亢进病史;(3)伴不同程度眼胀、突眼、畏光、流泪、眼球疼痛、眼眶水肿等眼征;(4)经眼部CT检查无球后占位病变;(5)接受糖皮质激素或环磷酰胺或奥曲肽治疗;(6)临床资料完整。排除标准:(1)合并严重心肝肾肺功能不全;(2)合并糖皮质激素应用禁忌证(骨质疏松、消化性溃疡、精神疾病、糖尿病、高血压等);(3)眼眶炎性甲瘤、硬脑膜动脉海绵窦瘘或颈动脉海绵窦瘘患者;(4)眼部肿瘤或颅内肿瘤患者;(5)近视、青光眼等其他眼部疾病患者;(6)全身感染性疾病及其他自身免疫性疾病患者;(7)已接受球后放疗或糖皮质激素治疗或其他药物干预者。根据治疗方式分为糖皮质激素组(33例51眼)、环磷酰胺组(38例59眼)、奥曲肽组(31例42眼)。三组患者性别、年龄、病程、体质量指数(body mass index,BMI)、GO分级、眼内压(IOP)、甲状腺刺激性抗体(thyroid stimulating antibody,Ts-Ab)阳性例数比较,差异均无统计学意义(P>0.05,表1)。本研究已获得医院伦理委员会审查通过,所有患者均对治疗方案知情同意。
1.2方法
1.2.1治疗方法三组均给予常规对症处理[8],控制甲状腺功能亢进(呋塞米,口服,每次20mg,每日2次,用药4wk;螺内酯,口服,每次20mg,每日2次),戒烟,禁含碘食物,低盐饮食,眼部护理(日常戴深色眼镜或眼罩,避免强光、异物或灰尘等刺激,每日睡前患眼均涂红霉素眼膏),保持充足睡眠。糖皮质激素组给予糖皮质激素治疗,甲基强的松龙(国药准字H20060054)0.5g溶于500mL 5%葡萄糖溶液,静脉滴注,每日1次,持续2wk后调整为强的松片(国药准字H33021207)治疗,口服,30mg/d,每2wk逐渐减量(每次5mg),持续治疗10wk,总疗程12wk。环磷酰胺组采用环磷酰胺(国药准字H32020857)治疗,环磷酰胺0.2g溶于500mL 5%葡萄糖溶液内,静脉滴注,间隔1日1次,2wk后改为每次0.4g,2wk 1次,总疗程12wk。奥曲肽组采用奥曲肽(国药准字H20020229)治疗,肌内注射,每次0.1mg,每日1次,2wk后调整为每次0.1mg,每周3次,总疗程12wk。
1.2.2观察指标(1)眼征评估。治疗前、治疗12wk均对患者突眼、复视、眼内压及视力进行检查,采用亨氏突眼计测定眼球突出度,国际标准对数视力表测定裸眼视力,非接触式眼压计测定眼内压,并要求患者对自觉复视情况进行自我评估,分为无复视、间断复视、持续复视。(2)眼部活动度评分。治疗前、治疗12wk均采用甲状腺相关眼部活动度评分(clinical activity score,CAS)量表进行眼部活动度评价,包括自发性球后疼痛、眼球运动疼痛、眼睑红斑、结膜充血、结膜水肿、眼睑水肿、泪阜肿胀等7项内容,每项1分,总分0~7分,CAS≥4分表示活动,积分越高,提示活动度越高。(3)眼部超声检查。治疗前、治疗12wk均行眼部超声检查,高频电子线阵扫描,探头频率7.5~10MHz,平卧,双眼仰视,眼睑皮肤涂耦合剂,眼部纵横切面扫描,晶状体位于中央且可清晰显示球后方眶尖、双侧眶骨回声及视神经断面图时,采集图像,测量眼轴、球横径、球尖距、球后软组织周长、面积及体积。(4)甲状腺激素相关受体及抗体检测。治疗前、治疗12wk均采集外周静脉血,采用放射免疫法测定促甲状腺激素受体抗体(thyrotropin receptor antibody,TRAb)、甲状腺过氧化物酶抗体(thyroid peroxidase antibody,TPOAb)的变化。(5)甲状腺体积。治疗前、治疗12wk均行甲状腺超声检查,探头频率5~14MHz,测定甲状腺体积变化。(6)记录治疗期间不良反应发生情况。
疗效评估:三组患者均于总疗程结束后参照文献[9]相关标准评估治疗效果:(1)显效:软组织受累明显改善,眼球突出减少超过3mm,眼外肌受累明显改善;(2)有效:软组织受累减轻,眼球突出减少2~3mm,眼外肌受累减轻;(3)无效:眼征无明显改变或有加重,眼球突出未见任何改善。总有效率=(显效眼数+有效眼数)/总眼数×100%。

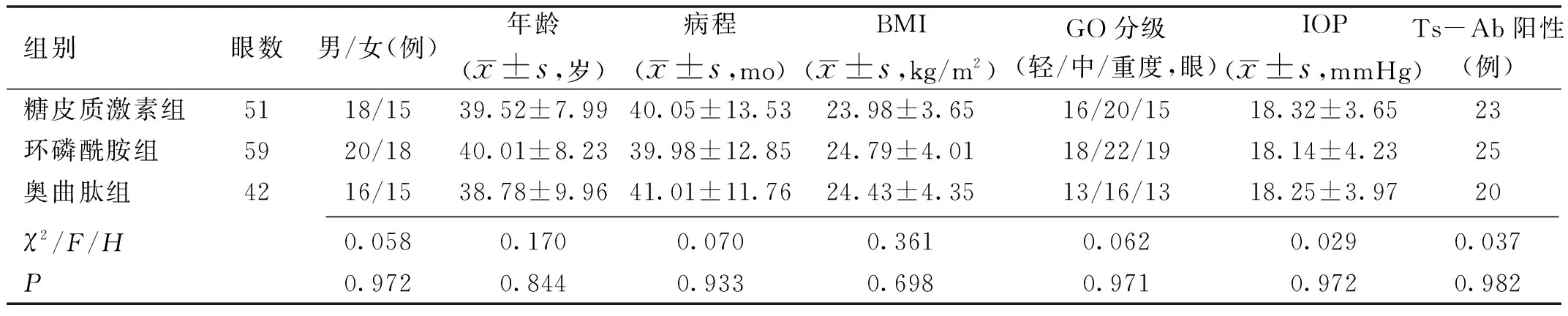
表1 三组患者一般资料比较

表2 三组患者治疗效果比较 眼(%)

表3 三组患者治疗前后突眼、眼内压、视力及CAS评分比较
2结果
2.1三组患者治疗效果比较三组患者疗效比较,差异有统计学意义(H=8.992,P=0.011)。糖皮质激素组、环磷酰胺组疗效优于奥曲肽组(H=11.662,P=0.001;H=10.223,P=0.001),糖皮质激素组与环磷酰胺组疗效比较差异无统计学意义(H=0.021,P=0.986,表2)。
2.2三组患者治疗前后眼征评估及CAS评分比较三组患者治疗前后眼内压无明显改变(均P>0.05)。治疗12wk,三组患者眼球突出度、CAS评分均降低,视力改善,与同组治疗前比较差异有统计学意义(均P<0.05)。治疗12wk,糖皮质激素组、环磷酰胺组患者眼球突出度、CAS评分均低于奥曲肽组(均P<0.05),但糖皮质激素组、环磷酰胺组各观察指标对比差异均无统计学意义(P>0.05,表3)。
2.3三组患者治疗前后自觉复视情况比较治疗前和治疗12wk,三组患者自觉复视症状情况比较差异均无统计学意义(H=0.001,P=0.999;H=3.062,P=0.216)。治疗12wk,三组患者自觉复视情况均改善,糖皮质激素组、环磷酰胺组均优于同组治疗前(Z=3.102,P=0.002;Z=2.632,P=0.008),奥曲肽组与治疗前比较差异无统计学意义(Z=1.132,P=0.257,表4)。
2.4三组患者治疗前后眼部超声检查结果比较三组患者治疗前后眼轴长度、球横径比较差异无统计学意义(均P>0.05)。治疗12wk,三组患者球尖距、球后软组织周长、面积及体积均较同组治疗前降低(均P<0.05)。治疗12wk,糖皮质激素组、环磷酰胺组患者球尖距和球后软组织周长、面积、体积均低于奥曲肽组(均P<0.05),但糖皮质激素组、环磷酰胺组组间比较差异均无统计学意义(P>0.05,表5)。
2.5三组患者治疗前后TRAb、TPOAb及甲状腺体积比较治疗前,三组患者TRAb、TPOAb、甲状腺体积比较差异均无统计学意义(P>0.05)。治疗12wk,三组患者TRAb、TPOAb、甲状腺体积较同组治疗前降低(均P<0.001)。治疗12wk ,糖皮质激素组、环磷酰胺组患者TRAb、TPOAb、甲状腺体积低于奥曲肽组(均P<0.05),但糖皮质激素组、环磷酰胺组组间比较差异均无统计学意义(P>0.05,表6、7)。

表4 三组患者治疗前后自觉复视情况比较 眼(%)

表5 三组患者治疗前后眼部超声检查结果比较
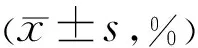
表6 三组患者治疗前后TRAb和TPOAb比较
2.6三组患者治疗不良反应发生率比较治疗期间,糖皮质激素组体质量增加及总不良反应发生率均高于环磷酰胺组与奥曲肽组(均P<0.0167),环磷酰胺组、奥曲肽组组间不良反应发生率比较差异无统计学意义(P>0.0167,表8)。三组不良反应均可耐受,经护胃、补钾等对症处理后症状均有不同程度缓解。
3讨论
GO为Graves病常见甲状腺腺外症状,约1/4~1/2 Graves病患者可能伴发GO,约65%轻中度GO患者可自行缓解,约20%患者眼征无明显改变,约15%患者眼征可能继续恶化,影响视功能[10]。GO病理机制尚未完全明确,目前尚缺乏特异性治疗药物和理想治疗手段,系困扰内分泌科医师及眼科医生的难题[11]。主流观点认为GO为细胞免疫与体液免疫自身作用的结果[12-13],对其治疗多建议选择免疫抑制剂干预[14]。早期报道证实,免疫抑制剂抑制GO患者球后组织自身抗原生成,缓解突眼症状[15]。糖皮质激素为GO治疗常用免疫抑制类药物,被证实可降低GO局部免疫活性细胞水平,降低眼眶成纤维细胞表达,减少眼部炎症浸润及细胞免疫反应,促进GO症状改善[16]。环磷酰胺同样为免疫抑制类药物,可通过杀伤免疫细胞,抑制机体自身免疫活性,改善结膜充血、肿胀、畏光等眼部刺激征[17]。早期报道环磷酰胺作为免疫抑制剂对诸多自身免疫疾病机体免疫调节均有明显作用[18-19]。奥曲肽具有类似生长抑素的药理作用,对内分泌肿瘤控制有效[20]。药理学研究发现,奥曲肽可抑制成纤维细胞增殖,抑制球后成纤维细胞DNA合成[21]。相关报道显示,奥曲肽可直接抑制T淋巴细胞活化及增殖,抑制自身免疫反应[22]。冯希敏等[23]发现,奥曲肽与肾上腺皮质激素联合应用可减轻突眼症状。但对上述三种药物治疗GO疗效的比较尚缺乏临床报道。樊琳琳等[24]采用小剂量环磷酰胺治疗GO发现其与糖皮质激素药效类似,且可减少不良反应发生风险。但对环磷酰胺与奥曲肽治疗GO疗效差异尚未明确。本研究三组患者分别采用糖皮质激素、环磷酰胺、奥曲肽治疗,结果发现,治疗12wk,糖皮质激素组与环磷酰胺组疗效相似,这与Halstenberg等[25]研究结果相似,且糖皮质激素组、环磷酰胺组疗效皆优于奥曲肽组,表明糖皮质激素、环磷酰胺较奥曲肽治疗GO疗效更典型。
表7 三组患者治疗前后甲状腺体积比较
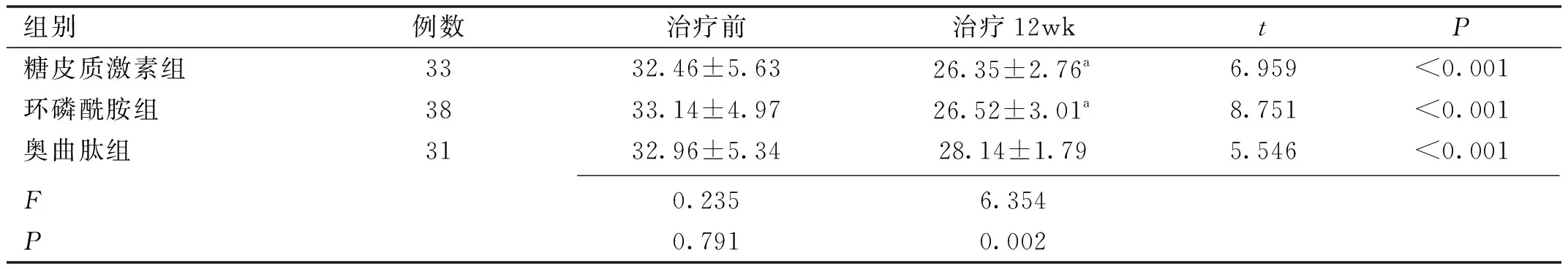
表7 三组患者治疗前后甲状腺体积比较
组别例数治疗前治疗12wktP糖皮质激素组3332.46±5.6326.35±2.76a6.959<0.001环磷酰胺组3833.14±4.9726.52±3.01a8.751<0.001奥曲肽组3132.96±5.3428.14±1.795.546<0.001 F0.2356.354P0.7910.002
注:a P<0.05 vs 奥曲肽组。
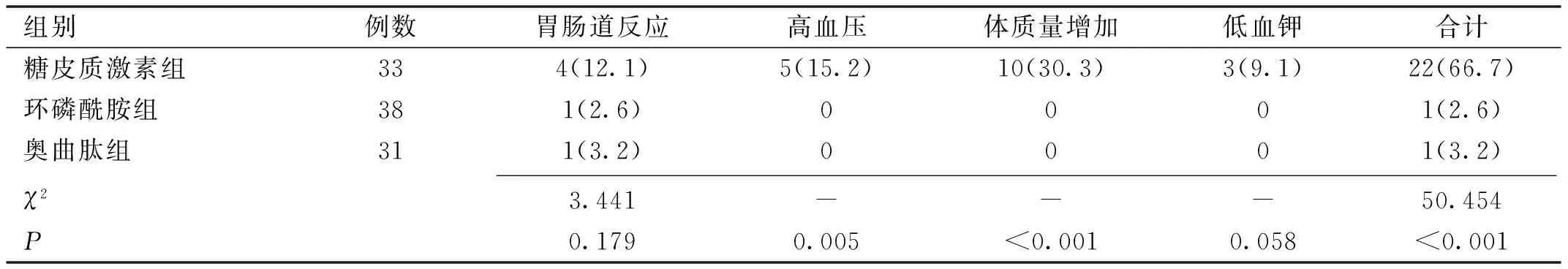
表8 三组患者治疗不良反应发生率比较 例(%)
目前关于糖皮质激素、环磷酰胺治疗GO对患者眼征及安全性的影响尚存在争论。郝海荣等[26]认为,环磷酰胺多用于无法耐受糖皮质激素治疗的患者。也有报道认为,环磷酰胺单药治疗效果不及糖皮质激素。本研究发现,治疗12wk,糖皮质激素组、环磷酰胺组及奥曲肽组患者眼征均有所改善,尤其以糖皮质激素组与环磷酰胺组眼球突出度、CAS评分、复视自觉症状改善更明显,同时患者球尖距和球后软组织周长、面积及体积均缩小,较奥曲肽组更明显,进一步证实糖皮质激素与环磷酰胺治疗GO有相似的疗效,均可缓解GO眼部症状,考虑两者均可抑制局部免疫活化,减轻机体免疫反应,减少眼眶成纤维细胞增生,改善眼外肌运动功能,减轻眼部充血、肿胀,避免炎症细胞浸润,进而减轻突眼症状,避免视神经损伤;同时可快速抑制T细胞、B细胞功能,抑制免疫母细胞分裂及增殖,避免浆细胞合成抗体,抑制致敏淋巴细胞生成,可降低局部炎症细胞浸润,抑制糖胺聚糖释放,故对GO疗效更确切[27]。相对而言,奥曲肽主要抑制T淋巴细胞分泌相关淋巴因子及增生反应,减少成纤维细胞分泌葡糖胺聚糖,缓解突眼症状,一般对眼眶内淋巴生长抑素受体阳性病例有更优的疗效[28]。本研究还发现,糖皮质激素组、环磷酰胺组患者治疗12wk后甲状腺体积和TRAb、TPOAb水平均较奥曲肽组更低,考虑经静脉注射糖皮质激素及环磷酰胺不仅可经由血液循环进入眼眶组织,避免眼肌淋巴细胞浸润,减轻眼眶组织水肿,避免免疫复合物形成[29];同时可直接作用于甲状腺组织内淋巴细胞及免疫复合物,减轻GO患者自身免疫反应,降低TRAb、TPOAb水平,逆转自身免疫病变所致甲状腺病理改变,缩小甲状腺体积[30]。在安全性方面,本研究发现,环磷酰胺组、奥曲肽组整体不良反应发生率低于糖皮质激素组,这与胡咏新等[31]相关报道结论类似,表明相比糖皮质激素,环磷酰胺、奥曲肽用药安全性更高。
本研究结果显示,三种药物中糖皮质激素、环磷酰胺治疗GO较奥曲肽疗效更确切,可改善GO眼征,缓解GO相关甲状腺病变,且环磷酰胺相比糖皮质激素治疗GO安全性更高,不良反应少,故认为环磷酰胺治疗GO可行性及安全性最高,可作为GO药物治疗的优先选择。
