2型糖尿病患者体质量指数、血脂与胰岛β细胞功能的相关性研究
2021-01-27姜国良汤智勤
薛 敏,冯 帆,姜国良,王 萍,汤智勤
上海市嘉定区南翔医院内分泌科,上海 201802
胰岛素抵抗及胰岛素分泌不足是2型糖尿病(T2DM)发病的重要病理生理机制[1],而胰岛β细胞功能在其中发挥着至关重要的作用。胰岛β细胞功能恶化的过程常伴随着脂代谢的异常,包括血清三酰甘油(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)水平升高及高密度脂蛋白胆固醇(HDL-C)水平降低。脂代谢紊乱又可引起肥胖、高血压等糖尿病慢性并发症[2]。既往研究发现,肥胖者常伴有明显的内脏脂肪蓄积、代谢紊乱、胰岛素抵抗等症状,其糖尿病患病率为正常体质量者的3倍[3]。而当体质量减轻后,组织对胰岛素的敏感性会提高,血液中胰岛素浓度降低,胰岛β细胞的代偿性分泌现象将会得到改善,胰岛素抵抗水平降低[4]。因此,血脂异常及肥胖在胰岛素抵抗和胰岛β细胞分泌功能缺陷上可能起着重要的作用。
本研究通过对比T2DM患者的年龄、病程、体质量指数(BMI)、血脂、空腹血糖(FBG)及空腹胰岛素(FINS)水平,评估胰岛素抵抗与胰岛β细胞功能,探讨T2DM患者胰岛素抵抗及胰岛β细胞分泌功能与BMI、血脂的相关性。
1 资料与方法
1.1一般资料 选取2018年12月至2019年12月本院内分泌科门诊收治的334例T2DM患者作为研究对象,其中男213例,女121例;平均年龄(58.62±14.27)岁;平均BMI(25.06±4.40)kg/m2。TC水平升高者164例,TG水平升高者169例,LDL-C水平升高者180例,HDL-C水平降低者219例。纳入标准:患者均符合WHO推荐的T2DM诊断标准[5],且正在接受降糖治疗,或者FBG≥7.0 mmol/L,同时排除妊娠期糖尿病、1型糖尿病和其他特殊类型糖尿病;近半年未接受胰岛素治疗。排除标准:有自发性酮症酸中毒倾向;有严重的心脏、肝、肾、脑功能不全;近期服用严重影响糖代谢及脂代谢药物;近期有感染或应激情况;恶性肿瘤者。本研究通过本院伦理委员会审查,研究对象签署知情同意书。
1.2方法 收集患者一般资料。受试者空腹8 h以上,于次日清晨取静脉血样。应用Cobas e 601全自动生化免疫分析仪测定FBG、FINS、TC、TG、LDL-C、HDL-C,所有试剂均为配套试剂。根据《中国2型糖尿病防治指南》[5],TC<4.5 mmol/L,TG<1.5 mmol/L,LDL-C<2.6 mmol/L,HDL-C>1.1 mmol/L认为达到糖尿病患者的血糖控制目标,血脂水平正常。统一由专人测量患者脱鞋、穿单衣下体质量、身高,并计算BMI=体质量/身高2(kg/m2)。依据《中国成人超重和肥胖症预防控制指南》建议[6],18.5 kg/m2≤BMI<24.0 kg/m2为正常,24.0 kg/m2≤BMI<28.0 kg/m2为超重,BMI≥28.0 kg/m2为肥胖。使用稳态模型评估法(HOMA)评估胰岛素抵抗指数(HOMA-IR):HOMA-IR=FBG(mmol/L)×FINS(mIU/L)/22.5;胰岛β细胞功能指数(HOMA-β):HOMA-β=20×FINS(mIU/L)/[FBG(mmol/L)-3.5]×100%;胰岛素敏感指数(HOMA-ISI)=1/[FBG(mmol/L)×FINS(mIU/L)]。
2 结 果
2.1胰岛β细胞功能与各指标的相关性分析 Pearson相关分析结果显示,HOMA-IR与BMI呈正相关(r=0.121,P=0.028),HOMA-ISI与HDL-C呈正相关(r=0.114,P=0.036),HOMA-β与年龄、病程、BMI、血脂水平均无相关性。见表1。

表1 胰岛β细胞功能与各指标的相关性分析
2.2不同BMI水平患者临床指标的比较 根据BMI将患者分为3组,即正常组、超重组、肥胖组。组间对比发现,3组患者FBG、HOMA-IR差异有统计学意义(P<0.05)。多元线性回归分析结果显示,BMI是HOMA-IR的独立影响因素(β=0.002,t=13.674,P<0.001)。见表2。
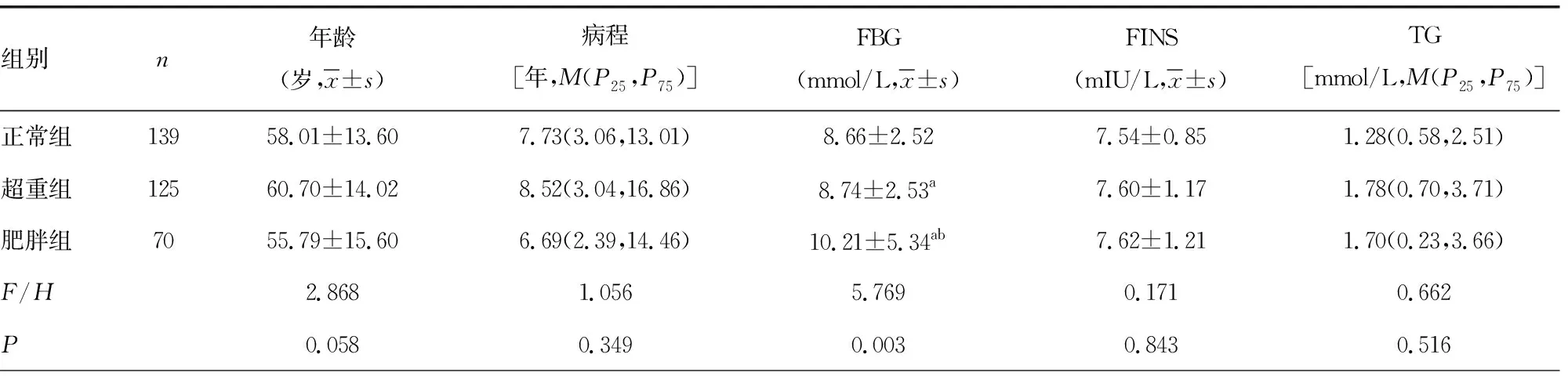
表2 不同BMI水平患者临床指标的比较
2.3不同HDL-C水平的患者临床指标的比较 根据HDL-C水平将患者分为两组,即HDL-C正常组(HDL-C>1.1 mmol/L),HDL-C异常组(HDL-C≤1.1 mmol/L),组间对比发现两组患者年龄、病程、FINS、HOMA-ISI差异有统计学意义(P<0.05)。多元线性回归分析结果显示,HDL-C是HOMA-ISI的独立影响因素(β=0.001,t=2.281,P=0.023)。见表3。
3 讨 论
胰岛功能的进行性变化在T2DM发生与发展中起到至关重要的作用:早期由于脂肪因子、炎性介质的作用,以及胰岛素自身信号传导异常,可导致机体对胰岛素的敏感性降低、胰岛素抵抗,使得胰岛β细胞超负荷分泌胰岛素。胰岛β细胞功能长期失代偿,最终导致β细胞衰竭、凋亡,T2DM患者病情逐渐恶化[7-8]。既往研究表明,脂代谢紊乱既是胰岛素抵抗的结果,也会加重患者胰岛素抵抗的病情,并引起胰岛素分泌不足[9]。而肥胖患者具有明显的糖脂代谢紊乱。因此,本研究选用稳态模型,即HOMA-β、HOMA-IR、HOMA-ISI评估胰岛β细胞功能及胰岛素抵抗,并探讨其与BMI、血脂的相关性。
本研究结果发现,在T2DM患者中,BMI与HOMA-IR呈正相关,HDL-C与HOMA-ISI呈正相关(P=0.036)。将患者按BMI水平分为正常、超重、肥胖3组,组间对比结果显示FBG、HOMA-IR差异有统计学意义(P<0.05)。相较于健康人群,肥胖及超重人群FBG水平更高,胰岛素抵抗更明显。多元线性回归分析显示,BMI是T2DM患者胰岛素抵抗的独立影响因素。肥胖影响血糖及导致胰岛素抵抗的可能机制为肥胖者脂肪体积较大,体内脂肪累积较多,脂肪细胞容易产生缺氧,易引起细胞的炎性反应和死亡,其产生的炎症因子进一步干扰胰岛素信号传导通路,导致骨骼肌、脂肪组织和肝脏发生功能障碍[10],并且,肝内脂肪变性能够导致肝脏分泌激素的功能发生异常,从而不同程度地影响胰岛素的效应,降低机体对胰岛素的敏感性,导致胰岛素抵抗[11]。此外,脂肪细胞分泌抵抗素降低细胞对葡萄糖的摄取量,使得胰岛β细胞无法摄取葡萄糖,进而抑制了胰岛β细胞分泌胰岛素。然而本研究并未观察到BMI与HOMA-β的相关性,原因可能为T2DM前期胰岛素分泌能力降低不明显,但是当病程超过10年后,其胰岛β细胞分泌胰岛素的能力会下降31.5%~39.1%[10]。
本研究还发现,以HDL-C为1.1 mmol/L作为界值将患者分为两组,两组年龄、病程、FINS、HOMA-ISI差异均有统计学意义(P<0.05)。HDL-C低于标准值的T2DM患者年龄更大、病程更长、FINS更低,且胰岛素敏感性显著低于HDL-C正常的T2DM患者。多元线性回归分析显示,HDL-C是T2DM患者胰岛素敏感性的独立影响因素。既往研究发现,HDL-C水平直接影响新诊断T2DM患者的胰岛β细胞功能[12],且在糖代谢受损的患者中,HDL-C水平与胰岛素生成指数及HOMA-ISI高度相关[13]。本研究证实了上述理论,血脂代谢紊乱导致胰岛β细胞功能障碍的可能机制有:(1)HDL-C参与TC逆向转运。HDL-C降低会使TC等脂质过量蓄积于机体胰岛素敏感组织中,产生局部炎性反应及巨噬细胞浸润,导致外周胰岛素抵抗[14-15]。(2)TC等成分在脂肪组织中沉积,可导致脂肪细胞体积增大、数量增多,使得胰岛素受体数目相对减少,活性相对降低,导致胰岛素敏感性降低[8]。(3)HDL-C降低及高胆固醇血症可引起血清可溶性P-选择素水平升高,后者可通过影响细胞代谢及介导免疫炎性反应而导致并加重胰岛素抵抗,进一步影响机体血糖水平[16]。
既往研究发现,LDL-C可以参与胰岛素抵抗,影响胰岛β细胞增殖、凋亡及胰岛素分泌[17],LDL-C水平升高是糖尿病发病的独立危险因素。国内研究发现,口服降糖药物治疗的老年T2DM患者中LDL-C与HOMA-IR具有相关性[18],而在本文中并无此发现,这可能是由于本研究样本量相对较小,可能影响研究结果。针对LDL-C与T2DM患者胰岛β细胞功能的相关性研究仍有待后续大样本临床试验验证。