原发性透明细胞肾细胞癌肺部转移的临床病理分析
2021-01-26黄清洁贺佳子李文才陈壬寅
李 莉,黄清洁,贺佳子,李文才,陈壬寅
(郑州大学第一附属医院河南省肿瘤病理重点实验室,河南 郑州 450052)
肾细胞癌是泌尿系统较常见的肿瘤,也是恶性程度较高的肿瘤[1]。新确诊的肾细胞癌中部分患者在就诊时就已发现远处转移[2],而进行过根治术患者中仍有部分患者出现远处转移[3]。肾细胞癌最常见的转移位置是肺部。本文通过对郑州大学第一附属医院2016年1月至2018年12月收治的16例原发性透明细胞肾细胞癌(clear cell renal cell carcinoma,CCRCC)肺部转移患者的临床资料进行分析,提高对原发性CCRCC肺部转移的认识。
1 资料与方法
1.1 一般资料收集郑州大学第一附属医院2016年1月至2018年12月收治的16例原发性CCRCC肺部转移患者的肺穿刺标本。入组前CCRCC术后患者9例,肾脏占位5例,肺部结节首发2例。其中男12例,女4例,男女比例为31。患者年龄35~72岁,中位年龄58.4岁。3例有吸烟史,均为男性。均无肿瘤家族史。9例有多源性肿瘤史。病理检查证实,13例肺部出现多发转移,3例单发转移。临床表现:15例患者以肺部症状为首发表现,包括呼吸困难、喘息、咳嗽、咯血、胸痛等,1例患者首发症状为腹部不适。影像学特点:16例患者均经计算机断层扫描(computed tomography,CT)发现肺部结节,其中13例为多发、3例为单发。见表1、图1。

图1 原发性CCRCC肺转移患者CT示肺部结节
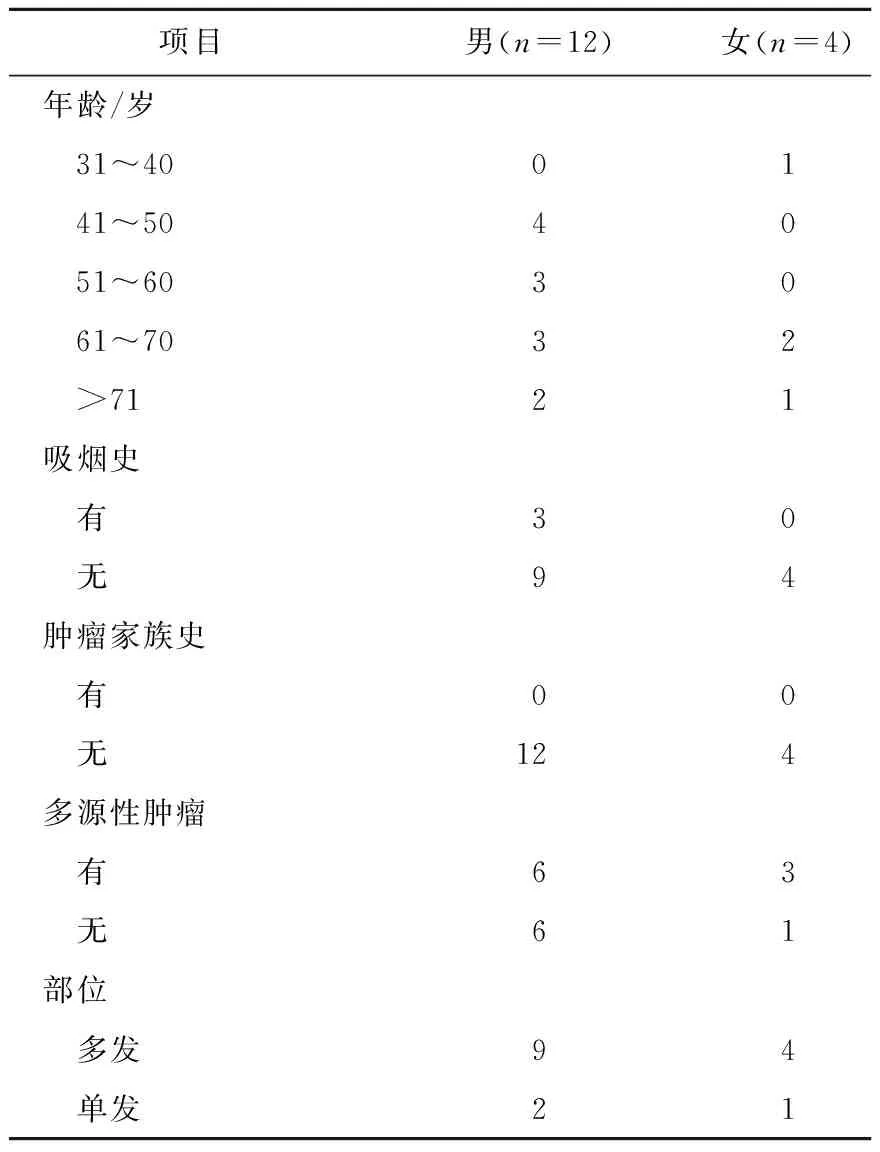
表1 16例原发性CCRCC肺部转移患者的临床病理资料
1.2 标本处理方法所有组织标本经质量分数4%多聚甲醛溶液固定,石蜡包埋,4 μm厚连续切片,然后进行HE染色和免疫组化S-P法染色,并进行镜下观察。免疫组化S-P法所用抗体包括CK、Vimentin、CD10、CA9、Ki-67、PAX-8、PAX-2、EMA、CK7、RCC、TFE-3等。
1.3 病理结果肉眼观察大体形态:原发性CCRCC呈实性,位于肾皮质。典型的原发性CCRCC大体为球形,自肾皮质呈圆形突出。肿瘤与周围肾组织界限清楚,形成推压式边界和假包膜。典型病例因肿瘤细胞内富于脂质而呈金黄色,高级别肿瘤含脂质和糖原较少,并因有出血和坏死而呈多彩状。
HE染色结果:低倍镜下:原发性CCRCC形态多样,最常见的是泡巢状和腺泡状结构。肿瘤组织中有小薄壁血管构成的网状间隔,这一特点有助于诊断。泡巢状结构中无腔,但在腺泡状结构中央有一圆形腔,其内充以淡染嗜酸性浆液或红细胞,泡巢状和腺泡状结构可以扩张形成大小不一囊腔。偶见肿瘤组织中出现小管结构。高倍镜下:大多数原发性CCRCC肿瘤细胞呈多角形或呈立方形。肿瘤细胞的细胞质内有脂质和糖原,在常规制片过程中脂质和糖原溶解,使细胞质变得透明,细胞膜清楚。许多原发性CCRCC中含有少量嗜酸性细胞,这在高分化肿瘤和坏死及出血附近尤为常见。在保存及处理良好标本中,肿瘤细胞的细胞核呈圆形,大小一致,染色质细颗粒状,均匀分布,根据不同分级,可见大小不等的核仁,偶见细胞核大而无核仁或出现奇异核。见图2。

图2 CCRCC患者HE染色图片(A:×100,B: ×200,C:×100)
免疫组化染色结果:CK阳性率88.89%(8/9),Vimentin阳性率100.00%(10/10),CD10阳性率93.33%(14/15),CA9阳性率100.00%(8/8),Ki-67阳性率100.00%(15/15例),PAX-8阳性率100.00%(14/14),PAX-2阳性率75.00%(3/4),EMA阳性率100.00%(5/5),CK7阳性率0.00%(8/8),RCC阳性率30.00%(3/10例),TFE-3阳性率40.000%(2/5)。见图3。

图3 CCRCC患者HE染色和免疫组化S-P染色图片
2 讨论
肾细胞癌是来源于肾实质泌尿小管上皮系统的恶性肿瘤[1]。相关文献[2]表明,肾细胞癌发病相关因素有吸烟、肿瘤家族史等。本研究纳入的16例原发性CCRCC肺部转移患者中有3例男性患者有吸烟史,但均无肿瘤家族史。
我国肾细胞癌发病率自35岁后开始上升,30岁以后男性发病率高于女性[3]。本研究纳入的16例原发性CCRCC肺部转移患者年龄范围为35~72岁,男女比例为31。
肾细胞癌早期常无明显的临床症状,大多是健康体检时发现的。国外文献[4]报道,肾细胞癌的肺部表现包括转移性疾病,包括支气管内、胸膜、实质或淋巴结转移,胸腔积液或血胸,肺栓塞和肿瘤栓塞是肾细胞癌的另一常见表现。我们发现15例患者是以肺部症状为首发表现,如呼吸困难、喘息、咳嗽、咯血、胸痛等,1例首发症状为腹部不适。这提示原发性CCRCC肺部转移以肺部首发症状较常见。本研究纳入的原发性CCRCC肺部转移与文献报道的肾细胞癌肺部临床表现略有不同。
肾细胞癌转移较早,部分患者在确诊就已发现转移。最常见的转移部位是肺部[5]。部分肾细胞癌在根治术后仍会发生远处转移。本研究纳入的16例原发性CCRCC肺部转移患者中9例发生在肾细胞癌根治术后,5例同时发现肾脏占位,2例以肺部结节首发。
本研究纳入的16例患者中13例CT显示双肺多发小结节,3例显示单侧小结节。肺部转移大多表现为双侧多发的肺部小结节,也可表现为单侧肺部结节。原发性肺癌的典型CT特征是短毛刺、分叶、胸膜凹陷等[6]。而原发性CCRCC肺部转移的CT多见边界清楚。
病理诊断对确定疾病的病因、发病机制、病理变化、治疗结局和转归都具有重要的临床意义[7]。在病理诊断中,除了观察细胞的形态变化,免疫组化技术也是病理科医师常用的诊断技术之一。本研究免疫组化染色结果如下:CK阳性率88.89%(8/9),Vimentin阳性率100.00%(10/10),CD10阳性率93.33%(14/15),CA9阳性率100.00%(8/8),Ki-67阳性率100.00%(15/15例),PAX-8阳性率100.00%(14/14),PAX-2阳性率75.00%(3/4),EMA阳性率100.00%(5/5),CK7阳性率0.00%(8/8),RCC阳性率30.00%(3/10例),TFE-3阳性率40.00%(2/5)。与国外有关文献[8]结果相似。
A: CK阳性(×100),B: Vimentin阳性(×100),C: CD10阳性(×200),D: CA9阳性(×100),E: Ki-67阳性(×100),F: PAX-8阳性(×100),G: PAX-2阳性(×100),H: EMA阳性(×100),I: CK7阴性(×100),G: RCC阴性(×100),K: TFE-3阴性(×100)
肺部原发性肿瘤中,具有透明细胞形态学表型:1)肺鳞癌透明细胞亚型主要是由细胞质透亮的细胞构成,但肺鳞癌透明细胞亚型免疫组化结果为P63阳性、P40阳性、PAX-8阴性、RCC阴性[9];2)具有透明细胞形态的肺腺癌免疫组化染色结果:TTF-1、PAX-8阴性、CK7部分阳性、RCC阴性[10]。原发性CCRCC肺部转移的病理形态学特征、免疫表型与肾细胞癌一致:PAX8、RCC均阳性,而P63、P40、TTF-1、CK7均阴性[11];3)肺透明细胞肿瘤是肺部原发的一种较罕见的良性肿瘤,容易与肺部具有透明细胞特征的原发性癌或转移癌相混淆[12]。肺透明细胞肿瘤是可能起源于血管周上皮样细胞的良性肿瘤,由含有大量糖原、有丰富的透明或嗜酸性细胞质的细胞组成。透明细胞肿瘤一般无临床症状,多被偶然发现。肿瘤直径通常约2 cm。界限清楚,呈孤立性,切面红褐色。透明细胞肿瘤由界限清楚、有丰富的透明或嗜酸性细胞质的圆形或卵圆形细胞组成。细胞核大小轻度不等,核仁可能明显,但核分裂相通常缺乏,坏死极少出现。薄壁窦样血管是特征性的。由于细胞质糖原丰富,通常有强的淀粉敏感的PAS阳性反应。肺透明细胞肿瘤特异性表达HMB-45,电镜检查显示大量游离的和有被膜包裹的糖原颗粒。肺透明细胞肿瘤与原发性CCRCC肺部转移的鉴别依据是:肺透明细胞肿瘤缺乏细胞的不典型性,肿瘤内呈现薄壁血窦样血管,S-100、HMB45阳性,CK阴性,TTF-1、CK7阳性[13]。原发性CCRCC肺部转移细胞质内可能含有糖原,但显示细胞的不典型性或伴有肿瘤性坏死和上皮标记阳性。本研究纳入的16例原发性CCRCC肺部转移中有2例患者S-100阴性。
原发性CCRCC高级别肿瘤中肿瘤细胞形态多样,有些细胞类似在上皮样血管平滑肌脂肪瘤中所见的巨细胞,但CCRCC高级别肿瘤可以在肉瘤样区域见到的梭形细胞。CCRCC通常CK、CAM5.2和EMA阳性,CA-9也常呈弥漫膜阳性。CD10细胞膜呈阳性,CK7一般呈阴性。而这些指标在血管平滑肌脂肪瘤呈阴性,血管平滑肌脂肪瘤HMB-45和SMA呈阳性。因此,免疫组化表型可以作为原发性CCRCC肺部转移和肺部原发性透明细胞癌鉴别诊断的确诊指标。
总之,原发性CCRCC术后极少发生肺部转移,原发性CCRCC肺部转移以肺部症状首发较常见,大多表现为双侧多发的肺部小结节,也可表现为单侧肺部结节。另外,原发性CCRCC的首选治疗方案是手术切除原发部位和转移部位病灶。目前发生转移的肾细胞癌治疗的亮点是肿瘤免疫治疗[14],同时靶向药物的治疗也有了进展[15]。随着新药物的引入和个性化的治疗,肾细胞癌转移性疾病的治疗效果会有更大的进展。
