基于学生主动建构的微粒观进阶研究
2021-01-22张灵丽
张灵丽








摘要: 立足微粒的认识进阶,以水和水溶液为素材,从物质的构成微粒、物质的溶解和结晶以及化学反应的本质三个阶段进行研究。借助实验、模型、类比、想象、视频、数字化实验等手段,探究宏观表象背后的微观实质,引导学生主动建构微粒观,发展学生的化学思维能力和学科素养。
关键词: 初中化学; 微粒观; 认识进阶; 水和水溶液
文章编号: 1005-6629(2021)10-0042-06
中图分类号: G633.8
文献标识码: B
课程标准强调,义务教育阶段的化学教育“要引导学生认识物质世界的变化规律,形成化学的基本观念”[1]。初中生学习化学时,普遍感到构成物质的奥秘、溶解现象、酸碱盐等概念比较难。学生学习化学困难的根源是什么?要克服学生学习化学的困难,需要让学生明白化学的核心问题只是几个简单的基本观念;大千世界看起来很复杂,但如果我们透过纷繁复杂的表面现象就会发现其核心问题,其实很简单,科学就是要讨论世界的核心问题。因此,如何在初中阶段建构物质的微粒观念,值得化学教师积极探索和实践。
1 初中阶段微粒观的学习要求和主要内容
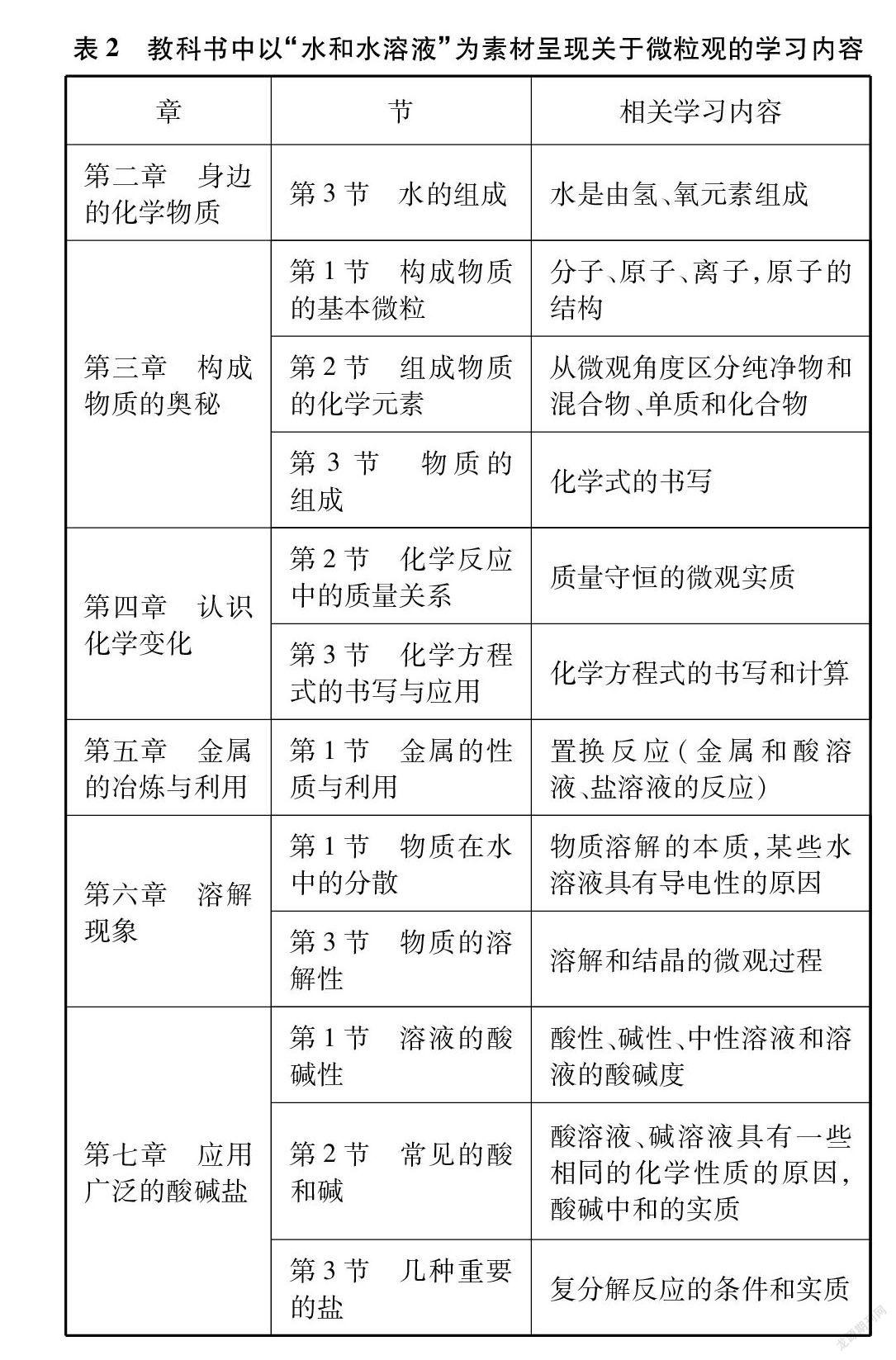
化学是在原子、分子水平上研究物质的组成、结构、性质、转化及其应用的一门基础学科,其特征是从微观层次认识物质,以符号形式描述物质,在不同层面创造物质。《义务教育化学课程标准》指出,化学学科应通过具体化学知识和概念的学习,促进学生形成化学学科思想和基本观念,逐步使学生从单一的定性与定量、宏观与微观的物质认识过程,过渡到定性与定量相结合、宏观与微观相结合的物质认识过程。从宏观到微观、从定性到定量,体现了化学学科的发展趋势。对物质组成的微观研究和定量研究使化学逐步成为能在实验和理论两个方面同时发展的一门自然科学[2]。课程内容在有关的一、二级主题中对微粒观的构建有明确的要求,具体见表1。水是生命存在和发展的必要条件,许多化学反应都是在溶液中进行的。“水和水溶液”是初中化学学习的重要主题。沪教版教科书《化学(九年级上、下册)》的有关章节中,以“水和水溶液”为素材,呈现了关于微粒观的学习内容,具体如表2所示。
从表2可以看出,教材中从第二章探究水的组成引入微粒观的教学;第三章以构成物质的奥秘进入原子、分子、离子的微观世界;第四章学习质量守恒定律的内容和微观实质;第五章学习金属和酸溶液、盐溶液的置换反应;第六章学习物质在水中的分散、溶解和结晶;第七章学习复分解反应的发生条件等,从宏观现象出发探寻微观本质,层层递进。
2 初中阶段微粒观学习的“进阶模型”
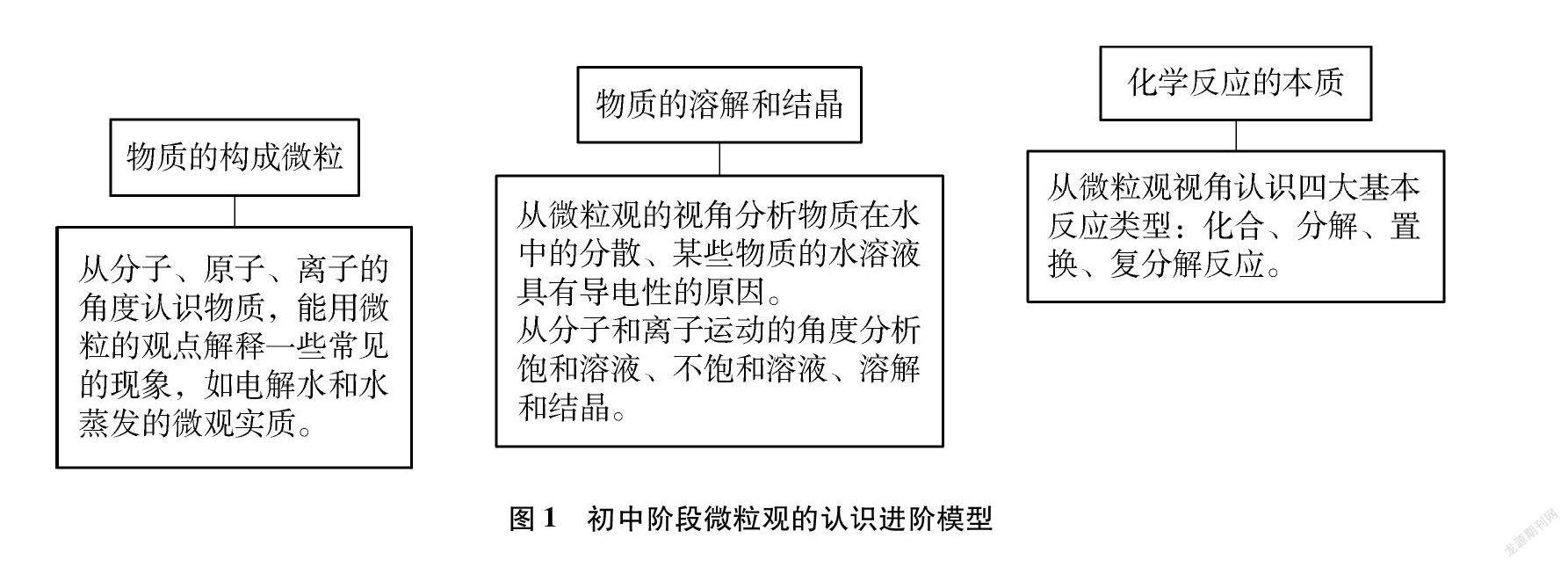
微粒观是人们对物质微粒性的基本看法,表现为在原子、分子、离子的水平上认识常见物质的组成、结构、性质、用途和变化现象的思维方式。微粒观的内容主要有: 物质是由微粒构成的;微粒的结构决定了微粒的性质,微粒间的相互作用方式决定了宏观物质的性质;微粒的结构影响着微粒之间相互转化的过程和方式。微粒观是义务教育阶段要求学生建构的核心观念,因此,教学要从学生已有的知识经验开始,先建构起微粒观和对微粒产生一定的认识,然后应用这些观念(观点)去分析和解决问题,使学生逐步增强抽象思维,形成微观思维,以及在微粒认识的基础上研究物质。笔者把初中微粒观学习的进阶模型分为三个阶段。第一阶段: 物质的构成微粒。先引导学生从分子、原子、离子的角度认识物质,物质是由微粒构成的,微粒在不断地运动,微粒之间有空隙,学生能用微粒的观点来解释一些常见的生活与自然现象;第二阶段: 物质的溶解和结晶。引导学生从微粒观的视角解析饱和溶液、不饱和溶液、溶解和结晶,让学生明晰微粒的结构决定微粒的性质,微粒间相互作用的方式决定了宏观物质的性质;第三阶段: 化学反应的本质。引导学生从微粒观的角度认识四大基本反应类型,让学生感悟化学反应的实质是原子、分子或离子等层次微粒的相互作用。微粒观学习的进阶模型源于教材又高于教材,它体现了在不同教学阶段的螺旋上升态势。这种思维模型的建构,有助于学生更清楚地认识物质的构成,理解化学变化的本质,对反应现象做出本质的判断和推理,形成认识一类问题的思路。初中生对微粒观的认识进阶模型如图1所示。
2.1 第一阶段: 物质的构成微粒
学生生活中认识的世界是一个能用感官感知的世界,自然形成了一种宏观思维方式。微观世界是抽象的。对微观世界的认识,需要学生的想象力,需要生动、形象、直观的载体。本章教学应关注学生的兴趣和认知特点,有策略地帮助学生搭建从宏观到微观的桥梁。恰当地利用实验、类比、图像、模型、视频动画等多种资源,使微观世界形象化,引导学生认识微观粒子與宏观物质的联系,初步建立化学微粒观[3]。结合学生熟悉的现象和已有的经验,创设直观的情境,从身边的现象(闻到花香、湿衣服晾干、物质的三态变化)、探究实验(氨分子扩散、酒精和水混合、压缩空气和水)、科学数据(1个水分子的质量是3×10-26kg、 1滴水约有1.67×1027个水分子)、科学技术成就(卢瑟福α粒子散射实验、扫描隧道显微镜获得苯分子图像、汤姆生发现电子、原子核爆炸)等,让学生认识到物质确实是由肉眼看不到的微粒构成,初步建立原子和分子的概念。然后通过具体的实例,引导学生认识物质的性质和变化与其构成微粒的联系。比如,通过水蒸发和电解水这两个变化过程类型、相关物质化学性质的改变情况,以及构成物质的分子进行分析,引导学生把物质性质的改变归因于分子的改变,从而建立分子的概念,形成“物质的性质主要由物质的结构决定”的观念。借助动画,模拟电解水的微观过程,让学生用水分子、氢原子、氧原子球棍模型来组建电解水和水蒸发的微观过程。如表3所示,让学生在微观上体验化学变化中分子变,物理变化中分子不变。由金属钠在氯气中燃烧生成氯化钠的演示实验,动画呈现钠与氯气反应的微观过程,展示氯化钠固体和氯化钠的结构模型,从核外电子排布特点,引导学生画出原子结构示意图,引入离子概念和氯化钠形成的微观实质,初步认识化学变化的本质。
通过本章的学习,学生从五彩缤纷的宏观世界步入充满神奇色彩的微观世界,激发了学生学习化学的兴趣。学生能够理解并建立物质构成的微粒观,能运用物质构成的知识解释一些简单的化学现象,初步理解化学现象的本质,通过对问题的探究和实践活动,提高了学生的想象力和抽象思维能力[4]。同时,通过探索原子结构的化学史(德谟克利特的原子论、道尔顿的原子理论、汤姆生发现电子、卢瑟福的行星模型),让学生了解科学家严谨求实的科学态度,培养学生坚毅求实的科学精神。
2.2 第二阶段: 物质的溶解和结晶
2.2.1 物质的分散
从日常生活以及前面章节的学习中,学生已了解一些物质在水中的分散现象,如虽知道物质溶于水逐渐消失,却不知道消失的根本原因;虽知道湿的手碰到电源容易触电,但却不知道其中的原因。本章的教学设计是从熟悉中感受新奇,新奇中探究其背后的微观实质,这种发现的过程和新奇的体验对于学生的发展是非常有意义的。教学难点是让学生知道某些物质在溶液中是如何以微观形式存在的。教学中,以氯化钠溶于水、固体消失的学生实验引入,动画或图片演示食盐的溶解过程(见图2),帮助学生理解物质溶解的实质。
演示某些物质水溶液的导电性实验,让学生知道某些水溶液具有导电性的微观原因是: 物质溶于水后产生了自由移动的离子,如表4所示。
通过物质在水中分散的微观实质的探讨,进一步加强了宏观和微观的结合,巩固提升学生的微粒观的概念,学生能从微粒观的视角分析溶液中的一些现象。
2.2.2 溶解和结晶
溶解和结晶教学的难点是如何从微观角度理解溶解和结晶的概念和过程。教学中,以学生分组实验引入,在一定温度条件下,以一定量的蔗糖放入一定量的水中,固体一开始消失,后来固体不再消失,引入饱和溶液和不饱和溶液的概念,通过动画和图片展示蔗糖溶解和结晶的动态过程。蔗糖在水中溶解和结晶的微观过程如图3所示[5]。
为强化物质溶解和结晶的微观过程,安排四组学生实验(见表5),让学生在实验中体会溶解与结晶的微观过程: 当把固体物质放入水中时,溶质表面的微粒(分子或离子)由于本身的振动和水分子对它的作用,离开固体的表面,均匀地扩散到水中,这是溶解过程。在溶解的同时,进入水中的分子或离子,由于不断地做无规则的运动,当一部分分子或离子撞击未溶解的固体表面时,又被吸引重新回到固体表面上,这是结晶过程。溶解和结晶是一个可逆的过程,是一种动态平衡状态[6]。当外部条件改变时,溶解速率和结晶速率便会发生改变,旧的溶解-结晶平衡被破坏,再形成新的溶解-结晶平衡。
硫酸铜晶体形状改变,质量不变溶解和结晶是一个动态平衡过程硫酸铜的溶解和结晶在同时进行
通过对溶解和结晶这一宏观现象背后的微观实质的探究,让学生学会从微观本质上分析宏观现象,主动建构微粒观的概念。
2.3 第三阶段: 化学反应的本质
初中生学习化学的难点往往在于不能透过宏观表象联系微观实质,因此教学中要训练学生养成从现象看本质的思维习惯,让学生不仅要知道为什么学化学以及化学的特征,更要追问化学的本源、化学反应的本质是什么。化学反应的本质是分子、原子或离子微粒间的相互作用、相互转化的过程,引导学生从微粒观的视角来认识四大基本反应类型(如表6所示)。
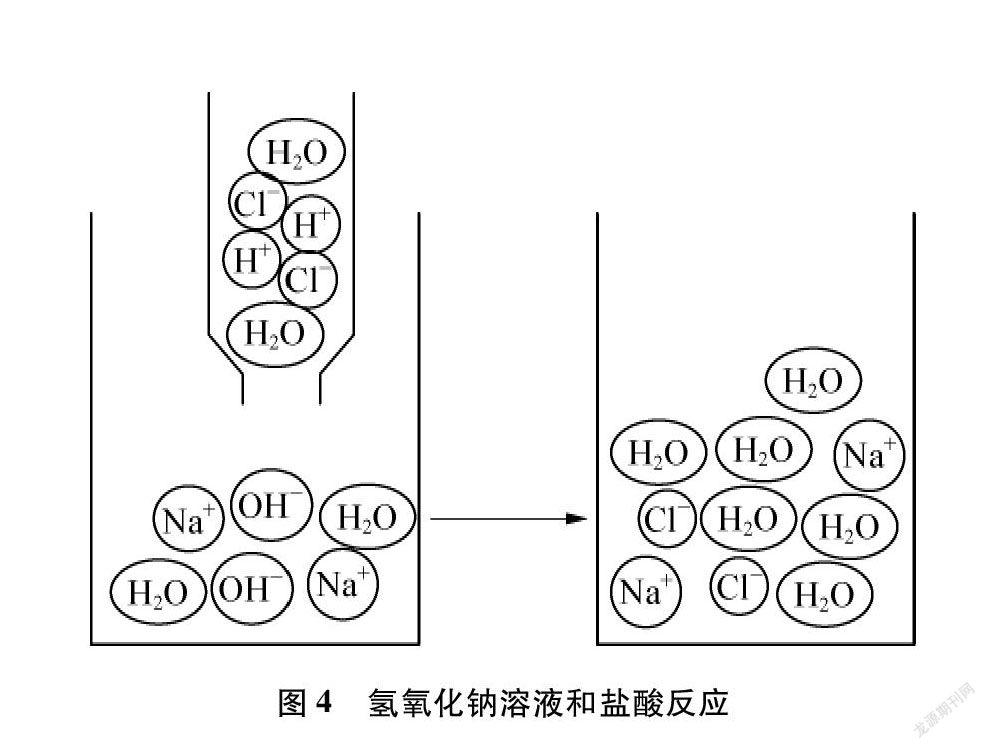
四大基本反应类型中,复分解反应的判断是难点。在学习复分解反应时,若只从宏观角度讲解复分解反应发生的条件,学生可能会死记硬背,不能理解复分解反应为什么要满足这些条件。如果从微粒观来分析和帮助学生理解化学反应的本质,就可以达到化繁为简的效果。以氢氧化钠和盐酸反应为例,向滴有酚酞的氢氧化钠溶液中逐滴加盐酸到红色突然消失,证实该反应的发生,让学生写出化学方程式,从宏观角度分析得出反应物是盐酸和氢氧化钠溶液、生成物是氯化钠和水;然后引导学生回忆酸碱盐的溶液具有导电性的原因是溶液中有自由移动的离子,从微观角度分析得出反应前后溶液中微粒的变化: 反应前的微粒是H+、OH-、 Cl-、 Na+,反应后的微粒是Cl-、 Na+、 H2O,通过对比前后溶液中的微粒,引导学生找到变化的微粒是H+、 OH-;再引导学生找出生成的微粒是H2O,从而得出: H+和OH-结合生成了H2O。为了帮助学生更直观地看到微粒前后的变化,可以借助微粒动画和微观粒子示意图,如图4所示。
学生通过实验、动画、微粒示意图得知,氢氧化钠和盐酸反应的实质是氢离子和氢氧根离子结合生成了水;再引导学生分析讨论,碳酸钠和稀硫酸反应的实质是H+和CO2-3反应生成了H2O和CO2、稀硫酸和氯化钡反应的实质是Ba2+和SO2-4反應生成BaSO4沉淀。通过微粒观的分析,帮助学生理解复分解反应的条件是生成物中有水或气体或沉淀产生。再进一步尝试着让学生从微粒观的视角找寻规律: 为什么有水或气体或沉淀产生,复分解反应就可以发生,其根本原因是什么?并总结出规律: 复分解反应的实质是离子的结合,它总是朝向自由移动的离子浓度减少的方向进行。另外,在学习复分解反应时,加强“宏-微-符”的三重表征思维,让学生熟练书写离子符号,只要看到酸碱盐的名称,学生就能写出相关的离子符号,并能联想到哪些离子易结合成沉淀、气体和水。学生从离子结合的特点上理解复分解反应,对一些题型就可以迎刃而解了。
3 微粒观的教学建议
3.1 创设真实情境
要充分认识到学生的认知水平,创设贴近学生的教学情境,情境的价值在于“学和思”。基于真实情境的学习,选取生活中熟悉又具有启发意义的事例,设计驱动性的问题,引导学生进一步思考、领悟和表达。比如: 从微观本质上解释: (1) 为什么温度计中的液柱随温度的改变上升或下降?(2) 为什么厨房里的白醋和纯碱混合会产生大量的气泡?(3) 为什么蚊虫叮咬后,涂肥皂水可以减轻痛痒?学生在这类活动体验和在解决问题中以及在师生平等交流对话中,主动地、自主地建构物质的微粒观。
3.2 注重实验验证
运用微粒观研究物质,要注重对学生强化微粒观有效性的体验,让学生获得并相信微粒观认识物质的科学性,最有效的手段就是实验验证。比如为了证明中和反应有水生成,做下列演示实验: 变色硅胶吸水后,从蓝色变为红色。把变色硅胶与氢氧化钠固体混合,无明显现象,变色硅胶和无水醋酸充分混合,亦无明显现象。将2mL无水醋酸迅速倒入装有3片NaOH固体和变色硅胶混合的试管中,变色硅胶由蓝色变为红色。学生通过观察变色硅胶颜色的变化相信: 中和反应生成了水。这类结合化学实验的教学,能让学生的理论分析和实践认识有机结合起来,进一步深化他们的微粒观的思维能力。
3.3 加强符号表征
化学符号是微观世界的缩影,它从微观上科学、简洁地反映宏观物质的性质和变化规律,成为联系宏观事实和微观世界的桥梁。教学中,要引导学生正确地认识元素符号、化学式、化学方程式等各种化学符号的宏观和微观含义,帮助学生借助化学符号“进入”物质及其变化的微观世界。
3.4 善用科技手段
初中生的微观知识在逐步进阶形成中,教学中要注重发挥学生的想象力,善于运用实物模型、动画模型、图示模型、数字传感器等形象直观的科学技术手段,帮助学生主动地建构物质的微粒观。比如,用电导率传感器测量氯化钠固体溶于水的电导率曲线的变化,让学生感知酸、碱、盐溶液具有导电性的微观实质。向0.025mol/L氢氧化钡溶液中逐滴滴加0.025mol/L稀硫酸溶液,根据电导率变化,可直观验证复分解反应的微观实质,如图5所示。
3.5 注意循序渐进
初中生微粒观的建构过程是一个循序渐进的过程。教学中要善于运用学生已有的经验知识,对教学内容做出整体规划,科学设计教学目标和教学内容,注意新旧知识的连贯性和渐进性,不强求一步到位。比如,从认识元素符号的练习开始,准确书写化学式,在熟练书写化学方程式的基础上,再从离子视角认识复分解反应,难度逐步提升,防止学生畏惧化学,失去对化学的学习兴趣。
立足学生主动建构微粒观的化学教学是以“观念建构”来促进“知識建构”。初中生微粒观模型的建构是一个不断深化、有机联系和螺旋式上升的过程,随着对微粒观不断地丰富和发展,把微粒观用作教学的方法,使学生避开纷繁复杂的表象,从本质上清晰地认识各种物质的区别和联系,以及各种化学规律,从而建构更加科学、深刻的化学知识系统。更为重要的是,让学生了解从微观的视角去研究化学知识的学习方法,对学科知识的理解更加本质化,自身的观念更加清晰化。微粒观模型的建构,有利于学生形成认识物质的思路: 深入到物质内部去看物质的本质,然后再跳出来看它的一些外观特征、变化的规律[7]。同时也为高中的学习打下良好基础,有利于学生的可持续发展和提升化学学科素养。
参考文献:
[1][2]中华人民共和国教育部制定. 义务教育化学课程标准(2011年版)[S]. 北京: 北京师范大学出版社, 2012.
[3][4][6]王祖浩. 化学教师教学指导书[M]. 上海: 上海教育出版社, 2012.
[5]人民教育出版社化学室. 全日制普通高级中学教科书(试验修订本·必修加选修化学)(第二册)[M]. 北京: 人民教育出版社, 2000: 37.
[7]钱海如, 赵华. 初中生化学微粒观建构的实践反思——以“离子”教学为例[J]. 化学教学, 2017, (5): 36.
