基于网络药理学的夏枯草治疗Graves病机制探讨
2021-01-22张丽丽赖倚文陈雪莹高天舒
张丽丽,赖倚文,陈雪莹,高天舒*
(1.辽宁中医药大学,辽宁 沈阳 110847;2.辽宁中医药大学附属医院,辽宁 沈阳 110032)
Graves病(Graves’disease,GD)是通过促甲状腺激素受体抗体(Thyroid stimulating hormone receptor antibody,TRAb)介导的自身免疫性甲状腺疾病,表现为甲状腺毒症的临床症状及体征,如弥漫性甲状腺肿大、特征性眼部表现及皮肤改变,严重时还引发甲亢甚至危及生命。目前,口服抗甲状腺药物存在毒副作用、复发率高等缺点,根治性治疗,如手术、I131则有引发手术并发症和永久性甲减的概率。中医以“瘿气”“气瘿”为病名对本病进行治疗已有两千余年的历史。查阅古籍发现,治疗此病除含碘中药外,夏枯草是应用较为普遍的中药之一,目前仍广泛应用于临床。网络药理学是以“疾病-基因-靶点-药物”多层次、多角度的相互作用网络为理念,运用专业的可视化网络分析软件及算法,对现有的数据库信息进行筛选和网络预测,进而综合观察药物对疾病网络的干预和影响[1]。本课题通过网络药理学方法筛选、判断夏枯草主要活性成分对GD的影响,探讨夏枯草治疗GD的机制,以期为进一步探究其治疗及作用机制提供理论支持和思路方向。
1 方法
1.1 夏枯草活性成分筛选及夏枯草调控的疾病靶标获取
在中药系统药理学数据库和分析平台(TCMSP,https://tcmspw.com/)中查询夏枯草成分。由于化合物的口服吸收程度由口服生物利用度(Oral bioavailability,OB)反映,类药性(Drug-like,DL)为化合物与已知药物的相似性,故筛选口服生物利用度(OB)≥30%,类药性(DL)≥0.18的化合物作为活性成分[2],并参考《中国药典》规定进行补充。应用TCMSP数据库查询筛选出的夏枯草活性成分对应的人源靶标,通过Uniprot(https://www.uniprot.org/)、DrugBank(https://www.drugbank.ca/)数据库进行靶标蛋白对应基因简称查询,并去除非人源的靶标,从而获得夏枯草调控GD的靶标。
1.2 Graves病人源基因靶标获取
利用GeneCards网站(https://www.genecards.org/)查询Graves病的相关基因,获得Graves病基因简称。
1.3 夏枯草活性成分-靶标网络构建
将夏枯草活性成分所对应的靶标基因与Graves病对应的靶标基因取交集,获得夏枯草活性成分治疗Graves病的靶标基因,应用Cytoscape7.1软件构建夏枯草活性成分-靶标网络。
1.4 构建夏枯草治疗Graves病蛋白互作网络
蛋白互作(Protein-protein interaction,PPI)是机体细胞功能的基础,在调节机体生理、病理活动方面发挥重要作用。蛋白互作网络是由蛋白的互作信息构建而成的网络。将交集得到的基因应用STRING(https://string-db.org/)数据库构建蛋白相互作用网络,选择物种为“Homo sapiens”进行操作,相互作用阈值设为“Highest confidence=0.9”,构建夏枯草治疗Graves病蛋白互作网络。利用Cytoscape7.1中的CytoNCA插件对上述网络进行拓扑参数分析,因度值(Degree)、最短路径(Closeness)、介数(Betweenness)这三个中心性参数在中药网络药理学研究中最重要且常用[3],而度值体现某一节点与其他节点的连接个数,度值越大该节点的影响力就越大;节点通过的最短路径数越多、度值越大则该点在网络中越重要。故对这三者进行分析,筛选出夏枯草治疗Graves病的重要靶点蛋白。筛选标准为度值>中位数2倍,介数、最短路径>中位数。
1.5 KEGG富集分析
使用Cytoscape7.1软件的ClueGO插件对最终筛选出的靶点进行KEGG富集分析。将筛选出的夏枯草治疗 GD的重要靶点导进 ClueGo插件,设置物种为人,设定阈值P=0.05,evidience设定为 all,进行 KEGG富集分析。
2 结果
2.1 夏枯草活性组分及人源靶标的查询筛选
以OB≥30%,DL≥0.18为限定条件筛选得到11个活性成分,参考《中国药典》补充芦丁、迷迭香酸[4]、熊果酸[5]3个活性成分,见表1。基于夏枯草人源靶标的筛选方法,筛选出235个夏枯草调控的疾病靶标。

表1 夏枯草活性成分
2.2 Graves病人源基因靶标获取
利用GeneCards获取Graves病人源基因靶标1 461个。将夏枯草调控的疾病靶标与Graves病基因靶标取交集获得98个夏枯草治疗Graves病的基因靶标,见图1。
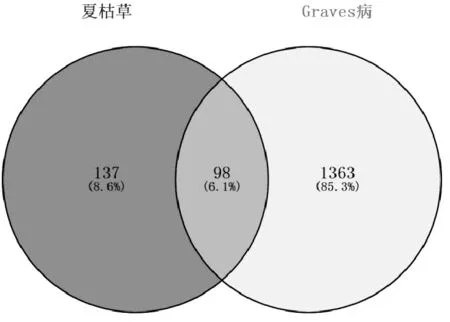
图1 夏枯草Graves病交集靶点
2.3 夏枯草活性成分-靶标网络构建
应用Cytoscape 7.1软件进行夏枯草活性成分-靶标网络构建,该网络包含112个节点,其中14个节点代表夏枯草活性组分,另外98个节点代表夏枯草调控的Graves病的靶点(以靶点基因简称表示),见图2。

注:椭圆形为夏枯草成分,长方形为夏枯草与Graves病交集靶点。
2.4 夏枯草治疗Graves病蛋白互作网络(PPI)
如图3所示,构建的 PPI网络中包含98个节点(有17个蛋白不符合筛选条件未显示)、325条相互作用连线。根据网络拓扑学参数分析,度值:7,最短路径:0.396 0,介数:54.884 4,按照筛选标准,共选出12个核心靶点(TNF、IL6、TP53、IL10、VEGFA、JUN、STAT3、CCL2、IL1β、IL4、CXCL8、EGFR),见表2。提示这些蛋白在夏枯草治疗Graves病药理机制中发挥关键作用。由此推测夏枯草的14种活性成分中beta-sitosterol(β-谷甾醇)、kaempferol(山奈酚)、luteolin(木樨草素)、quercetin(槲皮素)、rutin(芦丁)、ursolic acid(熊果酸)、rosmarinic acid(迷迭香酸)7种化合物为治疗GD的关键成分。

表2 夏枯草治疗GD的核心靶点
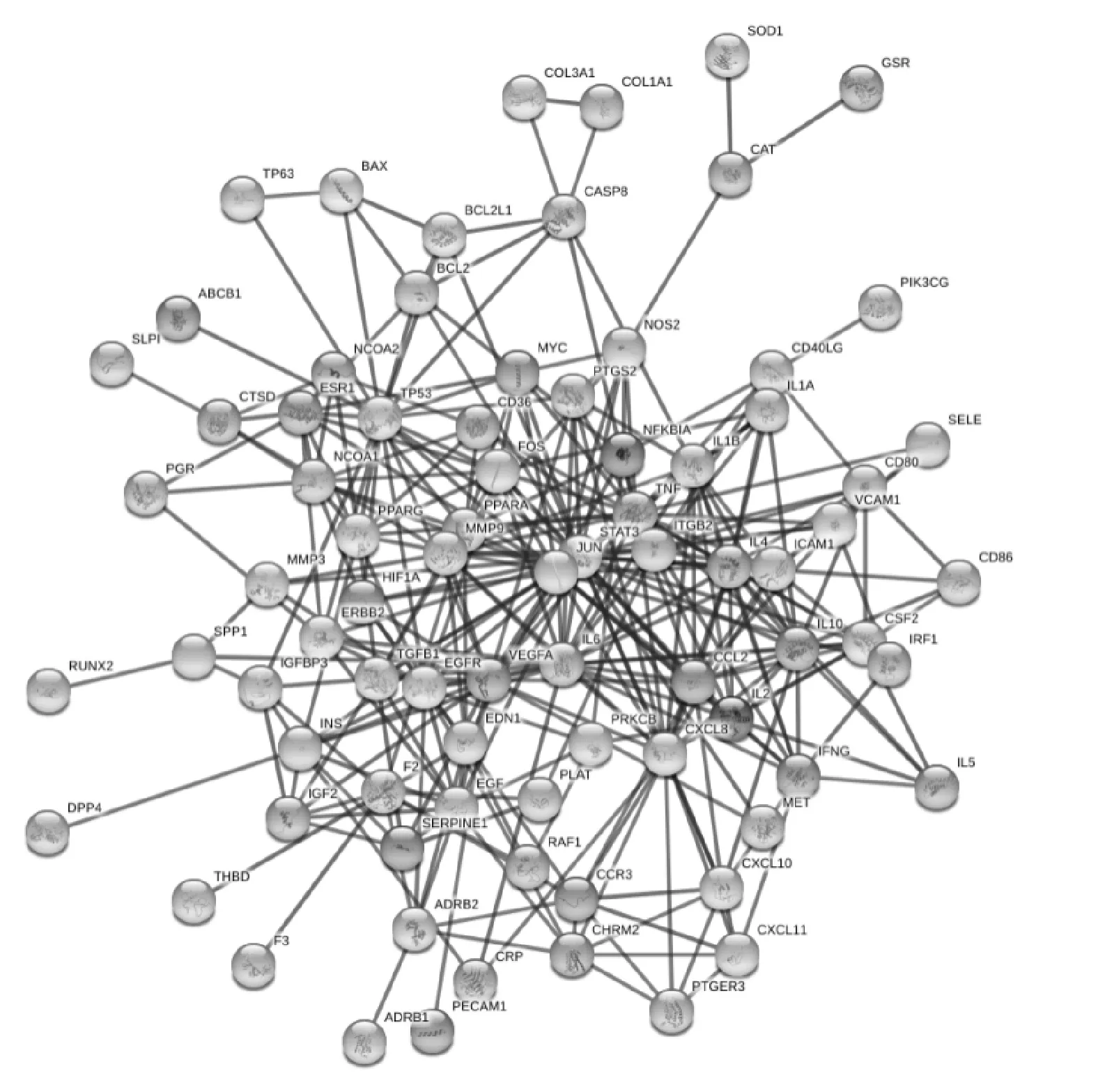
图3 夏枯草治疗Graves病PPI网络
2.5 KEGG富集分析结果
12个基因靶标应用ClueGO插件进行KEGG富集分析,得到IL-17 信号通路、Toll样受体信号通路、C型凝集素受体信号通路、TNF 信号通路、 AGE-RAGE 信号通路、低氧诱导因子信号通路6个信号通路,见表3。

表3 KEGG富集结果
3 讨论
GD以甲状腺功能亢进和甲状腺弥漫性肿大为特征表现,中医将其归属于“瘿气”“气瘿”之范畴。中医认为本病之本在于肝肾阴虚,气滞、火旺、痰凝、血瘀为本病之标,病变涉及肝、肾、心、脾等多脏,尤以肝脏为主。《杂病源流犀烛·颈项病源流》提到:“瘿之为病,其证隶属五脏,其原皆由肝火。”夏枯草为清肝泻火、消肿散结之常用药,其治疗瘿病由来已久。《神农本草经》载夏枯草可“散瘿结气”,《本草求真》云:“夏枯草……证知气虽寒而味则辛,凡结得辛散……是以一切热郁肝经等证,得此治无不效。”目前,在甲亢的中医药治疗中夏枯草仍是常用药,其不仅用于中药复方,夏枯草膏、夏枯草口服液、夏枯草胶囊、夏枯草颗粒等制剂也常被使用。夏枯草的应用使GD患者在改善症状、缩短病程、减少不良反应等方面受益[6-7]。
GD是受遗传、免疫、环境等多种因素影响的器官特异性自身免疫紊乱。GD的发病机制尚不完全明确,涉及遗传和环境因素、免疫紊乱、氧化应激[8]等,其中免疫因素是GD发生发展的核心因素。既往研究认为GD是由Th2介导的体液免疫[9)引发,进一步研究发现Th1、Th2细胞共同参与GD的发病[10],且Th1主要分泌IL-2、INF-γ、TNFα等细胞因子,在GD的早期起作用;Th2主要分泌IL4、IL-5、IL-6等细胞因子,在GD的晚期起主要作用。近年来研究发现,Thl7和 Treg细胞在GD的发病过程中也发挥着重要的调节作用,且Th17与GD的严重程度,GO的发生、发展有关[11-12]。Th17细胞的分化由IL-6与TNF-γ协同作用下诱导,起加强甲状腺组织局部免疫反应的作用。
本课题应用网络药理学方法,探索夏枯草治疗Graves病的机制。筛选出14个夏枯草活性成分,其中β-谷甾醇、山奈酚、木樨草素、槲皮素、芦丁、熊果酸、迷迭香酸7种化合物为夏枯草治疗GD的关键成分,得到98个夏枯草与Graves病共有靶点,其中TNF、IL6、TP53、IL10、VEGFA、JUN、STAT3、CCL2、IL1β、IL4、CXCL8、EGFR,这12个核心靶点在夏枯草治疗Graves病药理机制中发挥关键作用,通过对12个核心靶点的富集分析筛选出6条夏枯草治疗Graves病的信号通路(白介素17信号通路、肿瘤坏死因子信号通路、低氧诱导因子信号通路、Toll样受体信号通路等),说明夏枯草可能通过调节多个生物过程以及多个通路的协调发挥治疗GD的作用。
3.1 夏枯草可通过作用于VEGF靶点抑制GD患者的甲状腺肿大
GD又称毒性弥漫性甲状腺肿、甲状腺弥漫性肿。目前认为甲状腺肿大的机制与甲状腺细胞的增殖和内生血管的形成有关。本课题组前期研究证实,GD患者甲状腺体积与血清 VEGF水平呈正相关,且含有夏枯草成分的中药复方可降低血清 VEGF水平,减少甲状腺内新生血管的形成,进而缩小甲状腺体积[13]。VEGF具有促进内皮细胞的生长增殖及诱导血管形成的作用。VEGF家族包括VEGF-A、B、C、D和PIGF,其中VEGF-A与生理/病理情况下的血管生成、血管形成密切相关。有关研究[6,14]也证实,夏枯草制剂治疗Graves病可以缩小甲状腺肿。这与本课题得出的夏枯草治疗GD的核心靶点相符,故推测夏枯草可通过作用于VEGF来抑制GD患者的甲状腺肿大。此外,内皮生长因子(EGFR)是一种细胞膜受体,具有酪氨酸蛋白激酶活性,能够促进上皮细胞的增长,有研究[15-16]表明,EGFR在Graves病甲状腺组织中的表达高于正常组织,由此推测EGFR也可能为夏枯草治疗GD甲状腺肿大的靶点。
3.2 夏枯草治疗GD的主要调节机制预测
Th17在多种自身免疫疾病中均发挥重要作用,其在GD中的作用也逐渐受到重视。本课题发现IL-17信号通路显著富集。IL-17家族通过其相应的受体发出信号激活包括NF-κB、MAPK和C/EBP在内的下游途径,以诱导抗菌肽、细胞因子和趋化因子的表达。夏枯草能降低自身免疫性甲状腺炎(AIT)患者的Th17细胞水平,还可降低AIT模型大鼠的IFN-γ、TL-4、IL-17等细胞因子水平[17-18]。此外,Toll样受体信号通路(TLRs)也参与GD发病[19],Toll样受体与其配体结合,激活TLRs启动下游信号,激活细胞内 MAPK信号通路和 NF-κB信号通路,调节肿瘤坏死因子、白细胞介素、干扰素等细胞因子的产生。富集结果表明TNF信号通路也被显著富集,通过KEGG数据库查询,TNF信号通路也可激活NF-κB途径和MAPK途径,也有研究表明夏枯草颗粒可以降低GD患者TNF-α水平[20]。由于NF-κB是IL-17信号通路、Toll样受体信号通路、TNF信号通路的下游途径,已有文献研究证实甲亢患者的NF-κB通路处于激活状态[21-22],且夏枯草口服液可抑制NF-κB信号传导通路,减轻甲状腺炎症[23]。故推测夏枯草或可通过IL-17信号通路、Toll样受体信号通路、TNF信号通路治疗GD,但需进一步研究证实。
本课题运用网络药理学方法,对夏枯草治疗Graves 病的复杂分子网状关系进行了系统研究,推测夏枯草主要通过β-谷甾醇、山奈酚、木樨草素、槲皮素、芦丁、熊果酸、迷迭香酸这7种有效成分,作用于TNF、IL6、TP53、IL10、VEGFA、JUN、STAT3、CCL2、IL1β、IL4、CXCL8、EGFR这12个核心靶点,通过IL-17信号通路、Toll样信号通路等多个通路发挥治疗GD的作用。本课题为夏枯草治疗GD提供了理论支持,也为进一步研究夏枯草治疗GD的机制提供了方向和思路,但仍需进一步验证。
