来曲唑联合卵泡期高孕激素促排卵对高龄患者IVF/ICSI妊娠结局的影响
2021-01-21于岚赵艳何巧花张翠莲
于岚,赵艳,何巧花,张翠莲
(河南省人民医院 郑州大学人民医院,郑州 450000)
自80年代中期控制性促排卵逐渐应用于IVF/ICSI-ET助孕治疗中,其中控制早发LH峰一直是控制性促排卵过程中的关键[1]。随着制药技术的发展,促性腺激素释放激素(GnRH)激动剂和拮抗剂已经成熟的应用于IVF/ICSI-ET并取得了良好的效果。在临床上高龄患者因卵巢储备功能降低需行多次取卵周期以获得最终的妊娠,这类患者需要更加方便、经济的促排卵方案[2]。近年来,卵泡期高孕激素促排卵方案(PPOS)在抑制早发LH峰方面获得了良好的效果,同时冻融胚胎移植(FET)成功率的逐步提高促进了PPOS的发展并获得了理想的临床效果[3]。PPOS为高龄患者提供了一种经济、灵活的促排卵方案。来曲唑(LE)是一种广泛应用于促排卵的药物,属于具有高度特异性的第3代芳香化酶抑制剂,可以特异性抑制雌激素合成过程中的芳香化酶活性,从而减少外周雄激素向雌激素的转化,并最终降低血浆中雌激素的水平,从而发挥负反馈作用以促进促性腺激素(Gn)的释放,增加卵巢对Gn的敏感性,这一作用在多囊卵巢综合征(PCOS)患者促排卵中已经得到肯定[4-5]。研究证明在促排卵前5 d加用2.5 mg/d的LE提高了低反应人群的获卵数及种植率[6]。本研究通过评估在PPOS促排患者早卵泡期添加LE后获卵数、可用胚胎数及周期累积分娩率等相关指标,探讨添加LE是否可以改善高龄患者的临床妊娠结局。
资料与方法
一、研究对象
收集了2016年6月至2018年9月在我院生殖中心进行IVF/ICSI时应用PPOS促排卵助孕治疗的患者的临床资料。
纳入标准:年龄≥35岁且≤42岁因女方输卵管因素在我生殖中心行助孕治疗的患者;排除标准:子宫畸形、宫腔粘连、复发性流产、子宫内膜异位症、夫妇一方染色体异常。
本研究共纳入318个周期,根据在PPOS过程中是否在早卵泡期添加LE分组:在早卵泡期添加LE者为A组(n=120)和在早卵泡期不添加LE者为B组(n=198)。
二、研究方法
1.控制性促排卵方案:在月经第3~5天开始每天口服醋酸甲羟孕酮(MPA,浙江仙琚制药)10 mg至诱发排卵日,同时应用人绝经期促性腺激素(HMG,珠海丽珠制药)150~225 U/d开始促排卵,根据卵泡发育情况,调整HMG用量;当优势卵泡直径≥18 mm时,给予HCG(珠海丽珠医药)10 000 U肌肉注射,34~36 h后经阴道取卵。添加LE的控制性促排卵方案,在开始促排卵用药日加用LE 2.5 mg/d[6],连用5 d后停用,余治疗同前。
2.取卵、受精及胚胎培养:在经阴道B超引导下,采用单腔/双腔取卵针,抽取所有直径≥10 mm卵泡。根据取卵日男方精液情况或既往的受精情况行IVF或者ICSI,胚胎培养按本中心常规进行。根据伊斯坦布尔共识[7]及Gardner评分[8]对胚胎进行分级并记录可利用胚胎数。
3.冻融胚胎移植(FET):按照本生殖中心常规,根据患者的具体情况采用自然周期、激素替代周期或降调节-激素替代周期等个体化方案进行内膜准备。待内膜≥8 mm后,采用口服地屈孕酮(雅培,荷兰)或雌二醇地屈孕酮片(苏威制药,荷兰),阴道塞入黄体酮阴道缓释凝胶(默克雪兰诺,德国)进行内膜的转化及后期黄体支持。移植胚胎数量≤2个。
4.妊娠结局判断标准:在胚胎移植后14 d查血HCG值,β-HCG≥50 U/L判断为HCG阳性;在移植后28 d和35 d分别行阴道B超检查,见宫内妊娠囊及原始心管搏动者确定为临床妊娠。妊娠足月后通过电话随访分娩情况。
5.观察指标:患者一般资料;诱发排卵日基础激素水平、Gn用量、Gn天数、获卵数;受精率、可利用胚胎数;临床妊娠率、累积妊娠率和累积分娩率等。受精率=正常受精数/成熟卵子数×100%;临床妊娠率=临床妊娠数/移植周期数×100%;累积妊娠率=临床妊娠数/取卵周期数×100%;累积分娩率=成功分娩周期数/取卵周期数×100%;周期取消率=无反应、未取到卵、无可利用胚胎取消的周期数/总促排卵周期数×100%;流产率=流产的周期数/临床妊娠周期数×100%。
三、统计学方法
结 果
一、两组患者的基本资料比较
两组患者间年龄、不孕年限、体重指数(BMI)、抗苗勒管激素(AMH)水平、基础激素水平、移植日子宫内膜厚度比较均无显著性差异(P>0.05)(表1)。
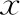
表1 两组患者的基本资料比较(-±s)
二、两组患者促排卵情况比较
A组患者Gn天数、诱发排卵日FSH水平及Gn总量均显著高于B组患者(P<0.05),但是诱发排卵日E2水平显著低于B组患者(P<0.05);两组患者间诱发排卵日孕酮(P)、LH水平比较均无显著差异(P>0.05)(表2)。
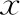
表2 两组患者促排卵情况比较(-±s)
三、两组患者促排卵及胚胎培养情况比较
两组患者间获卵数、成熟卵数、可利用胚胎数和周期取消率比较均无显著性差异(P>0.05);A组患者受精率显著低于B组患者(P<0.05)(表3)。
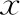
表3 两组患者促排卵及胚胎培养情况比较[(-±s),%]
四、两组患者FET周期妊娠结局比较
两组患者间FET周期内膜准备方案(自然周期、激素替代、降调节激素替代)比例无显著差异(P>0.05);两组患者间平均移植胚胎个数、HCG阳性率、临床妊娠率、累积妊娠率比较均无显著性差异(P>0.05);B组患者累积分娩率高于A组,但差异无统计学意义(P>0.05)(表4)。
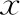
表4 两组患者妊娠结局比较[(-±s),%]
讨 论
上世纪80年代促排卵技术的应用极大地促进了辅助生殖技术的发展,其中控制早发LH峰是促排卵的关键。随着GnRH激动剂和拮抗剂的应用,很大程度上降低了由早发LH峰引起的周期取消率。近年来,由于玻璃化冷冻技术的不断发展,FET周期妊娠率及活产率均得到了显著的提高。国内匡延平团队基于黄体期促排时无早发LH峰出现这一现象,提出了PPOS方案[9-10]。研究表明,与拮抗剂方案相比,PPOS方案在获卵数、受精率、卵裂率及可利用胚胎数等方面均无显著差异,同时FET妊娠率以及新生儿出生缺陷方面与拮抗剂方案比较亦无显著差异[3,11]。
随着二胎政策的开放,高龄妇女成为辅助生殖技术中的关注人群,高龄妇女面临着卵巢功能低、可利用胚胎少、取卵周期长等不利因素[12]。有研究表明对于卵巢储备低的患者使用PPOS方案与拮抗剂方案有着相同的治疗结局,且PPOS方案简化了促排卵过程,与拮抗剂方案相比降低了治疗费用[13]。LE作为芳香化酶抑制剂在促排卵的方案中应用越来越广泛,其促排卵机制包括两个方面:一方面是雌激素合成的减少使下丘脑-垂体的负反馈抑制得以解除,从而内源性促性腺激素分泌增多,进而促进卵泡生长发育;另一方面LE在卵巢组织内阻断雄激素向雌激素的转化,引起卵泡发育微环境中雄激素暂时积聚,雄激素在卵巢局部刺激胰岛素样生长因子等自分泌和(或)旁分泌因子等的表达,从而改善卵泡发育微环境,发挥促卵泡生长的协同作用[14]。
本研究回顾性分析年龄大于35岁应用PPOS方案促排卵患者的318个周期的临床资料,以早卵泡期添加LE与否分为两组。两组患者在年龄、周期取消率、基础激素水平(FSH、LH、E2)、AMH水平比较均无显著性差异(P>0.05);与未添加LE组(B组)患者相比较,添加LE组(A组)患者的Gn总剂量和Gn天数显著增加,诱发排卵日E2水平显著降低(P<0.05)。LE半衰期为30~60 h,生物利用率高,对酶的抑制程度可达99%以上。LE可以显著降低雌激素水平,在促排周期中诱发排卵及取卵的时机是根据卵泡大小及雌激素水平而确定,因此在促排卵过程中加用LE可能会导致因雌激素增长不佳而造成的Gn用量和Gn天数的增加,但并不增加获卵数和可利用胚胎数。加用LE组的受精率显著降低,这种作用在拮抗剂方案添加LE时并未发现[15],是否与高孕激素及低雌激素环境相关尚不明确。研究表明促排卵早期添加LE可以显著提高胚胎种植率[6],但是本研究发现两组患者胚胎移植后的HCG阳性率和临床妊娠率比较均无显著性差异(P>0.05),这可能与胚胎移植方案相关。LE可以通过影响整合素的表达而改善子宫内膜容受性从而提高着床率[16],但是PPOS方案只能采用全胚冷冻后复融移植,因此失去了LE改善内膜而增加胚胎种植率的机会。累积分娩率作为一次促排卵的关键衡量指标,反映了单个促排周期的效率,其受年龄、BMI及获卵数的影响[17]。本研究显示,未添加LE组患者累积分娩率较添加LE组患者略高,但并无统计学意义(P>0.05),提示PPOS方案在早卵泡期加用LE并不能提高单个促排周期的效率。考虑到两组患者在年龄和BMI方面并无显著差异,认为LE虽然可能增加了卵泡对FSH的敏感性,但是受高龄患者卵巢储备低下的影响,在PPOS方案早卵泡期添加LE并不能提高累积分娩率。
综上所述,虽然有证据提示LE可以提高卵泡对FSH的敏感性,但是本研究数据分析提示,对于高龄的患者在使用PPOS方案时添加LE后增加了Gn天数及Gn用量,但是并不能显著提高获卵数及单个周期促排效率。这一结论还需要加大样本量来论证,同时添加LE后雌激素水平的降低及Gn用量的增加是否影响卵泡及胚胎的发育仍需要进一步研究。
