D-半乳糖诱导正常人口腔黏膜角质形成细胞衰老的研究*
2021-01-20张倩倩刘丽骏蒋伟文
张倩倩 刘丽骏 徐 盼 孙 陈 蒋伟文
正常人口腔黏膜角质形成细胞(normal human oral keratinocytes,NHOKs)是口腔黏膜上皮重要组成细胞,发挥防御、感觉等功能。衰老过程中,黏膜结构改变,功能受损,病变风险增加[1,2]。过量D-半乳糖(D-galactose,D-gal)能诱导细胞代谢发生改变,使活性氧(reactive oxygen species,ROS)产量增加,出现氧化应激,造成细胞损伤,发生衰老[3]。此时细胞周期停滞,细胞周期抑制蛋白p53,p21 表达升高,衰老相关半乳糖苷酶活性升高[4,5]。Sirt1 是sirtuin 蛋白家族一员,是具有NAD+依赖的去乙酰化酶活性蛋白,保护细胞免受氧化应激,衰老过程中表达下调,起到抗衰老作用[6,7]。D-gal 已被广泛用于构建多种器官组织衰老模型[8,9],但在NHOKs 中的作用罕见报道。本实验旨在研究D-gal 可否诱导NHOKs 衰老,探索其潜在作用机制为体外构建口腔黏膜衰老模型提供理论依据,对研究口腔粘膜黏膜老化、治疗口腔肿瘤疾病提供新的策略和思路。
1.材料与方法
1.1 主要材料 试剂主要试剂OKM 培养基(Sciencell)、DispaseⅡ中性蛋白酶(Roche)、鼠尾胶原、胰蛋白酶、青链霉素(Gibco)、磷酸盐缓冲液PBS(Hyclone)、细胞角蛋白抗体PCK、细胞波形蛋白抗体Vimentin(Gene tech)、CCK-8 试剂盒(新赛美)、D-半乳糖(北京索莱宝)、衰老相关β-半乳糖苷酶染色试剂盒、RIPA 裂解液、ROS 检测试剂盒(上海碧云天)、p53 抗体、p21 抗体、GAPDH 抗体、Actin 抗体(Cell Signaling)、sirt1抗体(SANTA CRUZ)。
1.2 细胞培养与鉴定 (1)NHOKs 原代培养从18~60 岁因拔除阻生齿的健康患者处,获得健康口腔黏膜组织。本研究通过上海交通大学医学院附属第九人民医院医学伦理委员会批准(批件号:沪九院伦审2018-63-T54 号)。患者入诊室后经专人评估基本情况,符合要求者,征得其允许后,由医生进行口腔黏膜组织取材。取材部位靠近阻生齿,大小约5mm×5mm,避免过多过大取材对患者造成不必要的伤害。样本取后立即保存于10%双抗PBS 溶液中运输至实验室,于无菌条件下去除组织下层多余的脂肪,用0.25%DispaseⅡ中性蛋白酶4℃过夜消化,分离上皮层,剪成约1mm3小块,用0.25%胰蛋白酶+0.02%EDTA 溶液于37℃、5%CO2细胞培养箱中充分震荡消化3min,离心,OKM 培养基重悬获得单细胞悬液,置于37℃、5%CO2饱和湿度细胞培养箱中,隔三天换一次液。当细胞密度达到70%~80%传代。本次研究使用P2 代细胞用于后续实验。
(2)NHOKs 细胞鉴定将P2 代NKOKs 以1×105个/ mL 的密度接种于放置细胞爬片的24 孔板中,细胞达到70%时,用4%多聚甲醛固定爬片15min,PBS 洗三次。0.1%Triton-X 通透细胞30min,PBS 洗三次。于不同孔中分别滴加一抗角蛋白抗体和波形蛋白抗体,室温孵育1h,PBS 洗三次。生物素标记二抗室温孵育半小时,PBS 洗三次。DAB 显色2min,苏木素复染2min,盐酸脱水,清水冲洗晾干,中性树胶封片。于光学显微镜下观察、摄取图像。
1.3 CCK-8 检测 细胞增殖活力将细胞悬液以5×104/ ml 密度种于96 孔板中,24h 后细胞贴壁,分别用0、10、20、40、80g/ L 的D-半乳糖处理细胞12h、24h、48h。0g/ L 作为对照组。每孔加入10ul CCK-8 溶液,37℃孵育4h,酶标仪检测450nm 处吸光值,计算增殖活力。
1.4 β-半乳糖苷酶染色 使用衰老相关β 半乳糖苷酶染色试剂盒进行衰老相关的β 半乳糖苷酶(senescence-associated-β-galactosidase,SA-βgal)染色,检测细胞衰老水平。在光学显微镜下摄取图像,取三个视野,每个视野300 个细胞,计算SA-β-gal 阳性细胞百分率。
1.5 ROS 含量检测 将细胞悬液以5×104/ ml密度种于24 孔板中,24h 后细胞贴壁。20g/ L D-半乳糖作用细胞。分别于12h、24h、48h 时向每孔加入250μL 稀释好的DCFH-DA,细胞培养箱孵育20min。用无血清培养液洗涤细胞3 次,充分去除未进入细胞的探针。检测488nm 激发波长,525nm 发射波长下的荧光值。
1.6 Western bolt 分析 细胞蛋白表达收集D-半乳糖处理过的NHOKs,RIPA 裂解液提取细胞总蛋白,BCA 蛋白定量检测样品浓度,用5×蛋白上样缓冲液将样品稀释至同一浓度,使用聚丙烯酰胺凝胶电泳分离蛋白,转模至0.2μm 的PVDF,封闭液室温封闭1h,目的蛋白一抗4℃孵育过夜,HRP 标记的二抗于室温孵育1h,使用ECL 显影液于凝胶成像分析仪中采集信号,分析目的蛋白灰度值。
1.7 统计分析 所有计量资料采用均数±标准差描述,应用Graphpad Prism 5.0 统计分析、作图,采用单因素和多因素方差分析比较组间差异,P<0.05 作为差异有统计学意义,*表示P<0.05,**表示P<0.01,***表示P<0.001。
2.结果
2.1 NHOKs 原代培养与细胞鉴定 细胞呈多边形,边界清楚,铺路石状,贴壁单层生长,肉眼见无混杂的成纤维细胞,符合NHOKs 形态学特征(图1A)。角蛋白免疫细胞化学染色呈阳性(图1B)。波形蛋白染色成阴性(图1C)。结果表明所培养的细胞特异性表达细胞角蛋白,但不表达波形蛋白,为角质形成细胞,并且无成纤维细胞混杂。
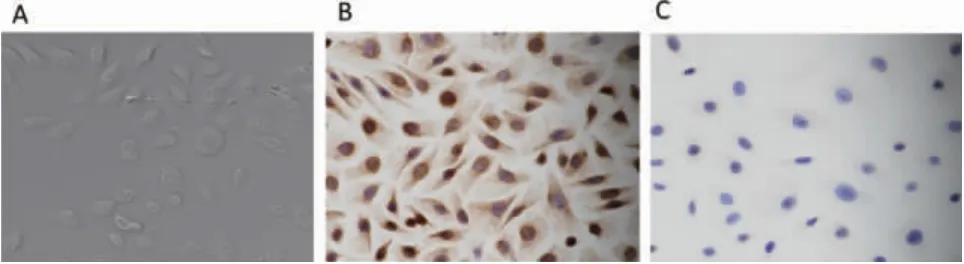
图1 NHOKs 细胞形态与细胞鉴定
2.2 D-半乳糖抑制细胞增殖活力 在NHOKs中加入0、10、20、40、80g/ L 的D-半乳糖,处理12h、24h、48h,结果显示,D-半乳糖浓度越高,处理时间越长,细胞增殖活力越低(图2)。与对照组相比,20g/ L、40g/ L 处理48h 具有统计学差异(P<0.001)。80g/ L 处理12h、24h、48h,与对照组相比差异有统计学意义(P<0.001)。D-半乳糖抑制细胞增殖活力,具有浓度依赖性和时间依赖性。选择20g/ L 处理细胞48h 进行后续实验。
2.3 D-半乳糖诱导NHOKs 发生衰老 D-半乳糖作用细胞后,SA-β-gal 阳性细胞数量明显增加(图3A,B)。细胞衰老相关蛋白p53 和p21 表达水平显著升高(图3C,D)。这些结果说明,D-半乳糖能够诱导NHOKs 发生衰老。
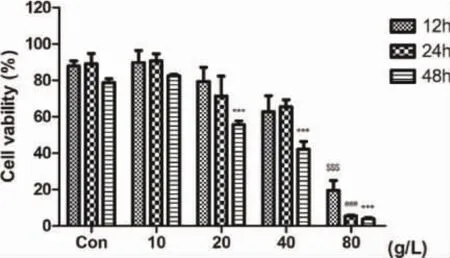
图2 D-半乳糖抑制NHOKs 增殖活力
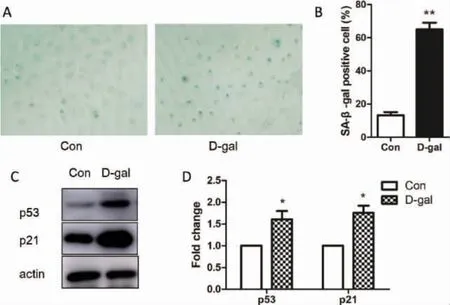
图3 D-半乳糖诱导NHOKs 发生衰老
2.4 D-半乳糖诱导NHOKs 衰老可能与氧化应激有关 与对照组相比,20g/ L D-半乳糖分别作用NHOKs 的12h、24h、48h 后,细胞内ROS水平逐渐升高(图4A)。48h 时差异有统计学意义。Sirtuin-1(sirt1)是sirtuin 蛋白家族的一员,研究发现其与衰老过程的ROS 产生有关。本研究提取D-半乳糖处理了48h 的细胞蛋白,WB 结果显示sirt1 表达显著降低(图4B,C)。因此,我们推测D-半乳糖诱导NHOKs 发生衰老可能与sirt1 相关的氧化应激过程有关。
3.讨论
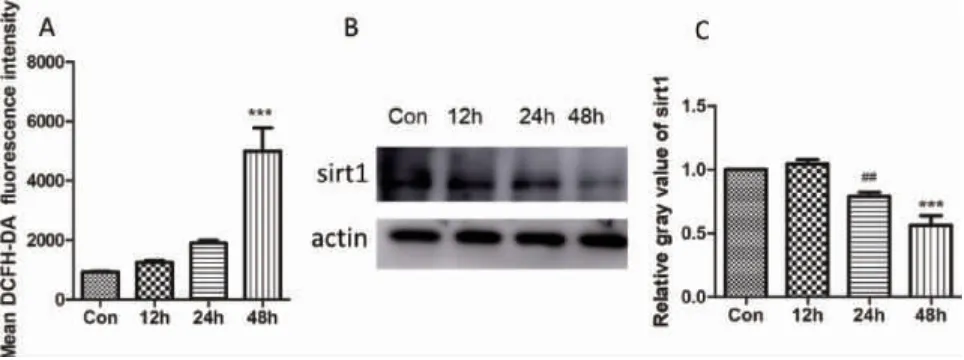
图4 D-半乳糖诱导NHOK 衰老可能与氧化应激有关
口腔黏膜层起到防御、感觉、温度调节和免疫等功能,角质形成细胞广泛存在于皮肤和黏膜表层,口腔黏膜的角质形成细胞比皮肤具有更快的增殖、迁移能力[10]。口腔黏膜表面不断受到各种机械、生物、化学刺激。并且菌群种类丰富,容易积累炎症和免疫细胞,产生炎症介质。随着年龄增长,口腔黏膜弹性纤维减少,胶原束增厚紊乱,黏膜弹性变差,且微血管减少,上皮厚度减少,不仅导致黏膜组织防御能力下降,创口愈合能力降低,感觉功能减退[11],对老年人后期义齿修复也带来诸多困难[12,13]。加上吸烟等环境因素的影响,口腔黏膜发生癌前病变和恶性病变的风险增加[1,2]。因此,体外构建稳定的口腔黏膜衰老模型对研究口腔黏膜衰老有重大意义。本研究首次证实,D-gal 可以在体外诱导NHOKs 发生衰老。
细胞衰老具有线粒体功能障碍、基因组不稳定、衰老相关分泌表型、干细胞衰竭等表现等特征,主要机制包括ROS 产生、端粒酶缩短、线粒体损伤、细胞周期停滞等[5,14]。细胞衰老与线粒体功能障碍关系密切。当细胞的线粒体功能损伤,发生氧化应激,产生大量包括ROS 在内的自由基,被认为是导致衰老和疾病的一个重要因素[15]。多种上皮细胞的衰老研究证实衰老过程中p53-p21 信号通路激活[16],且衰老过程中sirt1 表达显著降低。Sirt1 与细胞早衰关系密切,被认为是一种抗衰老因子[17]。参与应激反应、线粒体生物合成、增强代谢效率等[18]。
D-gal 是一种广泛存在于乳制品、水果、蔬菜等食物中的单糖,可作为诱导衰老的人工老化药物[19]。D-gal 诱导的老化垂体细胞与正常细胞相比,p53,p21 蛋白表达增加,p53/ p21 通路被激活[20]。D-gal 诱导大鼠心脏衰老的模型中,也发现p53-p21 通路被激活,同时ROS 含量升高并加速衰老[21]。P53 是一种转录因子,参与细胞周期调控、DNA 修复、细胞凋亡和细胞应激反应。P53激活可以诱导细胞生长停滞和调亡,还能调节细胞衰老和机体老化,对于肿瘤抑制和机体衰老至关重要[22]。P21 是DNA 损伤下p53 诱导细胞周期停滞,导致细胞衰老的重要调节因子。P53-p21 信号通路是调节细胞周期停滞和细胞衰老的经典通路[5]。晶状体上皮细胞研究中发现,d-gal 不但抑制增殖,还具有时间和浓度依赖性[23]。本次实验CCK-8 检测结果显示,与对照组相比,20g/ L、40g/ L、80g/ L 浓度的D-gal 对NHOKs 增殖具有抑制作用,且浓度越高,抑制作用越显著。各个浓度组均显示12h、24h、48h 细胞增殖活力逐渐降低,20g/ L 开始,差异开始显著。因此我们认为,D-gal抑制NHOKs 增殖,且具有浓度依赖和时间依赖性。我们通过WB 检测20g/ L D-gal 诱导48h 的NHOKs 细胞周期相关通路蛋白p53 和p21 表达,发现D-gal 处理后,蛋白表达均下调,说明细胞周期停止,增殖受到抑制,这与以往研究结果一致。
Sirt1 是NAD+依赖性去乙酰化酶,也是细胞能量代谢的感受器。通过p53、NICD、FOXO、NF-κB 等多种途径调节应激反应,发挥抗衰老作用[17]。NAD+/ NADH 比值增加从而激活sirt1。促进线粒体蛋白表达调节因子的活性,修复线粒体质量,降低ROS 产生,延长细胞寿命[24]。衰老细胞sirt1 表达下降与这一机制相一致。过量D-gal 诱导可线粒体功能障碍,出现氧化应激,产生大量ROS,损伤线粒体功能[19]。我们的数据显示,20g/ L D-gal 诱导NHOKs 后,细胞ROS 含量随时间延长而升高,48h 升高最显著,此时sirt1 表达逐渐降低,48h 时达到最低。与上述研究一致。我们推测,D-gal 作用于NHOKs,线粒体功能出现障碍,导致电子传递过程电子泄露,ROS 产生增加,且由于NADH 呼吸链受损,NADH 无法继续向NAD+传递电子,NAD+含量下降,NAD+/ NADH 比值降低,sirt1 活性抑制,对ROS 的调控作用下降。因此ROS 呈上升趋势。
综上所述,本研究证明D-gal 可在体外诱导NHOKs 发生早衰,这一过程可能与sirt1 参与调控的氧化应激反应相关。这一结论为体外构建口腔黏膜衰老模型提供依据,但尚需体内实验进行验证,以期为研究口腔黏膜老化提供更多工具。
