超声造影鉴别诊断肝上皮样血管平滑肌脂肪瘤与肝癌的价值
2021-01-13张春美
张春美 彭 林
上皮样血管平滑肌脂肪瘤(epithelioid angiomyolipoma,EAML)是一种少见的间叶源性肿瘤,常见于肾脏,其次见于肝脏。肝脏EAML 的临床表现和影像学表现均缺乏特异性,容易误诊为肝癌,误诊率达60%[1],准确诊断EAML和肝癌可以指导临床制定合理的治疗方案。超声造影(contrast-enhanced ultrasound,CEUS)可以显示病变的灌注情况,已广泛应用于肝脏、肾脏及胰腺等腹部器官的检查,CEUS 定量灌注分析弥补了MRI 不能显示病灶增强水平动态变化的缺点,为病灶的诊断提供了新的依据[2]。本研究旨在探讨CEUS 鉴别诊断肝脏EAML与肝癌的临床应用价值。
资料与方法
一、临床资料
选取2014 年6 月至2019 年1 月我院收治的经病理确诊的40例EAML患者(EAML组)和40例肝癌患者(肝癌组),EAML组男7 例,女33 例,年龄26~64 岁,平均(46.36±6.98)岁,CA125 为(14.87±2.70)U/ml,甲胎蛋白为(2.11±0.67)mg/ml,有乙肝病毒感染史9 例;肝癌组年龄31~73 岁,男29 例,女11 例,平均(54.30±5.02)岁,CA125为(15.05±2.12)U/ml,甲胎蛋白为(4.89±1.00)mg/ml,有乙肝病毒感染史33例。EAML组年龄、男性患者数、甲胎蛋白及乙肝病毒感染患者数均低于肝癌组(均P<0.05)。本研究经我院医学伦理委员会批准,所有患者均签署知情同意书。
二、仪器与方法
1.仪器与试剂:使用百胜MyLab Twice彩色多普勒超声诊断仪,常规超声检查使用LA523线阵探头,频率4.0~13.0 MHz;超声造影检查使用LA332 线阵探头,频率4.5~7.5 MHz。造影剂为声诺维(意大利博莱科公司)。
2.超声检查:所有患者术前禁食8 h,取平卧位或左侧卧位,先应用常规超声和CDFI 观察病灶形态、边界、内部回声及血流特征。然后行CEUS 检查,经肘静脉团注声诺维2.4 ml,尾随生理盐水5.0 ml 冲管。CEUS 检查的实时增强过程包括动脉相(0~30 s)、门脉相(31~120 s)及延迟相(121~360 s)。使用Qontrast 软件对图像进行分析,生成时间-强度曲线(time intensity curve,TIC)。以整个病灶为目标区域,勾画区域时避开灌注区、钙化灶及大血管。从软件导出各指标结果,定性分析包括不同增强时期的强化程度,定量分析包括造影剂抵达时间、峰值强度、达峰时间、增强斜率及开始消退时间。
三、统计学处理
结 果
一、两组常规超声检查结果比较
常规超声检查显示,肝癌组与EAML 组回声类型和病灶数量比较差异均有统计学意义(均P<0.05);两组血流信号强度、病灶位置及病灶边缘特征比较差异均无统计学意义。见表1。
二、两组CEUS检查结果比较
与肝癌组比较,EAML组向心性增强例数较多,延迟相低强化例数较少,差异均有统计学意义(均P<0.05),两组动脉相和门脉相增强程度比较差异均无统计学意义。与肝癌组比较,EAML组峰值强度较高,而达峰时间和开始消退时间均较短,差异均有统计学意义(均P<0.05);两组增强斜率和抵达时间比较差异均无统计学意义。见表2和图1,2。
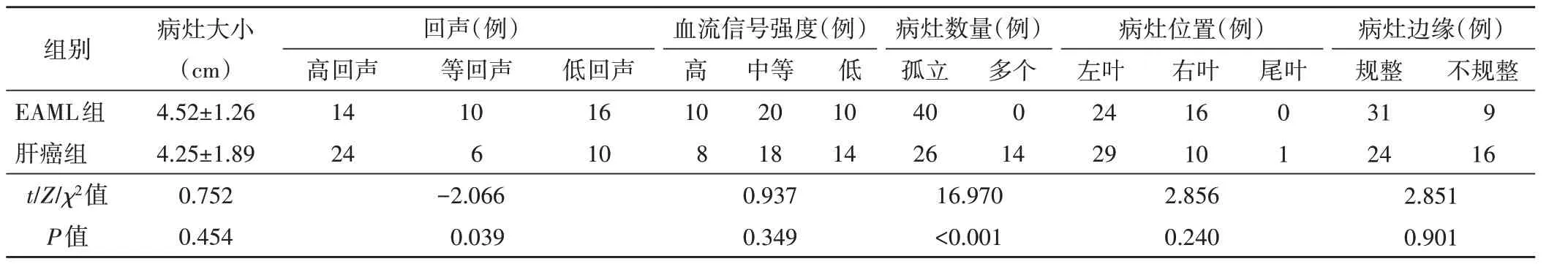
表1 两组常规超声检查结果比较
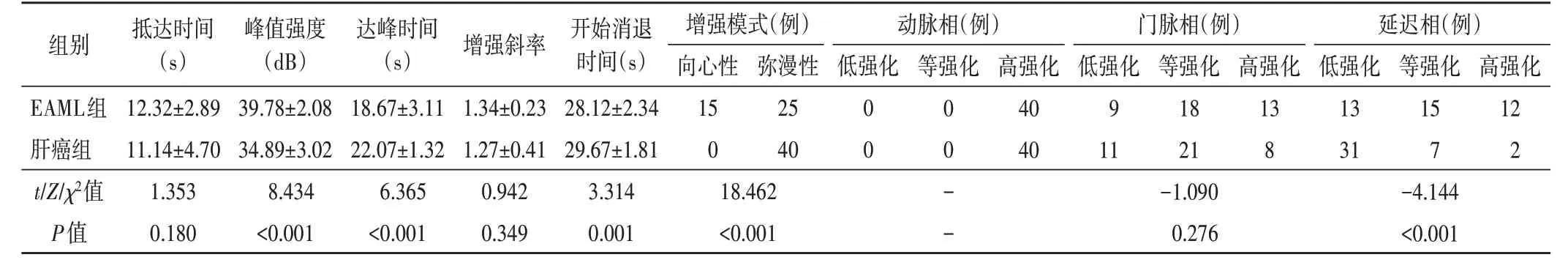
表2 两组CEUS检查结果比较
讨 论
肝脏EAML 是一种罕见的间充质实体瘤,由脂肪组织、平滑肌细胞及血管组成,容易误诊为肝癌,特别是当EAML 为低脂病变时[3]。早期鉴别诊断肝脏EAML与肝癌有助于临床制定合理的治疗方案,改善患者预后。常规超声是诊断肝脏肿瘤的主要方法,但其鉴别诊断肝脏EAML 与肝癌的价值较低[4]。本研究中常规超声检查显示两组血流信号强度、病灶位置及病灶边缘特征比较差异均无统计学意义。CEUS 利用造影剂使后散射回声增强,明显提高超声诊断的分辨力、敏感性及特异性,可观察正常组织和病变组织的血流灌注情况。研究[5]显示,CEUS鉴别诊断肝癌和肝脏EAML 的价值较高。本研究旨在探讨CEUS鉴别诊断肝脏EAML和肝癌的临床应用价值。
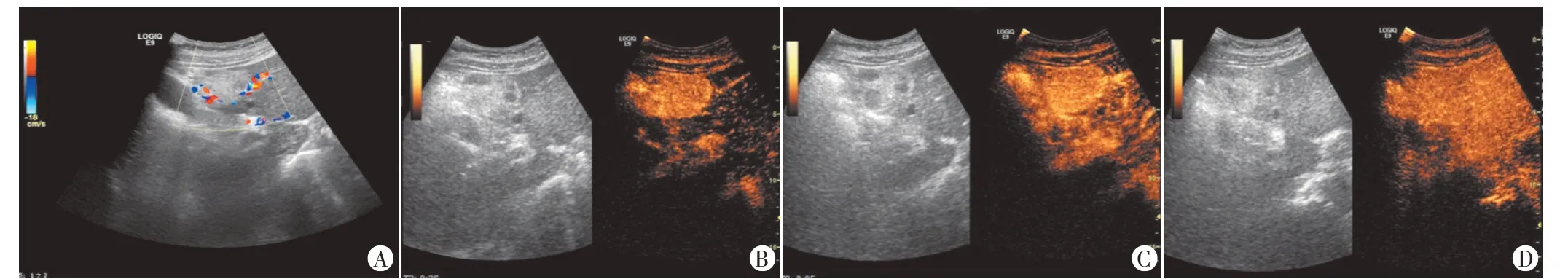
图1 一51岁女性EAML患者超声图像
本研究发现,与肝癌患者比较,EAML患者更具有向心性增强模式,与既往研究[6]结论一致。CEUS 检测动脉相时肝脏EAML 患者均呈高强化,原因是病变部位血管存在不同程度扩张[7]。CEUS 动脉相增强模式有助于鉴别肝脏良性与恶性局部病灶[8]。然而,本研究未发现两组患者动脉相强化程度有所差异,可能与样本量较少有关。EAML 组中延迟相低强化者较肝癌组明显减少(P<0.001),提示CEUS 检测结果定性分析有助于肝脏EAML的鉴别诊断。
CEUS 可很好地显示病灶的动态血流灌注特征,能对病灶进行定量分析,进一步提高了CEUS 的诊断效能[9]。本研究结果显示与肝癌组比较,EAML组峰值强度较高,而达峰时间和开始消退时间均较短,差异均有统计学意义(均P<0.05);两组增强斜率和抵达时间比较差异均无统计学意义,提示肝脏EAML患者和肝癌患者存在不同的血流灌注特征,这可能是由两种疾病的不同病理特点决定的。EAML 存在异常粗大的畸形动脉,管径较肝癌的滋养动脉管径大,导致动脉相血流灌注量和速度高于一般肝癌[10]。
本研究的局限性:①本研究为回顾性研究,未来需开展前瞻性研究证实CEUS 诊断肝脏EAML 的价值;②未结合病理特征对肝脏EAML进行分析;③由于肝脏EAML发病率较低,本研究样本量较少。
综上所述,肝脏EAML 与肝癌存在不同的血流灌注特征,CEUS有助于对其进行鉴别诊断,具有较好的临床应用价值。
