疑难肝病的临床病理诊断
2021-01-09廖冰
廖冰
肝脏疾病病因复杂繁多,分析临床病史、进行实验室和影像学检查是肝病诊断的重要手段,而病理检查可直接观察患者的病变形态,提供其疾病形态学信息,在疑难肝病诊断中的作用也愈发受到重视。本文通过介绍病理检查在疑难肝病诊断中的应用,以期为疑难肝病诊断提供更全面的认识。
一、病理检查在疑难肝病诊断中的作用
1.正常肝组织结构
肝脏具有双重血液供应,门静脉及肝动脉终末支经肝窦汇入肝静脉,形成肝脏独特的微循环和肝小叶结构。肝小叶中央为中央静脉,其周围是呈放射状排列的肝细胞和肝血窦。汇管区位于肝小叶周围,由疏松结缔组织及其内相伴行的小叶间胆管、小叶间动脉及小叶间静脉构成。肝腺泡是最小的微循环结构单位,以汇管区血管发出的终末肝门微静脉和终末肝微动脉及胆管分支为中轴,两端以相邻两个中央静脉为界,分为3个带,从近中轴血管至近中央静脉区域依次为Ⅰ带、Ⅱ带和Ⅲ带,而肝细胞获得血供条件、细胞代谢活跃程度和再生能力也依次减弱,因此Ⅲ带易对缺氧和其他损伤敏感,易发生病理改变。
2.肝活检常用特殊染色和免疫组化方法
适当的特殊染色(组织化学染色)或免疫组化标记可更好显示肝组织结构或凸显肝组织病理改变。常用的特殊染色包括Masson、网状纤维和淀粉酶消化-PAS(D-PAS)染色。Masson和网状纤维染色均可显示肝脏纤维组织是否增生,此外,网状纤维染色通过显示肝小叶网架结构塌陷来辅助判断肝细胞坏死情况。常用免疫组化标记物有CK7、CK19、乙型病毒性肝炎(简称乙肝)病毒表面抗原(HBsAg)、乙肝病毒核心抗原(HBcAg),其中CK7和CK19常用于显示胆管结构,进一步评估胆管损伤(如缺失)程度。在实践中需根据诊断选择染色项目(表1、2)。

表1 肝脏病理常用特殊染色和免疫组化染色
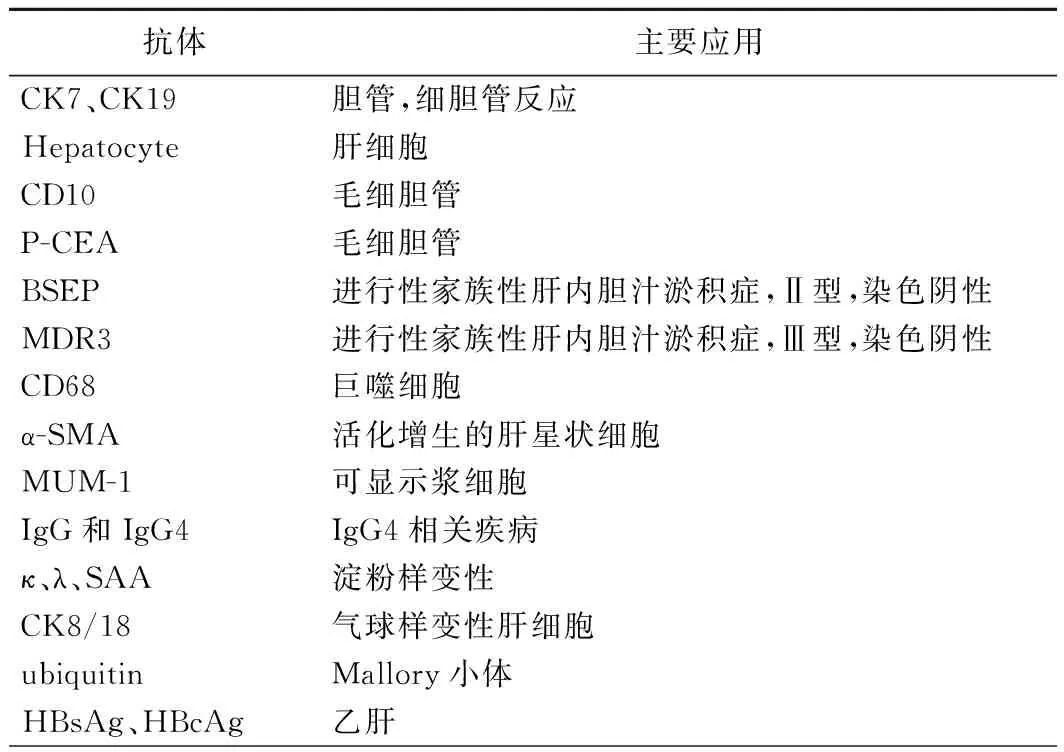
表2 肝脏病理常用免疫组化染色标记物
3.基于病理损伤模式的诊断思路
相同病因可能有不同的病理形态,而相似的病理形态也可能由不同病因导致。这两种现象分别为“同病异形”与“同形异病”,是导致病理诊断困难的重要原因。基于形态改变的病理损伤模式,如病变主要累及汇管区、肝小叶或两者兼有,考虑多种可能的病因和疾病,初步划定疑难肝病的范围,从而进一步通过细致的形态分析以及临床病理、基因检测等综合分析来明确诊断。专著Practical Hepatic Pathology归纳了7种病理损伤模式与相应的多种肝病,每种病理损伤模式可由多种疾病或病因导致,这7种损伤模式包括汇管区细胞浸润、细胆管反应、肝小叶损伤、脂肪变性、接近正常形态、纤维化及肿块(图1)。
4.病理诊断在疑难肝病诊断中的作用
(1)明确诊断的“金标准”:病理诊断被誉为疾病诊断的金标准,是基于不同疾病有不同的病理特征。病理诊断有助于诊断肿瘤、肝硬化及一些代谢性肝病与感染性疾病,大多数非肿瘤性肝病的诊断需要临床与病理检查结果密切结合。
(2)提供病因学和疾病诊断的线索:一些形态改变未能明确诊断特定的疾病,但可为疾病的诊断提供线索,提示这些疾病的可能性,如肝组织汇管区淋巴细胞浸润、肝细胞轻度脂肪变性、气球样变,并见多量糖原核,罗丹宁染色结果显示肝细胞铜沉积,提示Wilson病可能。
(3)评估病变损伤程度和疗效:病理诊断有助于疾病分期及预后判断。如肝组织活检结果显示胆管缺失预示原发性胆汁性胆管炎(PBC)患者对熊去氧胆酸(UDCA)治疗反应差和病变进展。
(4)探索疾病发生发展的规律:病理学诊断主要从形态学角度阐明疾病的本质,反映疾病发生发展的规律。
二、几种疑难肝病的临床鉴别难点
1.肝硬化和门脉高压的病因鉴别
肝硬化是多种肝病的晚期阶段,其病因包括病毒性肝炎、酒精性肝病、代谢相关脂肪性肝病(MAFLD)、血色病、Wilson病、肝内外慢性胆汁淤积、肝静脉流出道受阻、自身免疫性肝炎等。尽管我国肝硬化患者多由慢性病毒性肝炎所致,但肝硬化病因鉴别仍是临床的难点之一。肝硬化的共同病理特征是纤维组织增生并分隔肝实质,形成弥漫性假小叶。从这一共同特征中甄别病理形态的细微差异有助于病因鉴别。纤维组织分隔的肝实质呈犬牙交错的拼图样,实质部分与增生的纤维组织之间有浅染带,提示为胆汁性肝硬化,可由PBC等胆道病变而非病毒性肝炎引起。肝硬化呈小结节状,假小叶间为较宽阔的血管纤维间隔伴血窦扩张,假小叶内见肝细胞脂肪变性、气球样变和多量Mallory小体,伴中性粒细胞为主的炎症细胞浸润,合并窦周纤维化和终末静脉纤维化,提示为酒精性肝病导致的酒精性肝硬化。慢性乙型病毒性肝炎(CHB)肝硬化的活动期可形成大小不等的结节,纤维间隔内淋巴细胞浸润,伴界面炎,静止期多形成大结节,纤维间隔窄,假小叶边界清晰光滑,间隔内门静脉扩张,可见毛玻璃样肝细胞(HBsAg在滑面内质网聚集引起的病理表现)。
CHB患者如出现门脉高压,组织病理学检查中需注意辨认是否发生肝硬化;若为肝硬化,是否符合CHB肝硬化。肝硬化常表现为门脉高压,但并非等同于肝硬化。笔者曾遇到一位女性患者15岁时出现门脉高压、脾脏肿大,血清学检查结果提示CHB,肝脏组织病理活检诊断CHB肝硬化。患者30岁时再次就诊,笔者会诊当年肝脏组织病理活检玻片,于肝实质间见多量宽阔纤维组织内分布较多小胆管,胆管腔内胆汁淤积,未见正常汇管区3个管道伴行,炎症细胞不明显,肝实质与宽阔的纤维组织间的边界较清晰,无界面炎,因此诊断为先天性肝纤维化(CHF),见图2。基因检测结果进一步证实了病理诊断。CHF是遗传相关肝病,与胆管板发育畸形相关,可致门脉高压。门脉高压进行肝脏病理组织活检时需要辨认是否肝硬化或CHF、血管性肝病等引起的门脉高压,即非硬化性门脉高压。
2.胆汁淤积性肝病的病因鉴别
引起胆汁淤积的病因较多,主要包括病毒、细菌、寄生虫、药物和(或)毒物、自身免疫、酒精、结石、肿瘤和遗传代谢等,可引起肝细胞和(或)胆管细胞损伤及胆管系统梗阻,导致肝内胆汁淤积和(或)肝外胆汁淤积。以累及胆管系统的自身免疫性肝病为例,病理检查有助于进一步鉴别其病因而采取不同治疗策略。汇管区多量淋巴细胞浸润,且表现为聚集于小叶间胆管周围为主,胆管上皮细胞排列不整齐、胞浆红染,伴肉芽肿形成,则病理形态符合PBC。因此,病理检查对抗线粒体抗体(AMA)及AMA-M2抗体阴性的PBC诊断尤为重要。原发性硬化性胆管炎(PSC)可累及肝外及肝内各级胆管,病理表现为胆管周围纤维组织增生呈洋葱皮样,胆管腔狭窄,胆管上皮细胞变性、萎缩,小叶间胆管数量减少甚至消失,汇管区炎症细胞浸润程度较PBC稍轻。肝脏病理组织活检对诊断影像学检查显示胆道无明显特征性改变的小胆管型PSC是必需的。胆管壁及其周围有大量浆细胞浸润,纤维组织席纹状增生,血管壁增厚呈闭塞性静脉炎,则提示IgG4硬化性胆管炎(IgG4-SC),需通过IgG4和IgG免疫组化协助诊断。免疫组化IgG4阳性细胞>10个/每高倍视野(活检标本)或50个/每高倍视野(手术切除标本),同时IgG4/IgG阳性细胞>40%有助于组织学诊断IgG4-SC。笔者遇到不止1例表现为胆汁淤积性肝病的患者影像学检查结果提示胆管梗阻,怀疑胆管癌而进行手术切除,经病理检查结果诊断为IgG4-SC而非肿瘤。因此,此类可疑患者通过血清IgG4检测和病理组织活检可使其避免不必要的手术处理,而通过糖皮质激素治疗获益。当然,部分IgG4-SC患者血清IgG4水平可不升高,同时,病理诊断也需要排除其他原因引起的浆细胞增多,甚至IgG4阳性浆细胞增多。胆汁淤积性肝病的病理诊断中,遗传相关性肝病是不能忽略的病因,如Alagille综合征、良性复发性肝内胆汁淤积(BRIC)和进展性家族性肝内胆汁淤积(PFIC)等。Alagille综合征患者的肝脏病理形态主要表现为汇管区的小叶间胆管缺失。BRIC和PFIC可表现为毛细胆管胆汁淤积、多核巨肝细胞形成(巨细胞肝炎)、细胆管增生,甚至小叶间胆管的缺失等。其中,不同PFIC类型的病理形态不尽相同,病理诊断时应结合患者的临床表现、肝脏生化检查结果尤其是血清谷氨酰转肽酶(GGT)和胆汁酸水平及基因检测结果等综合进行分析。
3.药物性肝损伤与自身免疫性肝炎的鉴别
药物性肝损伤(DILI)的靶细胞包括肝细胞、胆管上皮细胞及肝血管内皮细胞,因此DILI的病理形态多种多样,其中以肝细胞损伤引起的急性小叶性肝炎改变最为常见,慢性DILI可呈慢性肝炎形态。自身免疫性肝炎(AIH)多为慢性发病,典型的病理特征为汇管区大量浆细胞及淋巴细胞浸润,伴淋巴细胞、浆细胞性界面炎,肝细胞呈玫瑰花环样排列。AIH少数可急性发作,此时病理形态表现为小叶炎症坏死,如肝腺泡Ⅲ带融合性坏死。因此,急性DILI与急性发作AIH、慢性DILI与AIH需加以鉴别。组织病理学检查有助于DILI与AIH的鉴别诊断。相较于AIH,DILI主要为混合性炎症细胞,包括淋巴细胞、中性粒细胞和嗜酸性粒细胞的浸润,可出现肝细胞或毛细胆管淤胆,腺泡Ⅲ带的融合坏死灶边界清晰,而淋巴细胞和浆细胞性界面炎则不明显。组织病理学诊断与鉴别诊断需密切结合患者临床病史如既往史和用药史、临床表现和实验室检查结果。AIH与伴自身免疫特征的DILI(AL-DILI)的鉴别是临床的难点之一,病理形态难以鉴别时,临床停用可疑药物后病情是否改善、应用糖皮质激素和其他免疫抑制剂治疗后应答是否较好、使用糖皮质激素1~6个月后停药病情是否复发等临床情况均有助于鉴别诊断。
4.多重因素导致肝损伤的诊断
有些肝损伤同时由多种因素导致,理清其多重因素有助于指导临床治疗。如表现为血清转氨酶升高的CHB患者,肝脏病理组织活检结果可见病毒性肝炎引起的汇管区淋巴细胞浸润、毛玻璃样肝细胞、伴或不伴界面炎,若同时可见腺泡Ⅲ带为主的肝细胞大泡性脂肪变性、气球样变且伴窦周纤维化则形态提示同时存在代谢相关脂肪性肝病(MAFLD)可能。重叠综合征是自身免疫性肝病中需要关注的,可通过组织病理活检协助诊断。采用巴黎标准,PBC患者肝脏组织病理活检可见AIH典型的中到重度浆细胞、淋巴细胞性界面炎,则形态提示PBC-AIH重叠综合征,结合血清ALT或IgG水平,可明确诊断。
5.几种疑难罕见肝病的病理特征
一些肝脏疾病具有较为特异的病理特征,通过病理检查可以显示这些病理特征,大多能对疾病起到明确诊断的作用。在此仅列举几种相对少见的肝病的病理特征:(1)Dubin-Johnson综合征:肝组织肉眼呈黑色或墨绿色,苏木素-伊红(HE)染色切片见肝细胞内较粗的棕褐色色素颗粒,主要分布于腺泡Ⅲ带肝细胞的毛细胆管侧。(2)红细胞生成性卟啉病:毛细胆管见棕褐色色素,偏振光显微镜下观察呈双折光的红-黄色,其中央见十字结构(Maltese cross)。(3)肝淀粉样变性:肝组织汇管区纤维间质内、血管壁、肝窦周隙可见多量团片状分布的云雾状粉染物质(图3),刚果红染色呈橘红色,偏振光显微镜下观察呈苹果绿色。电镜观察在以上代谢性肝病中亦有较特征性的表现。(4)肝窦阻塞综合征/静脉闭塞病(SOS/VOD):以肝腺泡Ⅲ带为主的肝窦扩张充血,红细胞进入窦周Disse间隙,肝索可变窄,肝细胞萎缩或消失,中央静脉内皮细胞损伤脱落、内膜增厚、管腔狭窄或闭塞。SOS/VOD可见于土三七(含吡咯烷生物碱)导致的DILI,亦由某些化疗药物或免疫抑制剂等导致。
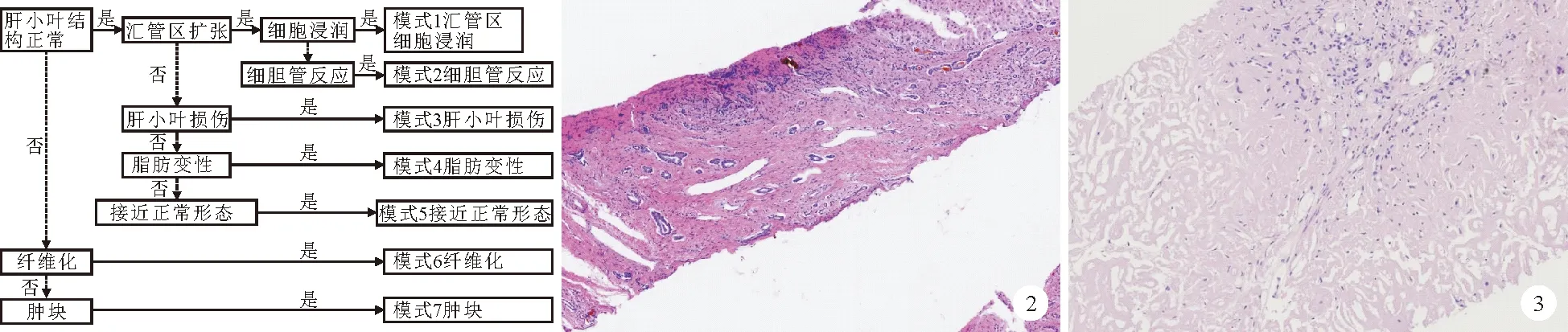
图1 肝组织病理损伤模式 图2 先天性肝纤维化患者肝脏组织病理HE染色结果(×100) 图3 肝淀粉样变性患者的肝组织病理HE染色结果(×100)
三、提高疑难肝病的病理诊断水平
病理医生首先需熟悉一种疾病可能的形态改变类型,导致形态改变的疾病或病因类型,即上述肝组织病理损伤模式的诊断思路。病理诊断时,了解患者年龄和性别后,屏蔽病史,先根据病理形态作出初步诊断方向,避免先了解病史而先入为主,之后再结合病史来反复阅片、思考。其次,必须密切结合临床,这点如何强调也不为过。因此,病理医生也应掌握一定临床知识。最后,广泛阅读病理学相关专著,多参加临床病理讲座,多学习病例,从实践中思考、归纳、总结和提高。
临床医生应认识到疑难肝病病理诊断的重要性,掌握一定肝病病理知识,密切结合临床病理,为病理诊断提供临床病史资料及诊断意见,提供合格的病理标本,有助于疑难肝病的诊断。建议肝穿刺活检组织长度≥2 cm,汇管区数量≥11个。怀疑代谢性肝病时,建议同时送检电镜标本协助诊断。
此外,肝病尤其非肿瘤肝病的病理诊断具有较强的专科性。注重肝脏病理的专科化建设和肝脏病理医生的培养能更好提高疑难肝病的诊断水平。
综上,病理检查提供了疾病的形态学信息,在疑难肝病诊断中发挥重要作用。同时,疑难肝病的病理诊断需密切结合临床,采用多学科协作的方式。
