《邻菲罗啉分光光度法测定水中微量铁》实训改进研究
2021-01-08张悦君何旭伦黎喜云刘文敏
张悦君,何旭伦,黎喜云,刘文敏
(广东环境保护工程职业学院,广东 佛山 528216)
1 引言
目前学院《仪器分析技术》课程中《邻菲罗啉分光光度法测定水中微量铁》这一实训项目的方案是参考行业标准HJ/T 345—2007《水质 铁的测定邻菲罗啉分光光度法》制定的,但实际实训中不涉及水样预处理的过程并且实践教学方案中铁标准使用液的浓度低于行业标准,因此实验条件存在优化改进的空间。为更好地开展实践教学,节约化学试剂,保护环境,本文探讨了《邻菲罗啉分光光度法测定微量铁》实验的波长、盐酸羟胺溶液的浓度、邻菲罗啉溶液的浓度、缓冲溶液的用量对实验的影响,进而得出了最佳的实验条件。
2 实验
2.1 主要仪器和试剂
仪器:721(数显)分光光度计(上海菁华科技仪器有限公司),10 mm比色皿,pHS-25酸度计(成都世纪方舟科技有限公司)。
试剂:铁贮备液(100 μg/mL):准确称取0.7020 g分析纯((NH4)2Fe(SO4)2)·6H2O),溶于50 mL(1+1)H2SO4,转移至1000 mL的容量瓶中,并用水稀释到刻度,摇匀。
铁标准使用液(20 μg/mL):准确移取铁贮备液20.00 mL于100 mL容量瓶中,用水稀释至刻度,摇匀。
醋酸-醋酸铵缓冲溶液:40 g乙酸铵加50 mL冰乙酸用水稀释至100 mL;0.5%(m/V)邻菲罗啉水溶液(临用现配);10%(m/V)盐酸羟胺溶液(临用现配)。
2.2 实验原理
邻菲罗啉分光光度法以盐酸羟胺作为还原剂将三价铁还原为二价铁,在一定酸度条件下二价铁进一步和邻菲罗啉生成稳定的橙红色络合物,用分光光度计测定其吸光度,溶液铁含量与吸光度呈正比。
3 结果与讨论
3.1 最优波长的选择
通过测定不同波长下溶液的吸光度值,以确定《邻菲罗啉分光光度法测定微量铁》实验的最优波长。移取铁标准使用液(20 μg/mL)10.00 mL置于50 mL比色管中,加入10%盐酸羟胺1 mL,摇匀,加入缓冲溶液5 mL,摇匀,加入0.5%邻菲罗啉2 mL,加去离子水至刻度线,摇匀。显色15 min后,用10 mm比色皿,以去离子水为参比,在480~530 nm之间每隔10 nm测定一次吸光度,结果如图1所示。

图1 波长对吸光度的影响
由图1可知,在480~530 nm之间溶液吸光度呈先上升后下降的趋势,并在510 nm处有最大的吸光度,因此确定本实验最优波长为510 nm。
3.2 还原剂浓度选择
该实验一般以盐酸羟胺作为还原剂将三价铁还原为二价铁。由于盐酸羟胺属于有毒试剂[1],为减少化学试剂的使用,降低环境污染,本实验拟研究盐酸羟胺浓度对吸光度的影响。
采用单一变量原则,移取铁标准使用液10.00 mL于6支50 mL比色管中,分别加入0%、1%、2.5%、5%、7.5%、10%不同浓度的盐酸羟胺1 mL,再依次加入缓冲溶液5 mL,0.5%邻菲罗啉2 mL,加水定容至刻度线,测得相应吸光度,结果如图2所示。
由图2可知,溶液吸光度随着盐酸羟胺浓度增高而增大,当盐酸羟胺浓度达2.5%以后,吸光度趋于平稳。因此,改用2.5%盐酸羟胺于邻菲罗啉分光光度法测定微量铁实验中是可行的。

图2 盐酸羟胺对吸光度的影响
3.3 显色剂浓度选择
该实验采用邻菲罗啉作为显色剂,为减少试剂浪费同时保证亚铁离子完全显色,本实验拟研究邻菲罗啉浓度对吸光度的影响。
采用单一变量原则,移取铁标准使用液10.00 mL于7支50 mL比色管中,依次加入2.5%盐酸羟胺1 mL,缓冲溶液5 mL,再分别加入0.01%、0.05%、0.1%、0.2%、0.3%、0.4%、0.5%不同浓度的邻菲罗啉溶液2 mL,加水定容至刻度线,测得相应吸光度。结果如图3所示。
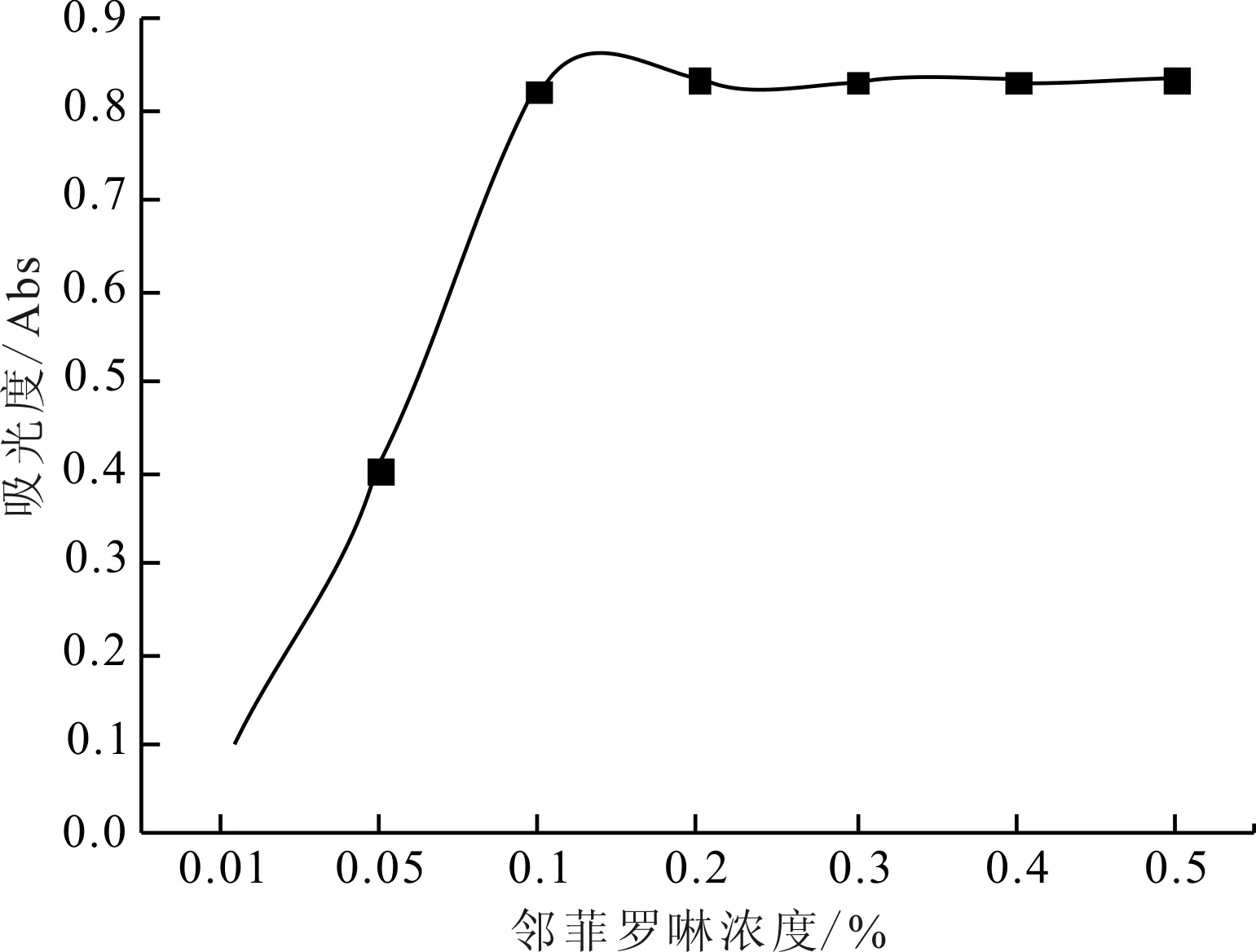
图3 邻菲罗啉对吸光度的影响
由图3可知,溶液吸光度随着邻菲罗啉浓度增高而增大,当邻菲罗啉浓度达0.1%以后,吸光度呈平稳趋势。理论上,1 mol的Fe2+与3 mol的邻菲罗啉完全反应,本实验最高取10 mL浓度为20 μg/mL的铁标准使用液,即Fe2+约为3.57×10-3mmol,对应所需邻菲罗啉为1.08×10-2mmol[2]。2 mL浓度为0.1%的邻菲罗啉约为1.01×10-2mmol ,2 mL 浓度为0.2%的邻菲罗啉约为2.02×10-2mmol,2 mL浓度为0.2%的邻菲罗啉可以满足Fe2+完全显色时所需显色剂的量,又因邻菲罗啉对水生生物有极高毒性,可能导致水体环境的长期不良影响,所以为了节约试剂用量和保护环境,同时保证实验效果,选择0.2%邻菲罗啉溶液为最优条件。
3.4 缓冲溶液加入量选择
为了研究缓冲溶液用量对本实验的影响,移取铁标准使用液10.00 mL于6支50 mL比色管中,依次加入2.5%盐酸羟胺1 mL,再分别加入0 mL、1 mL、2 mL、3 mL、4 mL、5 mL不同体积的缓冲溶液,最后加入0.2%邻菲罗啉2mL,加水定容至刻度线,测定相应吸光度及pH值。测定结果如图4所示。

图4 缓冲溶液加入量对吸光度的影响
根据图4得知,溶液吸光度随着缓冲溶液加入量的增加而增大,当缓冲溶液加入量达2 mL以后,吸光度趋于平稳。加入2~5 mL缓冲溶液在溶液中的pH值近似相等,满足邻菲罗啉与Fe2+发生络合反应所需pH3~9之间的酸度条件。pH值过高或过低都会对实验造成影响,当pH<2时邻菲罗啉会发生副反应,当pH<3时邻菲罗啉与Fe2+显色速度变慢,当pH>9时二价铁会被盐酸羟胺还原为铁单质,无法与邻菲罗啉络合显色,进而使溶液褪色[3]。为保证实验条件并节约教学实际成本,减少缓冲溶液的使用体积,可选择2 mL的缓冲溶液进行测定微量铁实验。
3.5 加标回收率实验
在四次优化实验探究后,选择510 nm作为实验的最优波长,2.5%盐酸羟胺1 mL,0.2%邻菲罗啉2 mL,缓冲溶液2 mL作为改进方法的实验试剂。通过绘制标准曲线并选择一个浓度的样品进行加标回收率实验。实验结果见表1~2。

表1 改进方法的标准曲线

表2 改进方法的加标回收率
改进方法的标准曲线线性良好,相关系数为0.99994,加标回收率为96.5%~97.0%,准确度较高。
3.6 精密度实验
移取铁标准使用液2.00 mL、4.00 mL、8.00 mL各6次于比色管中,进行精密度实验,结果见表3。
由表3得知,优化后3种不同浓度铁浓度实验的RSD值均小于1%,证明优化后的实验具有良好的精密度。
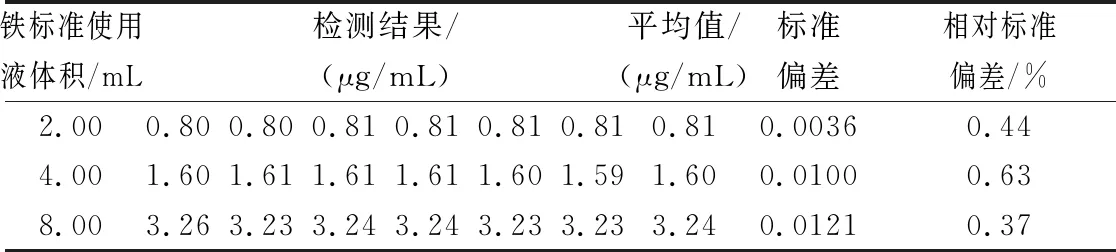
表3 改进方法的精密度
4 结语
对邻菲罗啉分光光度法测定水中微量铁的实验试剂进行优化,改进后的方法具有良好的准确度和精密度,克服了传统方法有毒试剂用量大的不足,可应用于仪器分析等课程的日常实践教学中。
