逍遥散及其加减方的抗抑郁作用比较研究
2021-01-06林映仙杨文静曹宁宁赵利斌陈宇洲肖学凤
林映仙,杨文静,曹宁宁,赵利斌,裴 帅,陈宇洲,肖学凤
逍遥散及其加减方的抗抑郁作用比较研究
林映仙1,杨文静2,曹宁宁1,赵利斌3,裴 帅1,陈宇洲1*,肖学凤1*
1. 天津中医药大学中药学院,天津 301617 2. 天士力医药集团股份有限公司,天津 300402 3. 山西振东制药股份有限公司,山西 长治 047100
比较逍遥散及其加减方的抗抑郁作用,精简组方、明确药效,为抗抑郁新药的研发提供参考。SD大鼠随机分为对照组,模型组,氟西汀(0.01 g/kg)组,加味逍遥散(16.20 g/kg)组,逍遥散(10.13 g/kg)组,逍遥散去生姜、薄荷(9.79 g/kg)组,逍遥散去生姜、茯苓、薄荷(8.10 g/kg)组。采用慢性温和不可预知刺激(chronic unpredicted mild stress,CUMS)结合孤养建立大鼠抑郁模型,同时对照组和模型组ig生理盐水,其余各组ig相应药物。观察给药后大鼠行为学指标(体质量、糖水消耗率、敞箱实验运动得分)的变化;采用ELISA试剂盒检测大鼠血浆中皮质酮,皮质和海马中多巴胺、去甲肾上腺素(norepinphrine,NE)、5-羟色胺、神经营养因子(brain derived neurotrophic factor,BDNF)水平。模型组大鼠行为学指标显著降低(<0.05),皮质和海马中多巴胺、NE、5-羟色胺、BDNF水平显著降低(<0.05),血浆中皮质酮水平显著升高(<0.05),表明CUMS结合孤养大鼠抑郁模型建立成功;与模型组比较,各给药组大鼠行为学指标显著升高(<0.05),皮质和海马中多巴胺、NE、5-羟色胺、BDNF水平均显著升高(<0.05),血浆中皮质酮水平显著降低(<0.05),其中逍遥散去生姜、茯苓、薄荷组疗效最佳。逍遥散及其加减方具有抗抑郁作用,其中逍遥散去生姜、茯苓、薄荷组抗抑郁作用最强,表明柴胡、当归、白芍、白术、甘草是逍遥散发挥抗抑郁作用的主要配伍药味。
逍遥散;抗抑郁;慢性温和不可预知应激;柴胡;当归;白芍;白术;甘草
抑郁症是以抑郁心境为主要特征的精神障碍疾病,具有高发病率、高致残率、高复发率的特点,临床表现为食欲减退、情绪低落、活动迟缓、无助感、易怒等症状,且重度抑郁症患者有自杀倾向[1-2]。目前,临床上常用的治疗抑郁症多为基于单胺假说的药物如吗氯贝胺、丙咪嗪、氟西汀等;基于谷氨酸假说的药物如美金刚、拉莫三嗪、依利罗地等;基于应激假说的药物如米非司酮、地昔帕明、阿米替林等[3-4]。常用于治疗抑郁症的中药复方有逍遥散、开心散、血府逐瘀汤等[5]。化学药物虽然在临床上被广泛应用,但其安全性、耐受性一直饱受争议[6-7]。中药复方因不良反应小、安全性高、具增效减毒等优势,越来越受到人们的关注[8-11]。
中医学认为抑郁症是一种情志疾病,属于“郁证”“百合病”等范畴,病位涉及五脏,主要为肝,并以情志所伤、气机郁滞、五脏气血失调为病机[12-13]。肝主疏泄和藏血、运行气血、情志调畅。逍遥散源自《太平惠民和剂局方》,全方由柴胡、当归、白芍、白术、茯苓、生姜、薄荷、甘草8味药组成,具有疏肝解郁、健脾养血之功效[14]。方中柴胡为疏肝解郁之要药,白芍、当归为补血活血之圣药,血和则肝和,血充则肝柔,三者均归于肝经,抗抑郁作用较强;木郁不达而致脾虚不运,脾为后天之本,营血生化之源在于脾,脾失健运则反侮于肝,故佐以白术、甘草健脾益气,使营血生化有源,实土以御木侮,以助柴胡疏肝解郁[15]。茯苓利水渗湿,生姜温中止呕,薄荷疏散风热,三者均归于肺经,疏肝解郁作用相对较弱[16-19]。本研究从中医角度出发依据中药配伍和归经特点将逍遥散加减方拆方为加味逍遥散组,逍遥散去生姜、薄荷组和逍遥散去茯苓、生姜、薄荷组,比较逍遥散及其加减方的抗抑郁作用,揭示逍遥散中发挥抗抑郁的主要药味,使其组方精简、药效明确,为研发疗效更佳的抗抑郁新药奠定基础。
本研究采用慢性不可预知温和刺激(chronic unpredictable mild stress,CUMS)结合孤养建立大鼠抑郁模型,考察大鼠行为学指标(体质量、糖水消耗率、敞箱实验运动得分),血浆中皮质酮水平,皮质和海马中多巴胺、去甲肾上腺素(norepinphrine,NE)、5-羟色胺、神经营养因子(brain derived neurotrophic factor,BDNF)水平的变化,比较逍遥散及其加减方抗抑郁疗效差异,为抗抑郁的新药研发提供依据。
1 材料
1.1 动物
SPF级雄性SD大鼠100只,7~8周龄,体质量180~200 g,购于中国食品药品检定研究院,许可证号SCXK(京)2017-0005,饲养于天津中医药大学实验动物中心,温度(22±2)℃,湿度(50±10)%,自然光照,大鼠自由摄食和饮水。动物实验遵循天津中医药大学实验动物管理和使用的规定,均符合3R原则。
1.2 药品与试剂
逍遥散(由柴胡、当归、白芍、白术、茯苓、生姜、薄荷、甘草组成,批号20190307),加味逍遥散(由逍遥散加牡丹皮、栀子组成,批号20190306),逍遥散去生姜、薄荷(批号20190310),逍遥散去生姜、茯苓、薄荷(批号20190308),以上浸膏均由天士力医药集团股份有限公司提供,各组方主要药味生药量相当,且主要化学成分柴胡皂苷B2质量分数>0.001 8%,芍药苷质量分数>0.045%。盐酸氟西汀胶囊(批号8784A,规格20 mg/粒)购于礼来苏州制药有限公司;皮质酮、BDNF、5-羟色胺、多巴胺、NE ELISA试剂盒均购自美国R&D Systems公司;生理盐水购自石家庄四药有限公司。
1.3 仪器
LTD0114子弹头警灯(浙江安华安全设备有限公司);G6805-1治疗仪(青岛鑫升实业有限公司);TD21001电子天平(天津市天马仪器厂);IKAT18型超声组织破碎仪(宁波新芝生物科技有限公司);3K15型冷冻高速离心机(美国Sigma公司);Infinite M200 Pro型多功能酶标仪(瑞士Tecan公司);−80 ℃低温冰箱(美国Thermo Fisher Scientific公司);大鼠敞箱实验行为测试箱(自制,100 cm×100 cm×50 cm,内部四壁及底面涂成黑色,底部用白线划出100个边长为10 cm的正方形小格)。
2 方法
2.1 动物分组及给药
SD大鼠适应性饲养7 d后,在安静环境下进行敞箱实验,根据水平运动和垂直运动得分相近的原则剔除得分过高或过低的大鼠。根据体表面积折算,大鼠给药剂量为人临床等效剂量的15倍。
将筛选出大鼠随机分成对照组,模型组,氟西汀(0.01 g/kg)组,加味逍遥散(16.20 g/kg)组,逍遥散(10.13 g/kg)组,逍遥散去生姜、薄荷(9.79 g/kg)组,逍遥散去生姜、茯苓、薄荷(8.10 g/kg)组,每组12只。对照组大鼠常规饲养,4只/笼,自由进食饮水,其余各组大鼠采用CUMS结合孤养造模,持续9周。造模同时各给药组ig相应药物(10 mL/kg),对照组和模型组ig等体积生理盐水。
2.2 CUMS结合孤养大鼠抑郁模型的建立
参考文献方法[20]并结合课题组前期实验方法造模,大鼠单笼饲养,每天随机接受以下2种不同应激刺激且相同刺激不可连续出现,从而使大鼠不能预料何种刺激,避免其产生适应性。CUMS刺激因子包括:束缚2 h;冰水高台2 h;噪音刺激(110 dB,30 min);足底电击(电流4 mA,50次,每次间隔5 s);光照刺激(100 000 lx,30 min);昼夜颠倒24 h;潮湿垫料12 h;夹尾(距离大鼠尾尖1 cm左右,2 min)。持续造模9周,每周测量各组大鼠体质量、糖水消耗量、敞箱实验水平运动与垂直运动得分。
2.3 逍遥散及其加减方对大鼠行为学的影响
2.3.1 体质量变化 实验第0、7、14、21、28、35、42、49、56、63天分别测定大鼠体质量,计算各组大鼠体质量增长量。
体质量增长量=(第63天体质量-第0天体质量)/第0天体质量
2.3.2 糖水消耗实验 实验第0、7、14、21、28、35、42、49、56、63天对大鼠进行糖水消耗实验。实验前3 d进行糖水适应,在笼子上放置2瓶1%蔗糖溶液24 h,然后放置1%蔗糖溶液1瓶、纯水1瓶24 h,上下午调换水瓶位置,第3天禁食禁水24 h。正式实验时,笼子上分别放置1%蔗糖溶液1瓶、纯水1瓶,上下午调换水瓶位置,记录24 h内糖水消耗量和纯水消耗量,计算糖水消耗率。
糖水消耗率=糖水消耗量/(糖水消耗量+纯水消耗量)
2.3.3 敞箱实验 实验第0、7、14、21、28、35、42、49、56、63天对大鼠进行敞箱实验。将大鼠放在中心固定的方格内,排除人为干扰,记录大鼠3 min内活动路线。以大鼠穿越底面小方格的数量为水平运动得分,大鼠每穿越1格(3爪以上跨入)均计为水平运动1分,若实验大鼠沿直线行走,则以每10厘米计为1分。以大鼠直立次数为垂直运动得分,大鼠双前肢离开敞箱底面为标志,以大鼠放下双前肢计为垂直运动1分。每只大鼠测试完毕后,清理敞箱,进行下一只大鼠的测试。记录每只大鼠的水平运动得分及垂直运动得分。
2.4 逍遥散及其加减方对大鼠血浆中皮质酮水平的影响
行为学实验后,大鼠眼眶取血1.5 mL于肝素浸润的离心管中,4 ℃、8000 r/min离心10 min,取上清液,于−80 ℃低温冰箱保存备用,按ELISA试剂盒说明书测定大鼠血浆中皮质酮水平。
2.5 逍遥散及其加减方对大鼠海马和皮质中BDNF、5-羟色胺、多巴胺、NE水平的影响
大鼠眼眶取血后,脱颈椎处死,迅速剥离皮质和海马组织,称定质量,于液氮迅速冷冻,然后转至−80 ℃低温冰箱保存备用。分别取皮质、海马组织适量,剪碎并称定质量,加入10倍量生理盐水,用组织破碎仪低温匀浆,4 ℃、8000 r/min离心10 min,取上清液,按ELISA试剂盒说明书测定大鼠皮质和海马组织中BDNF、5-羟色胺、多巴胺、NE水平。
2.6 统计学分析
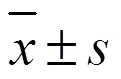
3 结果
3.1 逍遥散及其加减方对大鼠行为学的影响
3.1.1 体质量变化 如表1所示,与对照组比较,模型组大鼠体质量增长量显著下降(<0.05),表明CUMS结合孤养造模影响大鼠食欲,导致大鼠体质量增长缓慢,模拟了抑郁症患者食欲减退、体质量减轻症状。与模型组相比,各给药组大鼠体质量增长量显著升高(<0.05),表明各给药组均可改善抑郁模型大鼠食欲减退、体质量减轻症状。
各给药组大鼠体质量增长量大小顺序依次为氟西汀组>逍遥散去生姜、茯苓、薄荷组>逍遥散去生姜、薄荷组>逍遥散组>加味逍遥散组,氟西汀与逍遥散去生姜、茯苓、薄荷组,逍遥散组与加味逍遥散组间无统计学差异,表明逍遥散去生姜、茯苓、薄荷组疗效与氟西汀组相当,且加味逍遥散组效果最弱。

表1 逍遥散及其加减方对大鼠体质量增长量的影响()
与对照组比较:▼<0.05;与模型组比较:#<0.05;与逍遥散组比较:■<0.05;与逍遥散去生姜、薄荷组比较:□<0.05;与逍遥散去生姜、茯苓、薄荷组比较:▽<0.05;与氟西汀组比较:◆<0.05,下表同
▼< 0.05control group;#< 0.05model group;■< 0.05Xiaoyao Powder group;□< 0.05Xiaoyao Powder group without ginger and mint group;▽< 0.05Xiaoyao Powder group without ginger, tuckahoe and mint group; ◆< 0.05fluoxetine group, same as below tables
3.1.2 糖水消耗量变化 如表2所示,与对照组比较,模型组大鼠糖水消耗率显著下降(<0.05),表明CUMS结合孤养造模降低大鼠糖水消耗率,模拟了抑郁症患者兴趣缺失症状。与模型组比较,各给药组大鼠糖水消耗率显著升高(<0.05),表明各给药组均可改善抑郁模型大鼠的兴趣缺失症状。各给药组大鼠糖水消耗率大小顺序依次为氟西汀组>逍遥散去生姜、茯苓、薄荷组>逍遥散去生姜、薄荷组>逍遥散组>加味逍遥散组,氟西汀与逍遥散去生姜、茯苓、薄荷组间无统计学差异,表明逍遥散去生姜、茯苓、薄荷组疗效与氟西汀组相当,且加味逍遥散组效果最弱。

表2 逍遥散及其加减方对大鼠糖水消耗率的影响()
3.1.3 敞箱实验 如表3所示,与对照组比较,模型组大鼠敞箱水平运动得分显著下降(<0.05),表明CUMS结合孤养造模可显著降低大鼠的情绪和自主活动能力,模拟了抑郁症患者的自主活动能力低下症状。与模型组比较,各给药组大鼠敞箱水平运动得分显著升高(<0.05),表明各给药组均可有效改善抑郁模型大鼠的自主活动能力低下症状。各给药组大鼠水平运动得分大小顺序依次为氟西汀组>逍遥散去生姜、茯苓、薄荷组>逍遥散去生姜、薄荷组>逍遥散组>加味逍遥散组,氟西汀与逍遥散去生姜、茯苓、薄荷组间无统计学差异,表明逍遥散去生姜、茯苓、薄荷组疗效与氟西汀组相当,且加味逍遥散组疗效最弱。
如表4所示,与对照组比较,模型组大鼠敞箱垂直运动得分显著下降(<0.05),表明CUMS结合孤养造模可显著降低大鼠的空间探索能力,模拟了抑郁症患者对新鲜环境好奇程度降低症状。与模型组比较,各给药组大鼠敞箱垂直运动得分显著升高(<0.05),表明各给药组均可改善抑郁模型大鼠对新鲜环境好奇程度降低症状。各给药组大鼠垂直运动得分大小顺序依次为氟西汀组>逍遥散去生姜、茯苓、薄荷组>逍遥散去生姜、薄荷组>逍遥散组>加味逍遥散组,且各组间大鼠垂直运动得分均无统计学意义,表明逍遥散去生姜、茯苓、薄荷组疗效与氟西汀组相当,加味逍遥散组疗效最弱。
3.2 逍遥散及其加减方对大鼠血浆中皮质酮水平的影响
如表5所示,与对照组比较,模型组大鼠血浆中皮质酮水平显著升高(<0.05),表明CUMS结合孤养造模显著升高大鼠血浆中皮质酮水平,造成下丘脑-垂体-肾上腺(hypothalamic-pituitary- adrenal,HPA)轴功能亢进,从而造成大鼠抑郁。与模型组比较,各给药组大鼠血浆中皮质酮水平显著下降(<0.05),表明各给药组均可改善模型抑郁大鼠HPA轴功能亢进,从而发挥抗抑郁作用。各给药组大鼠血浆中皮质酮水平高低顺序依次为氟西汀组>逍遥散去生姜、茯苓、薄荷组>逍遥散去生姜、薄荷组>逍遥散组>加味逍遥散组,且各组间血浆中皮质酮水平均有显著差异(<0.05),逍遥散去生姜、茯苓、薄荷组疗效与氟西汀组接近,加味逍遥散组疗效最弱。

表3 逍遥散及其加减方对大鼠敞箱实验水平运动得分的影响()

表4 逍遥散及其加减方对大鼠敞箱实验垂直运动得分的影响()

表5 逍遥散及其加减方对大鼠血浆中皮质酮水平的影响()
3.3 逍遥散及其加减方对大鼠皮质和海马中BDNF、5-羟色胺、多巴胺、NE水平的影响
如表6、7所示,与对照组比较,模型组大鼠皮质和海马中多巴胺、NE、5-羟色胺、BDNF水平显著降低(<0.05),表明CUMS结合孤养造模显著降低大鼠皮质和海马中单胺类神经递质多巴胺、NE、5-羟色胺及脑源性神经营养因子BDNF水平,从而造成大鼠抑郁。与模型组比较,各给药组大鼠皮质和海马中多巴胺、NE、5-羟色胺、BDNF水平显著上升(<0.05),表明各给药组均可提高抑郁模型大鼠皮质和海马中单胺类神经递质水平,且通过上调皮质和海马中BDNF水平,促进神经元的修复与再生,从而发挥抗抑郁作用。各给药组大鼠皮质和海马中多巴胺、NE、5-羟色胺、BDNF水平高低顺序依次为氟西汀组>逍遥散去生姜、茯苓、薄荷组>逍遥散去生姜、薄荷组>逍遥散组>加味逍遥散组,氟西汀组与逍遥散去生姜、茯苓、薄荷组间无统计学意义,表明逍遥散去生姜、茯苓、薄荷组与氟西汀组疗效相当,且加味逍遥散组疗效最弱。

表6 逍遥散及其加减方对大鼠皮质中多巴胺、NE、5-羟色胺、BDNF水平的影响()

表7 逍遥散及其加减方对大鼠海马中多巴胺、NE、5-羟色胺、BDNF水平的影响()
综上,逍遥散及其加减方抗抑郁作用为逍遥散去生姜、茯苓、薄荷组>逍遥散去生姜、薄荷组>逍遥散组>加味逍遥散组,其中逍遥散去生姜、茯苓、薄荷组抗抑郁作用最强,加味逍遥散组抗抑郁作用最弱,表明逍遥散中柴胡、当归、白芍、白术、甘草对抗抑郁作用影响较显著,其余药味对抗抑郁作用影响较弱。
4 讨论
逍遥散具有疏肝解郁、养血健脾之功效,是主治肝郁、血虚、脾弱等证的经典方剂,临床应用历史悠久,方中君药柴胡疏肝解郁,使肝气调达;当归养血和血,白芍养血敛阴、柔肝缓急,共为臣药。白术、炙甘草益气健脾,缓肝之急,茯苓利水消肿,为佐药;薄荷疏散风热,生姜温胃和中,为使药[21]。本方配伍立法于“调和”之中,调和肝脾,以“肝”为重。全方共奏疏肝调肝养肝、益气健脾之效[22]。本研究结果显示,逍遥散及其加减方抗抑郁作用依次为逍遥散去生姜、茯苓、薄荷组>逍遥散去生姜、薄荷组>逍遥散组>加味逍遥散组,其中逍遥散去生姜、茯苓、薄荷组抗抑郁作用最强,表明逍遥丸抗抑郁作用的主要药味为柴胡、白芍、当归、白术、甘草。研究表明,逍遥散的抗抑郁成分柴胡皂苷A、柴胡皂苷D、芍药苷、阿魏酸、甘草苷、甘草酸、白术内酯主要来源于柴胡、白术、当归、白芍、甘草5味药材[23-24],与本研究结果一致,从中医配伍、归经和活性成分角度阐明了柴胡、白术、当归、白芍、甘草5味药材为主要抗抑郁药味。
抑郁症又称抑郁障碍,是一种以持久性心境低落、兴趣缺失、自主意志活动减退、无快感体验、睡眠障碍为主的躯体症状综合征[25]。抑郁症形成原因复杂,其中竞争压力、不合理的生活习惯、对社会环境较弱的适应能力等原因尤为突出,其临床主要表现为情绪低落、食欲不振、兴趣缺失、自主意志活动减退等[26]。CUMS结合孤养抑郁大鼠模型是与临床抑郁症最接近的动物模型,在造模过程中将大鼠暴露于持续温和不可预见的刺激条件之下,充分模拟了抑郁症患者社会生活环境,诱导大鼠产生与抑郁症患者类似的行为学异常症状,如大鼠体质量降低模拟了抑郁症患者食欲不振、体质量减轻症状,糖水消耗率降低模拟了抑郁症患者兴趣缺失症状,敞箱运动得分减少模拟了抑郁症患者的自主活动能力低下症状等[27-29]。本研究采用CUMS结合孤养抑郁大鼠模型,通过行为学指标分析,探究逍遥散及其加减方的抗抑郁作用。结果显示,模型组大鼠行为学指标显著降低,表明抑郁模型大鼠造模成功;逍遥散及其加减方组大鼠行为学指标显著升高,表明逍遥散及其加减方具有抗抑郁作用。
抑郁症发病机制复杂,目前被广泛认可且研究较深入的假说包括单胺类神经递质、HPA轴功能亢进、神经可塑性[30]。其中单胺类神经递质为抑郁症最经典的一种假说,认为抑郁症的发生与大脑中枢神经系统内单胺类神经递质如5-羟色胺、多巴胺、NE等缺乏密切相关,是临床大部分抗抑郁药物的作用靶点[31];HPA轴功能亢进假说认为HPA轴功能亢进可导致机体皮质酮水平异常升高,高浓度的皮质酮与其受体结合后产生神经毒性,造成海马区神经元损伤,从而引起抑郁[32];神经可塑性假说认为BDNF参与调控神经细胞的生存、生长、分化和凋亡,可对抗应激状态下神经元的损伤,促进神经元的修复与再生,提高神经元的可塑性,其水平下降可导致抑郁症的发生[33-34]。基于中药复方多途径、多靶点的作用特点[35],本研究以HPA轴功能亢进假说中血浆皮质酮,单胺类神经递质假说中多巴胺、NE、5-羟色胺和神经可塑性假说中BDNF水平为考察指标,探究逍遥散及其加减方抗抑郁的作用机制。结果显示,模型组大鼠皮质和海马中多巴胺、NE、5-羟色胺、BDNF水平显著降低,血浆中皮质酮水平显著升高;各给药组大鼠皮质和海马中多巴胺、NE、5-羟色胺、BDNF显著升高,血浆中皮质酮水平显著降低,表明逍遥散及其加减方可能是通过抵抗HPA轴功能亢进、提高单胺类神经递质含量、提高神经元可塑性协同发挥抗抑郁作用,充分体现了中药复方多途径、多靶点、协同增效的作用特点。
综上所述,逍遥散及其加减方可能通过影响单胺类神经递质、HPA轴功能亢进、神经可塑性发挥抗抑郁作用,柴胡、当归、白芍、白术、甘草是逍遥散发挥抗抑郁作用的主要药味。
利益冲突 所有作者均声明不存在利益冲突
[1] 罗珺钰, 刘芳, 罗耀辉, 等. 抑郁症的中西医药物治疗进展 [J]. 云南中医中药杂志, 2019, 40(5): 84-87.
[2] Huang W Y, Meng X J, Huang Y,. Nitric oxide and cyclic guanosine monophosphate signaling mediates the antidepressant effects of acupuncture in the rat model of chronic unpredictable mild stress [J]., 2019, 25: 9112-9122.
[3] 陈炜, 蔡秋伶, 蒋凌飞, 等. 壮医佩戴疗法联合盐酸帕罗西丁片治疗抑郁症的临床疗效观察 [J]. 时珍国医国药, 2015, 26(12): 2949-2951.
[4] 凌佳, 吴梦瑶, 杨琴, 等. 下丘脑-垂体-肾上腺轴紊乱对焦虑性抑郁模型大鼠海马结构的影响 [J]. 基础医学与临床, 2018, 38(9): 1231-1238.
[5] 张涛, 赵芳, 张潇, 等. 复方柴归方抗抑郁作用及其调控5-羟色胺代谢途径机制研究 [J]. 中草药, 2018, 49(6): 1338-1344.
[6] 翟倩, 丰雷, 张国富, 等. 阿戈美拉汀治疗抑郁症的研究进展 [J]. 中国药房, 2019, 30(17): 2435-2440.
[7] 许腾, 张潇, 高耀, 等. 柴归颗粒对抑郁症伴发症状的改善作用研究 [J]. 中草药, 2019, 50(16): 3846-3851.
[8] 王睿, 何小燕, 马梁红. 舒肝解郁胶囊联合帕罗西汀治疗抑郁症的疗效观察 [J]. 天津药学, 2019, 31(4): 50-52.
[9] 赵洪庆, 杜青, 柳卓, 等. 不同抑郁模型大鼠行为学及神经营养因子表达的对比研究 [J]. 湖南中医药大学学报, 2019, 39(7): 822-826.
[10] 贺栋业, 张萍, 罗新星, 等. 抗抑郁药用植物研究进展 [J]. 现代生物医学进展, 2016, 16(13): 2552-2558.
[11] 王睿, 王琪, 金明顺, 等. 中药复方抗抑郁研究进展 [J]. 中国中医基础医学杂志, 2016, 22(3): 440-443.
[12] 宗阳, 陈婷, 董宏利, 等. 基于网络药理学四逆散治疗抑郁症的作用机制探讨 [J]. 中草药, 2019, 50(20): 4995-5002.
[13] 刘军莲, 李勇枝, 高建义, 等. 中医药抗抑郁研究进展 [J]. 中药材, 2008, 31(6): 931-934.
[14] 杨子博. 逍遥散治疗糖尿病的网络药理学分析[J]. 现代药物与临床, 2020, 35(9): 1733-1744.
[15] 刘进国, 杨亚峰. 加味逍遥散改善心理应激性失眠患者焦虑抑郁及睡眠质量的效果分析 [J]. 中国民间疗法, 2017, 25(3): 43-44.
[16] 倪付勇, 谢雪, 温建辉, 等. 茯苓非多糖类化学成分的抗补体活性 [J]. 中草药, 2019, 50(11): 2529-2533.
[17] 吴佳妮, 夏书雪, 李雪梅, 等. 薄荷标准汤剂的指纹图谱及成分分析 [J]. 中国实验方剂学杂志, 2019, 25(16): 128-134.
[18] 王清然, 周斌, 张泽安, 等. 栀子水提物致大鼠肝脏毒性的时效与量效关系 [J]. 中成药, 2017, 39(4): 689-694.
[19] 宣伟东, 卞俊, 袁兵, 等. 生姜化学成分的研究 [J]. 中草药, 2008, 39(11): 1616-1619.
[20] Lu S H, Guo J, Cai C,. Effects of Kaixin Powder on expression of 5-HT receptor in hippocampus of depressed rats induced by CUMS [J]., 2015, 7(2): 150-154.
[21] 李传朋, 刘玉, 魏品球, 等. 逍遥散及其类方与有效成分抗抑郁作用机制研究进展[J]. 中国实验方剂学杂志, 2020, 26(6): 243-250.
[22] 曹关月, 赵淑英, 王瑞霞, 等. 逍遥散在治疗绝经前后诸证中的临床应用[J]. 山西中医药大学学报, 2020, 21(1): 55-57.
[23] 李肖, 宫文霞, 周玉枝, 等. 逍遥散中抗抑郁有效成分及其作用机制研究进展 [J]. 中草药, 2015, 46(20): 3109-3116.
[24] 宫文霞, 周玉枝, 李肖, 等. 当归抗抑郁化学成分及药理作用研究进展 [J]. 中草药, 2016, 47(21): 3905-3911.
[25] Dillon D G, Pizzagalli D A. Mechanisms of memory disruption in depression [J]., 2018, 41(3): 137-149.
[26] 陈杰, 林小东, 刘立滢, 等. 表没食子儿茶素没食子酸酯对慢性温和不可预知应激抑郁小鼠的保护作用 [J]. 中草药, 2018, 49(6): 1351-1357.
[27] Shen Z F, Xu Y, Jiang X H,. Avicularin relieves depressive-like behaviors induced by chronic unpredictable mild stress in mice [J]., 2019, 25: 2777-2784.
[28] Zhang Y, Gu F H, Chen J,. Chronic antidepressant administration alleviates frontal and hippocampal BDNF deficits in CUMS rat [J]., 2010, 1366: 141-148.
[29] 高杉, 李苒. 抑郁症动物模型及其评价标准研究进展 [J]. 天津中医药大学学报, 2012, 31(1): 57-60.
[30] 张潇, 田俊生, 刘欢, 等. 抗抑郁中药新药研发进展 [J]. 中国中药杂志, 2017, 42(1): 29-33.
[31] 程雪, 郭忠信, 束会娟, 等. 神经营养因子在抗抑郁治疗中的作用研究新进展 [J]. 生命科学, 2019, 31(10): 1035-1040.
[32] 王学, 刘蓉, 罗杰, 等. 基于CUMS大鼠逍遥散拆方药队抗抑郁作用及BDNF/HPA机制研究 [J]. 中药药理与临床, 2018, 34(1): 14-19.
[33] Xie W J, Meng X B, Zhai Y D,. Antidepressant-like effects of the Guanxin Danshen formula via mediation of the CaMK II-CREB-BDNF signalling pathway in chronic unpredictable mild stress-induced depressive rats [J]., 2019, 7(20): 564.
[34] van den Buuse M, Buret L, Hill R. Involvement of brain-derived neurotrophic factor (BDNF) in the long-term memory effects of glucocorticoid stimulation during adolescence/young adulthood [J]., 2020, 377: 112223.
[35] 毕肖林, 马世堂, 狄留庆, 等. 中药药效物质筛选与辨识的研究思路及进展 [J]. 中草药, 2018, 49(22): 5229-5234.
Comparison on antidepressant effects of modified Xiaoyao Powder
LIN Ying-xian1, YANG Wen-jing2, CAO Ning-ning1, ZHAO Li-bin3, PEI Shuai1, CHEN Yu-zhou1, XIAO Xue-feng1
1. School of Chinese Materia Medica, Tianjin University of Traditional Chinese Medicine, Tianjin301617, China 2. Tianjin Tasly Pharmaceutical Co., Ltd., Tianjin 300402, China 3. Shanxi Zhendong Pharmaceutical Co., Ltd., Changzhi 047100, China
Antidepressant effect of Xiaoyao Powder (逍遥散) and its added and reduced formula were compared to simplify composition and clarify efficacy, with view to providing reference for the research and development of new antidepressant drugs.SD rats were randomly divided into control group, model group, fluoxetine (0.01 g/kg) group, Jiawei Xiaoyao Powder (16.20 g/kg) group, Xiaoyao Powder (10.13 g/kg) group, Xiaoyao Powder without ginger and mint (8.10 g/kg) group, Xiaoyao Powder without ginger, tuckahoe and mint (9.79 g/kg) group. Rats were given social isolation and chronic unpredictable mild stress to establish depression model. Concurrently, rats in control group and model group were ig normal saline, rats in the other group were ig corresponding drugs. Body weights, sugar preference rate, and opening behavior were observed after administration. Levels of corticosterone in plasma, dopamine, norepinephrine (NE), 5-hydroxytryptamine, brain derived neurotrophic factor (BDNF) in cortex and hippocampus were detected by ELISA.Behavioral of rats were significantly decreased (< 0.05), levels of dopamine, NE, 5-hydroxytryptamine and BDNF were significantly reduced (< 0.05), level of corticosterone was significantly increased in model group (< 0.05). Compared with model group, behavioral of rats were significantly increased (< 0.05), levels of dopamine, NE, 5-hydroxytryptamine and BDNF were significantly increased (< 0.05), level of corticosterone was significantly decreased in the administration groups (< 0.05), Xiaoyao Powder without ginger, tuckahoe and mint group had the best effect.Xiaoyao Powder and its added and reduced formula improve the symptoms of depression, Xiaoyao Powder without ginger, tuckahoe and mint has the strongest antidepressant effect.,,,, andetare the main compatibility of Xiaoyao Powder determining the effect of antidepressant.
Xiaoyao Powder; antidepression; chronic unpredicted mild stress;;;;;et
R285.5
A
0253 - 2670(2021)01 - 0137 - 08
10.7501/j.issn.0253-2670.2021.01.017
2020-06-01
国家自然科学基金资助项目(81973557);国家科技重大专项(2018ZX09303-024);国家科技重大专项(2018ZX09737-019)
林映仙(1992—),女,硕士,从事中药新药和药动学研究。Tel: 15202201879 E-mail: llinluoluo@163.com
肖学凤(1966—),女,教授,博士生导师,从事中药新药和药动学研究。Tel: (022)59596237 E-mail: kai1219@163.com
[责任编辑 李亚楠]
