利用铜片置换法回收含银废液中银的工艺实践
2021-01-05郑学军王涵睿史智锋孟志军蔡兴顺
郑学军,王涵睿,史智锋,董 蔚,孟志军,贺 慧,蔡兴顺
(1. 西部金属材料股份有限公司,陕西 西安 710201)(2. 西安诺博尔稀贵金属材料股份有限公司,陕西 西安 710201)
1 前 言
贵金属银具有良好的导电性、导热性及延展性,被广泛地应用于半导体、电子、化工等方面,市场需求量大。但是银在地壳中的含量稀少,直接提取的产量小,无法满足市场需求,因此银的二次资源回收占有举足轻重的地位[1]。从各种废料及阳极泥中回收的银,其纯度大部分不能满足工业生产,需要通过电解精炼后才能达到99.95%以上。在电解精炼过程中,电位比银负的锌、铁、铜、镍等贱金属也会发生阳极溶解,随之进入电解液中。在含量极微时,对电解过程影响不大,但随着逐渐积累会使电解液遭受污染,最终影响电解银粉的纯度,因此电解液需要定期更换,随之会产生大量的含银废液[2]。
含银废液的净化方法有很多,例如结晶法、氢氧化钠沉淀法、热分解法、铜置换法等[3]。铜置换法是重要的净化工艺之一,其利用铜和银标准电极电位的差异(银比铜的电极电位高),使得银被置换出来,而Pb2+、Ni2+、Bi3+、Sb3+等杂质离子的标准电极电位比铜低,仍留在溶液中,从而使银和其他杂质分离,其优点是可以脱除铜、铅、铋等多种杂质,但此法产出的银粉纯度低,银粉中铜含量高,纯度约在80%[3, 4]。本文针对铜置换法净化含银尾液存在的问题,提出采用铜片置换法处理含银尾液,研究了置换溶液pH值、置换时间、置换温度对置换过程的影响,并分析置换机理,确定了铜片置换法处理含银尾液的最优工艺条件。
2 实 验
2.1 实验原料与装置
本实验用水为去离子水,所用铜片尺寸为100 mm×15 mm×2 mm,所采用的含银废液为银电解废液,其成分如表1所示。

表1 含银废液成分Fig.1 Chemical composition of silver waste liquid
实验仪器主要有SPECTRO ARCOS ICP-OES光谱仪、AR224CN型电子天平、恒温电热套(温差±0.5 ℃)、2500 mL三颈烧瓶、冷凝器、pH电位计。
2.2 实验方法
实验在室温下开始,每次取1500 mL试液和一定量铜片放入三颈烧瓶中进行置换反应,烧瓶上装有冷凝器、温度计、取样口,用碳酸钠和硝酸调节溶液pH值。到设定实验条件(pH、时间、温度)后取样,整个反应过程可以观察到银在铜表面的析出、剥落,静置过滤后,利用光谱仪分析置换后溶液中Ag,Cu,Fe等元素的含量。置换后的银粉经洗涤烘干后,利用光谱仪分析国标中要求各杂质元素含量,将结果与GB/T 4135—2016对比,得到银粉纯度。
3 结果与讨论
3.1 溶液pH值对置换率的影响
在温度为30 ℃、置换时间为5 h的条件下,进行了pH值对置换率的影响的实验研究,其结果如图1所示。可以看到,pH值的持续增加对铜置换银的过程是不利的,随着pH值的增加,置换率呈现先增加再降低的趋势。pH值在1.5以下时,置换率随着pH值的增加而明显增加,当pH值从1.3增至1.5,置换率从87.5%增加至93.1%;当pH值从1.5增至2.0,置换率从93.1%降低至86.3%,可见pH值对铜置换银的过程有着显著影响。随着pH值的降低,也会使部分铜片直接溶解,造成置换过程耗铜量的增加。选择pH值在1.5~2进行置换反应较为合适。
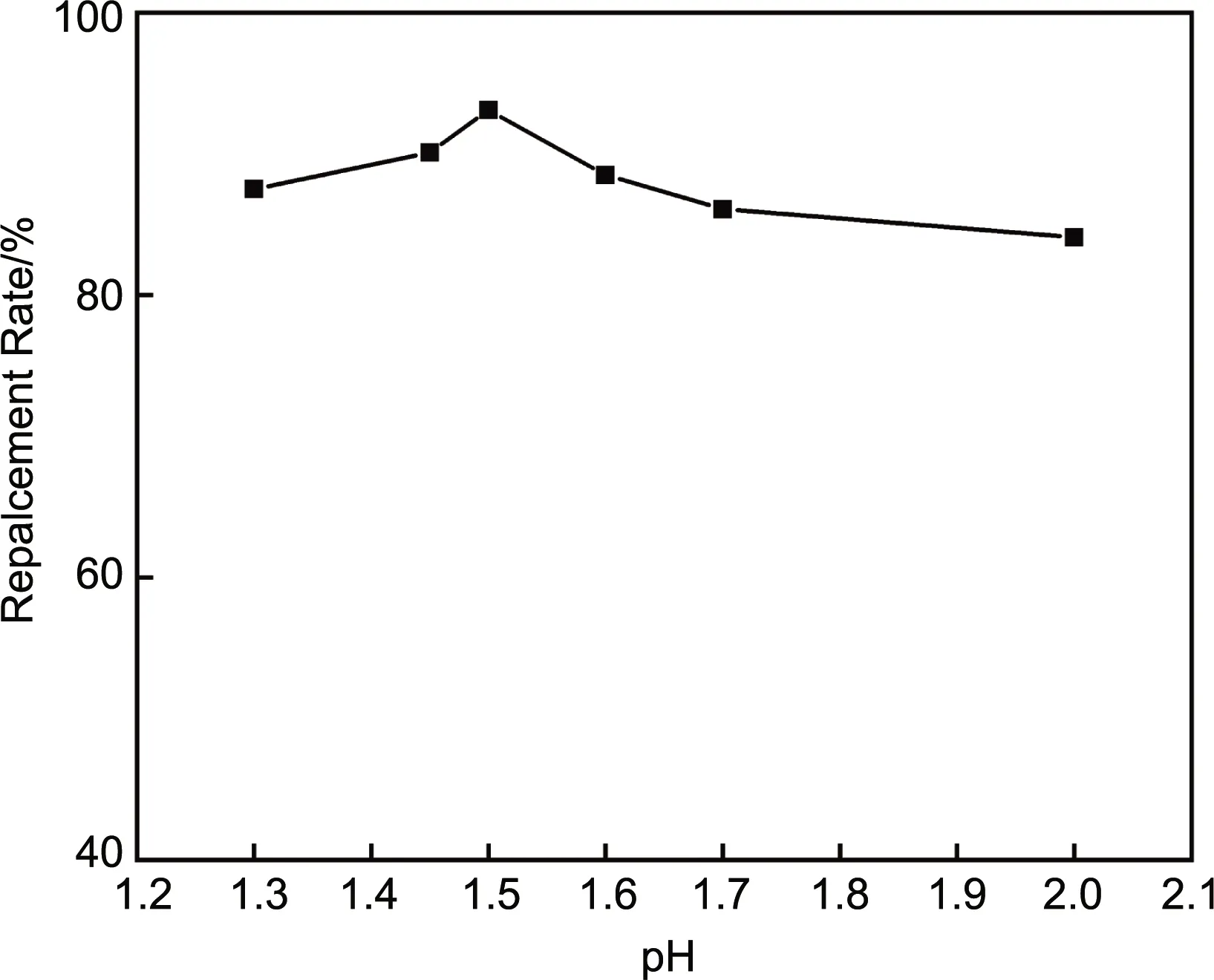
图1 pH值对置换率的影响Fig.1 Effect of pH value on replacement rate
3.2 时间对置换率的影响
在pH值为2、温度为30 ℃的条件下,进行了反应时间对置换率的影响的实验研究,其结果如图2所示。可以看到,置换率随反应时间的延长而增加。初始阶段的反应速度非常迅速,当反应进行至10 min时,银的置换率迅速提高到25.8%;在反应进行60 min后,银的置换率几乎接近64%;进一步延长反应时间,置换率则缓慢增大,溶液中的硝酸铜含量不断增加,导致反应速率变慢。如果出现硝酸铜结晶,会包裹在铜片和银粉上,难以洗涤,导致纯度和收率变低。由此可说明,铜置换银的反应速率随着时间的延长呈现初始急剧增加而后平稳增加的趋势,可见本实验采用5 h能够满足反应完全的条件。经置换后的溶液,银离子浓度由72降低至0.02 g/L,对置换得到的银粉分析可得,纯度大于98.5%,收率达到99.7%。
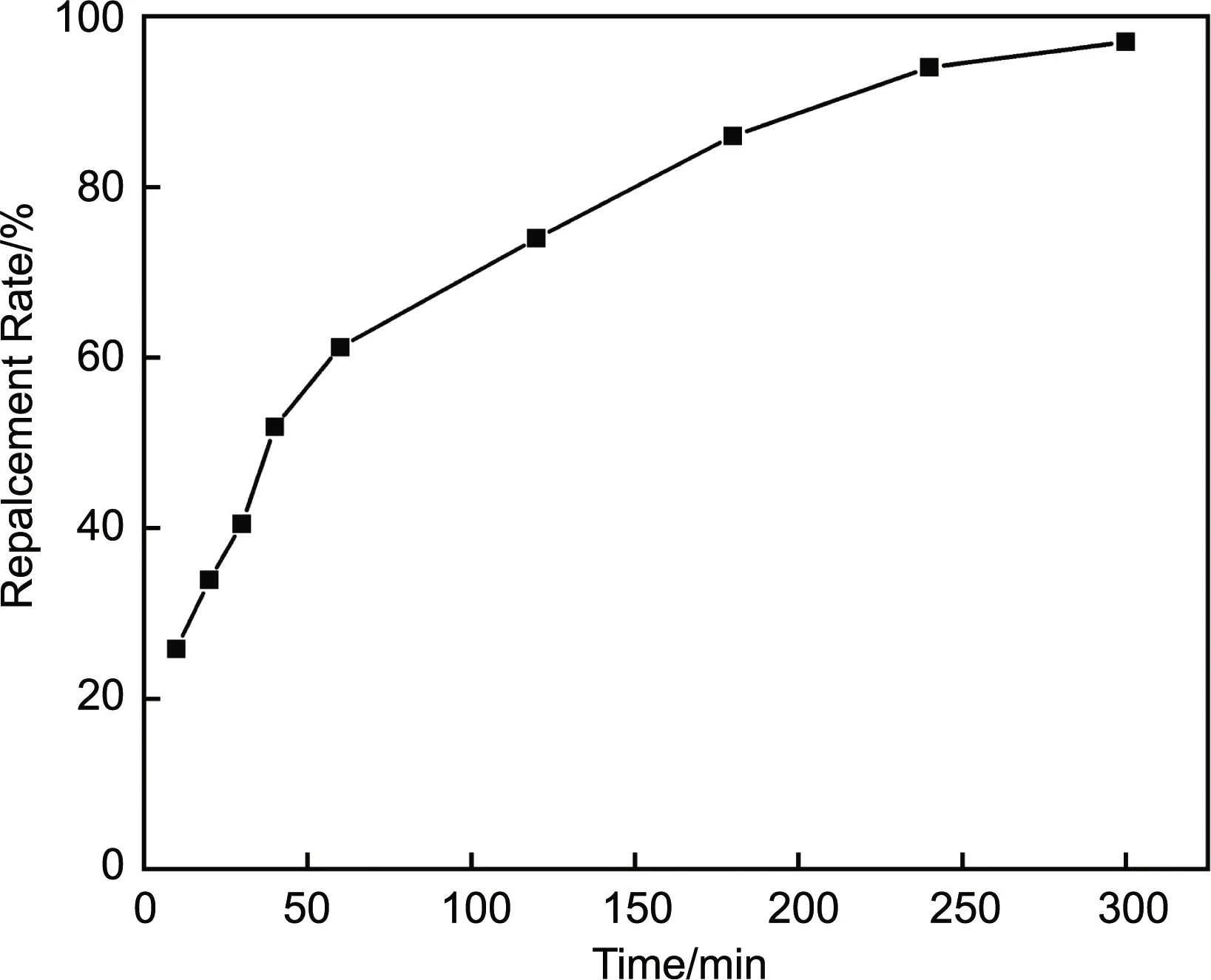
图2 时间对置换率的影响Fig.2 Effect of time on replacement rate
3.3 温度对置换速率的影响
在pH值为2、置换时间为5 h的条件下,进行了反应温度对置换速率的影响的实验研究,用log(Co/Ct)对时间t作图,Co为反应初始溶液浓度,Ct为反应某一时刻溶液浓度,其结果如图3所示。随着温度的升高,直线斜率增大,反应速度加快,符合置换规律。这是由于开始一段时间铜的表面沉积物很少,贵金属银离子浓度比较大,传质较快;随着置换沉积物增多,离子扩散变为反应的限制步骤,速度减慢。在初始阶段,40 ℃以上条件的置换速率明显提高,因此置换温度选在40 ℃以上。

图3 温度对置换速率的影响Fig.3 Effect of temperature on reaction rate
3.4 置换过程分析
铜的标准电极电势为+0.34 V,银的标准电极电势为+0.799 V,铜置换银的标准电动势为0.459 V,因此铜置换银的反应可自发进行。从动力学上,铜置换银的反应首先是由铜与银离子组成氧化还原体系,铜片上的铜失去电子,被溶解下来,溶液中的银离子得到电子,不断在铜片上生长。随着置换反应的进行,银颗粒逐渐长大,形成片状或块状从铜片表面脱落至溶液中;贵金属离子半径较大,移动缓慢,而溶液中的铜离子逐渐增多,贵金属银离子逐渐减少,反应速率变慢,即银的电极电位不断降低,铜的电极电位不断升高,当二者的电动势为零时,反应终止。
实际生产中,可添加搅拌装置,用以加快反应速率。置换后尾液可加热至50~60 ℃,用碳酸钠进行沉铜,生产的碱式碳酸铜可通过粗铜冶炼回收铜,沉铜尾液送污水系统进行处理。
4 结 论
(1)铜片置换法对银和其他贱金属杂质有良好的分离效果,经置换后,含银废液中的银离子浓度由72降低至0.02 g/L;采用铜片置换银,可以显著提高置换后银粉的纯度(纯度大于98.5%),收率达到99.7%。
(2)随着pH值的增加,置换率呈现先增加再降低的趋势,pH值过高或者过低均不利于置换反应进行;随着时间的延长,废液中的银可以被置换得很完全;温度的升高则会加快置换反应速度。
(3)在铜置换银的过程中,易出现硝酸铜结晶,会影响银的纯度和收率。
(4)该工艺流程短,设备简单,适用于含银废液的处理,置换后的银粉可以用于电解母液的制备或者二次电解。
