胰腺癌放射治疗专家共识(2020年版)*
2020-12-30胰腺癌放射治疗专家共识协作组2020
胰腺癌放射治疗专家共识协作组(2020)
近年来,胰腺癌发病率在国内外均呈明显上升趋势,据世界卫生组织统计,美国癌症协会2018年发布的数据显示,美国胰腺癌新发病例数男性列第11位,女性列第8位,居恶性肿瘤病死率第4位[1]。中国国家癌症中心最新统计数据显示,胰腺癌位居中国恶性肿瘤发病率的第10位,居恶性肿瘤病死率第6位[2]。
胰腺癌恶性程度高预后差,手术是其根治性治疗手段,但由于胰腺癌起病隐匿,发展迅速,解剖位置特殊,邻近大血管,80%的患者在初诊时已无法接受根治性手术治疗。因此,手术切除率仅为15%~20%。然而,即便是手术切除的患者,局部及区域复发率仍高达60%,5年生存率仅为3~15%[3]。因此,放化疗综合治疗,逐渐成为临床各期胰腺癌治疗的重要手段。
由于胰腺周围有众多消化道器官,导致传统放射治疗技术难以提高肿瘤照射剂量,限制了放射治疗在胰腺癌综合治疗中的价值。近年来,随着直线加速器、射波刀(Cyberknife)及螺旋断层放射治疗系统(Tomotherapy,TOMO)等精确放射治疗设备精确与技术快速发展,放射治疗在保护好周围正常组织的前提下,能够不断提高肿瘤局部放射治疗剂量,达到与手术相似的根治性治疗目的[4]。
目前,在众多胰腺癌治疗相关学会制订的胰腺癌诊治指南、共识或规范中,尚缺少对胰腺癌放射治疗系列问题的详细阐述。因此,专家组联合多家医院放疗科专家,通过查阅文献,结合自身临床经验,对国产和进口放射治疗设备,包括直线加速器、伽马刀及放射治疗计划系统(treatment planning system,TPS)等的各种物理参数、质检设备及应用情况详细调研,共同制订了《胰腺癌放射治疗共识》。本共识旨在使从事胰腺癌诊治的临床医生,了解放射治疗在胰腺癌综合治疗中的作用,清楚胰腺癌疾病进程不同阶段放射治疗在其治疗中的价值,并使从事放射治疗的医务人员规范掌握胰腺癌放射治疗的适应证、放射治疗实施过程的具体问题,从而使更多的胰腺癌患者能从放射治疗中获益。本共识仅对胰腺癌放射治疗部分进行论述,不讨论其诊断及其他治疗方式。
1 胰腺癌分期(AJCC分期第八版)
胰腺癌分期[美国抗癌协会(American Joint Committee on Cancer,AJCC)分期第八版]适用于胰腺导管腺癌、腺泡细胞癌、导管内乳头状黏液性肿瘤伴有浸润癌、导管内管状乳头状肿瘤伴有浸润癌、胶样癌、黏液性囊性肿瘤伴有浸润癌、神经内分泌癌以及胰母细胞瘤。胰腺癌TNM定义见表1,胰腺癌预后分期见表2。
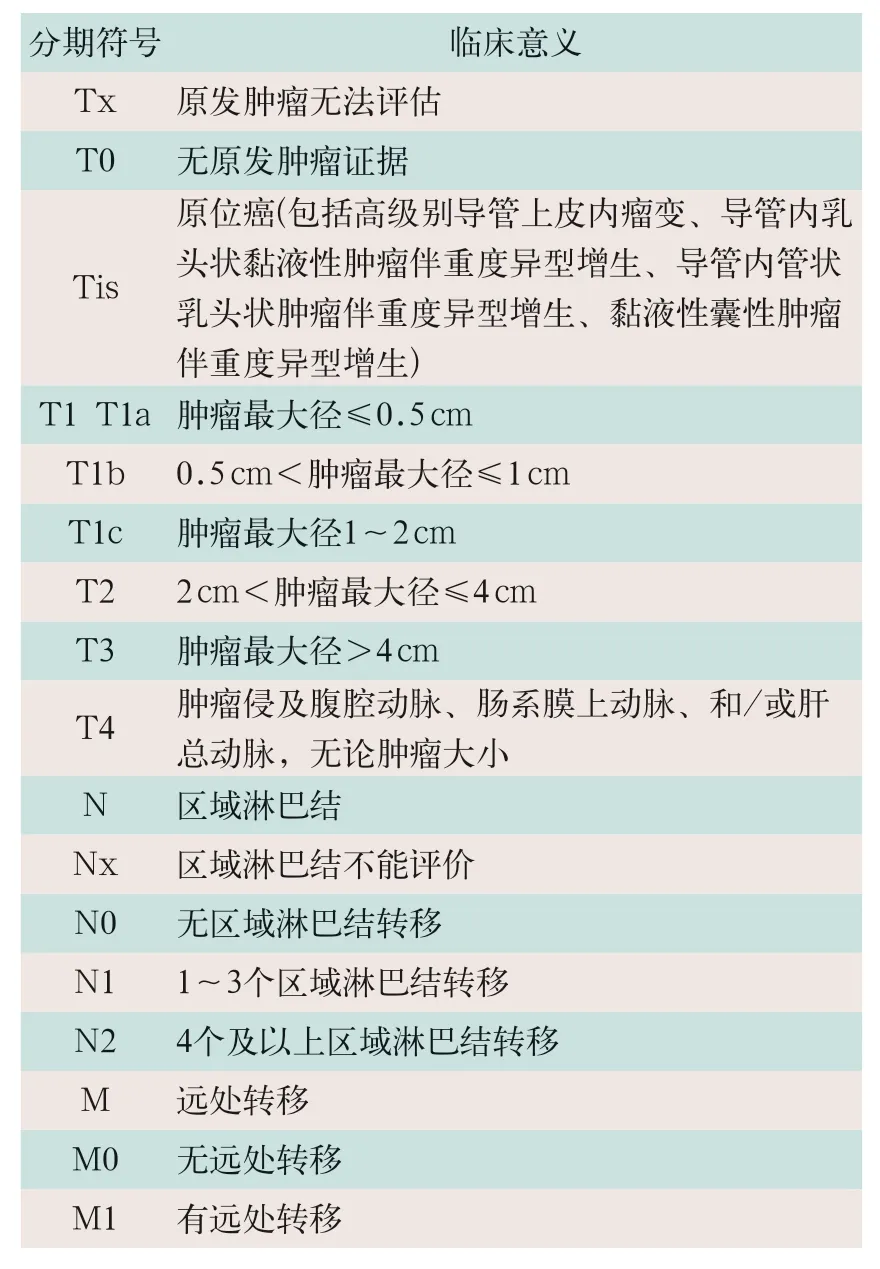
表1 胰腺癌TNM定义
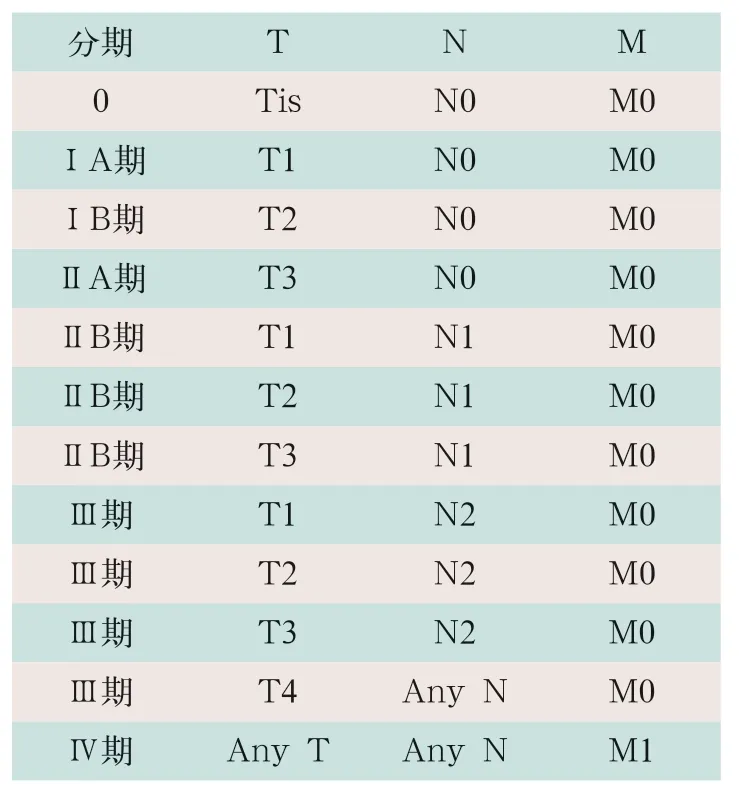
表2 胰腺癌预后分期
2 胰腺癌放射治疗适应证
2.1 胰腺癌术后放射治疗
早期胰腺癌以手术治疗为主,术后辅助治疗推荐行辅助化疗。术后根据病理及切缘情况,决定是否给予辅助放射治疗。迄今为止,各大指南及诊疗规范不推荐胰腺癌根治术后常规进行辅助放射治疗,具有以下高危复发因素的患者建议行术后放射治疗:淋巴结转移,尤其是淋巴结包膜外浸润;切缘阳性(R1);局部有病灶残留(R2)。
术后放射治疗照射范围包括瘤床、吻合口以及临近淋巴引流区。靶区勾画参考美国放射治疗肿瘤协作组(radiation therapy oncology group,RTOG)胰腺癌术后靶区勾画共识[5]:①腹腔干动脉自腹主动脉发出的1.5 cm部分,并三维外扩1 cm;②肠系膜上动脉自腹主动脉发出的2.5~3.0 cm部分,并三维外扩1 cm;③门静脉(自肠系膜下静脉汇入处至肝门部分分叉为左右门静脉处,包括胆肠吻合和肝管空肠吻合部以及肝门淋巴结),并三维外扩1 cm;④部分腹主动脉自上述腹腔动脉、门静脉或胰腺空肠吻合部区域的最上层,至腰2椎体下缘,如术前肿瘤下缘超过腰2椎体下缘,则下界需要延伸至腰3椎体下缘。左侧外扩2.5~3.0 cm,右侧外扩1 cm,前方外扩2.5~3.0 cm,后方至椎体前缘或前缘后0.5 cm。已行根治术的胰腺尾部或体部肿瘤,术后辅助放射治疗靶区应包括术后切缘+区域淋巴结,不需要包括门静脉周围或肝门区域淋巴结。
对于术后辅助放射治疗,推荐常规分割剂量,术后立体定向放射治疗(stereotactic body radiation therapy,SBRT)目前仅用于临床试验。放射治疗总剂量推荐45~46 Gy/(23~25次,周),适当的给予瘤床、吻合口局部加量5~9 Gy,同步化疗(首选卡培他滨口服,或者持续静滴氟尿嘧啶,其次吉西他滨)。美国约翰霍普金斯医院和梅奥诊所一项包括1200余例胰腺癌术后患者的回顾性研究结果显示,无论切缘如何,术后接受氟尿嘧啶同步放化疗的患者较观察的患者生存获益切缘阴性(RR,0.61;95%置信区间(confidence interval,95%CI)为0.47~0.77;切缘阳性(RR,0.52;95%CI为0.36~0.74;P<0.001)[6]。
2.2 可切除胰腺癌行新辅助放射治疗
对于临界可切除或部分局部晚期胰腺癌,一般在新辅助化疗后行同步放化疗[7-8]。同步放化疗推荐剂量为45~54 Gy/(25~30次,5~6周),也有采用36 Gy/(15次,3周)。对于部分不适合全身化疗的局部晚期患者,可以单独进行SBRT。既往研究发现,对于潜在可切除胰腺癌,经术前联合放化疗治疗后,可使患者获得根治性切除机会,达到切缘阴性,明显延长疾病复发时间及生存期,5年生存率>20%[9]。SFRO-FFCD 9704 Ⅱ期单臂临床试验采用总剂量50 Gy/(25次,5周)分割模式联合5-Fu术前新辅助治疗,26例接受根治性手术切除,R0切除率达80.7%,2年生存率32%[10]。另一项II期随机对照试验,采用总剂量55.8 Gy/(31次,7周),或50.4 Gy/(30次,6周)新辅助放射治疗联合化疗对比单独手术,中位总生存时间(OS)分别为25.0个月和18.9个月(P>0.05)[11]。PREOPANC研究是一项随机对照多中心Ⅲ期的临床研究,其目的是明确可手术胰腺癌患者术前行新辅助放射治疗对患者OS和R0切除率有无改善。246例入组患者随机分为两组,术前放化疗组119例,直接手术组127例。放化疗组采用2.4 Gy/次,共15次,同步吉西他滨单药化疗(1000 mg/m2,在第1 d、8 d和15 d给药),研究结果在2020年初发表于JCO杂志,术前放化疗组中位生存时间为16.0个月,直接手术组中位生存时间为14.3个月,两组手术切除率分别为61%和72%。术前放化疗组R0切除率为71%,直接手术组为40%(P<0.001)。术前放化疗可显著提高无病生存期和局部无复发间隔时间,并显著降低术后淋巴结、神经系统和静脉侵犯的发生率。对完成手术切除+辅助化疗的预先设定的亚组分析显示,新辅助放化疗可提高患者生存期,两组生存期分别为35.2个月和19.8个月(P<0.05)。两组发生严重不良事件的患者比例差异不大。
2.3 局部晚期胰腺癌根治性放射治疗
如不能通过降期达到手术切除的患者,推荐全身化疗+常规分割同步放化疗或SBRT[13-15]。靶区包括原发肿瘤和转移的淋巴结。同步放化疗推荐剂量为45~54 Gy/(25~30次,5~6周),如果选择做SBRT,放射治疗剂量及分割次数尚未达成统一意见。文献报道一般是25~45 Gy/(3~5次,1周)[16]。SBRT以分次剂量高和治疗次数少为特点,靶区内高剂量,靶区外低剂量,从而提高肿瘤剂量,同时不会对正常组织造成严重放射损伤。此外,放射治疗后肿瘤细胞发生再增殖起始时间多在3~5周后,而SBRT治疗次数少,多在数日至两周内完成,因此避免了肿瘤细胞出现加速再增殖,从而利于局控率的提高。因而,SBRT已日益成为一种极具吸引力的放射治疗技术,并逐步在胰腺癌中得到广泛应用。但是,如果在CT、MRI和(或)内窥镜检查中发现肠道或胃的直接侵犯,则不能进行SBRT治疗。美国国家癌症数据库(National Cancer Data Base,NCDB)一项回顾性分析显示,988例局部晚期胰腺癌患者接受SBRT治疗与常规分割放射治疗相比,中位O S 分别为1 3.9 个月和1 1.6个月(P<0.001),2年OS分别为21.7%和16.5%(P<0.001)[17]。2017年发表的一篇回顾性研究文章共纳入19项研究,包括1009例患者,在13项数据可用的研究中,1年OS为51.6%,OS中位时间从5.7~47个月(平均为17个月)。1年的局部控制(local control,LC)率为72.3%。一项前瞻性临床试验结果表明,与常规同步放化疗相比,SBRT极大降低了辐射引起的严重淋巴细胞减少,两组淋巴细胞减少率分别为13.8%和71.7%(P<0.001)[18]。总体而言,SBRT严重不良事件的发生率<10%[19]。
SBRT、TOMO等精确放射治疗技术的应用逐步提高了胰腺癌的放射治疗剂量,减少了照射次数,使得局部控制率、疼痛缓解率及生存率都获得了改善。目前,用于治疗胰腺癌的SBRT技术为真正意义的立体定向放射治疗、三维适形放射治疗和体部伽马刀治疗。在技术的选用上不同医院不同设备配制略有不同。现有国产放射治疗加速器,在进行三维适形放射治疗及普通调强放射治疗方面可满足临床需求,但无法有效实现SBRT和容积旋转调强放射治疗(volumetric modulated arc therapy,VMAT)技术。对于国产放射治疗设备,由于国产加速器输出剂量率不稳定,波动范围大,相同子野分布情况下,国产加速器治疗时间长于进口加速器。在标准条件下,国产加速器Gamma(2,2)通过率明显低于进口加速器。因此,现阶段国产放射治疗设备尚无法在不增加正常组织照射剂量的前提下有效提高胰腺肿瘤照射剂量,只能进行常规分割剂量放射治疗,故不推荐采用国产直线加速器进行胰腺癌SBRT治疗。国产体部伽马刀在胰腺癌SBRT治疗中的开展应用更多见于国内县市级三甲以下医院的放射治疗中心,国内大部分文献报道伽马刀放射治疗患者涵盖胰腺癌各个期别,不单单局限于局部晚期胰腺癌。单次分割剂量通常为3~5 Gy,共照射8~15次,联合或不联合化疗,中位生存期7~18个月,1年生存率为22%~48%,分期不同,预后有很大差别,而且目前的文献多为单中心、回顾性研究,证据级别不足,尚缺乏使用伽马刀进行胰腺癌SBRT治疗的高级别循证医学证据。
2.4 姑息放射治疗
姑息放射治疗可应用于胰腺癌原发灶或转移灶的减症治疗。对于非转移性或转移性胰腺癌,姑息放射治疗的目的是缓解疼痛和出血或改善患者局部梗阻性症状[20]。胰腺癌常伴有严重腹背疼痛,对于使用吗啡仍不能缓解疼痛的患者,或由于使用大剂量吗啡而无法耐受便秘等严重不良反应的患者,可以采用姑息放射治疗来镇痛,即使合并远处转移的胰腺癌,姑息性放射治疗同样可以缓解疼痛。有文献[21]报道,对20例年龄>75岁且无法手术的患者,采用总剂量30~36 Gy/(3~5次,1周)的照射方式,中位生存达6.5个月。对于转移性病变引起的剧烈疼痛如骨转移,也可以给予姑息放射治疗,总剂量为30 Gy/(10次,2周)。目前,国产放射治疗设备完全满足姑息放射治疗的要求,即便考虑到国产加速器散射线的影响,其总体放射剂量偏低,常规姑息治疗放射治疗剂量<45 Gy,因此并不因为危及器官(organ at risk,OAR)限量而影响姑息放射治疗效果。建议对于以姑息止痛、缓解梗阻等为治疗目的的胰腺癌患者,放射治疗剂量为18~45 Gy。对治疗效果较好,出现肿瘤明显缩小而又无严重放射性损伤的患者,可给予>50 Gy的照射剂量。
3 放射治疗前模拟定位
患者仰卧位,双手上举,平躺在固定装置中。推荐CT增强扫描,层厚2~3 mm。扫描范围从T4/T5至L5/S1。如果模拟定位前口服造影剂,建议每次治疗前饮相同量的水保持胃部形态体积一致。有部分学者认为,现代多期增强扫描CT定位,不建议口服造影剂以减少位移变量。
对于局限期的胰腺癌(可切除的、交界性的、局部进展期),如果给予患者SBRT治疗,推荐胰腺肿瘤及其周边植入金标1~5枚(理想≥3),每日影像引导放射治疗,给予肿瘤配准。推荐在影像引导放射治疗同时采用呼吸门控技术。若无呼吸门控,则推荐采用四维CT(4D-CT)来构建个体化内靶区(inner target volume,ITV)。
4 胰腺癌放射治疗质量控制
针对国产设备,胰腺癌放射治疗质量控制更需全流程质量控制,包含模拟定位系统质量控制、放射治疗设备质量控制、TPS质量控制、放射治疗计划质量控制、放射治疗实施质量控制、图像引导质量控制、肿瘤运动管理质量控制等。
4.1 模拟定位系统质量控制
对于CT模拟机不仅定期检测图像、几何性能指标,还需检测长期工作的稳定性,如CT值稳定性、扫描剂量稳定性。对于胰腺癌患者,摆位辅助装置普遍采用真空负压装置,部分采用负压设备,要定期检查负压装置的密封性、形状变化、腹压设备参数以及减少辅助装置带来的摆位误差。
4.2 放射治疗设备质量控制
放射治疗设备安装后应对放射治疗设备进行详细的测试,应包含机械、剂量、图像引导、安全联锁等。在按照既定方案完成厂家TPS所需的加速器基础数据采集、修正和验证之后,要对设备进行临床综合评估并建立基线文档,以提供日常质量保证参考。定期对放射治疗设备进行质量控制,对设备基本参数(包括等中心、多叶准直器、影像中心、加速器等中心)做稳定性检测。
4.3 TPS质量控制
对于国产TPS需要做详细、全面的质量控制,其中包含图像CT值有无失真、图像重建精度以及勾画准确性。根据调研发现,国产TPS普遍存在图像精度差,靶区边缘模糊的现象,因此定期测试靶区体积和位置重建精确度,尤其是在TPS软硬件相关模块或组件更换、升级之后需要对相关性能重新测试。TPS算法需要评估、测试,尤其针对密度不均匀和空腔脏器等。针对TPS,使用前应进行一次End To End的全流程测试。
4.4 放射治疗计划及实施质量控制
胰腺癌调强计划,尤其是单次大剂量放射治疗前进行放射治疗计划质量控制,推荐更严格的标准(如3%、2 mm的Gamma分析参数),对质量控制结果做分析、统计,即使达到质量控制标准,也希望发现放射治疗计划乃至整个放射治疗系统改进之处。
放射治疗实施过程需要有详细、规范的操作指南和培训,有治疗记录,要求放射治疗系统有放射治疗实施信息,包含治疗患者、治疗计划、执行时间、操作人员、执行情况及机器运行参数。
运动管理质量控制。肿瘤运动是胰腺癌放射治疗的难点之一,其原因很多,如呼吸、疼痛、体型等原因,可适当采用加腹压强制浅呼吸方法或其他相关控制呼吸运动方法,减少运动造成靶区移位。对于有条件施行呼吸门控的单位,至少每月检测射束输出量一致性、相位和(或)振幅射束控制及呼吸监控系统,每年至少检测一次射束能量一致性、相位和(或)振幅门控窗的时间精度和对呼吸相位/振幅替代装置的校准。
4.5 图像引导质量控制
图像引导是胰腺癌精准放射治疗的有效保证手段之一,国产设备的图像引导多采用正、侧位拍片,需要良好的图像质量以及经验丰富的技术人员做配准。在现有技术条件下,4D-CT是最易实施和接受的技术手段,国产放射治疗模拟定位机普遍缺少4D-CT,因此无法根据呼吸运动来排除运动误差的影响。目前,在临床使用的国产加速器缺少锥形束CT(CBCT)模块,不能有效减少摆位误差。因此,要建立严格的放射治疗质量控制制度和标准,规范放射治疗流程管理,防止进一步扩大由于技术缺陷所造成的误差。
各单位应完善质量控制设备,对相关质量控制设备定期校准。根据开展的放射治疗计划,配备合理的质量控制设备,如三维水箱、电离室、胶片等,其他的质量控制工具如固体水、精密水平仪、光敏探测器及仿真模体等,开展单次大剂量的需要增配小野数据测量设备以及高分辨的计划验证设备。此外,放射治疗质量控制也包括对放射治疗医生在放射治疗靶区勾画、放射治疗计划设计、放射治疗技术应用和放射治疗辅助设备应用等方面的质量控制。
5 其他注意事项
胰腺癌术后辅助治疗。如果术前未行新辅助治疗,术后无肿瘤复发及转移证据,建议先行化疗,然后同步放化疗以及序贯化疗[22]。对于临界可切除胰腺癌和局部进展期胰腺癌,一般推荐在2~6个周期化疗之后进行放射治疗[21]。推荐新辅助放化疗后4~8周进行手术,但放射治疗所致的纤维化可使手术难度增加。放射治疗期间推荐预防性应用止吐药物以减少恶心、呕吐的发生。
目前的国产加速器可以满足胰腺癌三维适形与普通调强常规分割剂量放射治疗临床需求,但不建议行单次2.5 Gy以上的低分割放射治疗及SBRT放射治疗。
6 结论
胰腺癌是恶性度非常高的肿瘤,手术是根治性手段。术后化疗是常规治疗方式,存在高危因素的患者需要术后辅助放射治疗。对于不能手术切除的患者,除了化疗以外,放射治疗占有非常重要的地位。本共识对不同分期的胰腺癌放射治疗适应证进行归纳,阐述不同放射治疗技术及分割剂量对患者生存的影响。同时,本共识详述胰腺癌放射治疗前定位流程、靶区勾画以及对胰腺癌放射治疗质量控制进行规范,对不同级别医院开展胰腺癌放射治疗具有指导作用。
胰腺癌放射治疗专家共识(2020年版)编审委员会委员名单
主任委员:董丽华(吉林大学第一医院)
副主任委员(按姓氏拼音排序):
高献书(北京大学第一医院)、康静波(解放军总医院第六医学中心)、曲宝林(解放军总医院第一医学中心)、王若雨(大连大学附属中山医院)、曾昭冲(复旦大学附属中山医院)
秘书:丁丽娟(吉林大学第一医院)
委员(按姓氏拼音排序):
蔡博宁(解放军总医院第一医学中心)、陈波(中国医学科学院肿瘤医院)、陈一兴(复旦大学附属中山医院)、邓立勇(长沙市中心医院)、杜乐辉(解放军总医院第一医学中心)、杜世锁(复旦大学附属中山医院)、胡凯(广西医科大学附属第一医院)、姜新(吉林大学第一医院)、黎功(清华大学附属北京清华长庚医院)、李平(四川大学华西医院)、李玉(解放军总医院第一医学中心)、梁平(广西中医药大学附属瑞康医院)、梁世雄(广西医科大学附属肿瘤医院)、刘孟忠(中山大学肿瘤防治中心)、刘施亮(中山大学肿瘤防治中心)、刘小亮(解放军总医院第一医学中心)、陆海杰(厦门大学附属中山医院)、马娜(解放军总医院第一医学中心)、孟岩(上海东方肝胆医院)、苏廷世(广西医科大学附属肿瘤医院)、孙菁(复旦大学附属中山医院)、孙建国(陆军军医大学附属第二医院)、王阁(陆军特色医学中心)、王辉东(吉林大学第一医院)、王竞(解放军总医院第一医学中心)、王建华(河南省肿瘤医院)、王强(吉林大学第一医院)、王维虎(北京大学肿瘤医院)、王颖杰(空军特色医学中心)、王跃辉(四平市肿瘤医院)、吴德华(南方医科大学南方医院)、吴莉莉(复旦大学附属中山医院)、吴志峰(复旦大学附属中山医院)、习勉(中山大学肿瘤防治中心)、肖蕾(新疆医科大学第一附属医院)、解传滨(解放军总医院第一医学中心)、徐本华(福建医科大学附属协和医院)、徐寿平(解放军总医院第一医学中心)、闫婧(南京大学医学院附属鼓楼医院)、俞伟(解放军总医院第一医学中心)、袁响林(华中科技大学同济医学院附属同济医院)、袁智勇(天津大学附属中山医院)、岳金波(山东省肿瘤医院)、张火俊(上海长海医院)、张建英(复旦大学附属中山医院)、赵向飞(解放军总医院第六医学中心)、周乐源(江南大学附属医院肿瘤)、竺鑫丽(浙江大学附属第一医院)
执笔:董丽华(吉林大学第一医院)