核苷(酸)类似物抗病毒药对HBV感染病毒学复发的影响
2020-12-29卢惠萍
卢惠萍
我国肝硬化患者乙型肝炎病毒(hepatitis B virus,HBV)感染率超过60%[1],当HBV感染者符合临床肝硬化诊断标准,具有抗病毒治疗适应证,给予一定疗程的规范化抗病毒治疗都可获益。核苷(酸)类似物抗病毒药物(nucleoside analogue/nucleotide analogue,NUC)是HBV感染常用药物,尤其在慢性乙型肝炎(chronic hepatitis B,CHB)中效果显著,分析其临床应用情况能指导用药管理,目前NUC维持治疗时间尚存争议,分析不同维持治疗时间停药后远期复发率十分必要,有学者指出NUC治疗至HBeAg转阴且HBV DNA低于检测下限仍需长期甚至终身用药,以期HBsAg血清学转换,但当下治疗方式、患者身心压力、远期用药安全性不明等导致终身用药执行难,故需要在理想时间停药并控制复发率[2]。为此笔者分析所在医院感染科HBV患者NUC应用情况,就单用某种NUC的CHB患者进行分析,研究不同维持治疗时间对复发率的影响,报道如下。
1 资料与方法
1.1 一般资料
回顾本院2014年5月—2015年5月感染科718例HBV感染者资料。男性409例,女性309例;年龄19~82岁,平均(46.27±12.32)岁;病程1~23年,平均(10.43±3.18)年;CHB患者699例。纳入标准:符合《慢性乙型肝炎防治指南(2015版)》[3]相关诊断标准;完成肝功能、凝血功能检测及HBeAg、HBV DNA、甲胎蛋白检测;明确用药史,临床资料完善。将最终完成36个月随访且单用某种NUC者448例分为HBeAg阳性组、HBeAg阴性组,分别为214、234例。HBeAg阳性组:男性118例,女性96例;年龄20~79岁,平均(46.45±10.95)岁;病程1~21年,平均(10.40±2.61)年。HBeAg阴性组:男性123例,女性111例;年龄19~82岁,平均(46.08±11.05)岁;病程2~23年,平均(10.50±2.79)年。两组统计资料具有同质性,组间性别、年龄、病程比较,差异均无统计学意义(P>0.05)。
将上述单用某种NUC且完成36个月随访的患者按维持治疗时间分为<12个月组、12~24个月组、>24个月组,分别为123、186、139例;<12个月组:男性68例,女性55例;年龄19~80岁,平均(46.16±12.03)岁;病程1~21年,平均(10.49±2.23)年。12~24个月组:男性101例,女性85例;年龄20~81岁,平均(46.61±11.49)岁;病程1~22年,平均(10.91±2.16)年。>24个月组:男性72例,女性67例;年龄21~83岁,平均(46.01±9.62)岁;病程1~23年,平均(10.54±2.37)年。各组统计资料具有同质性,组间性别、年龄、病程比较,比较差异均无统计学意义(P>0.05)。本研究所有分组均符合完备性原则、互斥性原则,均按照简单品质标志分组。
1.2 方法
1.2.1 用药分析和分组原则 统计干扰素α、NUC使用情况(总体使用率、单用以及联合用药率)。此外所有分组均符合完备性原则和互斥性原则,均按照简单品质标志分组。
1.2.2 治疗与随访 采用单一NUC治疗的患者均获得HBeAg血清学转换,HBV DNA检测下限低,且连续3~6个月ALT<1×ULN,之后继续口服初始治疗的NUC维持治疗,直至患者自愿停药。最长随访至停药后36个月,剔除失联者,将余下患者纳入进一步研究,记录其随访时肝病进展情况,检测病毒学复发情况。病毒学复发判断:HBV DNA>2 000 IU/mL。
1.3 观察指标
对比HBeAg阳性组与HBeAg阴性组以及<12个月组、12~24个月组、>24个月组停药后12个月、24个月、36个月时的病毒学复发率;分析维持治疗时间是否为HBeAg阳性与HBeAg阴性组停药后36个月病毒学复发危险因素。
1.4 统计学分析
采用SPSS 18.0统计学软件分析数据,符合正态分布的计量资料以(±s)表示,两组比较用t检验,计数资料用(%)表示,用χ2检验。Cox风险比例模型分析远期复发危险因素。P<0.05为差异有统计学意义。
2 结果
2.1 用药情况
718例患者中,仅22例(均为HBV感染但未发展为肝炎者)未用NUC,NUC使用率为96.94%(696例),干扰素α联合NUC治疗的共121例,联合应用和单用NUC的患者共575例。使用率由高至低依次为恩替卡韦(60.78%;423例)、替诺福韦酯(30.17%;210例)、拉米夫定(11.93%;83例)、替比夫定(7.76%;54例)、阿德福韦酯(0.43%;3例)。上述药物单用率依次为73.04%(309例)、82.38%(173例)、56.63%(47例)、57.41%(31例)、33.33%(1例),共561例,随访36个月丢失113例,余448例。
2.2 HBeAg阳性组与HBeAg阴性组停药后病毒学复发率比较
两组停药后12个月、24个月、36个月时复发率比较,差异均无统计学意义(P>0.05),见表1。
2.3 不同维持治疗时间组在停药后不同时间点的病毒学复发率比较
停药后12个月、24个月、36个月时,维持治疗时间<12个月组停药后病毒学复发率最高,>24个月组停药后病毒学复发率最低,比较差异均有统计学意义(P<0.05),见表2。
2.4 单用某种NUC的CHB患者停药后36个月复发危险因素分析
Cox回归模型分析确定维持治疗时间为HbeAg阳性和阴性者停药后36个月复发危险因素(P<0.05),见表3。
3 讨论
恩替卡韦、替诺福韦酯是目前最强抗HBV活性药物,恩替卡韦促使ALT复常,降低血清HBV DNA效果较好,与替诺福韦相比,恩替卡韦在我国应用时间更长,经验丰富,不良反应少,造价低[4-5];替诺福韦无需空腹便可用药,耐药率更低,几乎可治疗所有耐药性HBV,毒性低于阿德福韦酯,对于大多数患者而言比较安全,尽管如此也需要根据患者肾功能、肌酐清除率等合理使用,密切观察[6]。拉米夫定、替比夫定因为耐药率高导致使用率较低;阿德福韦酯因为有肾不良反应,故使用少[7]。
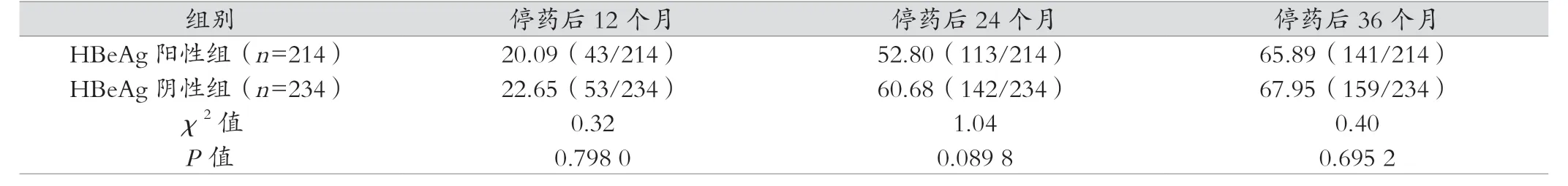
表1 HBeAg阳性组与HBeAg阴性组停药后病毒学复发率比较(%)

表2 不同维持治疗时间组在停药后病毒学复发率比较(%)

表3 单用某种核苷(酸)药物的CHB患者停药后36个月复发危险因素分析
本研究中单用某种NUC的HBV患者高达78.13%,这类患者初始治疗均获得HBeAg血清学转换,HBV DNA均至检测下降,但维持治疗停止后,无论是初始治疗HBeAg阳性或者阴性,其复发率逐渐走高且二者无显著差异。考虑是因为即使获得HBeAg血清学转换和HBV DNA低于检测下限,肝细胞核HBV cccDNA仍存在,HBsAg转录并未停止。无论初始治疗HBeAg是否阴性,在达到治疗满意终点后仍需要维持治疗。按照维持治疗时间分组,发现停药后12个月、24个月、36个月时复发率均以<12个月组最高,>24个月组最低;维持治疗时间在初始治疗HBeAg阳性和阴性患者中均为远期复发高危因素。这与吴妍等[8]研究者指出的维持治疗时间是初始治疗HBeAg阴性、阳性HBV患者停药36个月病毒学复发危险因素(OR=0.893,P<0.001;OR=0.907,P<0.01)的结果一致。说明在维持治疗时间越短,远期复发率越高。考虑既往研究指出HBV感染肝细胞半衰期可达数十年,因此需要长期使用抗病毒确保感染HBV的肝细胞清除,使cccDNA转录处于相对静止状态[9-10]。但关于长期NUC治疗引起HBV耐药和不良反应还不明确,因此不能单纯要求更长的维持治疗,一些研究者指出[11-12],维持治疗15个月复发率低于6个月者,但维持治疗30个月时复发率并未继续大幅下降。因此,关于维持治疗最佳时间还有待进一步研究。
综上所述,NUC是HBV感染者临床常用药,一般用于CHB患者中,以恩替卡韦和替诺福韦酯应用最多,主要为单一给药,适当延长维持治疗是降低停药后CHB复发率的重要途径。
