禾谷镰刀菌FgNST1对FgMGV1及DON毒素合成的影响
2020-12-29薛晓雯翟焕趁屈建航张帅兵吕扬勇李娜魏闪马平安蔡静平胡元森
薛晓雯, 翟焕趁, 屈建航, 张帅兵, 吕扬勇, 李娜, 魏闪, 马平安, 蔡静平, 胡元森
(河南工业大学生物工程学院,河南 郑州 450001)
禾谷镰刀菌(Fusariumgraminearum)是小麦、水稻和大麦等禾谷类作物赤霉病的主要致病菌,不仅造成作物产量降低,而且产生多种真菌毒素,严重威胁人畜和食品的安全[1]。随着全球气候变暖以及秸秆还田和轮作等耕作方式的改变,赤霉病在世界各地频发,脱氧雪腐镰刀菌烯醇(deoxynivalenol,DON)毒素污染日趋严重[2-3]。DON毒素的生物合成不仅受细胞外环境因素如水活度、温度[4]、碳源[5]、pH值[6]、氮源[7]和过氧化氢[8]等因素的影响,也受细胞内信号途径如环磷酸腺苷蛋白激酶途径[9]、雷帕霉素信号转导途径[10]、 促分裂原活化蛋白激酶(mitogen activated protein kinase,MAPK)[11]等信号通路的调控。MAPK信号途径是生物快速适应环境的变化而产生的一系列蛋白质级联反应,在真核生物中具有高度保守性[12-13]。禾谷镰刀菌通过3个MAPK调控菌体的生长、侵染、有性生殖和对不同胁迫的适应性[14]。其中,GPMK1参与信息素信号途径,FgHOG1参与高渗透性甘油(high osmolarity glycerol, HOG)信号途径,MGV1 参与细胞壁完整性(cell wall integrity, CWI)途径[15]。MGV1基因是禾谷镰刀菌中最先被发现的编码MAPK的基因,缺失该基因会导致菌丝生长和侵染植物的功能严重缺陷,且明显降低DON毒素的生物合成[16]。为了满足细胞的生理需要,不同MAPK信号途径之间存在着交互作用[17]。禾谷镰刀菌中FgHOG1基因被敲除后,通过过度激活GPMK1激酶影响与CWI和渗透调节相关的基因,最终抑制mgv1突变体的部分缺陷[15]。
盐胁迫负调控因子NST1其基因最早是在酵母菌中被分离出来的。NST1基因功能的获得引起酵母菌对盐耐受的降低,缺失NST1基因则引起相反的表型,表明该基因在酵母菌中对耐盐性有负影响[18]。LENG等[19]研究表明,在酵母菌中NST1介导STE11(参与 HOG信号途径和信息素信号途径)和MKK1(CWI 途径)的相互作用,从而将HOG途径、信息素途径和CWI途径这3个MAPK信号途径联系起来。朱丽红[20]在研究小麦赤霉病及镰刀菌DON毒素调控过程中发现,禾谷镰刀菌也存在NST1基因,并证明禾谷镰刀菌NST1基因缺失突变体对小麦的致病性有显著影响。中国小麦赤霉病的发生有明确的区域性,发病区域与年均降雨量和大气湿度等气候变化相关,降雨量较少的年份及低湿度地区小麦DON毒素污染比率较低,通常的解释是镰刀菌生长需要高湿环境,但从分子代谢层面并没有明确的答案[21]。作为盐胁迫调控因子,NST1对小麦赤霉病发生和DON毒素的产生是否具有直接的影响尚未见到相关报道。另外,通过研究禾谷镰刀菌NST1的功能、探讨NST1与其他蛋白的相互关系及对DON毒素合成的影响,将有助于更深入地解析小麦赤霉病发生机制及禾谷镰刀菌DON毒素合成的调控机制。本研究分析了禾谷镰刀菌FgNST1与MAPK信号途径中FgMGV1的相互作用关系,并利用已经构建的FgNST1基因敲除突变体探讨FgNST1对DON毒素生物合成的影响。
1 材料与方法
1.1 材料
1.1.1 供试材料 禾谷镰刀菌野生型菌株PH-1由福建农林大学功能基因组学研究中心惠赠;FgNST1基因(FGSG_04069)敲除突变体,命名为△FgNST1,由河南工业大学微生物学研究室构建保存;酵母双杂交所用菌株和载体购自美国Clotech公司。试验中涉及的菌株代号及培养条件如表1所示。

表1 菌株代号与培养条件
1.1.2 试剂及仪器 大肠杆菌DH5α 感受态细胞和酵母质粒提取试剂盒购自天根生化科技有限公司,SanPrep 柱式质粒抽提试剂盒和SanPrep 柱式DNA 胶回收试剂盒购自上海生工生物工程公司,呕吐毒素ELISA检测试剂盒购自北京华安麦科生物技术有限公司,PrimeStar GXL DNA polymerase、RNA 提取Trizol试剂、反转录试剂盒、荧光定量 PCR 试剂盒购自TakaRa生物公司,内切酶购自NEB(北京)有限公司,PCR扩增酶和ClonExpress II One step克隆试剂盒购自南京诺唯赞生物科技有限公司。
5427R冷冻离心机(Eppendorf 中国有限公司)、PCR仪(德国耶拿分析仪器股份公司)、StepOneTM 实时定量 PCR 仪(美国应用生物系统公司)、DYY-6C 型电泳仪(北京六一仪器厂)、NanoDrop2000 核酸浓度检测仪(赛默飞世尔科技公司)、KMF(E2.5)BINDER培养箱(德国 BINDER 公司)、QYC-2102C摇床(上海福玛实验设备有限公司)。
1.1.3 培养基 CM液体培养基:酵母粉6 g,酸水解酪蛋白6 g,蔗糖10 g,用蒸馏水定容至1 L,灭菌;SD培养基:缺失腺嘌呤(Ade)、组氨酸(His)、亮氨酸(Leu)和色氨酸(Trp)的DO添加剂(DO supplement-Ade,-His,-Leu,-Trp,美国Sigma公司)0.067 g,无氨基氮源0.67 g,双蒸水95 mL,灭菌冷却后加5 mL 质量分数40%的葡萄糖溶液,固体培养基再另加琼脂粉2 g;SD/-Trp/-Leu培养基:SD培养基加800 μL 100 x Ade、200 μL 500 x His;SD/-Trp/-Ade培养基:SD培养基加1 mL 100 x Leu、200 μL 500 x His;SD/-Leu/-Ade培养基:SD培养基加200 μL 500 x Trp、200 μL 500 x His;SD/-Leu/-His培养基:SD培养基加200 μL 500 x Trp、800 μL 100 x Ade;SD/-Trp/-His培养基:SD培养基加1 mL 100 x Leu、800 μL 100 x Ade;SD/-Leu培养基:SD培养基加800 μL 100 x Ade、200 μL 500 x His、200 μL 500 x Trp;SD/-Trp培养基:SD培养基加800 μL 100 x Ade、200 μL 500 x His、1 mL 100 x Leu;小麦基质培养基:参照孟瑶等[22]方法制备,调节小麦子粒水分质量分数25.0%,分装50 g于250 mL的三角瓶中。
1.2 试验方法
1.2.1 基因的序列分析 根据酿酒酵母菌NST1基因、SLT2基因的核苷酸序列在 NCBI数据库中进行比对分析,获得禾谷镰刀菌菌株PH-1中的NST1、MGV1基因及编码蛋白的序列,利用NCBI CDD 数据库(https://www.ncbi.nlm.nih.gov/Structure/cdd/wrpsb.cgi)分析2种编码蛋白的保守域;通过BlastP比对出其他真菌中与禾谷镰刀菌NST1同源的蛋白,利用MEGA7.0软件对同源蛋白多序列比对,基于邻接法(neighbor joining, NJ)法构建系统发育树,Bootstrap重复次数1 000。
1.2.2 禾谷镰刀菌总RNA提取和cDNA合成 参照SELVARAJ等[2]方法,将-80 ℃保存的禾谷镰刀菌野生型菌株PH-1的孢子活化后的菌丝块接种至CM 液体培养基中,28 ℃,150 r·min-1摇床培养3 d,将菌丝进行过滤,研磨后利用TaKaRa RNAiso 试剂盒说明书提取纯化RNA,利用质量分数1%的琼脂糖凝胶电泳检测RNA的完整性,运用核酸检测仪检测RNA的浓度和纯度,利用反转录试剂盒PrimeScriptTM Ⅱ 1st Strand cDNA Synthesis Kit(TaKaRa)合成cDNA,置于-20 ℃保存备用。
1.2.3 重组载体的构建FgNST1基因(FGSG_04069, NCBI数据库https://www.ncbi.nlm.nih.gov/gene/?term=FGSG_04069)和FgMGV1基因(FGSG_10313, NCBI数据库https://www.ncbi.nlm.nih.gov/gene/?term=FGSG_10313)的cDNA序列进行引物设计(表2),以野生型的cDNA为模板分别扩增FgNST1基因和FgMGV1基因片段,PCR产物经纯化回收备用。酵母表达载体 pGBKT7 质粒利用 NdeI 和 BamHI 进行双酶切,pGADT7质粒用NdeI和EcoRI进行双酶切,酶切体系为50.0 μL(Cutsmart buffer 5.0 μL,限制性内切酶20 U,质粒1.0 μg,ddH2O补足至50.0 μL ),37 ℃水浴4 h,纯化回收线性化载体。采用无缝克隆方法将FgMGV1片段与线性化载体pGBKT7连接、将FgNST1片段与线性化载体pGADT7进行连接,具体操作方法参照ClonExpress II One step Cloning Kit 说明书执行,将10.0 μL连接产物克隆至大肠杆菌DH5α感受态细胞,将含有重组质粒的菌液送去测序,序列正确即证明重组载体构建成功,分别命名为重组载体pGBKT7-FgMGV1、pGADT7-FgNST1。

表2 PCR扩增引物序列
1.2.4 重组质粒的细胞毒性和自激活检测 将构建好的重组质粒pGBKT7-FgMGV1、pGADT7-FgNST1分别转化入酵母菌AH109感受态细胞,空载体pGBKT7、pGADT7做对照,酵母感受态细胞的制备和转化参照MatchmakerTM Gold 酵母双杂交系统说明书进行,转化子通过质粒酶切进行验证。将pGBKT7-FgMGV1转化子单菌落接种于SD/-Trp(卡那霉素抗性)液体培养基,pGADT7-FgNST1转化子接种于SD/-Leu(氨苄青霉素抗性)液体培养基中,30 ℃摇床150 r·min-1培养24 h后,通过紫外分光光度计测定OD600判定细胞毒性。将 pGADT7-NST1转化子菌液分别划线在SD/-Leu、SD/-Leu/-Ade、SD/-Leu/-His、SD/-Leu/X-α-Gal 平板上,将pGBKT7-MGV1转化子菌液分别划线于SD/-Trp、SD/-Trp/-Ade、SD/-Trp/-His、SD/-Trp/X-α-Gal平板上,pGADT7-RecT+pGBKT7-P53 作为阳性对照,pGADT7、pGBKT7分别作为阴性对照,30 ℃培养3 d,观察菌落生长情况,检测重组质粒的自激活情况。
1.2.5 FgMGV1与FgNST1的相互作用检测 将pGADT7-FgNST1质粒和 pGBKT7-FgMGV1质粒共转化AH109感受态细胞,通过SD/-Leu/-Trp平板筛选阳性转化子 pGADT7-NST1+pGBKT7-MGV1,通过酵母质粒酶切验证后,将转化子菌液划线至 SD/-Leu/-Trp/-Ade/-His/X-α-Gal平板上,以pGADT7-RecT+pGBKT7-P53 做阳性对照,pGADT7-RecT+pGBKT7-Lam、pGADT7+ pGBKT7、pGADT7-FgNST1+pGBKT7、pGADT7+pGBKT7-FgMGV1为阴性对照,30 ℃培养3 d,观察菌落能否生长和是否变蓝色。
1.2.6 DON毒素的测定 将活化的禾谷镰刀菌野生型菌株 PH-1、△FgNST1突变体菌丝分别接种到灭菌的含NaCl(0、1.0 mol·L-1)小麦基质培养基中,静置于28 ℃ 培养箱培养,每天振荡 5 min,使病菌发酵均匀。测定7、14、21、28 d时小麦基质中的DON 毒素,检测方法参照华安麦科呕吐毒素 ELISA 测定试剂盒说明书进行。每个样品设置3个平行,试验重复3次。
1.2.7FgMGV1基因的实时定量表达分析 将活化的禾谷镰刀菌野生型菌株PH-1、△FgNST1突变体菌株分别接种在含NaCl(0、1.0 mol·L-1)的CM 液体培养基中,28 ℃培养7 d,提取RNA,反转录成cDNA,利用实时定量PCR分析FgMGV1基因的相对表达量,FgMGV1基因的扩增引物见表2,荧光定量PCR方法见参考文献[22]。试验重复3次,每个模板设置3个重复,Tublin做内参,根据反应的CT值,用2-△△CT法进行基因相对表达量的分析。
1.2.8 数据分析方法 利用SPSS Statistics 17软件进行试验数据的统计分析,采用方差分析进行变量的差异显著性检验,曲线图中不同字母表示差异达到显著水平(P<0.05)。
2 结果与分析
2.1 禾谷镰刀菌FgNST1与FgMGV1 的序列分析
根据酿酒酵母菌NST1和SLT2基因对应的氨基酸序列在NCBI数据库中进行比对发现,禾谷镰刀菌含有NST1保守域基因为FGSG_04069,本研究命名为FgNST1基因, DNA全长为3 742 bp,蛋白质编码区(coding sequence, CDS)为3 579 bp,编码1 192个氨基酸。对FGSG_04069 编码的蛋白进行保守域分析[23],如图1所示。该蛋白含有NST1、TolA和Atrophi-1共3个保守域,其中NST1保守域位于该蛋白的139~273个氨基酸位置,为盐耐受负调控因子。对FgNST1同源蛋白进行系统发育分析,如图2所示。禾谷镰刀菌FgNST1与黄色镰刀菌Fusariumculmorum的胁迫反应蛋白相似度最高,与多种镰刀菌属的NST1蛋白聚在1个相同分支;曲霉菌属Aspergillus的NST1蛋白聚在1个相同分支;酵母菌属的NST1蛋白聚在遗传距离较远的另外分支。这表明,该蛋白在各类真菌中具有极高的保守性,与盐胁迫反应相关。

图1 禾谷镰刀菌FgNST1蛋白的保守域结构预测
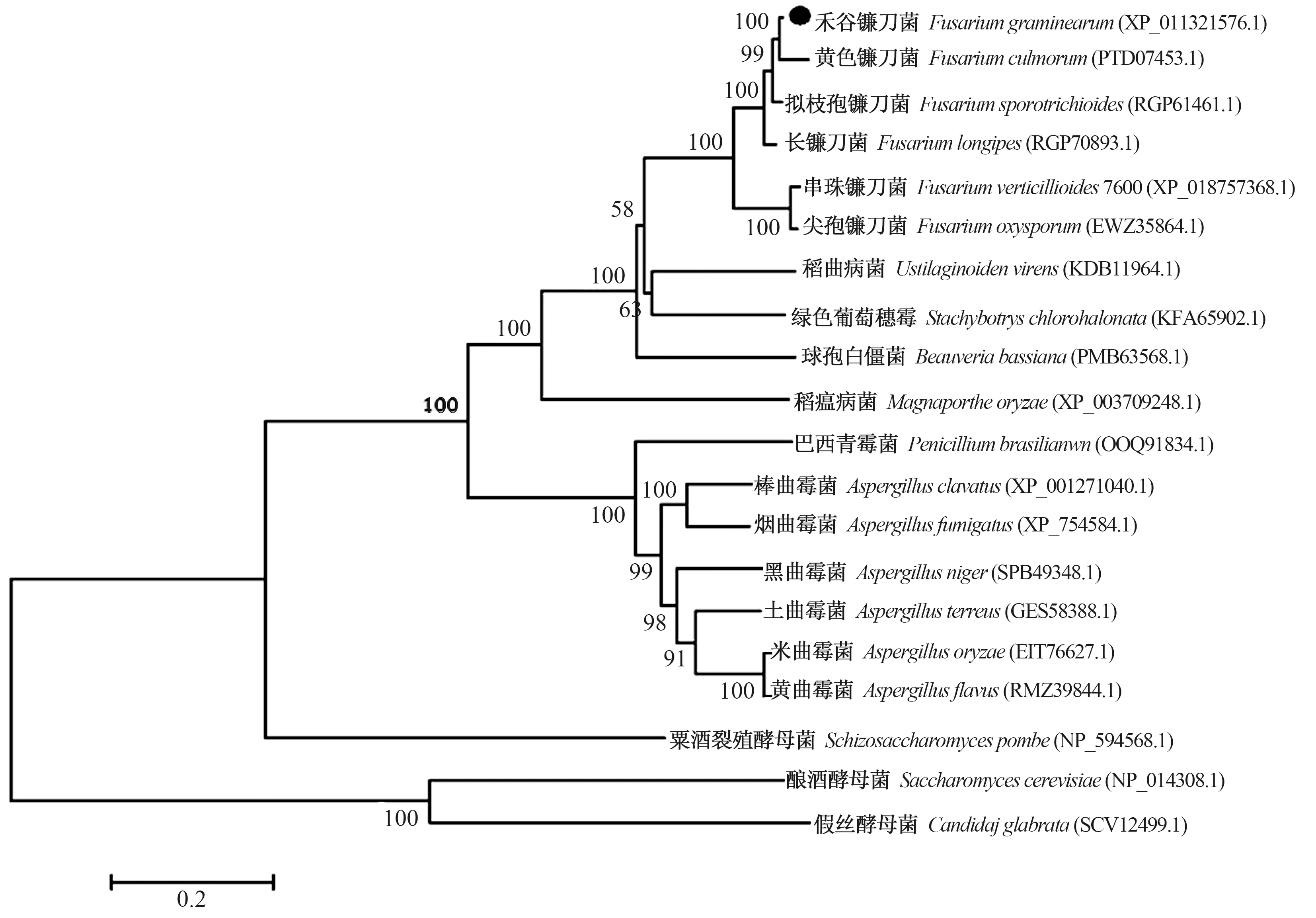
注:标尺表示遗传进化距离,黑色圆圈表示禾谷镰刀菌FgNST1序列,括号中的内容代表蛋白序列ID号。
禾谷镰刀菌MGV1基因(FGSG_10313)全长为1 810 bp,编码序列CDS为1 251 bp,编码416个氨基酸,编码产物为 MAPK spm1,本研究将MGV1基因命名为FgMGV1。对FgMGV1蛋白进行保守域分析,结果如图3所示。FgMGV1蛋白含有丝氨酸/苏氨酸蛋白激酶催化中心 (Serine/Threonine protein kinase catalytic center, STKc)保守域,STK是细胞响应外界信号的重要介质,是与细胞壁完整性途径相关的 MAPK,推测对响应胁迫有重要作用。
2.2 盐胁迫下禾谷镰刀菌FgNST1与FgMGV1基因的表达
以不添加NaCl和添加1.0 mol·L-1NaCl的CM液体培养基中培养7 d的禾谷镰刀菌野生型菌株cDNA为模板,采用荧光定量PCR 技术分析FgNST1和FgMGV1基因相对表达情况,结果如图4所示。与不加NaCl相比,FgNST1基因在NaCl处理后的野生型菌株中的相对表达量表现为显著下调响应,是对照的0.4倍;FgMGV1基因在NaCl胁迫的野生型菌株中的表达显著上调,为对照的1.4倍。这表明FgNST1和FgMGV1基因参与了禾谷镰刀菌盐胁迫的应答反应,FgNST1是盐胁迫负调控因子。

图3 禾谷镰刀菌FgMGV1保守域预测
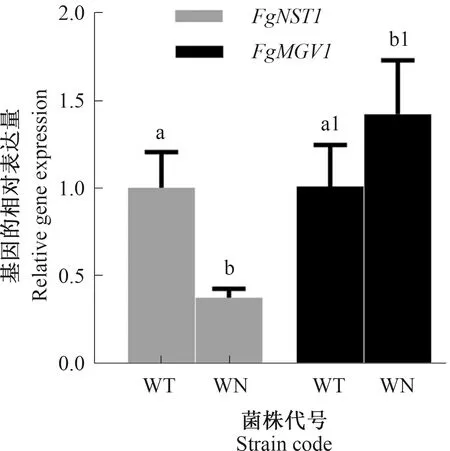
注:同组间不同字母表示差异显著(P<0.05)。下同。
2.3 重组载体的构建
为证明FgNST1与FgMGV1的相互作用关系,本研究首先构建重组载体。FgNST1编码蛋白的NST1保守域位于第139~273个氨基酸处,对FgNST1cDNA的1~819 bp长度的片段进行扩增。以PH-1的cDNA为模板,用引物WFNST1F/WFNST1R扩增到FgNST1保守域片段,大小为819 bp,如图5-A所示;用引物 WFHMGV1F/WFHMGV1R扩增FgMGV1片段,大小为1 251 bp,如图5-B所示。将质粒载体pGBKT7和pGADT7分别通过双酶切进行线性化,纯化回收的质粒pGBKT7与FgMGV1片段重组连接,pGADT7与FgNST1保守域片段重组连接,重组转化子通过酶切验证,分别得到质粒片段和目的条带,如图6所示。将重组转化子菌液进行测序,插入的FgMGV1片段、FgNST1保守域片段与数据库中核苷酸序列完全一致,表明重组载体pGBKT7-FgMGV1、pGADT7-FgNST1构建成功。

注:M, Marker QDL2000;1, FgNST1保守域片段(A)或FgMGV1片段(B)。
2.4 重组质粒的毒性及自激活检测分析
重组质粒pGADT7-FgNST1、pGBKT7-FgMGV1分别转化酵母菌AH109后,转化子分别在SD/-Leu液体培养基、SD/-Trp液体培养基中生长1 d后测定的OD600均大于0.8,说明重组质粒对酵母细胞无毒性。含有重组质粒pGADT7-FgNST1、pGBKT7-FgMGV1的转化子自激活检测结果如图7所示。pGADT7-FgNST1在SD/-Leu/-Ade和SD/-Leu/-His培养基上不能生长,在SD/-Leu /X-α-Gal培养基上可以生长,但不变蓝;pGBKT7-FgMGV1在SD/-Trp/-Ade、SD/-Trp/-His培养基上不能生长,在SD/-Trp/X-α-Gal培养基上可以生长,但不变蓝色。检测结果表明,FgNST1和FgMGV1蛋白均不能自激活载体上的ADE2、HIS3和MEL1报告基因,可以进行下一步酵母双杂交验证。

注:M, Marker P;1, 酶切前的质粒pGADT7-NST1(A)或 pGBKT7-FgMGV1(B);2, 酶切后的质粒pGADT7-NST1(A)或pGBKT7-FgMGV1(B)。
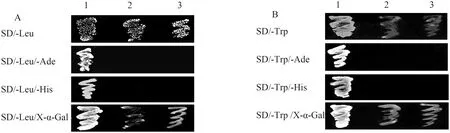
注:1, pGADT7-RecT+pGBKT7-P53转化子(阳性对照);2, pGADT7-FgNST1(A)或者pGBKT7-FgMGV1(B)转化子;3, pGADT7转化子(A)或者pGBKT7转化子(B)(阴性对照)。
2.5 禾谷镰刀菌FgNST1与FgMGV1的相互作用分析
将重组质粒pGADT7-FgNST1与pGBKT7-FgMGV1共转到酵母菌AH109中,转化子经质粒PCR验证显示,可以扩增出819 bp的FgNST1片段和1 251 bp的FgMGV1片段,证明共转成功,如图8所示。pGADT7-FgNST1+pGBKT7-FgMGV1转化子菌液在SD/-Leu/-Trp/-Ade/-His/X-α-Gal固体培养基上划线培养,结果如图9所示,pGADT7-FgNST1+pGBKT7-FgMGV1共转转化子可以生长,且菌落颜色呈现蓝色,表明禾谷镰刀菌FgNST1与FgMGV1蛋白相互作用,激活了ADE2、HIS3和MEL1报告基因的表达。

注:M, Marker S plus;1, FgMGV1片段;2, FgNST1片段。
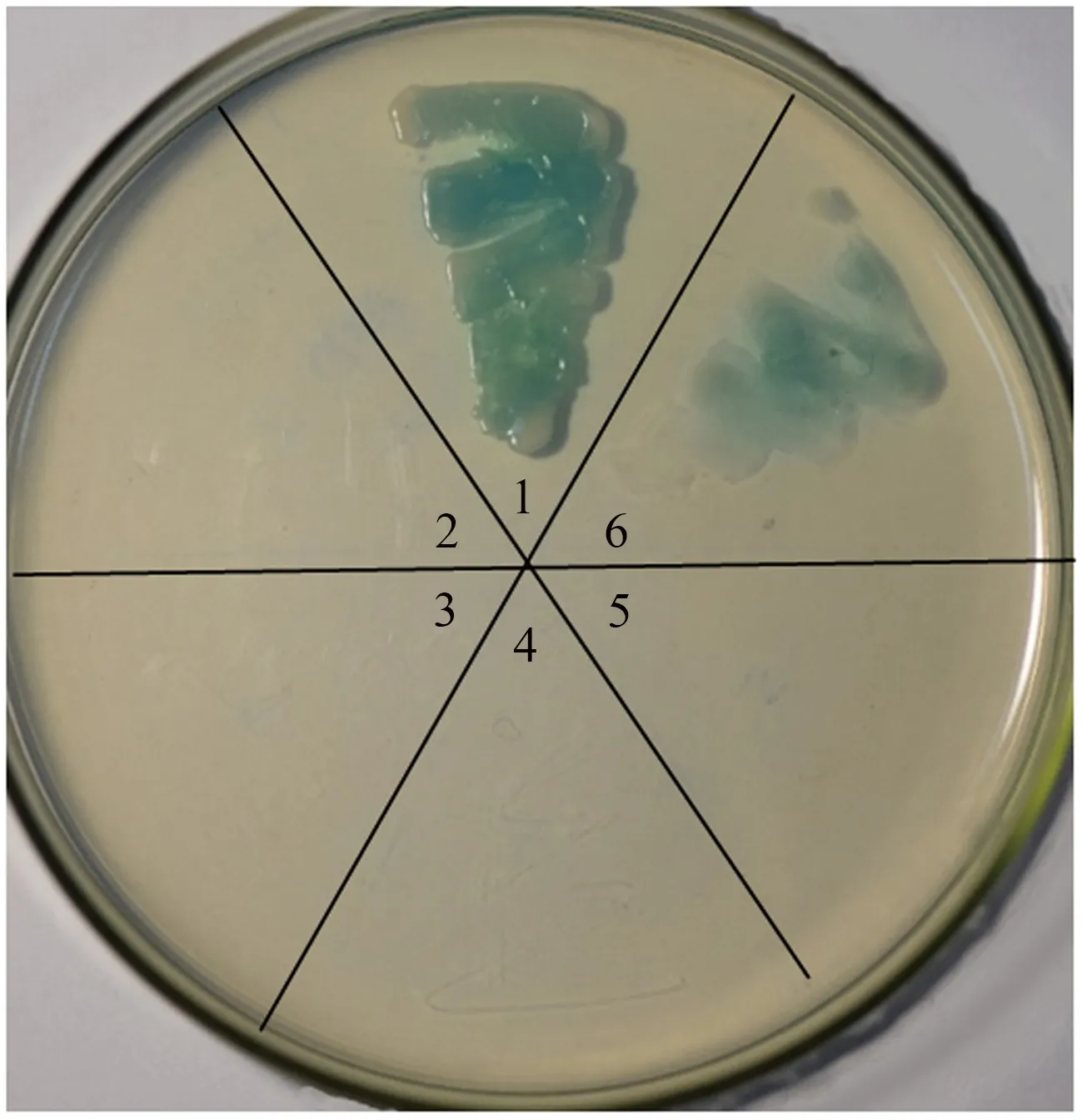
注:1, pGADT7-RecT+pGBKT7-P53(阳性对照); 2, pGADT7-RecT+pGBKT7-Lam(阴性对照);3, pGADT7+pGBKT7(阴性对照); 4, pGADT7-FgNST1+pGBKT7(阴性对照);5, pGADT7+pGBKT7-FgMGV1(阴性对照); 6, pGADT7-FgNST1+pGBKT7-FgMGV1。
为进一步探讨FgNST1与FgMGV1功能之间的相关性,本研究分析了FgMGV1基因在野生型和△FgNST1突变体菌株中的表达,结果如图10所示。在无NaCl胁迫时,FgMGV1在野生型中有表达,但是在△FgNST1中几乎不表达,这可能与FgNST1和FgMGV1之间存在相互作用有关;在有NaCl胁迫时,FgMGV1在野生型中的表达显著上调,是无NaCl胁迫时的1.4倍,且在△FgNST1突变体中的相对表达显著高于野生型,表明NaCl的高渗透胁迫信号激活了MAPK途径中的CWI 途径,使CWI途径中的FgMGV1基因的表达量上调, 从而抑制了因FgNST1缺失造成的对细胞的影响。因此,在外界存在盐胁迫时,FgNST1与FgMGV1在功能上具有相关性。
2.6 禾谷镰刀菌FgNST1对DON毒素合成的影响
生物在受到外界环境胁迫时通常会通过调节代谢以适应特异的环境,一些产毒真菌会通过调节次级代谢如真菌毒素作为适应环境胁迫条件的生态进化[24]。本研究将野生型菌株PH-1和△FgNST1突变体菌株接种到小麦基质培养基中进行产毒培养,DON毒素检测结果如图11所示。在无NaCl的小麦基质培养基中,△FgNST1突变体菌株在7 d时产生的DON毒素显著高于野生型菌株,而在随后的时期均显著低于野生型菌株,14 d时产生的DON毒素减少幅度达到野生型毒素产生量的50%;在加NaCl的小麦基质中,野生型和△FgNST1突变体菌株合成的DON毒素均比无NaCl的小麦基质中显著减少,在同一生长时期,△FgNST1突变体产生的DON毒素均比野生型稍高,但是2种菌株产生的DON毒素在培养开始前21 d增加并不显著。

图10 FgMGV1基因在野生型和△FgNST1突变体中的相对表达量
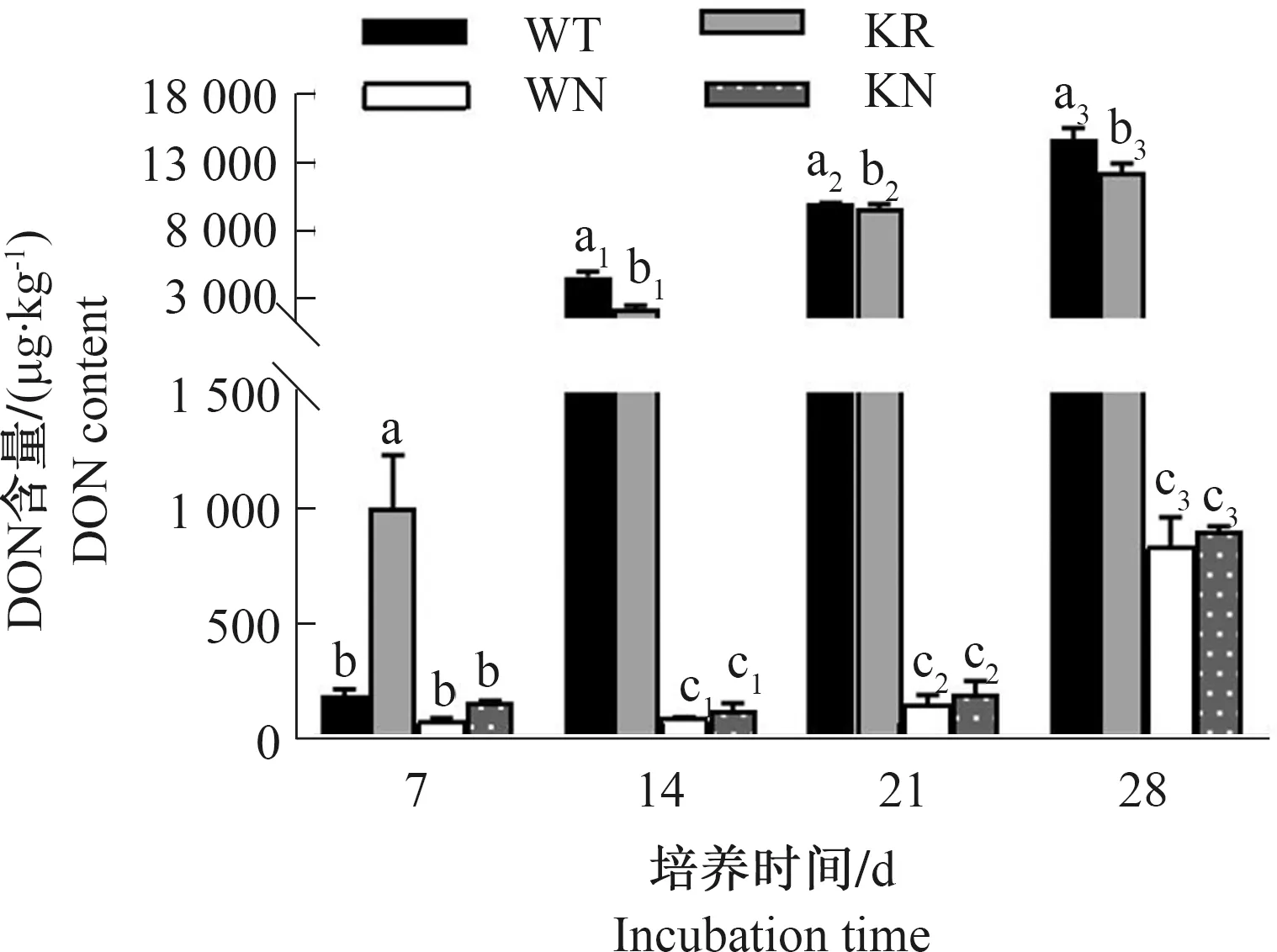
图11 不同生长时期的野生型和△FgNST1突变体菌株在小麦基质中产生的DON毒素
3 结论与讨论
本研究对禾谷镰刀菌FgNST1蛋白进行保守域分析,显示该蛋白含有盐耐受负调控因子NST1保守域;对FgNST1及其同源蛋白进行系统发育分析,显示FgNST1与多种镰刀菌属聚在相同分支,曲霉菌属的NST1蛋白都聚在另外相同分支,表明该蛋白在各属中具有极高的保守性和相似的生物学功能。由于在酵母菌研究中发现NST1与剪切因子Msl1p相互作用影响盐的耐受性,直接或间接参与对盐的敏感性反应[18],推测FgNST1基因也可能在禾谷镰刀菌对盐胁迫的适应性中具有调控作用。本研究分析显示禾谷镰刀菌FgMGV1基因编码的产物为 MAPK spm1,FgMGV1蛋白含有STKc保守域。STK是细胞响应热胁迫、渗透胁迫和氧化胁迫等外界信号的重要介质,对维持细胞形态、细胞壁建成和离子稳态产生重要影响[25],推测FgMGV1在对盐胁迫响应中具有重要作用。
通过分析FgNST1和FgMGV1基因对盐胁迫的响应,表明在盐胁迫下FgNST1基因表达显著下调,FgMGV1基因表达则显著上调。通过酵母双杂交试验显示,禾谷镰刀菌FgNST1与FgMGV1可以相互作用。LENG等[19]研究了酵母菌NST1的生物学功能,指出NST1可以与HOG 信号途径中的Ste11 相互作用,也可以与CWI途径中的Mkk1相互作用,从而使不同信号途径之间交互作用。在盐胁迫下,许多产毒真菌如黄曲霉属、青霉属和镰刀菌属等微生物通过MAPK、钙调信号等途径调控次级代谢产物的合成而维持自身生长[26]。HOU等[16]在研究禾谷镰刀菌MAP激酶MGV1时发现,mgv1缺失突变体在接种的小麦中积累的DON毒素显著降低,表明MGV1影响 DON 毒素的合成。MACHELEIDT等[12]对真菌次级代谢调控研究发现,在外界环境胁迫下,真核生物可通过信号级联反应将信号传导给细胞内的各类调控因子,以调控基因的表达和次级代谢物的合成,从而适应环境的变化维持自身生长。本研究结果表明,FgNST1对DON毒素合成有显著影响,并且FgNST1与FgMGV1具有相互作用的特性。在盐胁迫下,FgNST1可能通过MAPK途径中的FgMGV1调控DON毒素合成。
盐胁迫调控次生代谢产物合成具有不同的特点。本研究中禾谷镰刀菌在盐胁迫下引起DON毒素合成显著减少;在北欧青霉(Penicilliumnordicum) 中,NaCl质量浓度的增加反而诱导了赭曲霉毒素的合成[27];在烟曲霉中NaCl质量浓度增高到70 g·L-1时分泌胶霉毒素的能力达到最大[28]。这些研究表明,真菌毒素的合成与环境变化密切相关,环境胁迫相关基因具有间接调控的作用。探讨禾谷镰刀菌毒素调控基因的相互作用,对逆境条件下防控禾谷镰刀菌及其DON毒素污染具有潜在的应用价值,对保障食品安全具有重要的意义。
