116例增生硬化性IgA肾病患者的临床及病理特点分析
2020-12-23常美莹张昱
常美莹 张昱

[摘要] 目的 探討增生硬化性IgA肾病患者的临床及病理特点。 方法 回顾性分析2015年1月—2019年3月就诊于中国中医科学院西苑医院肾病科门诊并经肾活检证实为增生硬化性IgA肾病患者116例。根据慢性肾脏病(CKD)分期将其分为CKD 1~5期,比较各组24 h尿蛋白定量及合并症情况(包括有无高血压、高尿酸血症等);根据有无缺血性肾损伤分为伴缺血性肾损伤组和不伴缺血性肾损伤组,根据有无IgM沉积分为伴IgM沉积组和不伴IgM沉积组,比较各组的24小时尿蛋白定量、血肌酐水平及估算的肾小球滤过率(eGFR)。 结果 五组年龄,24 h尿蛋白定量,高尿酸血症、咽炎及扁桃体炎占比比较,差异均有统计学意义(均P < 0.05)。伴缺血性肾损伤组血肌酐、高血压占比高于不伴缺血性肾损伤组,eGFR低于不伴缺血性肾损伤组,差异均有统计学意义(均P < 0.05)。伴IgM沉积组年龄、eGFR水平低于不伴IgM沉积组,血肌酐水平高于不伴IgM沉积组,差异均有统计学意义(均P < 0.05)。 结论 增生硬化性IgA肾病患者临床与病理损伤较重,24 h尿蛋白定量、血肌酐、缺血性肾损伤及IgM沉积可能是其肾功能进展及肾脏预后不良的危险因素。
[关键词] 增生硬化性IgA肾病;临床特点;病理特点;血肌酐;预后
[中图分类号] R692 [文献标识码] A [文章编号] 1673-7210(2020)10(a)-0096-04
Clinical and pathological features of 116 patients with proliferative and sclerosing IgA nephropathy
CHANG Meiying ZHANG Yu
Department of Nephropathy, Xiyuan Hospital, China Academy of Chinese Medical Sciences, Beijing 100091, China
[Abstract] Objective To investigate the clinical and pathological features of patients with proliferative and sclerosing IgA nephropathy. Methods Retrospective analysis was performed on 116 patients with proliferative and sclerosing IgA nephropathy confirmed by renal biopsy in Department of Nephropathy, Xiyuan Hospital, China Academy of Chinese Medical Sciences from January 2015 to March 2019. According to chronic kidney diseases (CKD) stage, they were divided into CKD stage 1-5. The 24 h urinary protein quantification and comorbidities of each group were compared (including the presence or absence of hypertension, hyperuricemia, etc.). They were divided into group with ischemic kidney injury and group without ischemic kidney injury according to the presence or absence of ischemic kidney injury, and they were divided into group with IgM deposition and group without IgM deposition according to the presence or absence of IgM deposition group. The 24 h urinary protein quantification, serum creatinine level and estimated glomerular filtration rate (eGFR) of each group were compared. Results There were statistically significant differences among the five groups in age, 24 h urine protein quantification, and proportion of hyperuricemia, pharyngitis and tonsillitis (all P < 0.05). The serum creatinine and proportion of hypertension in group with ischemic kidney injury were higher than those of the group without ischemic kidney injury, and eGFR was lower than that of the group without ischemic kidney injury, with statistically significant differences (all P < 0.05). The age and eGFR level of group with IgM deposition were lower than those of group without IgM deposition, the serum creatinine level was higher than that of group without IgM deposition, and the differences were statistically significant (all P < 0.05). Conclusion The clinical and pathological lesions in patients with proliferation and sclerosing IgA nephropathy are severe, and 24 h urine protein quantitative, blood creatinine, ischemic kidney injury and IgM deposition may be risk factors for renal progression and poor renal prognosis.
[Key words] Proliferative and sclerosing IgA nephropathy; Clinical features; Pathological features; Serum creatinine; Prognosis
IgA腎病(IgAN)是我国最常见的原发性肾小球疾病,占原发性肾小球疾病的40%~47%[1],是导致终末期肾病(ESRD)的主要病因之一,其临床和病理表现多样,预后也各不相同[2-4],而增生硬化性IgAN患者是IgAN中病理相对较重的类型,其肾穿刺病理常伴肾小球硬化、肾小管萎缩、间质纤维化及血管壁增厚等表现,临床出现高血压、尿蛋白增多、肾功能下降等均是预后不良的提示,所以其对整个IgAN预后的影响至关重要。本文对116例增生硬化性IgAN患者的临床及病理特点进行统计分析,以期对该病的治疗及预后提供帮助。
1 资料与方法
1.1 一般资料
选取2015年1月—2019年3月中国中医科学院西苑医院(以下简称“我院”)肾病科门诊并经肾活检证实为增生硬化性IgAN患者116例为研究对象,年龄16~81岁,平均(37.41±10.06)岁。排除乙肝病毒相关性肾炎、系统性红斑狼疮性肾炎及过敏性紫癜性肾炎等继发性肾脏损害者。本研究经我院医学伦理委员会批准。
1.2 方法
收集患者年龄、性别、发病时24 h尿蛋白定量、血尿酸、肌酐等资料。根据慢性肾脏病(CKD)分期将患者分为CKD1~5期共5组,并对5组的临床资料进行分析。
收集患者肾穿刺资料。根据有无缺血性肾损伤、有无IgM沉积将患者各分为两组,分别为伴缺血性肾损伤组、不伴缺血性肾损伤组;伴IgM沉积组、不伴IgM沉积组,并对其数据进行分析。
1.3 疾病分期及诊断标准
按照国际通用的CKD分期标准[5]:CKD1期:肾小球滤过率(GFR)≥90 mL/(min·1.73 m2);CKD2期:GFR 60~89 mL/(min·1.73 m2);CKD3期:GFR 30~59 mL/(min·1.73 m2);CKD4期:GFR 15~29 mL/(min·1.73 m2);CKD5期:GFR<15 mL/(min·1.73 m2)。其中成人(简化MDRD公式)估算GFR[mL/(min·1.73 m2)]=186×(Scr)-1.154×(年龄)-0.203(女性×0.742)(Scr单位mg/dL)。
增生硬化性IgAN的病理诊断参照全国肾活检病理诊断研讨会意见[6]。光镜:≥50%肾小球呈球性硬化并伴有其他肾小球的增生病变;免疫荧光:系膜区弥漫性IgA免疫复合物沉积;电镜:系膜区电子致密物沉积。肾穿刺病理结果均由病理科医生阅片。
1.4 统计学方法
采用SPSS 20.0统计学软件进行数据分析,符合正态分布的计量资料以均数±标准差(x±s)表示,两组间比较采用t检验;非正态分布的计量资料用中位数(M),四分位数(P25,P75)表示,两组间比较采用Mann-Whitney U检验;计数资料以例数或百分率表示,组间比较采用χ2检验。以P < 0.05为差异有统计学意义。
2 结果
2.1 五组一般资料比较
五组年龄、24 h尿蛋白定量、高尿酸血症、咽炎及扁桃体炎比较,差异均有统计学意义(均P < 0.05)。见表1。
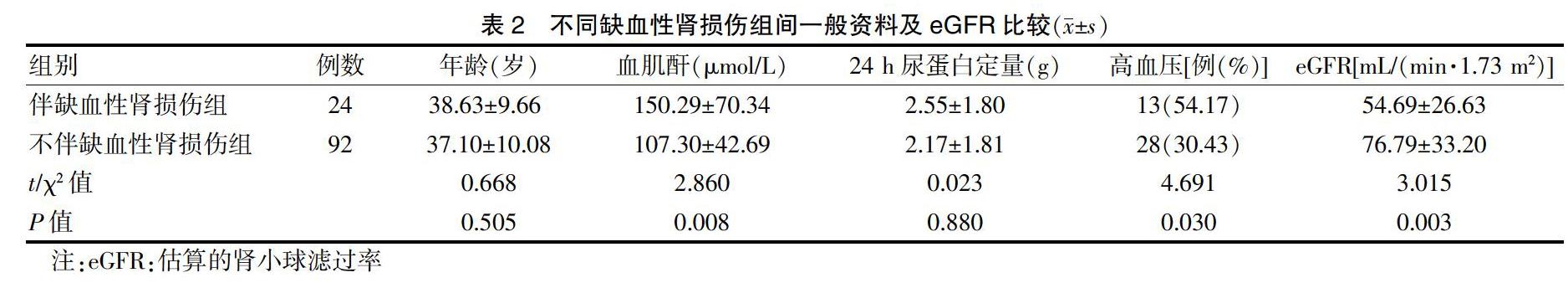
2.2 不同缺血性肾损伤组间一般资料及估算的肾小球滤过率(eGFR)比较
两组年龄、24 h尿蛋白定量比较,差异无统计学意义(P > 0.05);伴缺血性肾损伤组血肌酐、高血压占比高于不伴缺血性肾损伤组,eGFR低于不伴缺血性肾损伤组,差异均有统计学意义(均P < 0.05)。见表2。
2.3 不同IgM沉积组间一般资料及eGFR比较
两组24 h尿蛋白定量、高血压占比比较,差异无统计学意义(P > 0.05)。伴IgM沉积组年龄、eGFR水平低于不伴IgM沉积组,血肌酐水平高于不伴IgM沉积组,差异均有统计学意义(均P < 0.05)。见表3。
3 讨论
IgAN是一种进展性肾病,研究显示[7-10],约30%的IgAN最终可发展至ESRD。IgAN的临床表现多样,其预后亦不相同,更加细致地对IgAN进行分型很有必要,若增生硬化性IgAN未能得到早期诊断和治疗,其病情更容易发展至ESRD[10-11]。
本研究中3例患者以肉眼血尿为首发症状,10例患者病程中出现肉眼血尿,所占比例11.21%,低于既往报道[13-14]表现为血尿的IgAN患者所占比例,考虑与本研究纳入的病例为增生硬化性IgAN有关。有研究显示[15],以单纯性血尿为表现的IgAN患者的肾功能损伤和病理表现均较轻。但近来的报道倾向于以单纯血尿或少量蛋白尿为主的IgAN患者其病情仍可进展,会出现临床与病理表现不一致的情况,仍需引起足够的重视[16-18]。
本研究中高血压的发生率较高(43.97%),其中CKD1~3期约40.0%,CKD4期达71.4%,CKD5期甚至达到100.0%,考虑与本研究中CKD4~5期患者例数较少,误差较大有关。高血压是预测IgAN病情进展的强烈危险因素[4]。一项来自法国的332例IgAN患者的回顾性研究显示[19],与发病时不伴高血压比较,伴有高血压的患者在20年内进展至ESRD或死亡的风险由6%升至41%。临床应把积极控制血压作为重要手段,这有助于延缓疾病进展。
本研究中不同CKD分期患者高尿酸血症的发生率不同,CKD5期高于CKD1~4期,考虑与CKD5期的样本量太小相关。发病时伴血尿酸升高的有56例(48.28%),其中男36例,女20例,这与吕天洋等[20]的报道男性多于女性一致。本研究中47例患者有肾小管的萎缩和小动脉管壁的增厚,与文献报道[21]该类患者的血清基质金属蛋白酶抑制剂-1(TIMP-1)水平升高与肾小管间质病变和肾小动脉病变相关一致。国内一项为期8年的回顾性研究[22]发现血尿酸升高者的eGFR下降,进入终末期肾脏病的结局事件发生率均高于血清尿酸水平正常者。因此控制血尿酸水平也是延缓IgAN进展的一项重要手段。
有研究显示[23],增生硬化性IgAN患者通常伴有肾功能受损。本研究116例患者的血肌酐在43~391 μmol/L,平均(120.63±66.68)μmol/L。有研究显示[24],肾小球系膜区IgM沉积对IgAN的肾脏存活有一定的影响,IgM沉积可使血管病变及肾小球硬化的程度加重,认为IgM沉积可能是IgAN病理预后不良的早期指征。但是IgM沉积与IgAN预后及相关危险度之间的关系仍存在许多争议,IgM沉积在IgAN患者中的预测评估作用尚不明确[25-26]。本研究结果显示伴缺血性肾损伤组血肌酐高于不伴缺血性肾损伤组;伴IgM沉积组血肌酐水平高于不伴IgM沉积组(均P < 0.01)。伴缺血性肾损伤组eGFR低于不伴缺血性肾损伤组;伴IgM沉积组eGFR水平低于不伴IgM沉积组(均P < 0.01),这对临床判断患者的预后可能具有一定意义。与王建等[27]、豆利军等[28]的研究结果相似。但不同缺血性肾损伤组、不同IgM沉积组24 h尿蛋白定量比较,差异无统计学意义(P > 0.05),结合临床中一些就诊时以血肌酐升高为主诉却不伴蛋白尿的患者来看,无不是一种启示,一些患者发病时可能已有肾脏组织病理的损伤,因此这些患者需要进行更多的隨访与研究,其具体发病及作用机制有待研究。
由于本研究为单中心的回顾性研究,收集的病例数较少,且存在一定的局限性,因此,其结果尚需未来进行大样本量、多中心的临床研究及预后的随访工作加以验证。
[参考文献]
[1] 刘刚,马序竹,邹万忠,等.肾活检患者肾脏病构成十年对比分析[J].临床内科杂志,2004,21(12):834-838.
[2] Maixnerova D,Reily C,Bian Q,et al. Markers for the progression of IgA nephropathy [J]. J Nephrol,2016,29(4):535-541.
[3] Shu D,Xu F,Su Z,et al. Risk factors of progressive IgA nephropathy which progress to end stage renal disease within ten years:a case-control study [J]. BMC Nephrol,2017,18(1):11.
[4] Moriyama T,Tanaka K,Iwasaki C,et al. Prognosis in IgA nephropathy:30-year analysis of 1,012 patients at a single center in Japan [J]. PLoS One,2014,9(3):e91756.
[5] National Kidney Foundation. K/DOQI clinical practice guidelines for chronic kidney disease:e-valuation,classification,and stratification [J]. Am J Kidney Dis,2002,39(2 Suppl 1):S1-S266.
[6] 全国肾活检病理诊断研讨会.肾活检病理诊断指导意见[J].中华肾脏病杂志,2001,17(4):270-275.
[7] Min L,Wang Q,Cao L,et al. Comparison of combined leflunomide and low-dose corticosteroid therapy with full-dose corticosteroid monotherapy for progressive IgA nephropathy [J]. Oncotarget,2017,8(29):48375-48384.
[8] Zheng Y,Wang Y,Liu S,et al. Potential Blood Pressure Goals in IgA Nephropathy:Prevalence,Awareness,and Treatment Rates in Chronic Kidney Disease Among Patients with Hypertension in China(PATRIOTIC)Study [J]. Kidney Blood Press Res,2018,43(6):1786-1795.
[9] Tomino Y. Immunopathological predictors of prognosis in IgA nephropathy [J]. Contrib Nephrol,2013,181:65-74.
[10] 周悦玲,蒋更如.IgA肾病进展至终末期肾病临床预测的研究现状[J].上海交通大学学报:医学版,2016,36(2):296-301.
[11] 马明明,管保章,罗丽花,等.50例增生硬化性IgA肾病的临床病理特点及激素治疗疗效分析[J].中华肾脏病杂志,2016,32(8):568-572.
[12] 程根阳,王云,袁文明,等.增生硬化性IgA肾病伴贫血患者的临床病理特征及预后[J].中国全科医学杂志,2018, 21(18):2185-2189.
[13] 何玲艳,曹霞,杨淡昳,等.单纯血尿和/或轻度蛋白尿IgA肾病临床病理分析[J].中南大学学报:医学版,2019, 44(6):642-648.
[14] 段姝伟,张岩,吴杰,等.少量蛋白尿IgA腎病患者镜下血尿与病理指标的相关性分析[J].中华肾病研究电子杂志,2018,7(3):102-106.
[15] 廖莹,万启军,胡豪飞,等.单纯性血尿IgA肾病临床病理回顾性分析[J].深圳中西医结合杂志,2017,27(9):31-33.
[16] 刘扬,刘睿,杨再波,等.IgA肾病单纯性血尿患者牛津病理分型特点及临床预后分析[J].中国中西医结合肾病杂志,2019,20(6):498-500.
[17] 刘欢欢,尹良红,刘璠娜,等.IgA肾病单纯性血尿患者肾脏病理分级与临床的关系[J].临床医学工程,2017,S1:23-27.
[18] 刘杰,杨定平.少量蛋白尿IgA肾病临床特征及肾功能损伤相关因素分析[J].临床肾脏病杂志,2018,18(4):206-210.
[19] Berthoux F,Mohey H,Laurent B,et al. Predicting the risk for dialysis or death in IgA nephropathy [J]. J Am Soc Nephrol,2011,22(4):752-761.
[20] 吕天洋,张静,贾红彦,等.原发性IgA肾病并发血尿酸升高患者影响因素分析[J].中国实验诊断学,2019,23(9):1536-1537.
[21] 程根阳,李茹曼,李海剑,等.IgA肾病合并高尿酸血症患者血清TIMP-1水平与肾脏病理分型的关系[J].河南医学研究,2018,27(10):1763-1765.
[22] Cheng GY,Liu DW,Zhang N,et al. Clinical and prognostic implications of serum uric acid levels on IgA nephropathy:a cohort study of 348 cases with a mean 5-year follow-up [J]. Clin Nephrol,2013,80(1):40-46.
[23] 邹万忠.肾活检病理学[M].3版.北京:北京大学医学出版社,2014:126-133.
[24] Liu Z,Li L. Polymorphism in IgA nephropathy [J]. Nephrology,2015,3(1):63-66.
[25] Yin XL,Zou MS,Zhang Y,et al. Twenty-three-year review of disease patterns from renal biopsies:an experience from a pediatric renal center [J]. J Nephrol,2016, 26(4):699-707.
[26] Knoppova B,Reily C,Maillard N,et al. The Origin and Activities of IgA1-Containing Immune Complexes in IgA Nephropathy [J]. Front Immunol,2016,7:117.
[27] 王建,李庆士,李龙海,等.277例IgA肾病患者病理分型与临床特点分析[J].中国医学前沿杂志:电子版,2015, 7(8):85-88.
[28] 豆利军,王国平,闵瘤芳,等.IgM沉积预测原发性IgA肾病患者预后风险性及相关危险因素分析[J].现代中西医结合杂志,2019,28(28):3144-3148.
(收稿日期:2020-01-20)
