季节性流感病毒裂解疫苗在小鼠中的安全性和免疫原性研究∗
2020-12-23鹿双双师晓萌王昕昉刘晓宇
鹿双双 荣 蓉 庞 帅 师晓萌 王昕昉 刘 哲 刘晓宇
(中国疾病预防控制中心,北京 102206)
流行性感冒(简称流感)是由流感病毒引起的急性呼吸道传染病,其抗原性易变,具有高度的传染性,每年可引起季节性流行,在学校、托幼机构和养老院等人群聚集的场所可发生暴发疫情,是严重危害全球公众健康的呼吸道传染病,历史上曾多次引起大规模的世界性大流行[1-3]。近年来,不断出现的新型流感病毒仍然在威胁着人类的生命安全,2009年甲型H 1N1流感病毒在全世界范围大暴发,引起了较高的发病率及死亡率,对人类健康造成了巨大威胁[4]。根据世界卫生组织(WHO)估计,每年季节性流感可导致全球300万~500万重症病例,其中29万~65万死亡[5]。由于治疗流感至今尚无特效药,接种流感疫苗被认为是预防和控制流感大流行的最经济且行之有效的方法。世界卫生组织每年会根据全球流感流行情况,预测流感流行趋势,从而推荐适合本年度流感疫苗生产的毒株,目前市场上的人用流感疫苗主要是以鸡胚为生产基质制备的H1N1,H3N2和B型三价流感病毒裂解疫苗。为了验证季节性流感病毒裂解疫苗在动物体内的安全性和免疫原性,本研究参照《中国人民共和国药典(2015版)》第三部《生物制品》中“通则1141方法”规定[6],使用小鼠动物模型进行安全性和免疫原性评价。现将研究结果报告如下:
1 材料与方法
1.1 疫苗
华兰生物疫苗有限公司生产的流感病毒裂解疫苗(该公司已上市销售疫苗),注射剂型,规格为0.5 mL/支,含流感病毒株血凝素为 15μg/型。国药准字:S20083016,生产批号:201807B009。疫苗系用WHO推荐的甲型和乙型流感病毒毒株,分别为:A/Michigan/45/2015(H1N1)pdm09类似株、A/Sigapore/INFIMH-16-0019/2016(H3N2)类似株、B/Colorado/06/2017(Victoria系)类似株。
1.2 流感病毒标准参考抗原及标准参考抗血清
标准参考抗原:A/Michigan/45/2015(H 1N1),A/Sigapore/INFIMH-16-0019/2016 ( H3N2 ),B/Colorado/06/2017;标准参考抗血清:雪貂抗A/Michigan/45/2015(H1N1)毒株血清,雪貂抗A/Sigapore/INFIMH-16-0019/2016(H 3N2)毒株血清,雪貂抗B/Colorado/06/2017毒株血清;均为国家流感中心制备并提供。
1.3 实验动物
SPF 级雌性健康BALB/c小鼠(6~8周龄,),购自斯贝福(北京)生物技术有限公司,实验动物生产许可证号:SCXK(京)2016-0002。所有实验动物在接种疫苗前均未检测出相关流感抗体。
1.4 主要试剂耗材
受体破坏酶(RDE),WHO提供;1%的火鸡及豚鼠红细胞悬液,国家流感中心制备并提供;磷酸盐缓冲液(PBS),Gibco by life technology;96孔“V”型底微量板,CORNING。
1.5 小鼠异常毒性试验
参照《中国药典》三部(2015版)方法进行异常毒性检查。BALB/c小鼠在屏障区适应性饲养3 d后,每只小鼠称体质量,体质量符合药典要求18~22 g。将小鼠随机分为疫苗接种组和空白对照组,每组5只。疫苗接种组每只小鼠腹腔注射0.5 mL测试疫苗,空白对照组以相同的方式注射0.5 mL PBS。接种后连续观察7 d,每天记录动物的活动、饮食、体质量及精神状况,判断是否有不良临床反应。
1.6 小鼠免疫原性试验
BALB/c小鼠在屏障区适应性饲养3 d后,将小鼠随机分为试验组和空白对照组,每组10只。试验组每只小鼠均肌肉注射0.1 mL测试疫苗,空白对照组每只小鼠注射0.1 mL PBS。接种后连续观察49 d,每天记录动物的活动、饮食及体质量情况。分别于接种后 0、14、28、35 和 49 d,采用小鼠眼眶后静脉丛方法采血并分离血清。
1.7 血清抗体检测
用红细胞凝集抑制试验(hemagglutination inhibition,HI)检测血清中抗体水平[全国流感监测技术指南(2017年版)],用于评估免疫原性。判定标准:免疫前HI抗体效价<1∶10,免疫后HI抗体效价≥1∶40判为阳转;或免疫前HI抗体效价≥1∶40,免疫后HI抗体效价4倍或4倍以上增长判为阳转[7]。
1.8 试验设施
中国疾病预防控制中心实验动物中心ABSL-2实验平台。
2 结果
2.1 小鼠接种疫苗的异常毒性试验
空白对照组和疫苗接种组小鼠在7 d观察期内均全部存活,小鼠外观体征、行为活动、呼吸、粪便等均未见异常。小鼠饮食、饮水及精神状况均正常,未见明显的不良临床反应。观察期内空白对照组和疫苗接种组小鼠体质量均增加(图1)。本试验表明,该疫苗的安全性良好,对小鼠的生长无影响,符合《中国药典》三部(2015版)判定标准。

图1 小鼠异常毒性试验的体质量变化情况注:C为空白对照组,T为疫苗接种组Fig.1 The Changes in body mass of mice in toxicity testNote:C means the negative control group,T means the test group
2.2 小鼠免疫原性试验结果
本试验模拟人体疫苗接种,只进行一次免疫,观察免疫后不同时间的抗体水平。免疫接种组结果:免疫前,所有小鼠的HI抗体滴度均为检测水平以下<10;免疫后14 d,4只小鼠血清抗A(H 1N1)pam09阳性,2只小鼠抗 A(H3N2)阳性,所有小鼠抗 B(Victoria系)均为阴性;免疫后28 d,所有小鼠血清抗A(H1N1)pam09和 A(H3N2)抗体均阳性,B(Victoria系)抗体依然没有明显变化,均为阴性。免疫后35 d,小鼠血清抗体水平均继续升高,达到峰值,抗A(H1N1)pam09和 A(H 3N2)抗体最高值达到了 1 ∶320;B(Victoria系)抗体水平明显升高,7只小鼠抗体阳性,最高 HI滴度达到了1∶80。免疫后49 d,小鼠血清抗体仍然维持在35 d的水平。对照组的所有小鼠血清抗体在观察期间均为检测水平以下<10(表1)。本试验表明,该季节性流感病毒裂解疫苗对小鼠进行一次性免疫,即能达到良好的免疫效果。
2.3 免疫后小鼠血清H I抗体阳转率分析
小鼠疫苗免疫后,28 d血清抗A(H1N1)pam09和A(H3N2)HI抗体阳转率均达到了100%,此时抗B(Victoria系)抗体水平没有变化,为0%;免疫后35 d,B(Victoria系)的抗体水平明显上升,阳转率达到70%。小鼠抗A(H1N1)pam09、A(H3N2)和 B(Victoria系)抗体水平均达到峰值。HI抗体阳转率分析表明,对该疫苗进行一次接种,合格率达到了70%及以上(表2)。
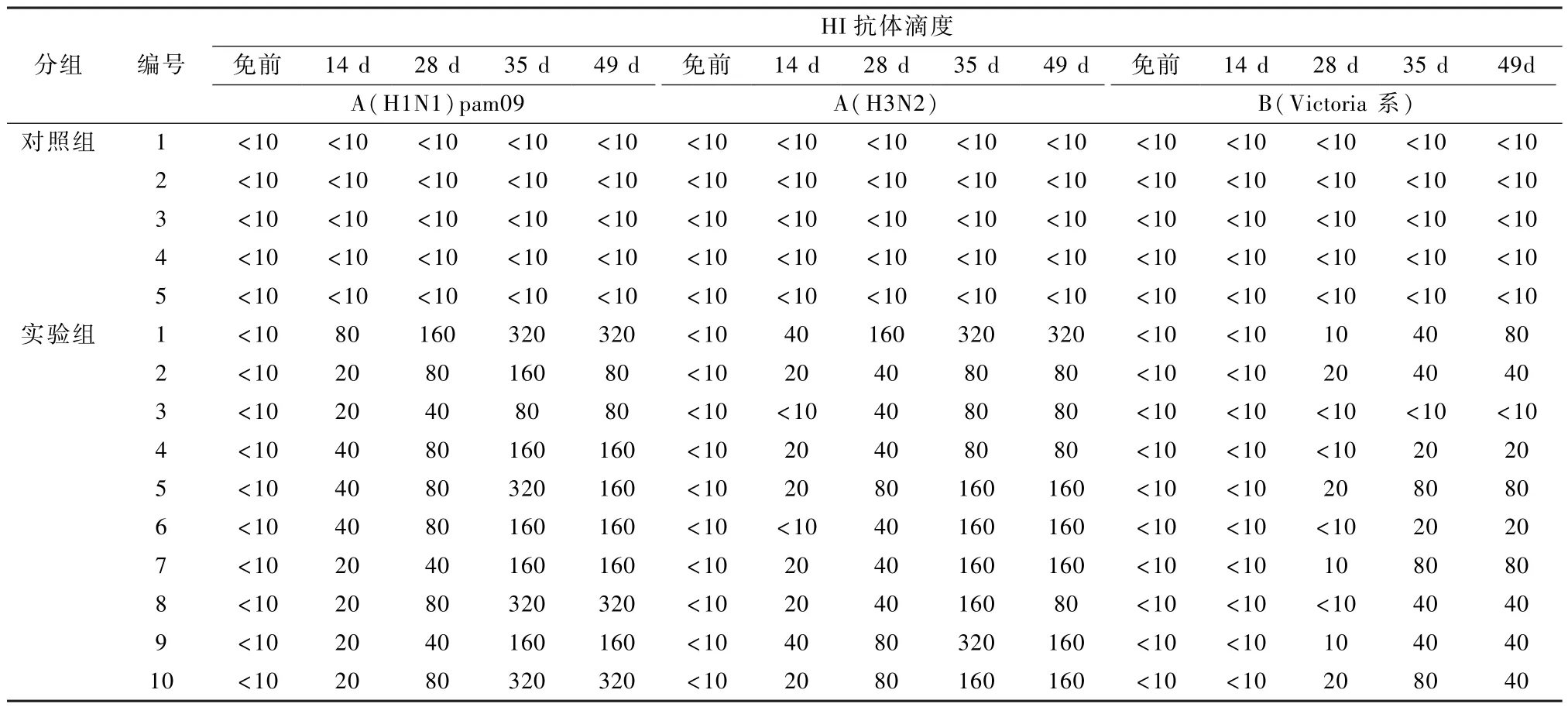
表1 裂解疫苗免疫小鼠血清抗体检测试验结果Table 1 Results of serum antibody test in mice immunized with spilt vaccine
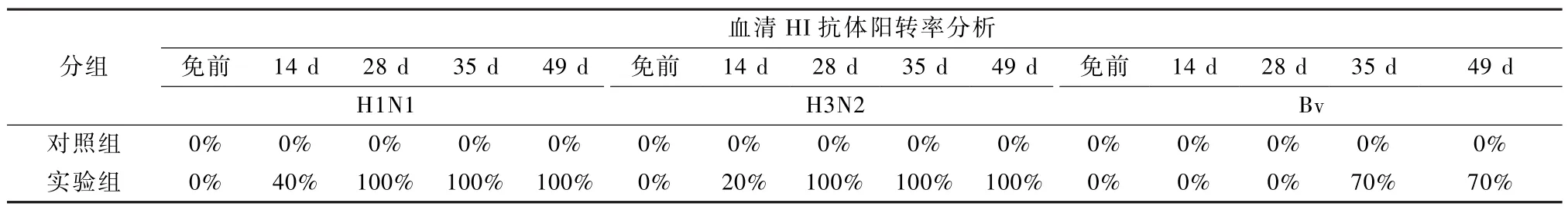
表2 裂解疫苗免疫小鼠血清阳转率分析Table 2 The analysis of serum positive conversion rate in mice immunized with spilt vaccine
3 讨论
3.1 疫苗免疫是必要的
流感的发生是因机体在遭受流感病毒感染后所引起的一种急性呼吸道感染症状,特点是“突然暴发,迅速蔓延,发病率高,并发症重”,严重危害人群健康。由于流感病毒基因多变和宿主多样的生物学特性,不断出现新的变异毒株,因此可在人群中广泛传播,造成反复感染和发病[8]。流感流行在人群中导致较重的健康和经济负担,不同人群的流感疾病负担差异较大,婴幼儿、老年人和慢性基础疾病患者等高危人群,患流感后出现严重疾病和死亡的风险较高。有报道表明,老年人和慢性疾病流感患者常引起肺炎、心肌炎、中耳炎及脑炎并发症,老年流感患者的死亡率可高达7%[9]。在流感大流行期间,儿童受袭击的可能性最大,大量研究表明,流感是导致儿童就诊和住院的重要原因。据估计,每年约有10%~15%的儿童因流感感染而需就诊[10],尤其是<1岁婴儿就诊率最高[11]。
中国是被世界公认为流感的高发地区,因此国内流感流行动态已引起WHO和世界各国的瞩目。我国A型流感呈多样化的空间模式和季节性特征:北纬33°以北的北方省份,呈冬季流行模式;北纬27°以南的最南方省份,呈夏季流行模式;而两者之间的中纬度地区,每年1~2月和 6~8月的双周期高峰。B型流感在我国大部分地区呈单一冬季高发[12]。在中国北方城市和南方城市,流感相关呼吸和循环系统疾病超额死亡率年均分别为12.4例/10万人和8.8例/10万人[13],至目前为止,还未找到理想的防治流感的药物,流感疫苗的免疫接种仍为当今防治流感疾病发生和流行最有效的一种手段,每年接种流感疫苗可以显著降低接种者罹患流感和发生严重并发症的风险。药物预防不能代替疫苗接种,只能作为没有接种疫苗或接种疫苗后尚未获得免疫能力的重症流感高危人群的紧急临时预防措施。
3.2 疫苗是安全的
目前,流感灭活裂解疫苗是目前全世界最为广泛使用的流感疫苗,在国内外经过多年的临床验证,已证明具有较好的安全性。我国市场上最多的为三价流感病毒裂解疫苗,流感裂解疫苗可降低全病毒灭活疫苗的接种不良反应,并保持相对较高的免疫原性,不仅接种保护效果好,而且临床不良反应极少,适合各年龄段的人群接种[14]。本次观察结果显示,大剂量腹腔注射接种该批次疫苗,小鼠饮食、饮水及精神状况均正常;疫苗接种后小鼠体质量稳定增长,说明疫苗对小鼠生长无影响。动物试验结果提示,本试验使用的该批次疫苗,异常毒性检查结果符合《中国药典》三部(2015版)相关规定,表明该批次流感病毒裂解疫苗是安全和可靠的,可以放心接种。
3.3 疫苗是有效的
流感疫苗免疫原性的评价指标主要为病毒株特异性HI抗体水平和血清抗体阳转率,根据欧盟药品评价局和美国食品药品管理局的标准要求流感疫苗接种后:(1)HI抗体≥1 ∶40;(2)血清阳转率,即免疫接种前HI抗体<1 ∶10,免疫后HI抗体≥1 ∶40,或免疫接种前HI抗体≥1∶10,免疫接种后HI抗体几何平均滴度(geometric mean titers,GMT)增长4倍及以上。小鼠免疫原性试验结果表明,免疫后28 d,所有小鼠血清抗 A(H1N1)pam09和 A(H3N2)抗体均阳性(HI滴度为 40~160),抗体阳转率达到了100%;到35 d,B(Victoria系)的抗体阳转率也达到了70%,提示该三价流感裂解疫苗具有较好的免疫原性,免疫接种小鼠是有效的。
综上所述,本研究使用的流感季节性裂解疫苗免疫小鼠,通过大剂量安全试验,未见小鼠有不良临床反应及疫苗副反应,对生长无影响,说明疫苗安全性较好;效力试验表明,免疫后 28 d,A(H 1N1)pam09和A(H3N2)抗体合格率均可达到100%,免疫后35d,B(Victoria系)的抗体合格率均可达到70%,提示疫苗保护效果较好。Essen等[15]曾对50个发达国家和发展中国家进行了流感疫苗使用概况的统计分析,结果发现全世界67%的流感疫苗被用于北美、西欧、澳大利亚、新西兰等发达国家,而占世界人口绝大多数的发展中国家仅使用了33%的疫苗。目前我国每年接种流感疫苗约600万人份,按城镇人口估算接种率为10‰,接种率非常低,尚未形成有效的流感免疫屏障。因此,减少感染流感的机会,防止流感大流行紧急事件的发生,普及流感疫苗的接种,积极推广流感疫苗接种是十分必要的。
