微型化学实验莫尔法测定云南某磷肥厂锅炉水中氯*
2020-12-16聂鹏飞王奕舒王学文黄永丽余慧茹
聂鹏飞,彭 桦,龚 丽,姜 威,王奕舒,张 慧,王学文,黄永丽,余慧茹
(1 云南磷化集团有限公司,云南 昆明 650600;2 国家磷资源开发利用工程技术研究中心,云南 昆明 650600)
锅炉水中氯离子浓度过高会使水质变差,引起锅炉设备内部结垢与腐蚀,即使十万分之几级别剂量的存在,在加热蒸发过程中,锅炉腐蚀也不可避免,尤其是对不锈钢造成应力腐蚀[1]。因此需要重点监控锅炉水中氯离子的含量。
《工业锅炉水质》(GB/T 1576-2008)[2]要求:软水器再生后出水氯离子含量不得大于进水氯离子含量的1.1倍,日常检测中经常出现锅炉给水中氯离子含量远大于原水中氯离子含量的1.1倍,且实际情况是多数生产单位直接不检测,造成锅炉排污率高,给水氯离子含量较高,锅炉水含盐量相应增加,水中含盐量越高,腐蚀速度越快,金属表面直接暴露在高温高氯水中,极易造成金属接触面腐蚀。通过微型化学实验[3]可现场即时报样,适当给锅炉水加药和定期排污,使锅炉水满足标准要求,避免结垢引起大量热能损失。
1 实 验
1.1 实验原理
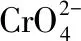


1.2 仪器试剂
分析天平(0.0001 g),自动滴定仪-德国VITLAB自动回零滴定仪(10 mL);移液管(10 mL),锥形瓶(50 mL),容量瓶(50 mL),烧杯(50 mL),吸量管(1 mL、5 mL、10 mL),HCl(1:1),K2CrO4(0.5%),AgNO3(0.005 mol/L)。
1.3 实验步骤
锅炉水取样(微型实验法和常规法一样),水深大于1 m时,在表层1 m下采样;小于1 m时,在水深二分之一处采样,取500 mL左右水样,样品经中速定量滤纸干过滤后备用(也可经过0.45 μm水系滤膜过滤);准确移取10 mL过滤后的水样装入150 mL锥形瓶中,加入1~2滴K2CrO4(0.5%)作为指示剂,用AgNO3标准溶液(0.005 mol/L)进行中和滴定,滴定终点特征:由黄色浑浊(黄色K2CrO4在白色絮状沉淀中)变成砖红色,记下AgNO3溶液消耗的体积,平行测定3份,计算锅炉水中 Cl-的含量。
2 结果与讨论
2.1 标准溶液配制与标定-微型化和实验室常规化比较
本实验所用标准溶液均可用微型化实验和实验室常规化进行配制。(1)在现场配制好标液后,现场即可标定使用是微型化实验的显著特征,因此与实验室测定时结果基本相同,系统误差极低。(2)实验室常规化可一次性配好大量标准溶液,可稳定在密闭瓶中3个月保持物化属性不变(3个月之后则需重新标定),如此可保证现场工作量大幅缩减,在外部气候温差改变不大的前提下,笔者常在实验室常规化配制大量标准溶液保存使用,去往现场则取适量标液使用,既能达到分析精度标准要求,也大大提高了工作效率。
2.1.1 微型化-AgNO3(0.005 mol/L)标准溶液的配制与标定
(1)用微量天平称0.085 g硝酸银,加入到100 mL不含氯的蒸馏水中,摇匀后密封储存于实验室柜中,此时AgNO3溶液浓度约为0.005 mol/L,待标定。
(2)准确称取0.07~0.08 g NaCl置于小烧杯中,加入一定量蒸馏水,然后转移至250 mL容量瓶中,稀释至刻度,摇匀备用。
(3)用吸量管移取NaCl溶液10 mL置于150 mL锥形瓶中,加入1滴K2CrO4(0.5%)指示剂,在充分摇动下,用AgNO3溶液进行滴定(注意边摇边滴),滴定至呈现砖红色即为终点,平行测定3份,计算AgNO3溶液的准确浓度。
计算公式:
式中:C——AgNO3溶液的摩尔浓度,mol/L
m——NaCl质量,g
M——58.44 g/mol
V——AgNO3的消耗体积,L
氯标准储备溶液(国家有色金属及电子材料分析测试中心):1 mg/mL
氯标准工作溶液:1 mg/L,经过氯标准储备溶液逐级稀释而成
2.1.2 实验室-AgNO3(0.005 mol/L)标准溶液的配制与标定
(1)称8.5 g硝酸银,加入1000 mL不含氯的蒸馏水,转移到带玻璃塞的棕色试剂瓶中,AgNO3溶液浓度约为0.05 mol/L,待标定。
(2)准确称取1.46 g NaCl置于小烧杯中,加入蒸馏水溶解后,转移至500 mL容量瓶中,稀释至刻度,摇匀备用。
(3)用移液管移取NaCl溶液100 mL置于150 mL锥形瓶中,加入1~2滴K2CrO4(0.5%)指示剂,充分摇匀,用AgNO3溶液逐步滴定(控制滴定速度、保持边滴边摇),滴定至呈现砖红色即为终点,平行测定3份,计算AgNO3溶液的准确浓度。
微型化实验和常规实验的标准溶液配制和标定方法都可以用于微型化实验,按照所用试剂对比,微型化实验试剂用量是常规实验的十分之一。
2.1.3 微型实验样品测定
准确移取过滤后的10 mL水样,置于150 mL锥形瓶中,加入1~2滴K2CrO4(0.5%)指示剂,用AgNO3标液(0.005 mol/L)开展滴定,滴定终点:至滴液由黄色浑浊(黄色K2CrO4在白色絮状沉淀中)呈现砖红色,记下消耗的AgNO3溶液体积,平行测定3份,计算锅炉水中 Cl-的含量。
计算公式:
式中:C——硝酸银标准溶液的浓度,mol/L
V1——测定水样所消耗硝酸银溶液的体积,mL
V0——空白实验所消耗硝酸银溶液的体积,mL
V——所取水样的体积,mL
2.2 微型实验的加标回收率
加标实验:采用氯标准储备溶液(国家有色金属及电子材料分析测试中心)1 mg/mL。氯标准工作溶液:1 mg/L,经过氯标准储备溶液逐级稀释,进而配制不同浓度标准溶液,然后随机加入锅炉水,用于回收率试验。每个浓度于不同天数测定 6次,测定结果见表 1。

表1 微型实验锅炉水加标回收试验结果
从结果可以看出,加标回收率在98.6~104.1之间,结果差异不显著。
2.3 微型实验的准确度
对比实验:采用常规莫尔法和微型实验法,对水样进行对比实验,每个浓度于不同天数测定 5次,测定结果见表2。
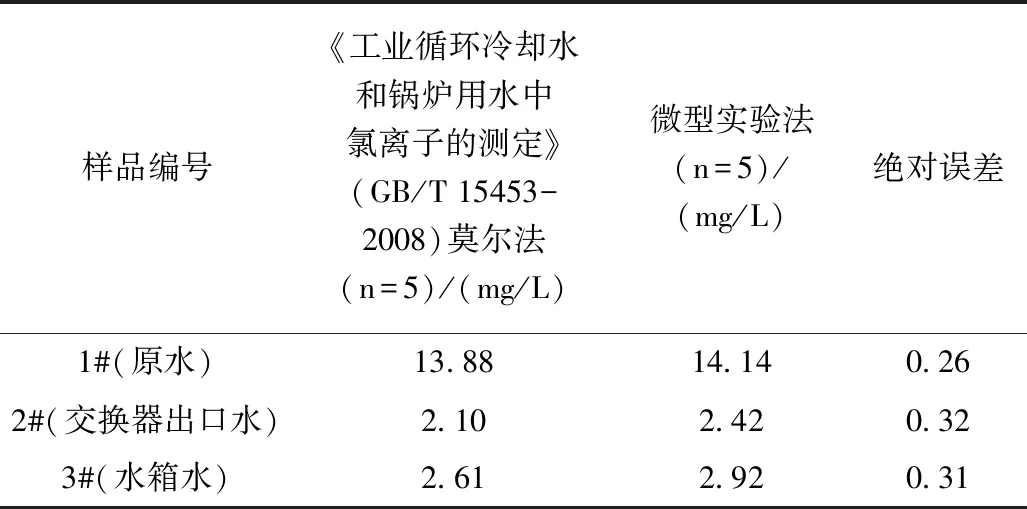
表2 锅炉水准确度试验结果
实验结果表明,微型实验法绝对误差在0.5以下,符合允许差标准。
2.4 微型实验所产生废液中银的回收
银为贵金属,含AgCl的废液应回收处理。微型实验所产生废液可用塑料桶收集,加盖储存,待超过5 L后回收处置。
主要反应方程式如下:


操作过程:
(1)生成氯化银沉淀:将大量的氯化钠加入到含氯化银的废液中,使氯化银完全沉淀,然后过滤、洗涤、烘干。
(2)提取银粉:将铁片置于AgCl沉淀中,再加入浓盐酸,然后加热至沸腾,恒速搅拌,至白色AgCl沉淀全变成灰白色的银粉为止,最后用自来水洗涤两遍,烘干即可。
2.5 锅炉水氯含量监控重点
司炉工一般把锅炉的主体操作作为工作重点,而忽略水处理工作。锅炉的省煤器、水冷壁、对流管束会因氯离子含量高而引起腐蚀,使这些金属构件变薄、凹陷甚至穿孔,强度显著降低,缩短了锅炉的使用年限。定期监控处理锅炉水中的氯离子,及时给锅炉水加药和定期排污[4],能避免锅炉结垢、胀管、变形或爆管事故。
2.6 其 它
(1)微型化学实验法的最低检出限为10 mg/L。
(2)允许误差同《工业循环冷却水和锅炉用水中氯离子的测定》(GB/T 15453-2008)方法[5]。同一操作者使用相同仪器,按相同测试方法,在短时间内对同一被测对象平行测定结果的误差值应满足表3要求。

表3 同一被测对象平行测定结果的误差值
(3)锅炉水中氯离子检测酸度范围应为pH=6.5~7.2(广泛pH试纸),若水样碱性太强,可用稀硝酸中和;酸性太强,可用碳酸氢钠或四硼酸钠中和。
(4)所取样品剂量、标准溶液及其浓度选择、滴定方式和速度等均会给测定结果带来相关误差,为此,必须增加空白实验辅助校正。
(5)实验结束后,滴定管应先用蒸馏水洗2~3次,再用自来水冲洗,以免产生氯化银沉淀,难以洗尽。
(6)可制作便携式塑料仪器箱(520 mm×130 mm×110 mm),盛装全部玻璃仪器及实验操作台,体积小,携带、使用、保管便利,统一配发。
3 结 论
对取水方法、微型实验试剂用量等实验参数的最佳组合条件及其关系进行了探索,从结果可以看出,加标回收率在98.6~104.1之间;大量实验结果表明,微型实验法绝对误差在0.5以下,符合允许差标准。用微型化学实验分析代替或补充传统分析方法,因其具有:试剂用量小、易于观察、现场可直接报样[6]、方法简单、安全、高效、便于携带和避免破坏环境等特点[7],提高了分析效率,便于推广,其结果与《工业循环冷却水和锅炉用水中氯离子的测定》(GB/T 15453-2008)莫尔法测定锅炉水中氯离子法比较,无显著性差异,适合大批量锅炉水快速控制分析。
