沉淀/吸附法处理电镀废水中的重金属
2020-12-14贾彦松葛庆
贾彦松 葛庆


摘 要:针对电镀废水中不仅存在重金属离子还存在金属络合物,通过化学沉淀与离子交换树脂吸附法联用深度处理电镀废水中的Cu2+、Zn2+及其金属络合物。通过考察pH值、吸附时间、温度等影响因素对重金属离子及其络合物去除效果的影响,选取最佳条件。结果表明:利用NaOH调节pH为12,在室温条件下搅拌8 min然后静置40 min,通过化学沉淀法去除Cu2+和Ni2+,去除率达95%以上;热失重分析结果证明离子交换树脂能够有效地吸附重金属络合物。在离子交换树脂吸附重金属络合物的实验中,增加离子交换树脂质量和吸附时间,重金属络合物EDTA-Cu、EDTA-Ni去除率达99.5%以上。
关 键 词:去除率;化学沉淀;重金属离子;离子交换树脂;重金属络合物
中图分类号:TQ 325.7 文献标识码: A 文章编号: 1671-0460(2020)10-2133-05
Abstract: Aiming at the existence of heavy metal ions and metal complexes in electroplating wastewater, chemical precipitation and ion exchange resin adsorption were used to deeply treat Cu2+, Zn2+ and their metal complexes in electroplating wastewater. The influence of pH value, adsorption time, temperature and other factors on the removal effect of heavy metal ions and their complexes was investigated, the best conditions were determined. The results showed that, after using NaOH to adjust the pH to 12, stirring at room temperature for 8 min and then standing for 40 min, the removal rates of Cu2+ and Ni2+ both were as high as 95% or more by chemical precipitation; the analysis of thermal weight loss proved that the ion exchange resin could effectively adsorb heavy metal complexes. In the experiments of ion exchange resin adsorption of heavy metal complexes, increasing the ion exchange resin dosage and adsorption time, the removal rates of heavy metal complexes EDTA-Cu and EDTA-Ni both were as high as 99.5%.
Key words: Chemical precipitation; Heavy metal ion; Ion exchange resin; Heavy metal complex
电镀在汽车、工业制造等领域应用广泛,是现代电镀行业中最常见的应用[1-3],主要是通过电化学法对金属材料表面进行涂层处理改性,从而实现其外观、物理和化学性能等特征的改变,得到所想要的材料。电镀废水中最常见的重金属是铜和镍离子及其在电镀过程中产生金属络合物,其直接排放会对环境和人类健康造成极大危害[4-8]。目前,致力于电镀废水的处理工艺已有很多,最常用的方法有化学沉淀法、离子交换法、絮凝法和吸附法等[9-11]。刘伟[12-14]等采用Na2S作为沉淀剂处理电镀废水,研究Na2S在不同pH下的沉淀效果。靳志龙[15-17]等先后研究了絮凝剂、吸附材料在不同温度、时间下去除电镀废水中重金属络合物。沉淀法主要去除废水中的重金属离子,吸附法主要去除废水中的重金属络合物[18-19]。电镀废水成分复杂,单一的处理方法效果有限,为了更好地去除电镀废水中重金属,本文采用化学沉淀/吸附法深度处理电镀废水中的重金属离子及其络合物,研究不同pH值、搅拌时间、静置时间,离子交换树脂质量、吸附时间、温度等条件下的去除效果。
1 实验
1.1 试剂与仪器
试剂:NaOH(分析纯)、盐酸(分析纯)、NaCl、CuSO4、NiSO4(固体)、EDTA、717阴离子交换树脂、去离子水;仪器:电子天平、pH计、搅拌器、离心机、原子吸收分光光度计,以及离心管、烧杯、玻璃棒、搅拌子若干。
1.2 方法
配置质量浓度为50 mg·L-1 的硫酸铜、硫酸镍溶液,10 mg·L-1的EDTA-Cu、EDTA-Ni混合溶液(金属离子与络合物质量比例为5∶1),模拟电镀废水,在室温和转速为300 r·min-1的条件下,调节pH值,搅拌,静置,离心后,取其上清液,用原子吸收分光光度计测定清液中重Cu2+、Ni2+的质量浓度,通过公式计算Cu2+、Ni2+去除率。通过控制变量法,测量不同搅拌时间、初始pH值和静置时间下,重金属离子Cu2+、Ni2+的去除率。考虑沉淀法去除重金属络合物效果有限,通过离子交换吸附法,去除水中的重金属络合物EDTA-Cu和EDTA-Ni,改变阴离子交換树脂投加量、吸附时间和温度,选择最佳吸附条件。
Q(去除率)=(ρ初始质量浓度-ρ上清液质量浓度)/ρ初始质量浓度 。
2 结果与讨论
2.1 pH对Cu2+、Ni2+去除率影响
在硫酸铜、硫酸镍的初始溶液中,利用1 mol·L-1 HCl和NaOH溶液来调节pH,搅拌5 min , 静置30 min,观察重金属离子去除率。向其中加入NaOH溶液调节pH,离心后取其上清液,测定重金属离子的质量浓度,并计算出其中的去除率,去除效果如图1所示。
在 pH 从 7.5不断增加到14 的过程中,重金属离子Cu2+、Ni2+对应的去除率也随之不断增加。当 pH 为 7.5 时,Cu2+、Ni2+去除率分别为 49.8%、31.7%;当 pH 增加到12时,Cu2+、Ni2+去除率分别提升为 98.8%、98.3%,再继续调高pH,去除率增加效果不太明显。
Mn+ + nOH1- ? M(OH)n↓ 。
在碱性条件下重金属离子与OH-会生成难溶性的盐,这是因为随着碱性的增强,OH-质量浓度增大,整个反应会向生成难溶性盐方向反应,Cu2+、Ni2+会加速生成难溶性Cu(OH)2和Ni(OH)2。当pH达到12以后,随着沉淀物的增加,金属离子质量浓度相对下降,反应趋于平衡,去除率效果达到阈值,再增加pH对于去除重金属离子的意义不是很大。
2.2 搅拌时间对Cu2+、Ni2+去除率影响
在初始质量浓度为50 mg·L-1的硫酸铜和硫酸镍溶液中,调节pH到12,搅拌不同时间后,静置30 min,测定重金属离子的去除率,实验结果如图2所示。随着搅拌时间的增加,无论是Cu2+还是Ni2+,去除率都有所增加。到搅拌 6 min 以后,Cu2+去除率基本不变,去除效果趋于稳定,因此去除Cu2+的搅拌时间应超过6 min。随着搅拌时间从 2 min 增加到 8 min,Ni2+的去除效果明显,搅拌时间达到 8 min后,溶液中的是Ni2+质量浓度基本不变,故去除Ni2+搅拌时间应超过 8 min。综上所述,最佳搅拌时间为8 min。随着搅拌时间的不断增加,重金属离子Cu2+、Ni2+会增加与氢氧根离子的接触,反应会加速向生成难溶性盐方向进行。随着难溶性盐质量浓度的不断增加,重金属离子与氢氧根离子接触变少,反应变慢,最终趋于稳定。
2.3 静置时间对Cu2+、Ni2+去除率影响
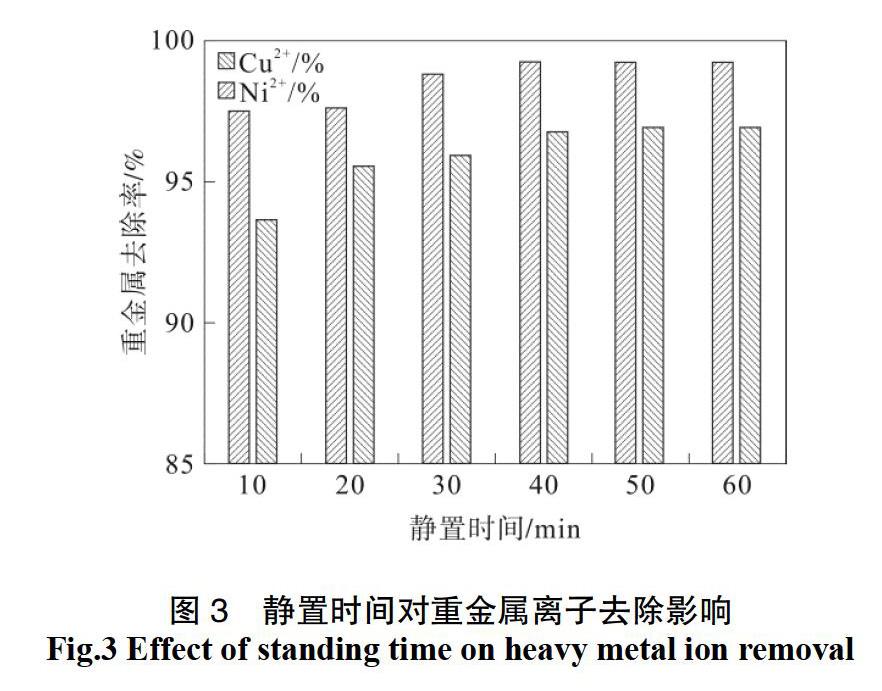
在初始质量浓度为50 mg·L-1的硫酸铜和硫酸镍溶液中,调节pH到12,搅拌8 min后,静置 10~60 min,测定Cu2+、Ni2+的去除率,结果如图3所示。从 10 min 到60 min,静置时间对处理重金属离子的影响不明显,随着静置时间的增加,Cu2+、Ni2+的去除率都有所上升,但变化非常小,40 min以后基本无变化。沉淀静置时间对去除效果的影响并大,另外考虑沉淀物形成的密度及稳定性等影响,确定静置最佳时间为40 min。随着反应的不断进行,生成的难溶性盐不断增加,难溶性盐间相互碰撞会加剧重金属离子Cu2+、Ni2+与氢氧根离子间的接触,使反应向生成难溶性盐方向进行。但该反应彻底、迅速,随着静置时间的增加,静置10 min和静置1 h去除重金属离子效果相差不大。
2.4 吸附剂质量对EDTA-Cu、EDTA-Ni去除率的影响
预处理717离子交换树脂:用饱和NaCl溶液浸泡24 h后,用去离子水清洗3遍,先用质量分数为5% 的盐酸浸泡8 h,洗干净后再用质量分数5% NaOH溶液浸泡8 h,洗干净烘干备用。调节模拟废水的pH至3.5,加入717阴离子交换树脂进行离子交换,室温条件下震荡1 h后,测定上清液中络合物的质量浓度,并计算去除率,实验结果如图4所示。
随着吸附剂质量不断增加,重金属络合物的去除率也随着上升。对于EDTA-Cu,当投加量从 0.5 g 增加到2 g时,去除率提高很快,从62.6%提高到83.6%,随后去除率呈现缓慢增加并保持稳定的趋势;对于EDTA-Ni,当投加量从0.5 g增加到2 g时,去除率提高最快,从41.8%提高到79.4%,然后吸附速率变慢,吸附剂增加到2.5 g时达到平衡,再增加吸附剂,吸附效果不再明显提高。随着吸附剂的继续增加,EDTA-Ni去除率基本上趋于平衡。去除重金属络合物EDTA-Cu、EDTA-Ni的效果与717阴离子交换树脂投加量呈正比,当树脂质量增加到一定时,吸附趋于稳定。因此从成本考虑和吸附效果来看,质量2 g是吸附的最佳条件。
717阴离子交换树脂通过树脂中的季胺基与重金属络合物EDTA-Cu、EDTA-Ni中的络合阴离子进行离子交换,从而去除水中的重金属络合物。随着717阴离子交换树脂投加质量不断增加,吸附的比表面积增加,树脂上的吸附位点明显增多,与重金属络合物的接触几率增大,进而能吸附更多的重金属络合物,吸附效率提高。当所加树脂的质量增加到一定时,吸附达到饱和,再增加树脂质量,吸附效率无明显变化。
2.5吸附时间对EDTA-Cu、EDTA-Ni的去除率影响
调节模拟废水 pH为3.5,然后准确称量 2.0 g 经过预处理的717离子交换树脂加入其中,放入预先设定好温度为 25 ℃的往复式水浴恒温摇床中,不同时刻取样测定重金属的质量浓度,取样的时间点设定为 0.25、0.5、1、2、3、4、5、6、24 h,并计算重金属在不同时刻的去除率,得到如图5所示的结果。
树脂对重金属络合物的去除率均为随着时间的增长先上升然后趋向稳定。对EDTA-Cu来说,在时间从 15 min 变化到 60 min 时,去除率提高最快,从 17.8%提高到83.6%,接着时间从 1 h 提高到 6 h,去除率仍保持一定的增加,只是增长速率变缓,到 6 h 时,去除率已达到 99.2%,到 2 4 h 时,取样测定,去除率为 99.8%,吸附趋于稳定;对EDTA-Ni的去除在最初的 1 h时间内,去除效果增速很快,10 min 时去除率为 19.6%,而1 h时去除率为79.4%,随后增速变慢,然后趋向稳定,到 6 h 时去除率已达到 99.5%,到 24 h 时去除率已能达到 99.5%。在6 h之后,阴阳离子树脂对重金属络合物的去除率趨于稳定,因此反应的最佳时间为 6 h。
这是因为随着吸附时间的延长,树脂上的吸附位点与重金属络合物接触时间变多,反应几率增加,吸附效率升高,从而使得重金属络合物去除率升高。当时间增加到一定值时,吸附效率达到饱和,再延长时间,去除效果无明显变化。
2.6 温度对EDTA-Cu、EDTA-Ni去除率的影响
在不同温度下(25、35、45、55 ℃),吸附 1 h后,EDTA-Cu、EDTA-Ni去除效果如图6所示。
从图6中可以看出,随着温度的升高,重金属络合物的去除效果增加,这说明随着温度的升高,吸附效果越来越好。这是因为吸附反应是一个吸热反应,随着温度的不断上升,重金属络合物更容易扩散到树脂内部,更容易发生离子交换。随着温度的升高,离子交换树脂的吸附过程加剧,离子间的流动加快,增加树脂与重金属络合物的接触几率,从而提升了吸附效率,增加了重金属络合物去除率。
2.6 热失重分析
将反应前后的树脂烘干后放入热失重分析仪,逐渐升温至1 000 ℃,进行热失重分析,结果如图7所示。从图7中可以看出,树脂吸附前后热失重曲线类似,说明吸附前后基团的变化不大,从树脂上失去的成分类似。未经任何处理的树脂在温度为1 000 ℃时质量仅为初始时20.40%,而吸附重金属络合物的树脂在1 000 ℃时质量为初始时24.87%。这是因为铜和镍等金属在高温下并不发生分解,而树脂主要成分为有机物,随着温度的升高有机物会逐渐分解,吸附前后残余质量之差即为吸附金属的量,这说明了717阴离子交换树脂能够有效地吸附重金属络合物。
3 结 论
本文通过化学沉淀法与离子交换树脂吸附法联合使用深度处理电镀铜锌废水,先用化学沉淀法处理重金属离子基础上,再用树脂吸附技术处理深度处理有机络合重金属,得到了如下结论。
1)通过调节pH,碱性条件下去除游離重金属离子效果非常好,去除率高达95%以上。
2)通过控制变量法,研究不同pH、搅拌时间、静置时间的重金属离子去除效果,从成本和效率来看,pH为12、搅拌时间8 min、静置时间40 min,为沉淀去除重金属离子的最佳条件。
3)针对重金属络合物,研究阴离子交换树脂对重金属络合物的去除影响因素,发现随着吸附时间和温度的增加,去除率明显提高,吸附时间24 h后重金属络合物去除率高达99.5%以上。
4)热失重分析结果证明了重金属络合物能够很有效地吸附在阴离子交换树脂上。
参考文献:
[1]戴琴,郑定成,曾威. 电镀行业现状及推行清洁生产的措施[J].广东化工,2012,39(14):124-125.
[2]张健军.铬系电镀污泥的重金属稳定化与固化研究[J].环保科技,2019,25(5):1-5.
[3]周光波,彭湘桂,陈加辉,等.光电子器件外壳脉冲电镀镍钴合金工艺及其耐蚀性[J].表面技术,2020,49(4):356-363.
[4]邹汉波,陈胜洲,赵朝晖,等.化学反应工程理论在电镀废弃物处理中的应用[J].电镀与涂饰,2019,38(23):1305-1310.
[5]谢堂锋,陈若葵,王明,等.废旧动力电池回收废料中镍含量的测定研究[J].矿冶工程,2020,40(1):121-124.
[6]刘备.高浓度难生化金属表面处理废水处理改造工程案例[J].工业水处理,2018,38(2):92-95.
[7]金艳青,周培培,祁高月,等.金属制品电镀废水的处理及回用工程[J].水处理技术,2015,41( 8):132-135.
[8]姜立萍.重金属废水处理技术综述[J].上海环境科学,2014, 33 (5):224-227.
[9] 张更宇,张冬冬.化学沉淀法处理电镀废液中重金属的实验研究[J].山东化工,2016,45(16):215-216.
[10] 陈松鹤.微电解在工业废水处理中研究进展[J].广东化工, 2019, 46 (8):118-119.
[11]杨世迎,薛艺超,王满倩.络合态重金属废水处理:基于高级氧化技术的解络合机制[J].化学进展,2019,31(8):1187-1198.
[12]刘伟.化学沉淀法处理电镀废液中总磷的实验研究[J].广东化工,2016,43(16):142-143.
[13]金艳青,周培培,祁高月,等.金属制品电镀废水的处理及回用工程[J].水处理技术,2015,41(8):132-135.
[14]孙琪娟,徐军礼,孙长顺.电镀污泥中Cr3+的堆浸工艺研究[J].当代化工,2017,46(10):2104-2107.
[15]杨金生,韩其利,王贤山,等.基于绿色发展的炼厂水处理技术集成[J].当代化工,2019,48(8):1877-1880.
[16]范晓慧,姚佳文,甘敏,等.活性炭净化烧结烟气过程的性能演变规律[J].矿冶工程,2019,39(06):70-74.
[17]陈宁标.重金属废水处理技术和资源化问题[J].建材与装饰,2019(5):155-156.
[18]彭丽花,董佳.化学法处理某工业园区电镀废水试验研究[J].中国资源综合利用,2018,36(9):27-30.
[19]林本兰,吴兰兰,崔升,等. 新型重金属离子吸附剂的研究进展[J].材料导报,2015,29(19):18-23.
