磁性三维还原石墨烯的制备及其在电化学免疫检测牛乳中结核杆菌H37Ra的应用
2020-12-13刘希雅田春妹郑鹭飞钟平胜张馨方任佳丽
刘希雅,田春妹,郑鹭飞,钟平胜,张馨方,任佳丽,
(1.林产可食资源安全与加工利用湖南省重点实验室,湖南 长沙 410004;2.中南林业科技大学食品科学与工程学院,湖南 长沙 410004;3.中国农业科学院农业质量标准与检测技术研究所,北京 100081)
结核病是一种人畜共患病,其病原菌主要为人型结核杆菌和牛结核杆菌,可通过污染乳及乳制品感染人类[1],成为继艾滋病后严重威胁人类健康的最大杀手,在世界范围内有爆发之势[2-4]。世界动物卫生组织将其列为B类动物传染病,我国将其列为二类动物传染病。2018年世界卫生组织在《全球结核病报告》中指出,全球结核病新增病例达1 000万,其中死亡人数约157万,中国成为世界排名第2的高发病率国家[5]。世界各国每年均花费大量的人力、物力和财力去防制此病的发生。在原料乳收购现场进行检测可从源头阻断结核杆菌的传播[6]。
目前常用的结核杆菌检测技术主要包括细菌学、免疫学和分子生物学等[7-9]。世界动物卫生组织指定的检测方法为结核菌素测试法,此法受生物、化学以及物理等因素的影响,导致结果敏感性和特异性均较低,细菌学方法是目前使用的“金标准”方法,由于结核杆菌增代时间长,生长缓慢,需要2~6 周才能长出颗粒状或絮状的菌落[10],极大延长了检测时间(一般需要4~8 周),等结果出来,疫情已经发生。对于原料收购环节和出入境检验检疫,乳及其制品中结核杆菌的现场快速检测方法显得尤为重要。因此,研制准确、灵敏、快速而且价格便宜的便携式方法迫在眉睫[11-13]。
电化学传感器具有灵敏度高、检测速度快、检测成本低且检测装置可微缩化等优点,为研制便携式现场检测设备奠定了基础[14-15]。电化学电极在微缩化的同时降低了检测能耗,但也降低了电子传输速率。石墨烯作为一种新兴材料,凭借其超高的比表面积、良好的机械性能和电化学性质[16-17],在化学修饰电极方面得到了广泛的应用[18-21]。而三维结构石墨烯材料不仅可降低电极阻抗,同时还弥补了电极微缩引起的比表面积下降的缺点,提高电子传输效率[22-24]。本研究制备了磁性三维还原石墨烯复合材料,对不同修饰材料进行了表征和电化学性能探究,并在此基础上建立了一种快速、灵敏、特异的乳品中结核杆菌H37Ra的检测方法。
1 材料与方法
1.1 材料与试剂
结核杆菌(Mycobacterium tuberculosisH37Ra)、大肠埃希氏菌(Escherichia coliATCC 25922)、肠炎沙门氏菌(Salmonella enteritidisATCC 14028)、金黄色葡萄球菌(Staphylococcus aureusATCC 25923) 湖南省胸科医院;石墨烯(graphene,G) 成都有机化学有限公司;牛血清蛋白 北京索莱宝生物技术有限公司;结核杆菌多克隆抗体 上海沪峥生物科技有限公司。
1.2 仪器与设备
CHI920D电化学工作站、玻碳电极、甘汞电极、铂丝电极 上海辰华仪器有限公司;Sigma HD扫描电子显微镜(scanning electron microscope,SEM) 德国Zeiss公司;Finder One微区激光拉曼光谱仪 美国Thermo Fisher Scientific公司;DHP-500电热恒温培养箱 北京市永光明医疗仪器有限公司。
1.3 方法
1.3.1 结核杆菌H37Ra母液制备
在无菌条件下,用接种环挑取结核杆菌于装有吐温/生理盐水缓冲液的痰瓶中,在涡旋振荡仪上振荡打散5 min,制成菌悬液。吸取1~2 mL菌悬液加入苏通液体培养基中,于37 ℃恒温摇床中培养1~2 周得到母液,母液通过麦氏比浊法调节至1×108CFU/mL。
1.3.2 磁性复合材料的制备
采用Hummers法制备氧化石墨烯(graphene oxide,GO)。称取3.2 g FeCl3·6H2O加入到40 mL去离子水中,再称取5.9 g C6H5Na3O7·2H2O加入到60 mL去离子水中。将配好的溶液在磁力搅拌下缓慢加入到已经超声分散2 h的氧化石墨烯中。然后,将6.0 mL的80%偏二甲肼溶液滴加到该溶液中,继续搅拌30 min。将混合物分装转移至50 mL内壁涂了聚四氯乙烯的高压反应釜中,在180 ℃高温恒温箱中反应12 h,待冷却后,冷冻干燥24 h,即可获得四氧化三铁/三维还原氧化石墨烯(ferroferric oxide/three-dimensional reduced graphene oxide,Fe3O4@3D-RGO)复合材料。将复合材料制备过程中的各种中间材料如G、GO和Fe3O4@3D-RGO复合材料进行SEM、光电子能谱(X-ray photoelectron spectroscopy,XPS)以及拉曼光谱表征。
1.3.3 修饰电极的制备与检测
将裸玻碳电极抛光,晾干备用。分别用25%、35%、45%、55%、65%、75%、85%、95%的乙醇溶液配制修饰液,考察其成膜稳定性,最终确定75%为乙醇溶液最佳体积分数。同时参照文献[25-26],采用0.1% Nafion溶液作为修饰玻碳电极的保护膜。用电子分析天平称取0.005 g Fe3O4@3D-RGO,以75%乙醇溶液和0.1% Nafion溶液为分散相配制5 mg/mL的修饰液。分别取15、20、25、30、35、40、45 μL修饰液滴涂于电极表面,将电极置于45 ℃恒温箱中干燥后,以修饰的玻碳电极为工作电极、饱和甘汞电极为参比电极以及铂电极作为对电极构成三电极体系,置于含有0.1 mmol/L铁氰化钾的磷酸盐缓冲液(phosphate buffer saline,PBS)(0.01 mol/L,pH 7.4)中进行交流阻抗(electrochemical impedance spectroscopy,EIS)测试,选择合适的修饰液体积进行后续实验。所有的测量均在开路状态下进行,测量频率为0.1~100 kHz,外加振幅为5 mV的交流扰动电压。
1.3.4 电化学免疫传感器的制备与结核杆菌H37Ra的检测
用移液枪吸取30 μL Fe3O4@3D-RGO修饰液滴涂于玻碳电极表面并在室温下干燥,再滴涂10 μL 1 mg/mL的结核杆菌抗体,使其覆盖于玻碳电极表面,于室温下保存2 h。然后,将电极置于45 ℃恒温箱中干燥后,在超纯水中浸泡5 min,使没有固定的抗体溶解到水中,用超纯水冲洗电极,氮气吹干,然后用1% BSA进行封闭,用同样方法清洗电极并干燥,修饰电极制备完成,保存于4 ℃冰箱中备用。检测时,将三电极体系置于含有不同浓度结核杆菌H37Ra(通过PBS稀释结核杆菌母液获得)的0.1 mmol/L铁氰化钾的PBS(0.01 mol/L,pH 7.4)中进行EIS测试。
1.3.5 电化学免疫传感器重复性、稳定性及特异性评估
分别配制不同浓度(104、105、106CFU/mL)的结核杆菌,用Fe3O4@3D-RGO复合修饰材料制备的电化学免疫传感器进行阻抗测定,每个浓度平行测3 次,评估该免疫传感器的重复性;将制备的修饰电极保存在4 ℃冰箱中,每天测定105CFU/mL结核杆菌菌液,通过10 次测定的阻抗值评估所制备传感器的稳定性;采用结核杆菌和一些食品中常见的致病菌(包括大肠杆菌、金黄色葡萄球菌、沙门氏菌),均制备成约103CFU/mL的菌液,记录电化学免疫传感器的阻抗变化,以评估该传感器的特异性。
1.3.6 电化学免疫传感器检测人工污染牛乳中结核杆菌H37Ra
用麦氏比浊法配制不同浓度的结核杆菌菌悬液各10 mL。取100 μL用传统方法涂布培养,置于37 ℃培养箱中2 周后进行菌落计数,做3 次平行。另取5 mL菌悬液4 000 r/min离心40 min,将得到的菌体分散于5 mL牛乳中,用Fe3O4@3D-RGO复合材料制备的电化学免疫传感器进行测定。牛乳样品在混匀器上充分混合后,4 000 r/min离心40 min,弃去上清液,加入5 mL生理盐水重悬沉淀,使用定性滤纸过滤,滤液经4 000 r/min离心40 min,再弃去上清液,加入5 mL含有0.1 mmol/L铁氰化钾的PBS重悬沉淀,混匀待测,每组样品测3 次,将实验结果带入标准曲线计算出结核杆菌浓度,与平板计数实验结果进行对比,并用SPSS软件配对样本t检验进行显著性分析。
2 结果与分析
2.1 不同纳米材料的结构表征

图1 G(A)、GO(B)、Fe3O4@3D-RGO(C)的SM图Fig. 1 SEM images of graphene (A), GO (B), and Fe3O4@3D-RGO (C)

图2 G(A)、GO(B)、Fe3O4@3D-RGO(C)的XPS图Fig. 2 XPS profiles of graphene (A), GO (B), andFe3O4@3D-RGO (C)
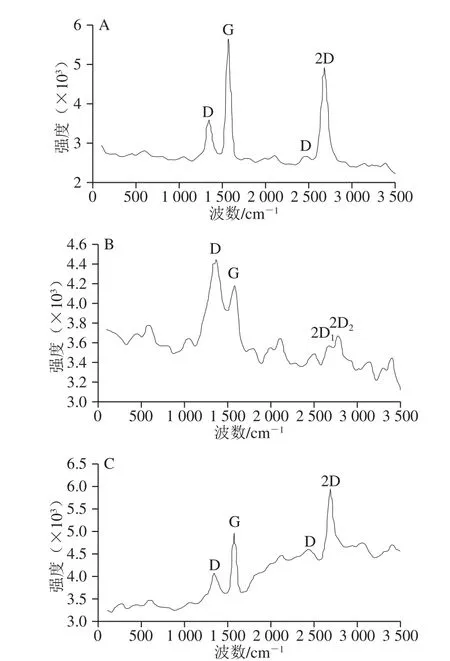
图3 G(A)、GO(B)、Fe3O4@3D-RGO(C)的拉曼光谱图Fig. 3 Rammam spectra of graphene (A), GO (B), andFe3O4@3D-RGO (C)
图1 ~3分别显示了修饰材料在制备过程中的结构特点、化学元素的含量变化以及石墨烯三维结构的变化。由图1和图2可以看出,未经修饰的石墨烯为平面单分子薄层结构,含氧量约为14%;经Hummer法制备的GO与石墨烯具有相似的层状结构,但更厚,这是由于氧化石墨烯表面嫁接了大量的活性基团,如羧基(—COOH)、酯基(—COO-)、羰基(—C=O)、环氧基[—CH(O)CH-]、羟基(—OH)等所造成的,其含氧量高达36%,约是石墨烯的3 倍,这也从另一方面证明了含氧官能团的存在;用水热一步还原法制备的Fe3O4@3D-RGO复合材料表面附着了许多直径约50~300 nm的球状颗粒,这是在制备过程中Fe3+与Fe2+一起附着到还原氧化石墨烯(RGO)表面所形成的Fe3O4纳米颗粒,与氧化石墨烯相比,复合材料厚度减小,比表面积增大,使其能够负载大量Fe3O4纳米颗粒。由图2C可知,RGO表面仍然存在部分—OH、—COOH等含氧基团,使Fe3O4纳米颗粒可以通过共价作用结合在RGO表面,同时,这种作用力也阻止了Fe3O4的团聚,从而获得了稳定的Fe3O4@3D-RGO磁性复合材料。从不同修饰材料的拉曼图谱(图3)可以看出石墨烯在514 nm波长的激光激发下产生2 个强特征峰,从这2 个峰的位置及形状可以大致推出石墨烯的层数,并依次可以推断所制备的Fe3O4@3D-RGO复合材料具有三维结构;氧化石墨烯具有较厚的堆积片层,这与石墨烯的氧化造成的结构缺陷有关。
2.2 不同纳米材料的电化学性能
测定裸玻碳电极(bare glassy carbon electrode,GCE)、氧化石墨烯修饰电极(GO/GCE)及复合材料修饰电极(Fe3O4@3D-RGO/GCE)在1 mmol/L铁氰化钾溶液中的交流阻抗谱。

图4 不同修饰电极的电化学阻抗图谱Fig. 4 Electrochemical impedance of different modified electrodes
一般情况下,修饰电极阻抗大小与阻抗图谱半圆直径呈正比。通过对比图4中GCE、GO/GCE和Fe3O4@3DRGO/GCE的阻抗图谱可知,GO/GCE的阻抗远大于GCE,而Fe3O4@3D-RGO/GCE的阻抗远小于GCE。这是因为GO表面含有大量的含氧活性基团,它们会阻碍电子传递,使阻抗增大。而对于Fe3O4@3D-RGO/GCE,含氧基团不仅能够增强复合材料的水溶性,减小信噪比,还可以与Fe3O4发生相互作用使修饰材料比表面积增大、导电性增强,阻抗减小。
2.3 修饰液体积对电化学阻抗的影响
为获得Fe3O4@3D-RGO磁性复合材料的最优阻抗特征,以不同体积的修饰液(质量浓度5 mg/mL)对电极进行修饰,用交流阻抗谱进行表征,获得Fe3O4@3D-RGO修饰电极的导电性能。
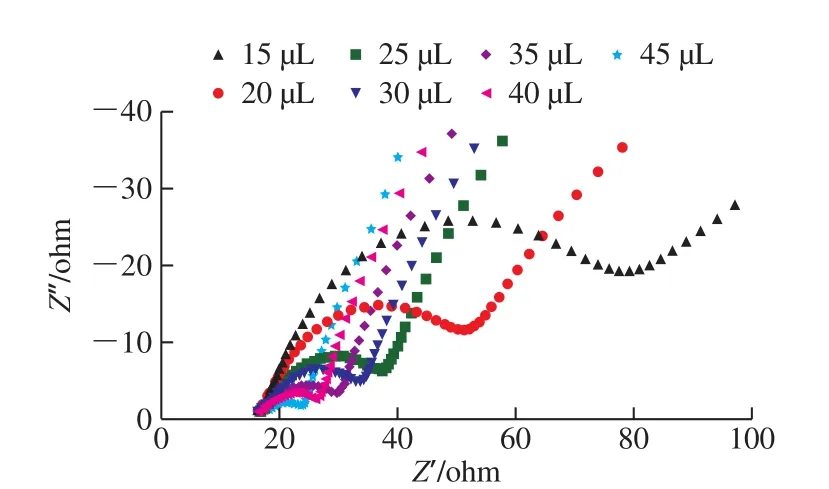
图5 不同体积三维磁性复合材料修饰电极阻抗谱Fig. 5 Electrochemical impedance of different electrodes modified with different volumes of Fe3O4@3D-RGO
由图5可知,电极经Fe3O4@3D-RGO磁性复合材料修饰后,阻抗随修饰液体积的增大显著减小。但由于修饰液体积为30 μL时即可在玻碳电极表面达到饱和,继续滴加会造成修饰液浪费,若分2 次滴加,又会使电极表面修饰膜太厚,不利于后期继续滴涂抗体制备免疫传感器,故在后续实验中,使用修饰液均为30 μL。
2.4 Fe3O4@3D-RGO复合材料修饰电极电化学性能
对免疫传感器制备过程中不同阶段的状态,即GCE、Fe3O4@3D-RGO/GCE、结核杆菌抗体修饰的Fe3O4@3D-RGO/GCE(Fe3O4@3D-RGO/Ab/GCE)以及用BSA封闭后的Fe3O4@3D-RGO/Ab/GCE(Fe3O4@3DRGO/Ab/BSA/GCE)以及结核杆菌吸附后的修饰电极(Fe3O4@3D-RGO/Ab/BSA/H37Ra/GCE)在铁氰化钾电解液中的电化学行为进行交流阻抗谱测试,它们的电子传递阻抗分别为85.76、34.62、39.31、49.62、115.00 Ω(图6)。结果表明,Fe3O4@3D-RGO复合材料的修饰增加了电极表面积并加速了电子转移,使得Fe3O4@3DRGO/GCE的阻抗远小于GCE。当修饰电极表面覆盖有结核杆菌抗体时,修饰膜的表面又增加了一层抗体膜,抑制了电子的传递,交流阻抗增大。用BSA对电极表面的非特异性部位进行封闭后,电极阻抗进一步增大,上述现象说明生物活性物质极大地阻碍了电子转移效率。尽管如此,修饰后的电极阻抗仍然小于裸电极,结果证明Fe3O4@3D-RGO复合材料可提高电子的传输效率。结核杆菌吸附后,电化学阻抗明显增大,说明所制备的电化学免疫传感器可以用来监测抗体与目标菌抗原结合所引起的阻抗变化。
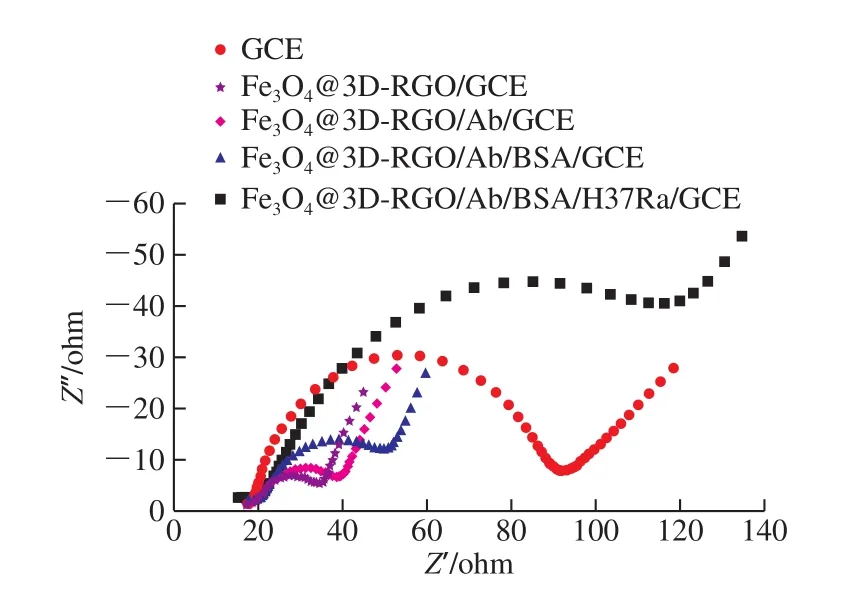
图6 电化学免疫传感器检测结核杆菌37Ra原理Fig. 6 Principle of electrochemical immunosensor for the detection of M. tuberculosis H37Ra
2.5 Fe3O4@3D-RGO复合修饰材料制备的电化学免疫传感器检测结核杆菌H37Ra
图7 为Fe3O4@3D-RGO复合修饰材料制备的电化学免疫传感器检测不同浓度结核杆菌H37Ra的交流阻抗图,其半圆曲线的直径表示溶液阻抗Z,而横纵坐标Z’和Z’分别为阻抗Z的实部和虚部。在H37Ra浓度为1×103~1×108CFU/mL的范围内,电极阻抗与目标检测物浓度的对数呈现较强的线性关系,回归方程为y=19.77lgN-49.14,相关系数为0.982。检出限为1×102CFU/mL,由D=3SD/k计算得到,其中SD是空白样品与检测阻抗信号的标准偏差,k为标准曲线的斜率(图8)。
将Fe3O4@3D-RGO复合修饰材料制备的电化学免疫传感器与其他相关方法[27-30]进行比较,其结果如表1所示。本实验基于Fe3O4@3D-RGO复合材料的免疫电化学方法检测结核杆菌H37Ra的线性范围宽,检出限略低,检测时间更快速,且不需任何昂贵的仪器设备,操作简单、无需样品前增菌和预富集。制备的电化学免疫传感器的优良性能可归因于多种因素:首先,Fe3O4@3D-RGO磁性复合材料促进了电极表面电子传输,提高了电化学性能。此外,水热一步还原法制备的Fe3O4@3D-RGO磁性复合材料克服了石墨烯片层之间脱离溶剂后容易产生p-π堆叠而导致比表面积降低的缺陷,获得更大的比表面积,使得所研制的电化学免疫传感器具有较低的检出限。
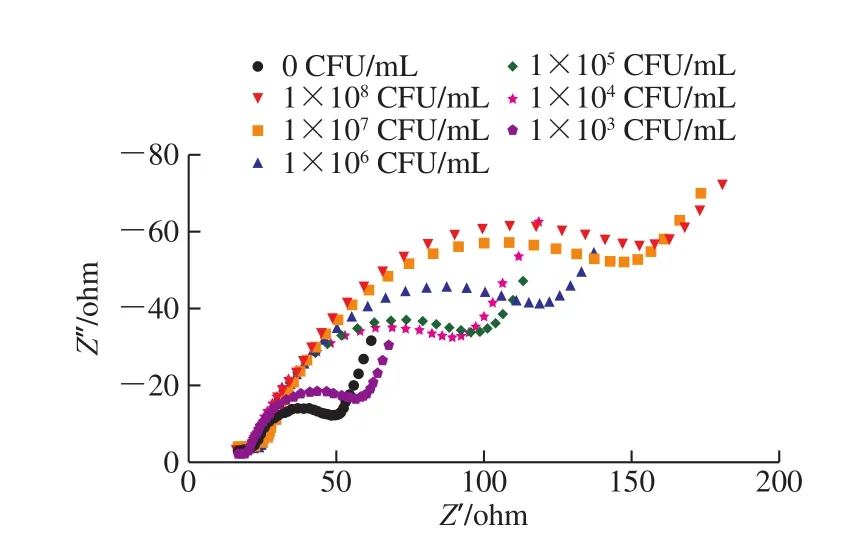
图7 电化学免疫传感器用于不同浓度结核杆菌37Ra的检测Fig. 7 Detection of different concentrations of M. tuberculosis H37Ra using electrochemical immunosensor
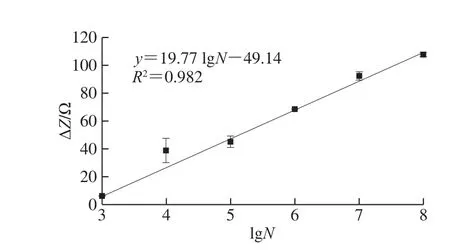
图8 修饰电极阻抗变化量与结核杆菌37Ra浓度对数关系图Fig. 8 Relationship between impedance change and logarithmic concentration of M. tuberculosis H37Ra

表1 电化学免疫传感器与其他方法比较Table 1 Comparison of the proposed electrochemical immunosensor with other methods
2.6 Fe3O4@3D-RGO复合修饰材料制备的电化学免疫传感器重复性、稳定性和特异性探究
传感器的稳定性、重复性和特异性是衡量其能否在实际检测中应用的关键指标。如表2所示,3 组菌液的相对标准偏差均小于5%,显示了较高的精密度,表明Fe3O4@3D-RGO复合修饰材料制备的电化学免疫传感器具有较好的重复性。电化学免疫传感器稳定性测试阻抗图谱见表3,当其阻抗响应值相对标准偏差小于5%,表明修饰电极具有较好的稳定性[31]。为了进一步测试免疫传感器的特异性,用大肠杆菌、金黄色葡萄球菌、沙门氏菌等非目标菌进行对照实验,结果如图9所示,结核杆菌引起的阻抗变化约为非目标菌的8 倍,说明该免疫传感器的特异性较好。
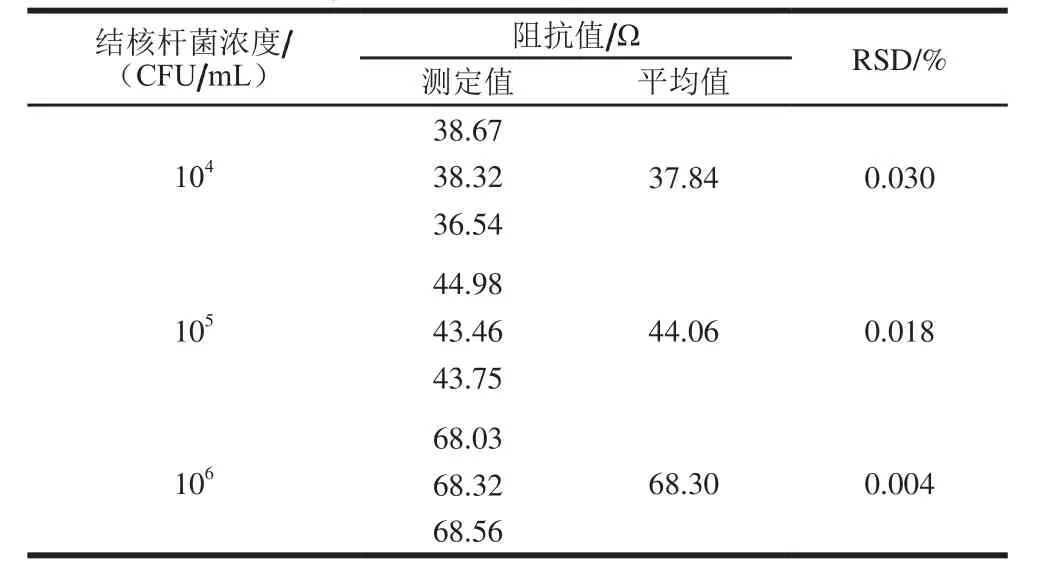
表2 电化学免疫传感器的重复性测试结果Table 2 Repeatability evaluation of the electrochemical immunosensor
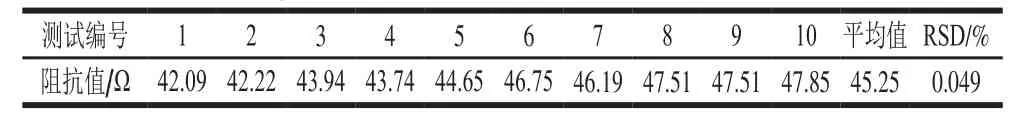
表3 电化学免疫传感器的稳定性测试结果Table 3 Stability evaluation of the electrochemical immunosensor

图9 电化学免疫传感器特异性分析Fig. 9 Specificity analysis of the electrochemical immunosensor
2.7 人工污染牛乳样品检测结果
将所制备的电化学免疫传感器用于人工污染牛乳样品检测,其结果与传统培养计数法进行对比,并用SPSS软件进行显著性分析(表4)。结果表明,电化学免疫传感器检测法与传统培养计数法结果一致(P=0.270>0.05),电化学免疫传感器法相对标准偏差为6.53%~8.19%,回收率在107%~118%之间。
表4 人工污染牛乳样品中结核杆菌37Ra的检测(n=3)Table 4 Detection of M. tuberculosis 37Ra in artificially contaminated milk (n= 3)

表4 人工污染牛乳样品中结核杆菌37Ra的检测(n=3)Table 4 Detection of M. tuberculosis 37Ra in artificially contaminated milk (n= 3)
样品号 传统培养计数法/(CFU/mL)电化学免疫传感法/(CFU/mL) RSD/% 回收率/%1 4.4×103 4.9×103 8.19 111 2 4.4×104 5.2×104 7.02 118 3 4.4×105 5.1×105 6.53 115 4 4.4×106 4.7×106 8.51 107
3 结 论
本实验采用水热一步还原法制备了Fe3O4@3D-RGO复合材料,利用75%的乙醇溶液和0.1% Nafion溶液作为分散体系,简便、高效地制备了电化学免疫修饰电极,并将其应用于牛乳中结核杆菌H37Ra的快速定量检测。所制备的电化学免疫传感器线性范围宽、灵敏度高、稳定性和重复性良好、在15 min内即可得到结果,与传统检测方法(2~8 周)相比,有效缩短了检测时间,为便携式传感器的构建及乳品中结核杆菌的现场快速检测提供了技术支撑。
