冰-水体系库仑滴定法测定LiPF6 电解液中游离酸
2020-12-12,,,,,
,,, ,,
(武汉理工大学化学化工与生命科学学院,武汉 430070)
当锂离子电池用LiPF6电解液中游离酸含量过高时,不仅会侵蚀阴极材料和固态电解质界面(SEI)膜,影响电极结构,还会消耗电解液中的Li+,使电池容量不可逆的增大[1-4]。中国电子行业标准SJ/T 11723-2018规定锂离子电池电解液中游离酸含量(以氢氟酸计,下同)不能超过50 mg·kg-1。因此,在锂离子电池及其电解液的生产、储存等环节中,必须对游离酸的含量进行严格管控。
目前,测定锂离子电池用LiPF6电解液中游离酸含量的方法主要有酸碱滴定法(HG/T 4067-2015)、电位滴定法[5-8]和浸蚀法[9]等,但这些测定方法均存在明显的缺点和不足:如酸碱滴定法和电位滴定法测定结果精密度较差,不适用于痕量分析;浸蚀法费时较长,操作繁琐。文献[10]提出利用库仑滴定法在非水体系中测定锂离子电池电解液中游离酸的方法,该方法具有快速、准确、自动的特点,但也存在一些不足:采用的电解质为LiCl-乙醇溶液,会导致电解体系内阻过大,最大恒电流仅为3.50 m A,不适用于游离酸含量较高样品的分析;需采用氮气消除支持电解质中溶解氧,检测效率较低。因此,本工作在文献[10]的基础上,开展了在水相中采用库仑滴定法测定LiPF6电解液中游离酸含量(以氟化氢计)的试验,以期能够为锂离子电池用电解质中的游离酸含量的监控提供技术支撑。
1 试验部分
1.1 仪器与试剂
自动游离酸滴定仪(自制)[11]包括电解系统、指示系统和计算机控制系统等3个部分:电解系统主要由恒流源、工作电极和辅助电极组成;指示系统主要由p H复合玻璃电极、信号调节电路和数据采集卡组成;计算机控制系统则由电子开关和计算机软件组成。G20型自动电位滴定仪;S210型酸度计;In Lab Expert Pro型p H复合电极,铂片电极,铂丝电极。
氢氟酸-碳酸酯溶液:2 000 mg·L-1,取40%(体积分数)的氢氟酸溶液0.45mL溶于体积比为1∶1∶1的碳酸乙烯酯-碳酸二甲酯-碳酸二乙酯(EC-DMC-DEC)溶液100mL中,其他质量浓度(10~100 mg·L-1)均由此溶液用体积比为1∶1∶1的EC-DMC-DEC溶液稀释制得。
KCl溶液:1.0 mol·L-1。
KCl冰块:将1.0 mol·L-1KCl溶液放在2 cm×2 cm×2 cm冰格中于冰箱中冷冻10 h以上。
试验所用试剂均为分析纯及以上。
4种LiPF6电解液样品均购自市场(电池级),编号分别为LIBE-01、LIBE-02、LIBE-03、LIBE-04。
1.2 仪器工作条件
p H复合玻璃电极为指示电极,铂片电极和铂丝辅助电极为工作电极对;以1.0 mol·L-1KCl溶液为支持电解质;恒电流(I)为0.25~20.00 m A;滴定终点为pH 7.40。
1.3 试验方法
在手套箱中称取2.000 0 g LiPF6电解液样品,置于含1.0 mol·L-1KCl溶液40mL的聚四氟乙烯烧杯中,加入4~5块KCl冰块,使测试体系温度保持在0~4℃。等待30 s,启动自制游离酸滴定仪开始电解,至终点时,计算机控制系统自动发出指令,停止电解并输出测定结果。按公式(1)计算LiPF6电解液中游离酸(以氟化氢计)含量:
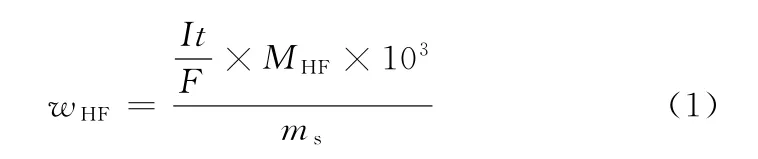
式中:wHF为锂离子电池用电解液中游离酸含量,mg·kg-1;I为电流,m A;t为电解时间,s;F为法拉第电解常数,96 500 C·mol-1;MHF为氟化氢的摩尔质量,20.01 g·mol-1;ms为加入的LiPF6电解液样品的质量,g。
2 结果与讨论
2.1 支持电解质及其浓度的选择
在保持溶液的离子强度一致的前提下,试验考察了分别以1.0 mol·L-1LiCl、1.0 mol·L-1KCl、0.33 mol·L-1K2SO4作为支持电解质时对测定结果的影响。结果表明:在LiCl体系中,指示电极所测p H无法保持稳定;K2SO4和KCl体系的p H均可保持稳定,滴定效率接近100%。考虑到使用的方便性,试验选择KCl溶液作为支持电解质。
在电流5.00 m A条件下,试验考察了支持电解质KCl溶液的浓度为0.10~1.5 mol·L-1时对100 mg·L-1的氢氟酸-碳酸酯溶液(1.5mL)测定的影响,结果见表1。
由表1可知:KCl溶液的浓度为1.0 mol·L-1时,测定结果的相对误差和相对标准偏差(RSD)均在0.20%以内。因此,试验选择1.0 mol·L-1KCl溶液作为支持电解质。

表1 KCl支持电解质浓度的选择(n=6)Tab.1 Selection of concentration of KCl supporting electrolyte(n=6)
2.2 恒电流的选择
试验考察了恒电流分别为0.25~20.00 m A时对100 mg·L-1的氢氟酸-碳酸酯溶液(1.50mL)测定的影响,结果见表2。
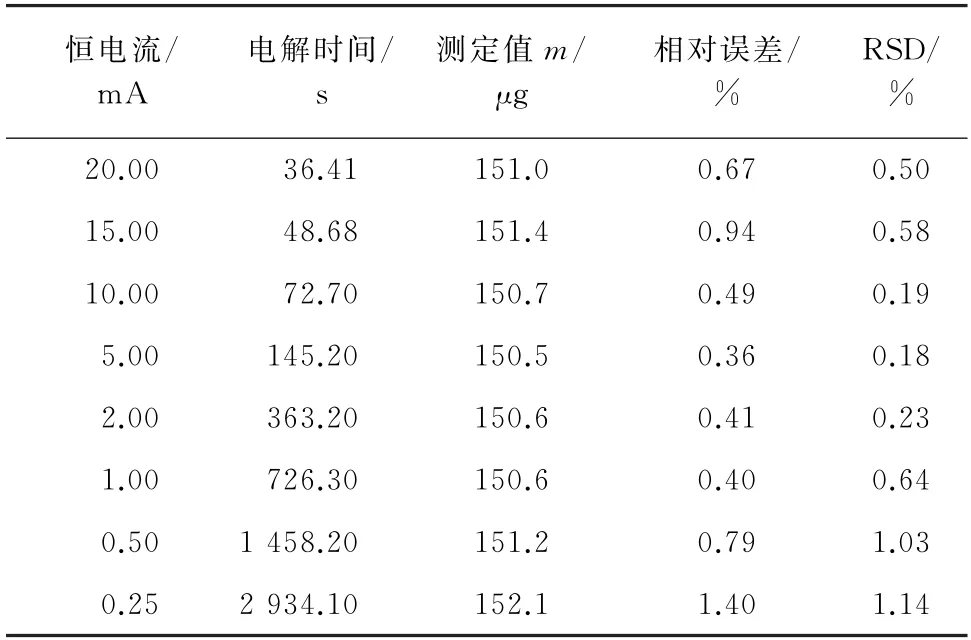
表2 恒电流的选择(n=6)Tab.2 Selection of constant current(n=6)
由表2可知:当恒电流在15.00 m A及以上时,测定值的RSD较大;当恒电流低于2.00 m A时,电解时间过长,测定值的RSD也较大。综合考虑,建议:当电解液中游离酸质量在10~100μg时,选取恒电流为2.00 m A;当游离酸质量大于100μg时,选择的恒电流应不小于5.00 m A,同时,应控制电解时间为90~150 s。
2.3 测定温度的选择
LiPF6电解液的热稳定性差[12-14],为了验证低温对LiPF6电解液热分解是否存在抑制作用,试验考察了测定温度分别为0~30 ℃时对样品LIBE-01中游离酸含量的影响,结果见表3。
由表3可知:当测定温度为0~4 ℃时,测定结果无明显差异,且精密度良好;当测定温度为6~30 ℃时,游离酸含量随温度的升高而增大,精密度变差,这是由于LiPF6在6 ℃以上时会发生不同程度的热分解,生成的PF5会进一步与H2O反应生成氢氟酸,使得测定结果偏高。因此,试验选择将测定温度控制在0~4 ℃内。
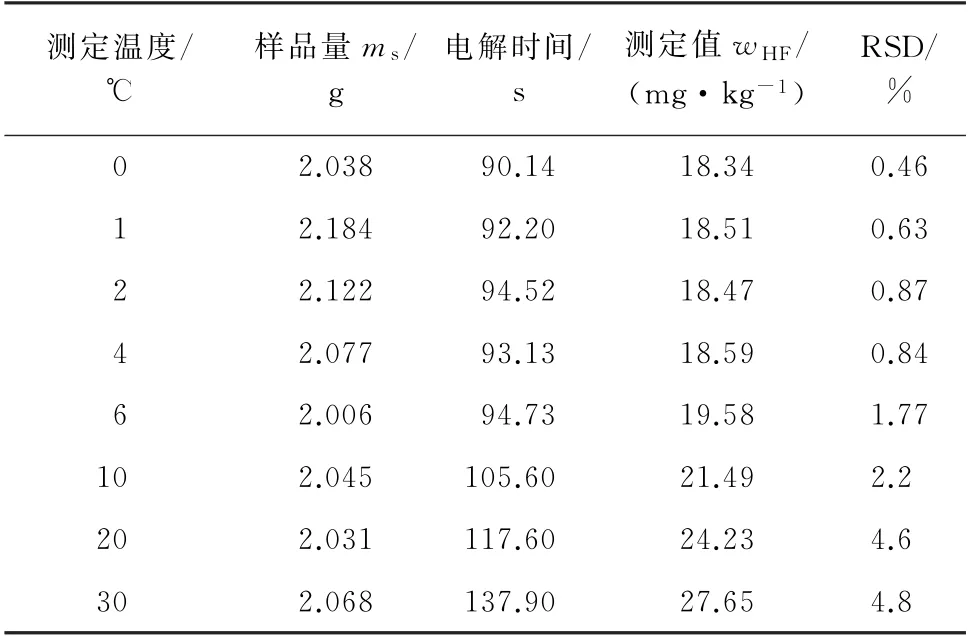
表3 不同温度下电解液中游离酸含量的测定结果(n=5)Tab.3 Determined results of free acid content of electrolyte at different temperatures(n=5)
2.4 库仑滴定终点的选择
按照试验方法对样品LIBE-03进行测定,得到的库仑滴定曲线见图1。
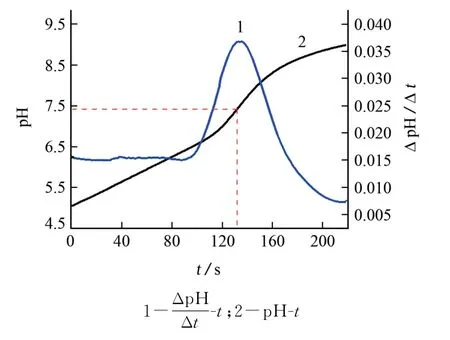
图1 LiPF6 电解液中游离酸的库仑滴定曲线(I=5.00 m A)Fig.1 Coulometric titration curves of free acid in LiPF6 electrolyte(I=5.00 m A)
由图1可知:测试可在5 min内完成,滴定突跃点在pH 7.40左右。因此试验选择pH 7.40为测定游离酸的滴定终点。
2.5 预滴定和溶解氧的消除
为了提高测定结果的准确度和精密度,一般可先通过通氮气去除支持电解质溶液中的溶解氧,再进行预滴定[15]。试验以样品LIBE-03为待测对象,考察了预滴定和通氮气去除溶解氧对测定结果的影响,结果见表4。其中:预滴定试验需向样品溶液中加入了100 mg·L-1氢氟酸-碳酸酯溶液1.0mL,并滴定至终点pH 7.40;通氮气试验需向样品溶液中通入氮气10 min。
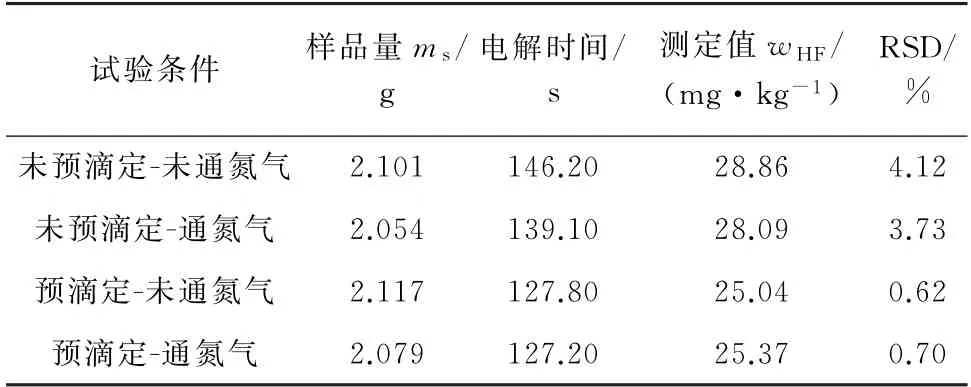
表4 预滴定和通氮气去除溶解氧对测定结果的影响(n=5)Tab.4 Effect of pre-titration and nitrogen removal of dissolved oxygen on the determined results(n=5)
由表4可知:未进行预滴定的两组试验结果明显偏高,且精密度差;而是否通氮气对测定结果的影响可以忽略。因此,在测定实际样品前,需进行预滴定的操作,而无需通入氮气去除溶解氧。
2.6 不同种类碳酸酯类溶剂的影响
为了探究不同碳酸酯类溶剂对测定结果的影响,试验选用EC、DMC和DEC等3种常用的碳酸酯类溶剂,以样品LIBE-01为测定对象,将单一碳酸酯和体积比为1∶1∶1的3种碳酸酯混合溶液以10%的体积比加入到支持电解质KCl溶液中,按上述1.3节方法进行游离酸含量测定,结果见表5。

表5 碳酸酯类溶剂对游离酸测定的影响(n=5)Tab.5 Effect of esters solvent on the determination of free acid(n=5)
由表5可知:加入不同碳酸酯类溶剂后,相对误差和RSD均在1.0%以下,表明游离酸的测定结果不受碳酸酯类溶剂种类的影响。综合考虑,试验选择了体积比为1∶1∶1的EC-DEC-DMC混合溶液作溶剂。
2.7 电解液添加剂的影响
将磷酸三甲酯、1,4-二氧六环、乙酸乙酯、乙酰胺和碳酸亚乙烯酯(VC)等5种不同添加剂以5%的质量分数加入到支持电解质KCl溶液中,以样品LIBE-01为测定对象,测定其中游离酸的含量,结果见表6。
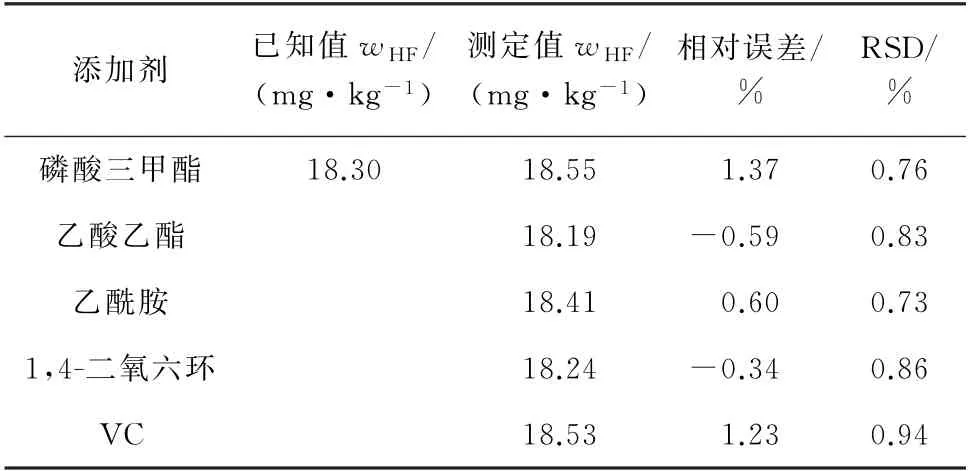
表6 电解液添加剂对游离酸测定的影响(n=5)Tab.6 Effect of electrolyte additive on determination of free acid(n=5)
由表6可知:在5种不同电解液添加剂中,游离酸测定值的相对误差和RSD在1.0%以下,表明游离酸的测定结果不受上述添加剂的影响。
2.8 标准曲线及测定下限
按照试验方法对游离酸质量分别为5.0,10.0,20.0,40.0,80.0,120,160,200μg的标准溶液系列进行测定,以游离酸的质量为横坐标,对应的响应值为纵坐标绘制标准曲线。结果表明:标准曲线的线性范围为5.0~200 μg,线性回归方程为y=18.58x-0.279 5,相关系数为0.999 9。当游离酸质量在5.0μg以下时,测定结果的精密度和准确度较差,故确定本方法的测定下限为5.0μg。
2.9 回收试验
在样品LIBE-01中加入4个不同浓度水平的氢氟酸-碳酸酯溶液,按照试验方法进行测定,计算回收率,结果见表7。由表7可知:游离酸的回收率为99.7%~102%,表明所提出的方法准确可靠。

表7 回收试验结果(n=6)Tab.7 Results of test for recovery(n=6)
2.10 方法比对
按照试验方法分析4个样品,并同非水库仑滴定法和电位滴定法进行比对,结果见表8。
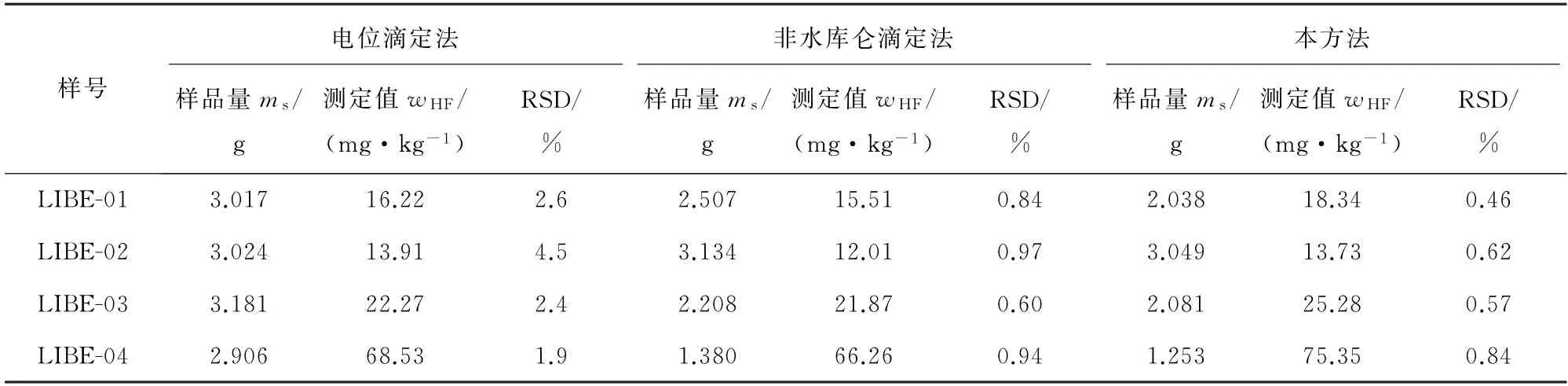
表8 不同方法得到的游离酸测定结果(n=5)Tab.8 Determination results of free acid obtained by different methods(n=5)
由表8可知:和电位滴定法相比,本方法和非水库仑滴定法的精密度均较高,RSD在1.0%以下,但本方法测得的游离酸含量略高于非水库仑滴定法的,其原因需要进行下一步研究。
本工作提出了用冰水体系库仑滴定法测定LiPF6电解液中游离酸含量的方法。相较于非水库仑滴定法,本方法同样具有简便、快速、自动的特点;本方法可选择的恒电流范围较大,可用于不同游离酸含量的LiPF6电解液中游离酸的定量分析;本方法无需用氮气消除溶解氧,检测效率更高,有利于本方法的普及和推广。
