黄连上清片微生物限度检查法的建立
2020-12-09张秀花刘艳平曲国晶
张秀花,刘艳平,曲国晶
(菏泽市食品药品检验检测研究院,山东 菏泽)
0 引言
黄连上清片收载于《中华人民共和国药典》(以下简称:《中国药典》)2015年版一部[1],清风清热、泻火止痛,临床应用广泛。由于黄连上清片中多种药材如黄连、黄芩、大黄、连翘、栀子等均具有明显的抗菌活性[2-10],进行微生物限度检查时,需要首先消除样品本身的抑菌作用,才能使被检生物能够正常繁殖[11]。作者对6家生产企业6个批次的样品进行试验,结果微生物计数采用增加稀释液法,控制菌检查采用常规法,该方法操作简单,重现性好,可供其他实验室参考使用。
1 仪器与材料
1.1 样品
安徽九方制药有限公司(批号:190401),福建乐尔康药业
有限公司(批号:190128),河南金鸿堂制药有限公司(批号:20181105),洛阳天生药业有限责任公司(批号:190405) 乐氏同仁三门峡制药股份有限公司(批号:20190107),仲景宛西制药股份有限公司(批号:20191101)。
1.2 培养基与稀释液
胰酪大豆胨琼脂培养基TSA(批号:190518),胰酪大豆胨液体培养基培养基TSB(批号:190712),沙氏葡萄糖琼脂培养基 SDA(批号:190625),肠道菌增菌液 EE(批号:180222)pH7.0无菌氯化钠-蛋白胨缓冲液(批号:190206)等均由北京陆桥技术股份有限公司提供。
2 方法与结果
2.1 菌液制备
按药典要求[12]将5种菌株依法制成不大于1000cfu/mL的菌液。
2.2 供试液制备
取“1.1”项下样品10g,研细,加入“1.3”项下稀释液至100mL,制成1:10 供试液;依法制成1:20、1:50、1:80[13]、1:100、1:1000 的供试液。
2.3 微生物计数试验
2.3.1 常规法
取“2.1”项下菌液0.1mL至9.9mL“2.2”项下1:10供试液中,为试验组;取稀释液0.1mL至9.9mL“2.2”项下1:10供试液中,为供试品对照组;取“2.1”项下菌液0.1mL至9.9mL稀释液中,为菌液对照组。
2.3.2 增加稀释液法
取“2.1”项下菌液0.1mL至9.9mL“2.2”项下1:20供试液中,为试验组;取稀释液0.1mL至9.9mL“2.2”项下1:20供试液中,为供试品对照组;取“2.1”项下菌液0.1mL至9.9mL稀释液中,为菌液对照组。1:50、1:80供试液依法操作。

表1 常规法预试验结果(n=3)
2.4 微生物计数结果
2.4.1 预试验
常规法测定5种菌株回收比,按“2.3.1”项下操作,平皿计数结果见表1。
由表1可以看出,不同企业生产的黄连上清片抑菌活性不同,针对本次试验的6家生产企业的样品,无法统一采用常规法进行试验;不同生产企业的样品对5种菌株的敏感性不同,其中对铜绿假单胞菌、枯草芽孢杆菌、金黄色葡萄球菌的抑菌性较强,回收比均小于0.5,可将这3种菌株作为敏感菌株进一步进行试验。
2.4.2 需氧菌总数计数方法的确定
根据预实验结果,选用上述3种菌株作为敏感菌株,采用增加稀释液法试验,按“2.3.2”项下操作,平皿计数结果见表2。
由表2可以看出,稀释倍数不同,供试液的抑菌性不同,稀释倍数越大,抑菌性越小。1:20供试液,6批样品中均存在回收比小于0.5的敏感菌株;1:50供试液,2批样品存在回收比小于0.5的敏感菌株;1:80供试液,6批样品5种菌株回收比均在0.5~2.0之间,符合药典要求。
2.4.3 正式试验
根据“2.4.1”及“2.4.2”项下确认的结果,采用增加稀释液法进行试验,按“2.3.2”项下操作,1:80供试液平皿计数结果见表3。
由表3可以看出,6批样品5种菌株回收比均在0.5~2.0范围内,符合药典要求,方法可行。

表2 敏感菌株回收比试验结果(n=3)
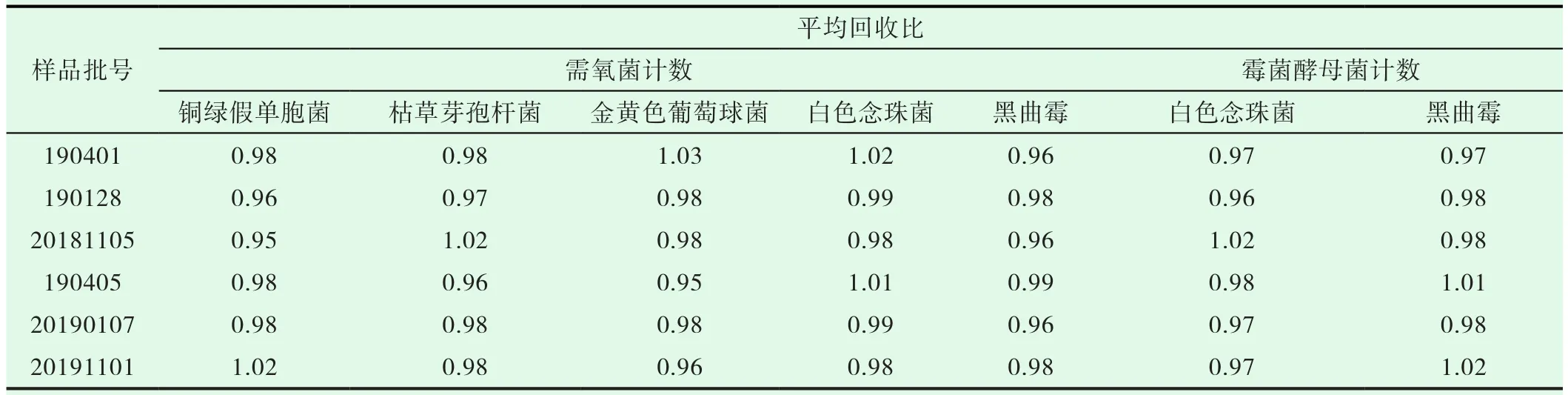
表3 黄连上清片方法适用性试验结果(n=3)
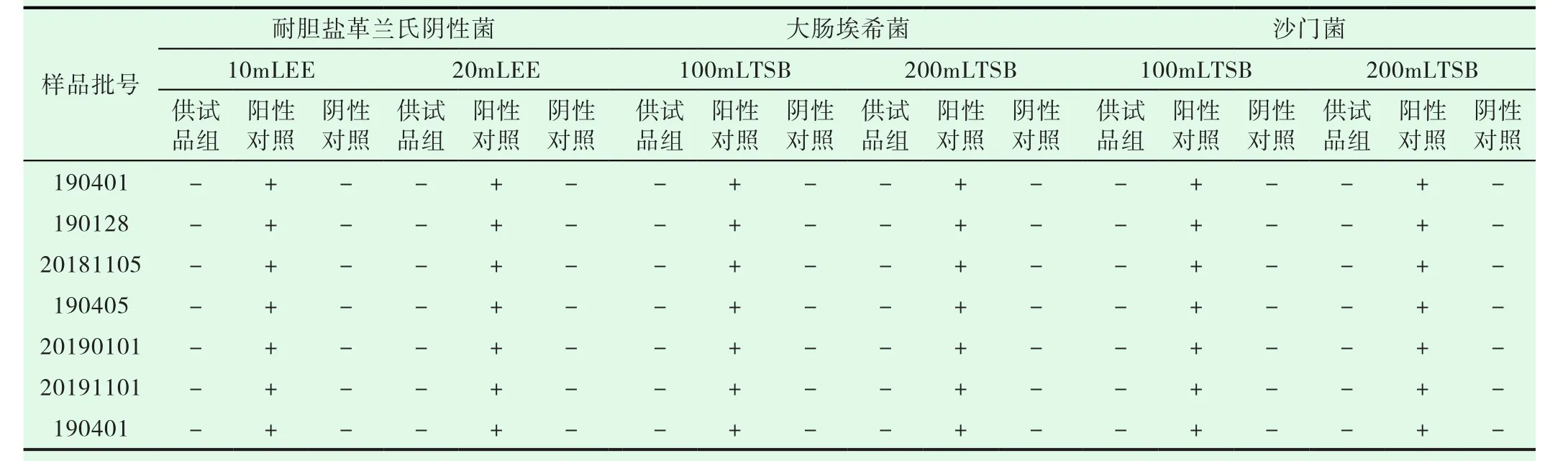
表4 黄连上清片控制菌检查结果
2.5 控制菌检查试验
2.5.1 耐胆盐革兰阴性菌
供试品组:取“2.2”项下 1:10、1:100、1:1000供试液各1mL分别至10mL及20mLEE中;阳性对照:取“2.2”项下1:10、1:100、1:1000供试液各1mL分别至10mL及20mLEE中,再加入“2.1”项下相应阳性菌0.1mL;阴性对照:以稀释液代替供试液,以上各组依法检查。
2.5.2 大肠埃希菌
供试品组:取“2.2”项下1:10供试液10mL至100mL及200mLTSB中;阳性对照:取“2.2”项下1:10供试液10mL至100mL及200mLTSB中,再加入“2.1”项下大肠埃希菌0.1mL;阴性对照:以稀释液代替供试液,以上各组依法检查。
2.5.3 沙门菌
供试品组:取“1.1”项下样品10g至100mL及200mLTSB中;阳性对照:取“1.1”项下样品10g至100mL及200mLTSB中,再加入“2.1”项下乙型副伤寒沙门氏菌0.1mL;阴性对照组:以稀释液代替供试液,以上各组依法检查。控制菌检查结果见表4。
由表4可以看出,常规法可用于黄连上清片控制菌检查。
3 讨论
微生物限度检查法最初收载于《中国药典》1995年版,2005年版首次引入方法验证试验,2015年版修订为方法适应性试验。从历年药典的修订情况可以看出,药品的安全性越来越受到重视。微生物污染指标菌检出与否,关键在于使用的计数方法是否有效,检查的重点和难点在于方法适用性试验的建立[14-17];当检验程序或产品发生变化可能影响检验结果时,计数方法应重新进行适用性试验[18]。
从表1可以看出,常规法6家生产企业的样品对5种菌株的抑菌性均不同。针对这一问题,首先将回收比小于0.5的菌株作为敏感菌株,采用增加稀释液的方法,逐渐增加稀释倍数,至所有敏感菌株的回收比均在0.5~2.0之间。从表3可以看出,1:80供试液,各试验菌回收比均在0.90以上,表明方法可行。
由于黄连上清片中抑菌成分复杂,考虑到对控制菌的抑菌作用,本试验采用常规法和增加培养基体积法同时进行控制菌检查,结果表明黄连上清片对控制菌无抑制作用,常规法可用于控制菌的检查。
