EB病毒实验室检测技术研究进展
2020-12-05麻婷婷许四宏周海卫
麻婷婷 许四宏 周海卫
EB 病毒(epstein-barr virus,EBV)于1964年在伯基特淋巴瘤(burkitt's lymphoma,BL)的活组织检查中发现并分离[1]。EBV 属于γ 疱疹病毒亚家族,是9 种已被确认的仅感染人类的病毒之一[2]。EBV 为二十面体、十二聚体门户结构(病毒的基因组转位装置)和衣壳相关的表皮复合体结构[3]。EBV 基因组约172 kb,由一个能编码多于85 种基因的线性双链DNA 分子组成。其编码基因目前已知有6 种核抗原(EBV nuclear antigen,EBNA),3 种潜伏膜蛋白(latent membrane protein,LMP),小非聚腺苷化RNAs,EBV 编码的小RNA(EBV encoded small RNA,EBER)1 和2,微小RNA 和几种早期裂解基因[4]。
EBV 主要在口咽部上皮细胞增殖,口咽分泌物中存在大量病毒,排毒时间可达数月,某些病毒携带者甚至可间断或持续排毒数年。EBV 可感染T 淋巴细胞、B 淋巴细胞、鼻咽和口咽鳞状上皮细胞、唾液腺和胃腺、甲状腺腺上皮细胞、平滑肌和卵泡树突状细胞等多种细胞和组织。依据国际癌症研究署对致癌因子的分类标准,EBV 被列为第一类癌因子[5]。EBV 感染与霍奇金淋巴瘤(hodgkin's lymphoma,HL)、非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL)、BL、鼻咽癌及部分类型胃癌和乳腺癌等有关[6-8]。EB 病毒感染孕妇后,会导致流产、胎死宫内、早产、胎儿畸形及新生儿感染等情况。EBV 感染儿童后的主要引发传染性单核细胞增多症(infectious mononucleosis,IM)、EBV 相关嗜血淋巴组织增多症和X 连锁淋巴组织增生综合征等。EBV 有多种实验室检测技术,本文主要介绍各种检测技术的特点和预期用途,以便选择有效的方法精准的监测和诊断疾病。
1 EBV 检测技术
EBV 在原发感染上皮细胞后,潜伏感染B 淋巴细胞[5]。正常携带者体内,病毒持续存在于记忆B细胞内,开始产生免疫球蛋白[9]。EBV 感染B 细胞后,延迟程序相关的基因和转录本会得到表达,使病毒在记忆B 细胞中保持休眠状态,在B 细胞存在的任意粘膜部位间歇性地激活。EBV 进入B 细胞后以两种形态存在,第一种是病毒基因组直接整合至宿主基因组上以原病毒形式存在,第二种是以圆形游离态存在于细胞核内,通过表达延迟基因,驱动宿主细胞的延迟和存活。B 细胞内延迟基因的表达使其转化为淋巴细胞系而导致形成B 细胞源性淋巴瘤。在免疫功能正常的个体内,EBV 特异性淋巴细胞发挥作用使病毒的滴度受到抑制[10]。然而,EBV 在上皮细胞裂解期基因表达时,病毒可转为潜伏期基因表达,导致上皮细胞向永久增殖细胞转化,形成上皮细胞源性恶性肿瘤。EBV 检测应用主要有以下几方面:①以EBV 作为生物标记物诊断和评估肿瘤扩散及治疗监测,②EBV 感染疾病的感染阶段分期,③器官移植和免疫缺陷疾病患者的EBV 相关疾病的早筛和监测等。目前,EBV 的检测方法主要包含血清学和分子生物学方法[11]。
1.1 EBV 细胞培养检测
细胞培养技术是一种精确的半定量方法,但EBV 仅在非洲淋巴瘤细胞、IM 患者血液、健康人脑细胞和白血病细胞等培养中繁殖,其生长条件要求比较苛刻,细胞培养技术需要专业人员在特殊实验室里操作,价格昂贵,且培养耗时较长(4~8周)。目前该技术主要用于检测和半定量病毒或潜伏感染的B 淋巴细胞;其在临床使用较少。
1.2 EBV 原位杂交检测
原位杂交是检测组织样本中EBV 的金标准。EBV 的转录本在其感染的肿瘤细胞和IM 患者的淋巴细胞中均得到表达。EBV 主要转录本是定位于细胞核或细胞质的EBER1 和EBER2。EBER1和EBER2 可以抑制干扰素介导的细胞凋亡和抗病毒活性。与处于沉默状态的病毒基因组相比它们有很高的拷贝数,可以作为检测组织样本中EBV潜伏感染的标记物[12]。原位杂交使用EBV 转录本作为标记物。该方法主要依据组织的细胞学和病理学对EBV 定位。由于EBV 相关的恶性肿瘤在早期已存在,EBER 信号也用于相关肿瘤的早期筛查。也可利用EBER 信号早期识别由EBV 引起的移植后淋巴增生性疾病(post-transplant 1ymphoproliferative disorder,PTLD)及鉴别诊断包括IM、HL和/或NHL 的疾病。该方法存在局限性如在口腔毛状粘膜白斑病中,EBV 转录本可能会下调。由于RNA 降解检测结果可能会出现假阴性。该方法只适用于细胞,操作繁琐耗时,同时需要特殊的技能。
1.3 EBV 嗜异凝集抗体检测
嗜异凝集抗体检测(heterophile antibody test,HAb)是常用的血清学试验,是一种简单但非特异性的检测。HAb 依赖于患者的血清或血浆对马、山羊或绵羊红细胞的凝集能力。正常情况下,抗体在IM患者中能检测到,但在许多其他疾病中没有。在EBV 感染过程中,85%~90%的成年人和青少年呈阳性,其中约50%在第一周的HAb 检测呈阳性[13]。HAb 通常用于原发性和复发性感染的诊断和筛查,它是IM 的一种敏感诊断测试。但是该方法存在非特异性,无法与其他原发性疾病(如病毒性肝炎、风疹、疟疾和艾滋病)、恶性肿瘤和自身免疫性疾病区分。只有大约10%~30%的两岁以下儿童和50%的2~5 岁儿童呈阳性,因此国内不推荐HAb 用于诊断儿童EBV 原发性感染引起的IM[14-15]。
1.4 EBV 特异性抗体检测
人类抵挡病毒入侵的第一道防线是免疫系统,其中的自然杀伤细胞和淋巴细胞发挥主要作用。然而,这种防御系统无法全部摧毁病毒,只可以使病毒维持较低的浓度或处于休眠状态。EBV感染细胞以后,可表达衣壳抗原(viral capsid antigen,VCA)、早期抗原(early antigen,EA)、膜抗原(membrane protein,MA)和EBNA 等,每种抗原会表达刺激相应抗体的产生,具体过程参见图1。原发感染过程中VCA 首先刺激产生IgM 和IgG 抗体,IgM 抗体在最早出现持续1~2 个月,IgG 抗体出现较迟持续数年。但原发性感染的儿童和成人并不总是VCA IgM 抗体呈阳性[16]。EA 是在病毒进入增殖期初期时形成的抗原,其IgG 抗体于发病后3~4 周达高峰,可持续3~6 个月是新近感染或EBV 活跃增殖的标志。MA 的IgG 抗体和EBNA的IgG 抗体于发病后3~4 周出现,终生持续存在,均是既往感染的标志。
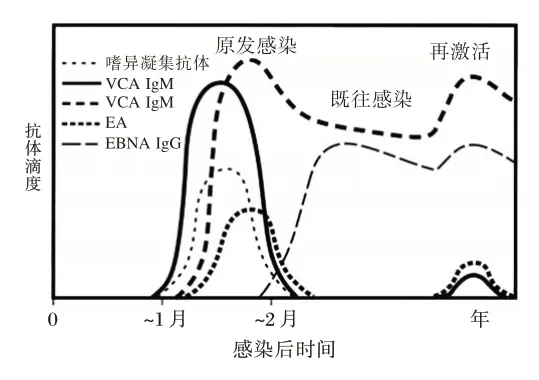
图1 EBV 感染后不同抗体的滴度变化[17]Figure 1 Titer changes of different antibodies after EBV infection[17]
与HAb 相比特异的EBV 抗体测试较为繁琐耗时,更昂贵。而且,这些检测需要特殊的底物或抗原。针对EBV 抗体(VCA-IgG、VCA-IgM、EBNAIgG、EBNA-IgM 和EA-IgG)有不同类型的特异检测。特异抗体检测在我国鼻咽癌临床检测中应用广泛。《鼻咽癌标志物临床应用专家共识》指出EBV是鼻咽癌标记物中应用最广泛、最成熟的诊断和预后判断标志物[18]。其中VCA-IgM 抗体可以作为急性感染的标志物,适用于病毒感染早期诊断;VCAIgG 抗体可以用于鼻咽癌筛查和早期诊断;NA-IgG抗体的滴度动态监测对鼻咽癌的疗效监测和预后判断有一定作用。多种抗体与DNA 联合检测能大大提高鼻咽癌检测的敏感度。EBV 抗体检测常规包括免疫荧光法(immunofluorescence assays,IFAs),酶联免疫法(enzyme immunoassays,EIAs)和与化学发光免疫分析法(chemiluminescence immunoassay,CLIA)联合的western blot 检测。
IFAs 是金标参照法,经常用于检测EBV 转化的BL 细胞系(如Raji 细胞系),EIAs 对该检测的特异性与IFAs 相似。因利用合成或纯化天然蛋白,EIAs 是检测EBV 特异性检测的主要方法。IFAs特异性较高,可以推算EBV 感染的分期,但其高度可变,缺乏标准化。EIAs 更加快速,可以大批量自动化检测,价格较低,但也欠缺标准化。一项研究表明,有些EIAs 与参考的IFAs 在感染分期方面结果非常一致,因此可能成为金标准IFAs 的替代品[19]。EIAs 和IFAs 仍需要免疫印迹和特异性IgG抗体的亲和测试辅助诊断测试以确证急性感染或其他感染阶段。CLIA 可以区分原发性感染和复发性感染且敏感度和特异性较好。Western blot 具有高特异性,能够从血清中对EBV 感染阶段分期,是针对几种抗原的EBV 的特异性抗体检测,但是其缺乏缓冲条件及重组抗原和细胞系裂解物的结合的标准且价格昂贵。为了更准确地诊断EBV 相关疾病仍需要一些辅助诊断试验如亲和性试验[20]。
亲和性检测是抗原-抗体复合物与尿素短暂孵育后测定其亲水性。高活性抗体能够与抗原结合,而低活性抗体在添加尿素后亲和性被消除[21]。亲和性提供了抗体与多价抗原结合强度的信息。特异性抗体检测主要用于确定病毒感染状态又可以用于疾病鉴别诊断;抗VCA-IgG、抗VCA-IgM和抗EBNA-IgG 抗体三者的检测结果可以评价患者免疫功能状态及EBV 感染的分期[14]。VCA IgG亲和度检测可以在VCA IgM 缺失的情况下区分原发性和既往感染。然而由于母体抗体的存在,亲和性检测不能用于新生儿[20]。
1.5 EBV 核酸载量检测
在过去的20年里,使用核酸扩增技术检测外周血中的EBV 载量已经成为诊断和监测免疫缺陷宿主EBV 感染和相关疾病的重要工具。实体器官接受者、干细胞移植接受者和其他免疫缺陷宿主中,EBV 病毒载量检测可以帮助诊断和管理EBV相关疾病。最重要的限制因素是缺乏定义临床相关断点的数据和适用于所有机构的试验的性能规范。由于EBV 载量监测尚未在实验室之间标准化,因此确定载量水平和EBV 疾病同这些患者中存在的可能性联系时存在困难。虽然在一个实验室EBV 病毒载量结果的连续监控已被证明与疾病结果是一致的,但是不同实验室之间EBV 载量测定的结果与疾病的关系无法确定。因此,各机构需要审查其EBV 载量的测定结果并将其与临床相关事件相关联,以确定患者的适当阈值。由于各实验室的结果不一致,接受连续监测的患者即使在出院后也需在同一实验室进行病毒载量测量,以确保随时间推移的病毒载量的可靠性。尽管世界卫生组织(world health organization WHO)已建立了第一代EBV 核酸国际标准品(NIBSC 编号为09/260),我国器审中心也已发布《EB 病毒核酸检测试剂注册技术审查指导原则》对试剂研发及生产进行指导,同时行业标准《EB 病毒核酸检测试剂盒(荧光PCR 法)》也正在制定中,但EBV 载量测定仍需要进一步标准化[22]。定量聚合酶链反应方法依赖于保守核酸序列的扩增,并利用荧光探针或插入染料来量化目的核酸。由于反应混合物包含在无菌、封闭的容器中,扩增子污染的风险较低。但是,不同实验室间诊断工具、设备和程序的变化可能会使检测结果不同。而且,对于用于研究EBV-DNA的理想样本类型(组织、外周血单核细胞、血清或血浆)存在很大争议[23]。EBV-DNA 的研究对免疫缺陷患者很有价值,因为他们的病毒载量比健康携带者高,特别是对于血清学检测结果阴性或不明确的患者[24]。此外,EBV-DNA 可在与EBV 相关的恶性肿瘤患者血液中裂解肿瘤的游离体或病毒粒子中检测到[24]。除了由于血脑屏障的保护而导致血液水平下降的艾滋病相关脑瘤患者外,检测EBV-DNA对EBV 相关肿瘤患者非常有价值。
2 总结与展望
研究表明EBV 与肿瘤(免疫细胞性淋巴瘤、BL、HL、NHL 和鼻咽癌)和许多自身免疫性疾病(类风湿关节炎、干燥综合征、系统性红斑狼疮和多发性硬化)存在相关性。上述EBV 病毒检测方法各有优缺点,应根据实际情况选择合适的检测手段,必要时可将两种或多种方法联合使用,保证检测结果更真实可靠。同时,需要进一步的证据和共识来对程序标准化,如样品类型、制备、引物/探针设计、设备、方案、报告单元和干预阈值。因此,研究者在努力阐明EBV 相关疾病发病机制和研发保护性疫苗的同时还需要标准化这些指标,为EBV 相关临床病症的诊断和治疗提供更可靠的依据和参考。
