电化学氧化工艺对NiO/Ni(OH)2电极材料电容性能的影响
2020-12-04曹中秋
张 轲, 高 晨, 周 岩, 曹中秋
(沈阳师范大学 化学化工学院, 沈阳 110034)
0 引 言
化石燃料引发的温室效应和环境污染日趋严重,迫使清洁能源成为全世界开发和利用的研究热点,其中具有代表性的有风能、潮汐能、太阳能、地热能等可再生能源。然而这些可再生能源发电系统由于运行的间歇性和地处偏远地区,使其并入输电供电电网变得技术上难以实现而且成本高昂,因此开发洁净、安全、高效方便的储能技术成为这些清洁能源利用的关键[1]。超级电容器作为介于物理电容器和化学电源之间的一种储能装置,是兼具电池和电容器二者部分特性的新型储能器件。相对于传统电容器和化学电池来说,超级电容器温度适用范围广且具备环保廉价的优势,同时其功率密度和能量密度都比较高,循环寿命也更长,基于上述特性,超级电容器在清洁能源发电储电领域、智能电网和新能源汽车等方面均有重要应用价值。超级电容器作为储能装置,它的组成部件都会对超级电容器的电化学性能产生影响,研究表明电极材料的性能对超级电容器的电化学性能起着决定性的作用,目前常用的电极材料主要有碳材料、过渡金属氧化物、导电聚合物以及复合材料电极[2-5]。其中过渡金属氧化物电极材料具有廉价、比电容高、电化学充放电性能优异的特点近年来受到广泛研究,特别是具有代表性的NiO/Ni(OH)2电极材料。NiO/Ni(OH)2电极材料的特点是制备方法简单易行,充放电平台宽,电化学可逆性好,比电容高等。NiO/Ni(OH)2电极材料的性能取决于将金属Ni转变为NiO/Ni(OH)2的技术方法,电化学氧化方法是其中一类重要技术,本文主要研究在电化学氧化电解液中加入助氧化剂对NiO/Ni(OH)2电极材料的电化学性能的影响。
1 试验方法
实验选用厚度为0.1 mm的纯铜片为基底材料,首先采用1000#水砂纸打磨铜片表面,接下来用浓度为10%的盐酸(HCl)浸蚀10 min除锈,并用蒸馏水清洗,再放入无水乙醇中超声清洗10 min除油吹干备用。采用化学镀的方法在其表面镀上一层厚度约为3 μm的纯Ni薄膜,然后经过电化学阳极氧化(以KOH为主的碱性电解液体系)转变成NiO/Ni(OH)2,最后对氧化后的NiO/Ni(OH)2电极材料进行SEM/EDX(SSX-550扫描电子显微镜,表面形貌分析)、XRD(美国Thermo VG公司ESCALAB 250 X射线衍射仪,测试2q范围35°~80°)、XPS(美国赛默飞世尔K-Alpha光电子能谱仪,表面氧化物分析)表征以及电化学测试(包括循环伏安测试、恒电流充放电测试、交流阻抗测试)。实验的侧重点在于电化学氧化碱性电解液体系中加入2种助氧化剂K2S2O8和NaNO2,研究其对NiO/Ni(OH)2电极材料的电化学充放电性能的影响。
化学镀纯Ni工艺为:化学镀液组成为18.4 g/L六水合硫酸镍(NiSO4·6H2O),123.6 mL/L联氨(N2H4),22.6 g/L酒石酸钾钠(C4H4KNaO6), 7.4 g/L乙二胺四乙酸二钠(C10H14N2Na2O8),调整镀液的pH为13.4,施镀温度60 ℃,时间40 min,蒸馏水清洗镀层吹干后进行直流恒压电化学阳极氧化,化学镀Ni试样做阳极,对电极选择用不锈钢惰性电极。阳极氧化工艺为:在1 mol/L的氢氧化钾水溶液基础上分别添加1 g/L的助氧化剂K2S2O8(标记为OA)和NaNO2(标记为OB),电压为1.2 V,时间为60 min,温度为60 ℃,电极间距为1 cm,未添加助氧化剂电化学氧化样品作为对比实验。阳极氧化后的试样电化学性能测试(循环伏安测试、恒电流充放电测试、交流阻抗测试)均采用电化学工作站CHI660在三电极系统中进行,工作电极为阳极氧化后的NiO/Ni(OH)2样品,对电极为Pt电极,参比电极为饱和甘汞电极(SCE),电解液为1 mol/L NaOH溶液。
2 结果与讨论
2.1 NiO/Ni(OH)2样品表征
图1为化学镀纯镍氧化前及采用不同阳极氧化工艺样品的表面形貌。可以看到,化学镀镍样品表面较为平整光滑,未见裂纹和孔洞(图1(a));采用未加助氧化剂阳极氧化后出现少量微坑(图1(b)),添加助氧化剂OA和OB后,微坑数量有所增加。微坑的增加有利于样品比表面积的增加,能提高NiO/Ni(OH)2样品的电容和充放电性能。电化学氧化并未破坏样品的整体表面形貌,因此可以判断氧化是在表面原位进行的。XRD图谱(图2)表明,电化学氧化后与氧化前均只检测到金属镍的3个衍射峰,并未检测到氧化物NiO和Ni(OH)2的存在,说明电化学氧化生成的氧化物较薄或者结晶度较差[6]。为了表征化学镀镍表面电化学氧化膜的相结构,对阳极氧化后的样品进行了XPS测试(图3)。3种电化学氧化后具有相似的XPS结果,均在Ni 2p图谱中出现4个XPS峰,显示了分配给Ni2+的2个自旋轨道双峰加上2个震动卫星峰,其中在结合能为872 eV和854 eV为Ni2+离子的Ni 2p1/2和Ni 2p3/2;O 1s图谱中在结合能为530~532 eV之间出现宽化的XPS峰,其对应Ni—O键以及一定程度的羟基化或者是羟基表面的氧取代集团[7-8],表明表面确实有氧化物并且其相结构为NiO/Ni(OH)2。

图1 NiO/Ni(OH)2样品SEM表面形貌,(a)化学镀镍未氧化,(b)电化学阳极氧化未添加助氧化剂,(c)添加助氧化剂OA,(d)添加助氧化剂OB

图2 NiO/Ni(OH)2样品表面XRD图谱,从下至上依次为未氧化(化学镀态),电化学阳极氧化未添加助氧化剂,添加助氧化剂OA,添加助氧化剂OB
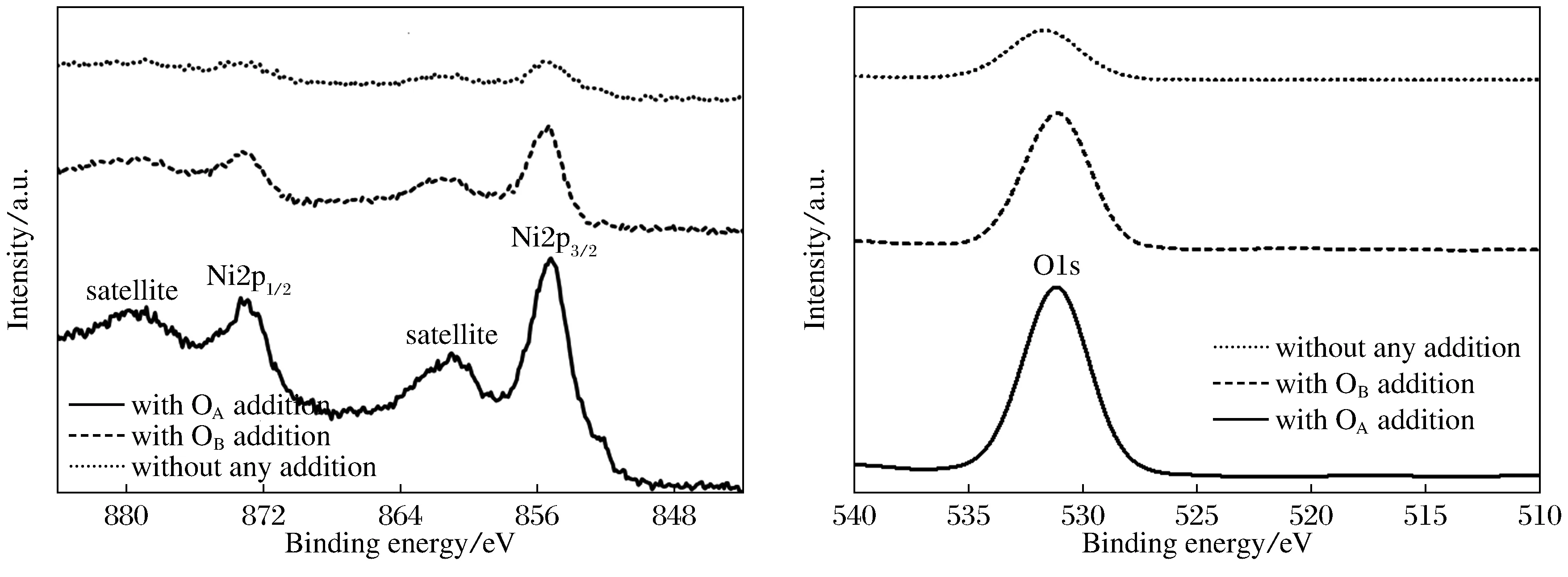
图3 NiO/Ni(OH)2样品氧化后在Ni2p和O1s区域的XPS图谱
由3种阳极氧化的XPS还可以看到,添加助氧化剂OA和OB后Ni 2p和O 1s峰强度显著增强,表明表面氧化物NiO/Ni(OH)2的量增大,这有利于NiO/Ni(OH)2样品比电容及电化学性能的提高,这一点在随后的循环伏安和恒电流充放电的测试中得到确认。未加助氧化剂进行电化学氧化时,在1MKOH溶液中,镍阳极上只发生如下反应:
在阳极氧化电解液中分别添加助氧化剂K2S2O8(OA)和NaNO2(OB)后,2种助氧化剂分别能在溶液中离解出具有氧化性的S2O82-、NO2-阴离子(见式(2)和(3),式(2)中[O]为氧原子具有氧化性),在化学镀镍镀层样品进行阳极氧化时,2种阴离子在电迁移的作用下也会向镍阳极表面传质,这样阳极氧化时镍阳极表面不但进行反应(1)电化学氧化并且还会发生化学氧化,从而提高表面氧化物的生成效率,使得阳极氧化后样品表面的氧化物的量增加,导致NiO/Ni(OH)2样品的比电容和充放电性能提高。
2.2 NiO/Ni(OH)2的电化学性能
图4左图为3种阳极氧化工艺下NiO/Ni(OH)2样品在1MNaOH溶液中扫速为50 mV/s时的循环伏安曲线。可以看出在所测试的循环伏安曲线中均出现了一对较强的氧化/还原峰, 对应于Ni2+和Ni3+的相互转化过程(反应(4))[9];3种阳极氧化工艺下氧化与还原峰均具有良好的对称性;随着氧化工艺的电解液中添加2种助氧化剂,氧化/还原峰电流均有所增加,而相应的峰电位向正方向移动较小,这表明所制备的NiO/Ni(OH)2样品具有良好的电化学活性和循环可逆性并且添加2种助氧化剂均能提高NiO/Ni(OH)2样品的比电容。峰电位向正方向移动的原因可能是添加助氧化剂后表面氧化物的致密性得到增加所致。循环伏安结果表明,NiO/Ni(OH)2样品的比电容主要来源于氧化还原反应(反应(4))法拉第赝电容的贡献。
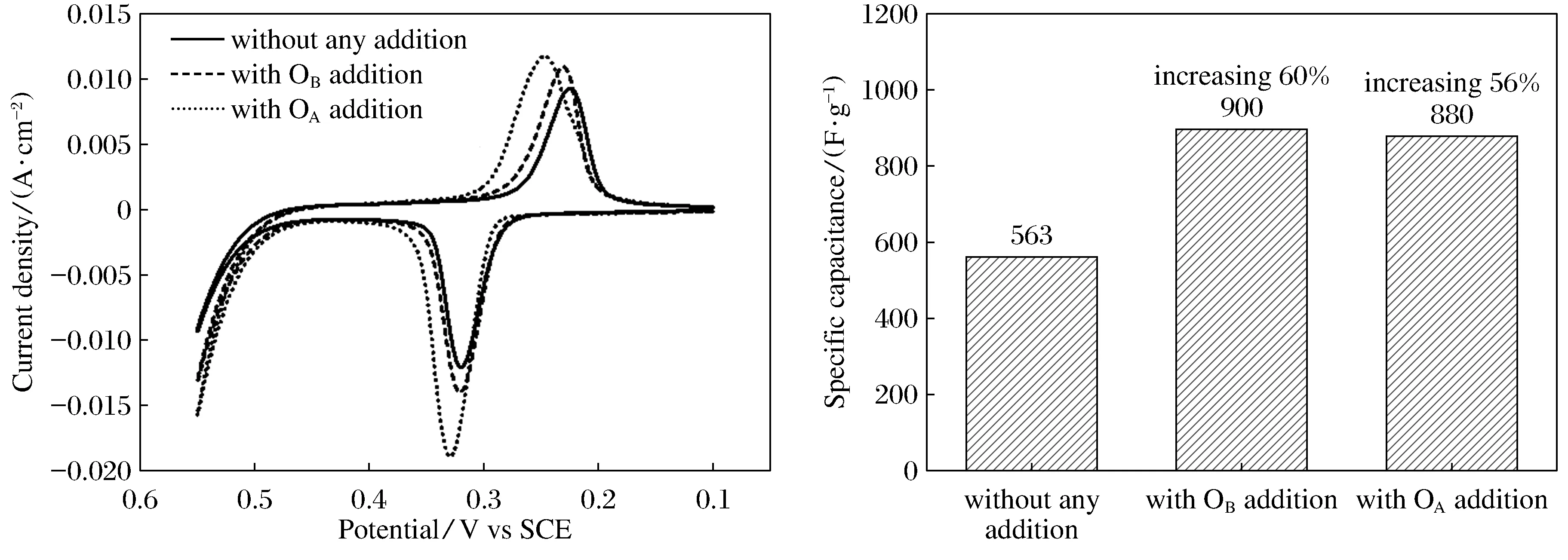
图4 不同氧化工艺的NiO/Ni(OH)2样品的循环伏安曲线及比电容对比图

(4)
图4右图为在循环伏安曲线的基础上根据式(5)[10]计算出来的3种NiO/Ni(OH)2样品的比电容值,可以发现,添加2种助氧化剂后,NiO/Ni(OH)2样品的比电容提高了50%~60%,助氧化剂OA稍好于OB。这可能与OA的氧化性较OB强所致。
(5)
其中C为NiO/Ni(OH)2样品的质量比电容量,单位F/g;I(V)代表循环伏安CV测试中的电流;m为活性物质的质量(在本文中为化学镀的Ni、NiO和Ni(OH)2的总质量,下同);V为扫描电势;ΔV则是扫描电势的范围;ν代表扫描速率,单位为mV/s。
相比较循环伏安法来讲,恒电流充放电更能精确揭示电极材料的比电容和电化学性能。图5(a)和(b)为所制备的NiO/Ni(OH)2样品在不同电流密度下的充放电曲线,所测试的充放电曲线均显示了明显的充放电平台以及良好的对称性, 对应于NiOOH与Ni(OH)2之间可逆氧化还原的电极反应(反应(4))。该结果进一步证实了NiO/Ni(OH)2样品的赝电容特性。添加助氧化剂OA的充放电平台稍宽于助氧化剂OB,说明其比电容稍大,这也与循环伏安的测试结果(图4)相一致。由充放电曲线根据式(6)[10]也可以计算电极的比电容值, 添加2种助氧化剂氧化后NiO/Ni(OH)2样品在不同充放电电流密度下的比电容见图5(c),可见随着充放电电流密度的增大,NiO/Ni(OH)2样品的比电容降低,添加助氧化剂OA的比电容始终稍大于助氧化剂OB。
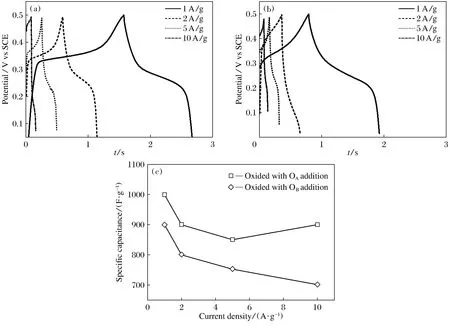
图5 不同氧化工艺的NiO/Ni(OH)2样品恒电流充放电曲线,(a)添加助氧化剂OA,(b)添加助氧化剂OB,(c)充放电电流密度对比电容的影响
(6)
图6给出了在1 A/g的充放电电流密度下2种添加了助氧化剂氧化后NiO/Ni(OH)2样品的电化学循环性能。在初始的2 000次充放电循环中,NiO/Ni(OH)2样品的比电容升高较快,之后趋于平缓,10 000次充放电循环后,NiO/Ni(OH)2样品的比电容分别到达1 410 F/g和1 380 F/g,显示了优异的电化学循环稳定性。与目前大多数文献[11-15]报道的结果相比(见表1), 本文采用化学镀再电化学氧化(添加助氧化剂)后制备的NiO/Ni(OH)2样品显示了较高的比电容和明显改善的电化学循环稳定性,这可能与本实验电化学原位氧化化学镀镍表面生成的NiO/Ni(OH)2为玻璃态的非晶组织有关。应该指出的是,尽管本文所制备的NiO/Ni(OH)2样品的比电容较高,但还是远低于相应材料的理论电容值(在0.5 V的电位窗口内NiO和Ni(OH)2的理论电容值分别为2 584和2 082 F/g)[16],说明NiO/Ni(OH)2材料的潜力还可以通过改进材料的制备方法、添加组元和改进表面组织形貌等进一步提高。

图6 NiO/Ni(OH)2样品在1 A/g电流密度下的充放电循环性能
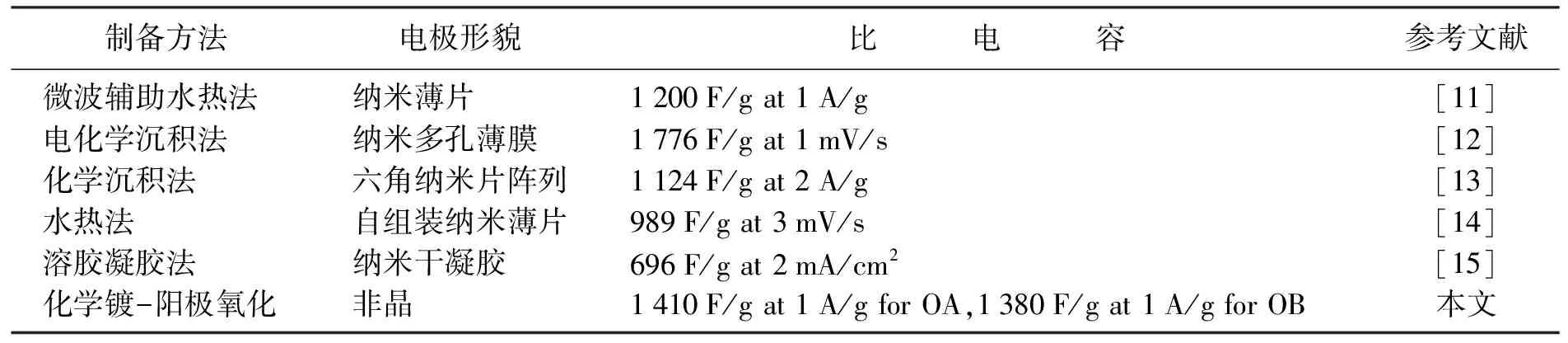
表1 不同制备方法的NiO/Ni(OH)2比电容文献值
能量密度和功率密度是衡量能量储存系统的2个重要参数,而Ragone图反映了能量密度和功率密度的关系,一般来讲两者具有反比关系,即能量密度越高功率密度越低,可以用于比较各种储能器件的性能优劣,电化学超级电容器的能量密度在1~10 kWh/kg之间,相应的功率密度在1~10 kW/kg之间[17-19]。本文制备的2种添加助氧化剂电化学氧化后的NiO/Ni(OH)2样品的Ragone图见图7。可见2种助氧化剂制备的NiO/Ni(OH)2样品能量密度和功率密度差别不大,助氧化剂OA较OB稍好。在功率密度为4.4kW/kg时,能量密度较低约为0.25 kWh/kg;当功率密度降低至3.75 kW/kg时,能量密度可以提高约至2.25 kWh/kg,说明采用添加助氧化剂电化学氧化制备的NiO/Ni(OH)2样品具有较高的功率密度和较低的能量密度。

图7 NiO/Ni(OH)2样品的能量密度与功率密度关系
3 结 论
采用化学镀再电化学氧化的方法在铜片表面制备出带有微坑的均一NiO/Ni(OH)2电极材料,通过电化学氧化电解液中添加2种助氧化剂过硫酸钾和亚硝酸钠均能提高电极材料表面NiO/Ni(OH)2含量。循环伏安测量表明,2种助氧化剂的添加提高了NiO/Ni(OH)2电极材料的比电容值50%~69%;在1 A/g的充放电电流密度下,2种助氧化剂存在下阳极氧化所制得的NiO/Ni(OH)2电极材料经历10 000次充放电循环后分别给出了1 410和1 380 F/g的比电容, 显示出良好的可逆性及电化学稳定性;Ragone曲线揭示了所制备的NiO/Ni(OH)2样品具有较高的功率密度和较低的能量密度。化学镀表面的非晶组织和添加助氧化剂进行电化学原位氧化使得表面氧化物含量增大及致密性提高是其显示优异赝电容性能的主要原因。