刺通草的化学成分及其肿瘤细胞毒活性研究
2020-12-03陈雪林卢志远贡潘偏抽张玉梅
陈雪林,卢志远,贡潘偏抽,张玉梅*
1中国科学院西双版纳热带植物园热带植物资源可持续利用重点实验室,昆明 650223;2中国科学院大学,北京 100049
五加科(Araliaceae)是药用植物资源非常丰富的一个科[1],有很多著名的传统药材,如人参、三七等;还有很多民间常用的中草药,如鹅掌藤、白簕等。刺通草(Trevesiapalmate(Roxb.)Vis.var.palmata)为五加科(Araliaceae)刺通草属(Trevesia)植物,主要分布于云南南部、广西上林和贵州贞丰[2]。目前针对刺通草属的化学成分研究比较少,从中分离得到的化学成分主要是齐墩果酸型三萜皂苷化合物,对刺通草的生物活性主要集中在抗肿瘤、降血糖、抗炎和抗病毒等方面[3-7]。
刺通草作为传统傣药,傣族人民主要用其治疗“风寒湿痹证”,且Nunziatina等[4]从刺通草中分离得到的三萜皂苷及其次皂甙元具有抑制细胞增殖的活性,这为其深度开发利用提供了科学依据。为进一步明确刺通草的化学成分及其抗肿瘤活性药效物质基础,以期为其刺通草在抗肿瘤方面的开发利用提供一定的理论依据,本课题组以生长在中国云南省西双版纳地区的刺通草作为研究对象,对其化学成分及抗肿瘤活性进行研究。
1 仪器与材料
1.1 仪器和试剂
核磁共振谱用Avance Ⅲ-600超导核磁共振仪测定,TMS为内标;ESI-MS用Water Auto Spec Premier双聚焦三扇形磁质谱仪测定;R-1001VN型旋转蒸发仪(郑州长城科工有限公司);DLSB-5L/25型低温冷却液循环泵(巩义市予华仪器有限公司);YP5001N型电子天平(2~5 000g)(上海舜宇恒平科学仪器有限公司);AL104型电子天平(0.000 0~110 g)(梅特勒-托利多仪器(上海)有限公司);SK52008型超声波清洗器(上海科导超声仪器有限公司);UV-1型三用紫外仪(上海顾村电光仪器);柱层析硅胶(80~100目,200~300目)及薄板层析硅胶(GF-254)均为青岛海洋化工厂生产;Sephadex LH-20(美国Pharmacia公司);Rp-C18(德国Merk公司);高效液相色谱仪(汉邦科技公司);所用化学试剂均为工业重蒸试剂或分析纯。
1.2 材料
刺通草于2015年10月采于云南西双版纳,并由中国科学院西双版纳热带植物园肖春芬老师鉴定为Trevesiapalmate(Roxb.) Vis.var.palmata,标本(NO.20151006)存放在中国科学院西双版纳热带植物园创新药物研究组实验室。
2 实验方法
2.1 提取与分离
将刺通草枝叶晒干,粉碎,称重得18 kg。用90%甲醇于室温分别提取3次(7天、3天、3天)。合并提取液,减压浓缩,制成甲醇浸膏。甲醇浸膏用水搅拌溶解稀释后,依次用石油醚、乙酸乙酯、正丁醇进行萃取,每种溶剂萃取四次,减压回收溶剂后得到石油醚萃取物503 g,乙酸乙酯萃取物69.7 g,正丁醇萃取物208 g。石油醚部分经硅胶柱(200~300目,5 kg),以石油醚-丙酮(V/V=9∶1、8∶2、7∶3、6∶4、1∶1、0∶1)梯度洗脱,得到A1-A7七个组分;A2经反复重结晶得到化合物13(203 mg);A5经反复硅胶柱层析和Sephadex LH-20纯化,得到化合物14(33 mg);乙酸乙酯部分经硅胶柱(200~300目,1.5 kg),以氯仿-甲醇(V/V=20∶1、10∶1、5∶1、2∶1、1∶1、0∶1)梯度洗脱,得到B1-B6六个组分;B2经反复硅胶柱层析, MCI和Sephadex LH-20纯化,得到化合物1(93 mg);B3经反复硅胶柱层析和Sephadex LH-20纯化,得到化合物12(13 mg);B5经反复硅胶柱层析,Rp-C18和Sephadex LH-20纯化,得到化合物3(22 mg);B6经反复硅胶柱层析,Rp-C18和Sephadex LH-20纯化,得到化合物2(15 mg); B7经反复硅胶柱层析,Rp-C18和Sephadex LH-20纯化,得到化合物8(17 mg); 正丁醇部分经硅胶柱(200~300目,1.5 kg),以氯仿-甲醇(V/V=50∶1、20∶1、10∶1、5∶1、2∶1、1∶1、0∶1)梯度洗脱,洗脱得到C1~C7七个组分;C1经反复硅胶柱层析和Sephadex LH-20纯化,得到化合物9(13 mg);C2经反复硅胶柱层析,Rp-C18和Sephadex LH-20纯化,得到化合物10(15 mg);C4经反复硅胶柱层析和Sephadex LH-20纯化,得到化合物11(22 mg);C5经反复硅胶柱层析,MCI和Sephadex LH-20纯化,得到化合物7(5 mg);C6经反复硅胶柱层析,MCI,Rp-C18和 Sephadex LH-20纯化,得到化合物4(7 mg)和5(7 mg);C7经反复硅胶柱层析,MCI和 Sephadex LH-20纯化,得到化合物6(4 mg)。化合物1~14的化学结构见图1。
2.2 抗肿瘤活性筛选
采用MTS法[8]测定部分单体化合物对人肿瘤细胞株SMMC-7721、Hela、MCF-7的体外肿瘤细胞毒活性。用含10%胎牛血清的培养液(DMEM或者RMPI1640)配成单个细胞悬液,以每孔5 000个细胞接种到96孔板,每孔体积100 μL,细胞提前12~24 h接种培养。加入待测化合物溶液(化合物用DMSO溶解,化合物以100 μg/mL浓度初筛),每孔终体积200 μL,每种处理均设3个复孔。37 ℃培养48 h后,细胞弃孔内培养液,每孔加MTS溶液20 μL以及培养液100 μL;设3个空白复孔(MTS溶液20 μL和培养液100 μL的混合液),继续孵育2~4 h,使反应充分进行。多功能酶标仪(MULTISKAN FC)测定492 nm处的OD值,计算得出抗肿瘤活性的抑制率。每次实验均设顺铂(DDP)和紫杉醇(taxol)两个阳性化合物,以浓度为横坐标,细胞存活率为纵坐标绘制细胞生长曲线,应用两点法计算化合物的IC50值。
具有抑制率超50%的待测样品进行复筛,在测试浓度基础上向下稀释5个浓度,测定OD值,计算抑制率,求出相应的半数抑制浓度IC50。
抑制率=(1-实验孔OD492 nm/空白孔OD492 nm)
×100%
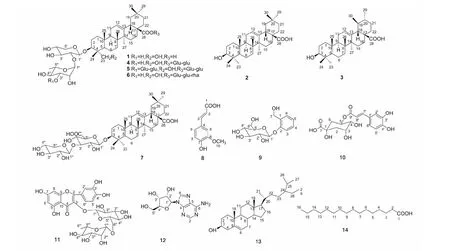
图1 化合物1~14的化学结构Fig.1 The chemical structures of compounds 1-14
IC50(50% concentration of inhibition)按Reed&Muench法计算。
3 实验结果
3.1 结构鉴定
化合物1白色粉末(甲醇);化学式为C41H66O12,ESI-MS:m/z749 [M-H]-;1H NMR(600 MHz,CD3OD)δ:5.24(1H,t,J=3.6 Hz,H-12),5.16(1H,d,J=1.2 Hz,H-1′),4.55(1H,d,J=5.4 Hz,H-l″),3.38(1H,dd,J=11.0,6.8 Hz,H-3),1.24(3H,d,J=6.0 Hz,H-6″),1.18(3H,s,H-27),0.98(3H,s,H-24),0.94(3H,s,26),0.91(3H,s,H-30),0.82(3H,s,H-25),0.70(3H,s,H-29);13C NMR(150 MHz,CD3OD)δ:39.8(C-1),26.7(C-2),82.4(C-3),44.1(C-4),48.2(C-5),18.1(C-6),34.0(C-7),40.7(C-8),48.4(C-9),37.8(C-10),24.7(C-11),123.8(C-12),145.4(C-13),43.1(C-14),29.0(C-15),24.1(C-16),47.8(C-17),42.9(C-18),47.4(C-19),31.8(C-20),35.0(C-21),33.5(C-22),64.7(C-23),13.9(C-24),16.5(C-25),17.9(C-26),26.6(C-27),182.1(C-28),33.7(C-29),24.2(C-30),104.5(C-1′),79.6(C-2′),76.8(C-3′),70.3(C-4′),65.0(C-5′),102.0(C-1″),72.2(C-2″),72.3(C-3″),74.1(C-4″),69.4(C-5″),19.0(C-6″)。以上数据与文献[9]报道一致,鉴定为3-O-α-L-鼠李糖-(1→2)-α-L-阿拉伯糖常春藤苷。
化合物2白色针状结晶(甲醇);化学式为C30H48O3,ESI-MS:m/z455 [M-H]-;1H NMR(600 MHz,CD3OD)δ:5.22(1H,t,J=3.6 Hz,H-12),3.15(1H,dd,J=11.4,4.2 Hz,H-3),1.16(3H,s,H-27),0.97(3H,s,H-23),0.94(6H,s,H-24,H-29),0.91(3H,s,H-30),0.82(3H,s,H-25),0.78(3H,s,H-26);13C NMR(150 MHz,CD3OD)δ:38.6(C-1),27.4(C-2),79.2(C-3),39.0(C-4),55.4(C-5),18.5(C-6),32.8(C-7),39.4(C-8),47.8(C-9),37.3(C-10),23.2(C-11),122.9(C-12),143.8(C-13),41.8(C-14),27.9(C-15),23.6(C-16),46.7(C-17),41.3(C-18),46.1(C-19),30.9(C-20),34.0(C-21),32.6(C-22),28.3(C-23),15.8(C-24),15.5(C-25),17.3(C-26),26.1(C-27),181.6(C-28),33.3(C-29),23.8(C-30)。以上数据与文献[10]报道基本一致,鉴定为齐墩果酸。
化合物3白色针状结晶(甲醇);化学式为C30H48O3,ESI-MS:m/z455 [M-H]-;1H NMR(600 MHz,CD3OD)δ:5.23(1H,t,J=3.5 Hz,H-12),3.15(1H,dd,J=11.6,4.5 Hz,H-3),1.09(3H,s,H-27),0.97(9H,overlapped,H-23,H-24,H-29),0.89(3H,d,J=6.4 Hz,H-30),0.85(3H,s,H-25),0.77(3H,s,H-26);13C NMR(150 MHz,CD3OD)δ:40.6(C-1),28.0(C-2),79.8(C-3),40.6(C-4),56.9(C-5),19.6(C-6),34.5(C-7),40.9(C-8),48.1(C-9),38.2(C-10),24.5(C-11),127.0(C-12),139.8(C-13),43.4(C-14),29.3(C-15),25.5(C-16),48.1(C-17),54.5(C-18),40.1(C-19),40.0(C-20),31.9(C-21),38.3(C-22),28.9(C-23),16.5(C-24),16.2(C-25),17.8(C-26),24.2(C-27),181.8(C-28),17.9(C-29),21.7(C-30)。以上数据与文献[11]报道一致,鉴定为熊果酸。
化合物4白色粉末(甲醇);化学式为C53H86O22,ESI-MS:m/z1119 [M+2Na-H]-、749 [M-2Glc-H]-;1H NMR(600 MHz,CD3OD)δ:5.33(1H,d,J=8.2 Hz,H-1‴),5.25(1H,brs,H-12),5.16(1H,s,H-1″),4.64(1H,s,H-l″″),4.55(1H,d,J=5.6 Hz,H-l′),3.25(1H,dd,J=5.6,1.9 Hz,H-3),1.17(3H,s,H-30),0.98(3H,s,H-29),0.94(3H,s,H-27),0.91(3H,s,H-26),0.80(3H,s,H-25),0.70(3H,s,H-24);13C NMR(150 MHz,CD3OD)δ:39.9(C-1),26.7(C-2),82.4(C-3),44.1(C-4),48.3(C-5),18.1(C-6),33.5(C-7),40.8(C-8),49.7(C-9),37.8(C-10),24.2(C-11),123.9(C-12),145.1(C-13),43.2(C-14),29.1(C-15),24.7(C-16),48.2(C-17),42.7(C-18),47.4(C-19),31.7(C-20),35.0(C-21),33.3(C-22),64.7(C-23),13.9(C-24),16.7(C-25),18.0(C-26),26.5(C-27),178.2(C-28),33.7(C-29),24.2(C-30),104.5(C-1′),76.8(C-2′),74.1(C-3′),70.3(C-4′),65.0(C-5′),102.0(C-1″),72.1(C-2″),72.2(C-3″),74.0(C-4″),69.4(C-5″),19.0(C-6″),95.9(C-1‴),73.9(C-2‴),78.1(C-3‴),71.0(C-4‴),77.9(C-5‴),69.6(C-6‴),104.8(C-1″″),75.3(C-2″″),78.3(C-3″″),71.6(C-4″″),78.1(C-5″″),62.9(C-6″″)。以上数据与文献[12]报道一致,鉴定为川续断皂苷B。
化合物5白色粉末(甲醇);化学式为C65H106O32,ESI-MS:m/z1073 [M-2Glc-H]-;1H NMR(600 MHz,CD3OD)δ:5.35(1H,d,J=8.2 Hz,H-1″″′),5.25(1H,br s,H-12),5.16(1H,s,H-1′),4.94(1H,overlapped,H-1″″″),4.64(1H,s,H-l″ ),4.54(1H,d,J=7.8 Hz,H-l″″),4.41(1H,d,J=7.9 Hz,H-l‴),3.38(1H,m,H-3),1.26(3H,d,J=6.2 Hz,H-6″),1.17(3H,s,H-25),0.98(3H,s,H-24),0.94(3H,s,H-27),0.92(3H,s,H-26),0.80(3H,s,H-30),0.70(3H,s,H-29);13C NMR(150 MHz,CD3OD)δ:39.9(C-1),26.8(C-2),82.5(C-3),44.1(C-4),48.3(C-5),18.3(C-6),33.5(C-7),40.8(C-8),48.2(C-9),37.8(C-10),24.2(C-11),123.9(C-12),145.1(C-13),43.2(C-14),29.1(C-15),24.7(C-16),48.2(C-17),42.7(C-18),47.4(C-19),31.7(C-20),35.0(C-21),33.4(C-22),64.7(C-23),13.9(C-24),16.7(C-25),18.0(C-26),26.5(C-27),178.2(C-28),33.7(C-29),24.2(C-30),104.7(C-1′),76.2(C-2′),74.3(C-3′),70.2(C-4′),66.0(C-5′),101.8(C-1″),71.7(C-2″),83.1(C-3″),72.7(C-4″),70.0(C-5″),19.0(C-6″),105.8(C-1‴),75.3(C-2‴),76.8(C-3‴),80.2(C-4‴),76.5(C-5‴),61.7(C-6‴),104.8(C-1″″),75.0(C-2″″),78.3(C-3″″),71.5(C-4″″),78.1(C-5″″),62.7(C-6″″),95.9(C-1″″′),74.0(C-2″″′),78.0(C-3″″′),71.0(C-4″″′),78.0(C-5″″′),69.6(C-6″″′),105.2(C-1″″″),75.2(C-2″″″),78.3(C-3″″″),71.(C-4″″″),78.2(C-5″″″),62.5(C-6″″″)。以上数据与文献[13]报道一致,鉴定为灰毡毛忍冬皂苷B。
化合物6白色粉末(甲醇);化学式为C59H96O26,ESI-MS:m/z749 [M-2Glc-Rha-H]-;1H NMR(600 MHz,CD3OD)δ:5.33(1H,d,J=7.8 Hz,H-1‴),5.25(1H,t,J=3.4 Hz,H-12),5.16(1H,d,J=1.2 Hz,H-1″),4.84(1H,d,J=1.2 Hz,H-1″″),4.54(1H,d,J=5.4 Hz,H-l″″′),4.40(1H,d,J=7.8 Hz,H-l′),3.23(1H,dd,J=9.0,8.4 Hz,H-3),1.27(3H,d,J=6.0 Hz,H-6″),1.24(3H,d,J=6.0 Hz,H-6″″′),1.17(3H,s,H-30),0.98(3H,s,H-29),0.94(3H,s,H-27),0.91(3H,s,H-26),0.80(3H,s,H-25),0.70(3H,s,H-2);13C NMR(150 MHz,CD3OD)δ:39.8(C-1),26.7(C-2),82.4(C-3),43.1(C-4),48.2(C-5),18.0(C-6),33.4(C-7),40.8(C-8),48.3(C-9),37.8(C-10),24.7(C-11),123.9(C-12),145.1(C-13),42.7(C-14),29.1(C-15),24.2(C-16),47.4(C-17),41.7(C-18),44.1(C-19),31.7(C-20),35.0(C-21),33.4(C-22),64.7(C-23),13.9(C-24),16.7(C-25),18.0(C-26),26.5(C-27),178.3(C-28),33.6(C-29),24.3(C-30),104.4(C-1′),76.7(C-2′),74.1(C-3′),69.4(C-4′),65.1(C-5′),102.0(C-1″),72.2(C-2″),72.2(C-3″),74.0(C-4″),70.3(C-5″),18.1(C-6″),95.9(C-1‴),73.9(C-2‴),79.6(C-3‴),71.0(C-4‴),78.2(C-5‴),69.5(C-6‴),104.6(C-1″″),75.4(C-2″″),76.9(C-3″″),78.3(C-4″″),77.0(C-5″″),62.0(C-6″″),103.1(C-1″″′),72.3(C-2″″′),72.6(C-3″″′),73.9(C-4″″′),70.8(C-5″″′),19.0(C-6″″′)。以上数据与文献[14]报道一致,鉴定常春藤皂苷C。
化合物7白色粉末(吡啶);化学式为C41H64O13,ESI-MS:m/z763 [M-H]-;1H NMR(600 MHz,Pyr)δ:5.37(1H,overlapped,H-1″),5.25(1H,brs,H-l2),5.03(1H,overlapped,H-1′),3.30(1H,d,J=10.8 Hz,H-3),1.33(3H,s,H-27),1.32(3H,s,H-23),1.01(3H,s,H-25),0.99(6H,s,H-24,H-29),0.97(3H,s,H-30),0.79(3H,s,H-26);13C NMR(150 MHz,Pyr)δ:39.0(C-1),26.7(C-2),89.6(C-3),40.0(C-4),56.1(C-5),20.0(C-6),33.8(C-7),40.2(C-8),48.4(C-9),37.4(C-10),24.2(C-11),123.0(C-12),145.3(C-13),42.6(C-14),28.5(C-15),24.1(C-16),47.1(C-17) 42.4(C-18),46.9(C-19),31.4(C-20),34.7(C-21),33.6(C-22),28.8(C-23),17.8(C-24),17.4(C-25),18.9(C-26),27.0(C-27),180.9(C-28),33.7(C-29),24.2(C-30),107.2(C-1′),75.1(C-2′),86.7(C-3′),72.0(C-4′),80.3(C-5′),180.7(C-6′),106.6(C-1″),75.7(C-2″),78.6(C-3″),71.4(C-4″),67.9(C-5″)。以上数据与文献[15]报道一致,鉴定为地肤子皂苷Ic。
化合物8白色粉末(甲醇);化学式为C10H10O4,EI-MS:m/z194 [M]+;1H NMR(600 MHz,CD3OD)δ:7.59(1H,d,J=16.2 Hz,H-3),7.17(1H,d,J=1.8 Hz,H-5),7.06(1H,dd,J=8.4,1.8 Hz,H-9),6.81(1H,d,J=7.8 Hz,H-8),6.31(1H,d,J=15.6 Hz,H-2),3.89(3H,s,H-10);13C NMR(150 MHz,CD3OD)δ:171.1(C-1),116.6(C-2),147.1(C-3),127.9(C-4),124.1(C-5),116.0(C-6),150.6(C-7),149.5(C-8),111.7(C-9),56.5(C-10)。以上数据与文献[16]报道一致,鉴定为阿魏酸。
化合物9白色粉末(DMSO);化学式为C13H18O7,EI-MS:m/z286 [M]+;1H NMR(600 MHz,DMSO-d6)δ:7.36(1H,d,J=7.2 Hz,H-6),7.20(1H,m,H-4),7.09(1H,d,J=7.9 Hz,H-3),7.00(1H,m,H-5),5.36(1H,d,J=4.2 Hz,H-1′);13C NMR(150 MHz,DMSO-d6)δ:131.5(C-1),154.7(C-2),114.7(C-3),127.7(C-4),121.7(C-5),127.1(C-6),58.2(C-7),101.4(C-1′),73.4(C-2′),77.1(C-3′),69.7(C-4′),76.5(C-5′),60.8(C-6′)。以上数据与文献[17]报道一致,鉴定为水杨苷。
化合物10白色粉末(甲醇);化学式为C16H18O9,EI-MS:m/z354 [M]+;1H NMR(600 MHz,CD3OD)δ:7.56(1H,d,J=16.2 Hz,H-7′),7.05(1H,d,J=1.8 Hz,H-2′),6.95(1H,dd,J=8.4,1.8 Hz,H-6′),6.78(1H,d,J=8.4 Hz,H-5′),6.26(1H,d,J=16.2 Hz,H-8′),5.33(1H,td,J=9.0,4.4 Hz,H-5),4.16(1H,m,H-3),3.73(1H,dd,J=8.4,3.0 Hz,H-4),2.21(2H,ddd,J=17.0,13.6,2.5 Hz,H-2),2.06(2H,ddd,J=14.1,9.0,6.7Hz,H-6);13C NMR(150 MHz,CD3OD)δ:76.2(C-1),38.3(C-2),71.4(C-3),73.5(C-4),72.1(C-5),38.9(C-6),177.1(C-7),127.9(C-1′),115.3(C-2′),146.9(C-3′),149.7(C-4′),116.6(C-5′),123.1(C-6′),147.2(C-7′),115.3(C-8′),168.8(C-9′)。以上数据与文献[18]报道一致,鉴定为绿原酸。
化合物11黄色粉末(甲醇);化学式为C27H30O16,EI-MS:m/z610 [M]+;1H NMR(500 MHz,CD3OD)δ:7.66(1H,t,J=3.5 Hz,H-2′),7.62(1H,dd,J=10.2,3.0 Hz,H-6′),6.86(1H,d,J=10.2 Hz,H-5′),6.39(1H,d,J=2.4 Hz,H-8),6.20(1H,d,J=2.4 Hz,H-6),5.10(1H,d,J=9.6 Hz,H-1″),4.51(1H,d,J=1.8 Hz,H-1‴),1.11(3H,d,J=7.8 Hz,H-6‴);13C NMR(125 MHz,CD3OD)δ:158.5(C-2),135.6(C-3),179.4(C-4),163.0(C-5),99.9(C-6),166.0(C-7),94.8(C-8),159.3(C-9),105.6(C-10),123.1(C-1′),116.0(C-2′),149.8(C-3′),145.8(C-4′),117.7(C-5′),123.5(C-6′),104.7(C-1″),75.7(C-2″),77.2(C-3″),72.2(C-4″),78.2(C-5″),68.5(C-6″),102.4(C-1‴),72.1(C-2‴),71.4(C-3‴),73.9(C-4‴),69.7(C-5‴),17.9(C-6‴)。以上数据与文献[19]报道一致,鉴定为芦丁。
化合物12白色粉末(DMSO);化学式为C10H13N5O4,EI-MS:m/z267 [M]+;1H NMR(600 MHz,DMSO-d6)δ:8.35(1H,s,H-8),8.13(1H,s,H-2),5.87(1H,d,J=6.0 Hz,H-1′),5.22(1H,d,J=4.2 Hz,OH-3′),4.60(1H,dd,J=11.4,6.0 Hz,H-2′),4.13(1H,dd,J=7.8,4.8 Hz,H-3′),3.96(1H,q,J=3.6 Hz,H-4′),3.59(2H,m,H-5′);13C NMR(150 MHz,DMSO-d6)δ:152.4(C-2),149.1(C-4),119.4(C-5),156.2(C-6),140.0(C-8),87.9(C-1′),73.4(C-2′),70.7(C-3′),85.9(C-4′),61.7(C-5′)。以上数据与文献[20]报道一致,鉴定为β-adenosine。
化合物13白色针状结晶;与β-sitosterol标准品对照,经薄层色谱(TLC)检测,其Rf值在三种不同溶剂体系中一致且显色相同,故确定为β-谷甾醇。
化合物14白色粉末(氯仿);化学式为C16H32O2,EI-MS:m/z256 [M]+;1H NMR(600 MHz,CDCl3)δ:2.35(2H,t,J=7.8 Hz,H-2),1.63(2H,dt,J=15.0,7.2 Hz,H-3),0.88(3H,t,J=4.8 Hz,H-16);13C NMR(150 MHz,CDCl3)δ:179.5(C-1),34.1(C-2),32.2(C-3),29.9~29.3(C-4~C-13),24.9(C-14),22.9(C-15),14.4(C-16)。以上数据与文献[21]报道一致,鉴定为棕榈酸。
3.2 体外肿瘤细胞毒活性筛选
对刺通草分离得到的化合物1~6和化合物8~11,共10个化合物进行了人肿瘤细胞株SMMC-7721、Hela、MCF-7的体外细胞毒活性研究。由表1可知,化合物1和3对所有人肿瘤细胞株均显示出明显的细胞毒活性。化合物1对人肿瘤细胞株SMMC-7721、Hela、MCF-7的抑制率分别为100%、99.64%、99.71%;化合物3对人肿瘤细胞株SMMC-7721、Hela、MCF-7的抑制率分别为87.47%、96.68%、93.46%。进一步的评估结果显示(表2),化合物1对人肿瘤细胞株SMMC-7721、Hela和MCF-7的细胞毒活性(IC50值)分别为10.37±0.19、28.57±0.93和4.92±0.49 μM;化合物3对人肿瘤细胞株SMMC-7721、Hela和MCF-7的细胞毒性(IC50值)分别为17.46±0.19、51.80±4.38和6.75±0.18 μM。
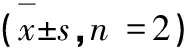
表1 刺通草单体化合物对SMMC-7721、Hela、MCF-7细胞株的细胞毒活性Table 1 Cytotoxicity of compounds on SMMC-7721,Hela and MCF-7 cell =2)
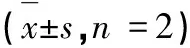
表2 化合物1和化合物3的细胞毒活性Table 2 Cytotoxicity of compound 1 and compound =2)
4 结论
本研究从刺通草中分离得到14个化合物,其中化合物2~14为首次从刺通草中分离得到。对人肿瘤细胞株SMMC-7721、Hela、MCF-7的细胞毒活性筛选结果显示,化合物1和3对3种人肿瘤细胞株均显示出较为明显的细胞毒活性,且化合物1对人肿瘤细胞株SMMC-7721、Hela和MCF-7的细胞毒活性(其对三种人肿瘤细胞株的IC50值分别为10.37±0.19、28.57±0.93和4.92±0.49 μM),均优于阳性药物顺铂DDP(其对三种人肿瘤细胞株的IC50值分别为38.79±2.97、42.59±4.23和39.86±2.10 μM);而化合物3对人肿瘤细胞株SMMC-7721和MCF-7的细胞毒活性(其对人肿瘤细胞株SMMC-7721和MCF-7的IC50值分别为17.46±0.19和6.75±0.18 μM)也优于阳性药物顺铂DDP。其中化合物1对宫颈癌细胞Hela的细胞毒活性为首次报道,具有一定的抗肿瘤药物开发潜力。本研究通过对刺通草化学成分和肿瘤细胞毒活性的研究,进一步明确了刺通草的抗肿瘤活性药效物质基础,为刺通草在抗肿瘤方面的开发利用提供了一定的理论依据。
