磷酸法荔枝核基活性炭的制备及其吸附性能
2020-12-01陈秋娟谢微莫福旺刘科讯向金宁胡月芳
陈秋娟 ,谢微,莫福旺 *,刘科讯,向金宁,胡月芳
1. 贺州学院材料与化学工程学院(贺州 542899);2. 广西碳酸钙资源综合利用重点实验室(贺州 542899);3. 贺州学院食品科学与工程技术研究院(贺州 542899)
近年来,活性炭由于本身有很大的比表面积、吸附效果好等优点,被广泛应用于工业、农业以及废水污染处理、催化、吸附等领域[1]。近年来植物类原料制备活性炭受到人们的广泛关注,如花生壳[2-3]、核桃壳[4-5]、玉米杆[6]、小麦秸秆[7]、大豆秸秆[8]等,但仍未见荔枝核活性炭制备的相关研究报道。
试验以荔枝核为原料,以磷酸为活化剂,进行荔枝核活性炭对亚甲基蓝吸附性能的研究,以期为荔枝的开发利用提供思路。
1 材料与方法
1.1 材料、仪器与设备
荔枝核:荔枝购于当地市场,取荔枝核,核清洗干净后于80 ℃恒温烘干箱中进行烘干至恒重,后用高速多功能粉碎机粉碎,供使用。
磷酸(湖北新河化工原料有限公司);亚甲基蓝(天津市福晨化学试剂厂);以上试剂均为分析纯,试验用水为蒸馏水。
722型可见分光光度计(上海光谱仪器有限公司),;SX2-4-13型马弗炉(上海跃进医疗器械有限公司);SHA-B型水浴恒温振荡器(金坛市医疗仪器厂)。
1.2 试验方法
1.2.1 吸附性能测试方法
1.2.1.1 亚甲基蓝溶液的标准曲线绘制
参照文献[9],采用分光光度法测亚甲基蓝的含量。分别向8支25 mL比色管中准确加入0.00,0.01,0.03,0.05,0.07,0.09,0.11和0.13 mL亚甲基蓝溶液(1.5 g/L),加蒸馏水稀释至刻度处,放置一段时间后,用分光光度计在665 nm条件下测定其吸光度,绘制标准曲线,得线性回归方程A=0.179 73C+0.008 86,相关系数R2=0.999 2。
1.2.1.2 吸附试验
取0.5 g活性炭放入250 mL具塞锥形瓶中,加入250 mL亚甲基蓝溶液,置于水浴恒温振荡器中,以280 r/min速度振荡,在室温下吸附6 h后过滤。采用1.2.1.1方法测定滤液的吸光度,按式(1)和(2)计算出活性炭对亚甲基蓝的吸附率和吸附量。

式中:Qe为吸附剂吸附量,mg/g;Re为吸附率,%;Co为亚甲基蓝初始质量浓度,mg/L;Ce为平衡时质量浓度,mg/L;V为用于吸附体积,mL;m为所用活性炭质量,g。
1.2.2 单因素试验
1.2.2.1 活化剂浓度对活性炭吸附性能的影响
分别称取6份5 g样品于60 mL坩埚中,固液比1∶2(g/mL),加入浓度20%,30%,40%,50%,60%和70%的磷酸充分搅拌后浸渍2 h,置于马弗炉中以10℃/min速率升温至400 ℃,恒温炭化活化3 h。冷却后抽滤,洗涤沉淀直至滤液约pH 7,烘干至恒重。采用1.2.1.2方法测定活性炭对亚甲基吸附性能,确定最佳活化剂浓度。
1.2.2.2 活化时间对活化碳吸附性能的影响
以50%磷酸为活化剂,固液比1∶2(g/mL),炭化活化时间1,2,3,4,5和6 h,按1.2.2.1方法得到活性炭,采用1.2.1.2方法测定活性炭对亚甲基吸附性能,确定最佳活化时间。
1.2.2.3 固液比对活化碳吸附性能的影响
以50%磷酸为活化剂,炭化活化温度400 ℃,活化时间3 h条件下,固液比1∶1,1∶2,1∶3,1∶4,1∶5,1∶6(g/mL),按1.2.2.1操作得到不同活性炭样品,采用1.2.1.2方法测定活性炭对亚甲基吸附性能,从而确定最佳固液比。
1.2.2.4 炭化活化温度对活性炭吸附性能的影响
50%磷酸为活化剂,固液比1∶3(g/mL),炭化活化温度400 ℃条件下,活化温度200,300,400,500,600和700 ℃,按1.2.2.1操作得到不同活性炭样品,采用1.2.1.2方法测定活性炭对亚甲基吸附性能,从而确定最佳活化温度。
1.2.3 正交试验
为了进一步研究荔枝核活性炭最佳工艺,在单因素基础上,对活化温度(A)、炭化活化时间(B)、固液比(C)、磷酸浓度(D)设计L9(34)正交试验,以确定制备荔枝核活性炭的最佳工艺条件,其中正交试验所用的因素与水平表见表1。
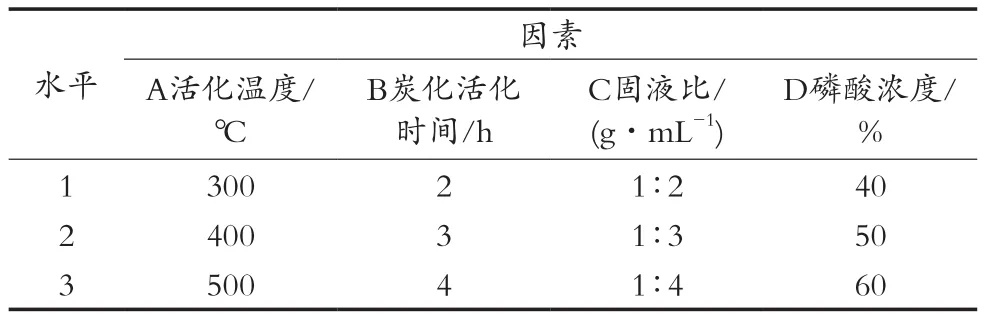
表1 正交试验因素与水平
2 结果与讨论
2.1 单因素试验
2.1.1 活化剂浓度对活性炭吸附性能的影响
按1.2.2.1的试验步骤进行操作,得到的活性炭对亚甲基蓝的吸附性能如图1所示。
活性炭对亚甲基蓝的吸附量和吸附率随着磷酸浓度增大而呈现出先升高再降低趋势,磷酸浓度50%时,活性炭吸附量和吸附率达到最大,分别为3.635 mg/g和93.21%。浓度大于50%,其吸附量和吸附率又分别开始下降。其原因可能是:磷酸浓度逐渐增加,可防止焦油和一些液体组分的形成,进而可以保护活性炭的孔隙结构,将所得活性炭洗涤后可以得到大量发达的微孔结构,所以其吸附性能逐渐增强,但磷酸浓度超过50%时,高浓度的磷酸会进行脱水作用,破坏活性炭的孔隙结构,从而降低活性炭的吸附效果[10],所以磷酸最佳浓度为50%。
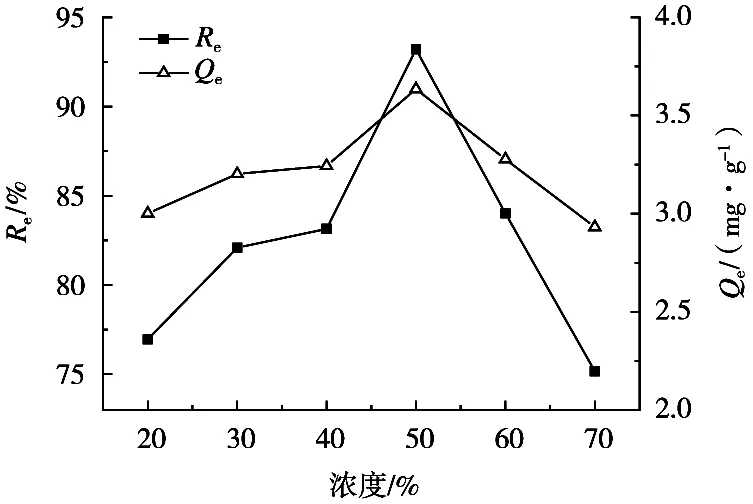
图1 活化剂浓度对活性炭的吸附性能的影响
2.1.2 活化时间对活化碳吸附性能的影响
按1.2.2.2的试验步骤进行操作,得到的活性炭对亚甲基蓝的吸附性能如图2所示。
活性炭对亚甲基蓝的吸附量和吸附率随着活化时间延长呈现出先上升再下降趋势,其原因可能是:反应起始时,物质之间还未完全反应,但随着时间推移,活性炭的孔隙结构越来越发达,比表面积较大,直到反应3 h时活性炭吸附性能达到最大,但随着时间进一步增加,其一部分微孔被破坏,比表面积缩减,所以吸附性能也降低[11]。因此试验的炭化活化最佳时间为3 h。

图2 活化时间对活性炭的吸附性能的影响
2.1.3 固液比对活化碳吸附性能的影响
按1.2.2.3的试验步骤进行操作,得到的活性炭对亚甲基蓝的吸附性能如图3所示。
活性炭的吸附量与吸附率随着固液比增加而呈现先上升再下降趋势,固液比1∶3(g/mL)时,活性炭的吸附量和吸附率达到最大,分别为5.908 mg/g和98.46%。从1∶3(g/mL)以后,活性炭的吸附量和吸附率迅速下降。其原因可能是:在固液比较小的情况下,其表面的微孔结构丰富,固液比1∶3(g/mL)时活性炭的吸附性能最大,但持续增大固液比时,其微孔结构转变为中孔或大孔,破坏其孔隙结构,导致比表面积下降[12]。所以最佳固液比为1∶3(g/mL)。

图3 固液比对活性炭的吸附性能的影响
2.1.4 炭化活化温度对活性炭吸附性能的影响
按1.2.2.4的试验步骤进行操作,得到的活性炭对亚甲基蓝的吸附性能如图4所示。
活性炭对亚甲基蓝的吸附量和吸附率随着活化温度上升呈现出先缓慢反应后迅速升高最后趋于平缓,温度400 ℃时,活性炭吸附量和吸附率达到最大,分别为14.98 mg/g和99.88%。而从400 ℃以后,亚甲基蓝吸附量和吸附率趋于平缓。其原因可能是,400 ℃以前,温度过低还没有达到反应所需要的温度,因此反应还未完全且反应速度较慢,而随着温度上升,反应也随之越来越激烈,直到400 ℃时反应达到最大,此时得到的活性炭的孔隙结构最发达,比表面积最大,然而随着反应进行,温度过高,活性炭的微孔结构被破坏,使其比表面积减小,因而导致吸附性能降低,当降低到一定程度以后基本保持不变,所以曲线趋于平缓[13]。所以最佳炭化活化温度为400 ℃。

图4 活化温度对吸附性能的影响
2.2 正交试验结果
由表2中的极差分析可以看出,各因素作用主次为活化温度>活化时间>磷酸浓度>固液比,说明活化温度对活性炭的吸附量影响最大,其次是活化时间,磷酸浓度,而固液比的影响最小。由正交表可以看出,理论所得的最佳工艺条件为活化时间3 h,活化温度500 ℃,磷酸浓度60%,固液比1∶3(g/mL)。
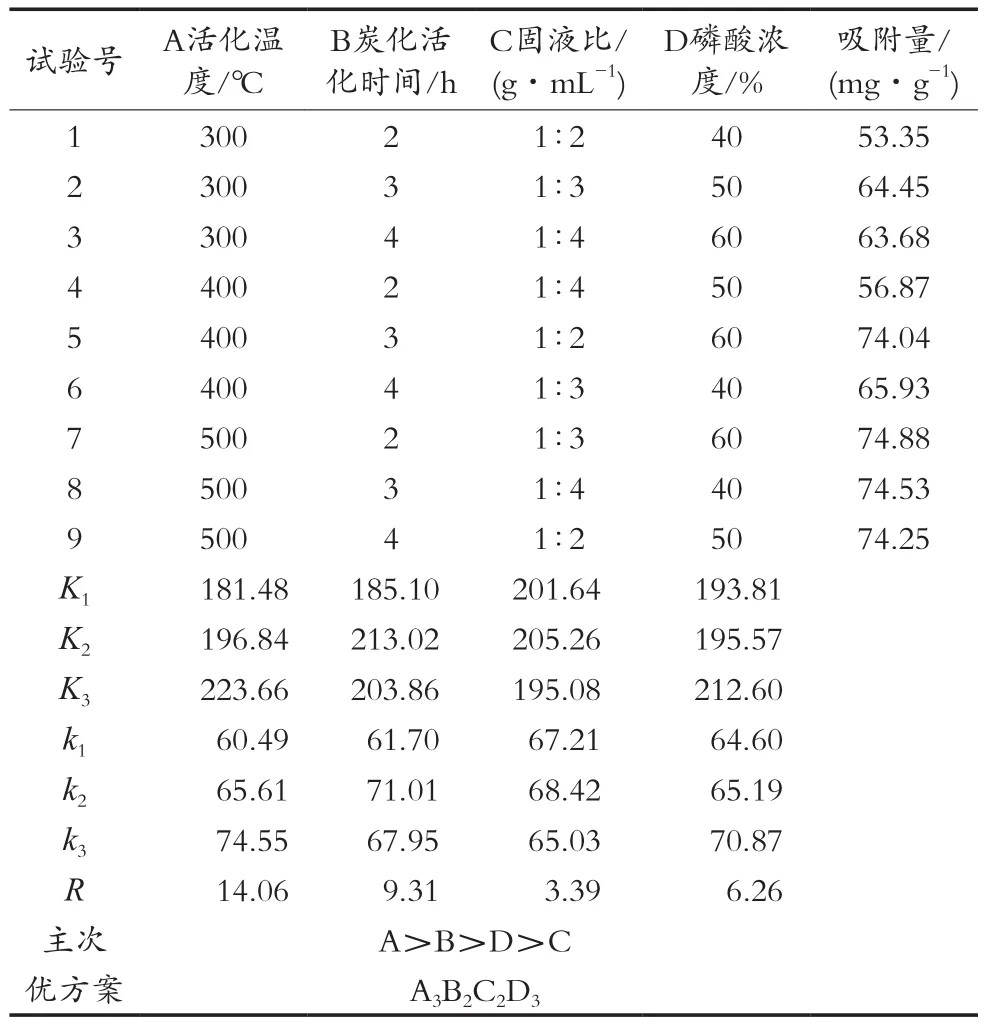
表2 正交试验结果
2.3 验证试验结果
因为通过极差分析得到的优方案A3B2C2D3,并不包含在正交表中已做过的9个试验方案中,所以将优方案A3B2C2D3(试验1)与正交表中最好的7号试验A3B1C2D3(试验2)进行验证,分别做平行试验3次,取平均值,试验结果见表3。
由表3可以看出,试验1所得活性炭比试验2所得活性炭的吸附能力强,可能是因为随着活化时间的增加,反应越来越完全,活性炭孔隙结构也越来越丰富,时间3 h时达到最大,此时有巨大的比表面积,因此吸附效果最好[24]。

表3 验证试验结果
3 结论
通过用荔枝核为原料制备活性炭,以其对亚甲基蓝的吸附率和吸附量为考察指标,结合所做试验及相关数据分析得到主要结论,将荔枝核经过磷酸处理并在高温的条件下进行炭化和活化之后确定活性炭的最佳工艺条件:活化时间3 h,活化温度500 ℃,磷酸浓度60%,固液比1∶3(g/mL)。在最佳工艺条件下,亚甲基蓝的吸附率为99.72%,吸附量为104.7 mg/g,吸附效果较好。
